氧钝化圆形孔缺陷石墨烯的电学特性
2014-08-03戴振宏
王 森,戴振宏,刘 兵,徐 雷
(烟台大学光电信息科学技术学院,山东 烟台 264005)
二维蜂窝状结构的石墨烯[1]由于有着很多奇异的电子性质和机械特性,近年来引起了人们极大的研究兴趣.在实际应用中有多种方法用于调节石墨烯的电子结构,如可以将其剪裁成纳米带[2],使用多种元素进行掺杂[3]或吸附过渡金属原子等[4-5].引入缺陷亦是改变石墨烯电子结构的一种有效手段[6-9],孔缺陷石墨烯的孔洞边缘存在着未钝化的 σ 键,通过使用其他元素对悬挂的 σ 键钝化,可实现对其电子结构的调节[7-8],其中使用氧元素进行钝化就是一种有效手段[10-11].在石墨烯纳米带的相关工作中,由于氧钝化后的石墨烯纳米带具有多样的边界结构和氧元素含有的孤对电子,使得氧元素钝化的石墨烯纳米带展现出了许多独特的性质[10,11],然而对氧元素在孔缺陷石墨烯中钝化悬挂的σ键的做系统研究的文献较少.作者对氧钝化的圆形孔缺陷石墨烯做了系统的研究,探讨氧钝化的圆形孔缺陷石墨烯的最稳定结构,并且讨论氧原子的钝化效应对圆形孔缺陷石墨烯导电性的影响.
1 模型与计算方法
模型参考Chshiev等[12]构建模型的方式,通过移除以六圆环结构为中心的碳原子获得圆形孔缺陷的石墨烯,根据移除的碳原子数目将结构标记为Cn,如图1中(a)(b)(c)所示.
所有计算使用基于量子力学第一性原理密度泛函理论的VASP[13]软件包来实现.计算中采用了投影缀加平面波方法(PAW)[14]和广义梯度近似(GGA)[15].采用6×6的石墨烯超级原胞模拟孔缺陷石墨烯结构,真空层距离取1.5 nm以消除层间相互作用.平面波基矢的截断能取500 eV,总能收敛标准取相邻两电子步间能量差小于1.0×10-5eV.原子位置优化方法使用共轭梯度法,电子占据用0.05 eV展宽的高斯涂抹方法,结构优化标准取原子受力小于0.1 eV/nm,且采用全弛豫方式.布里渊区积分采用 MP 机制的9×9×1的特殊K点取样.
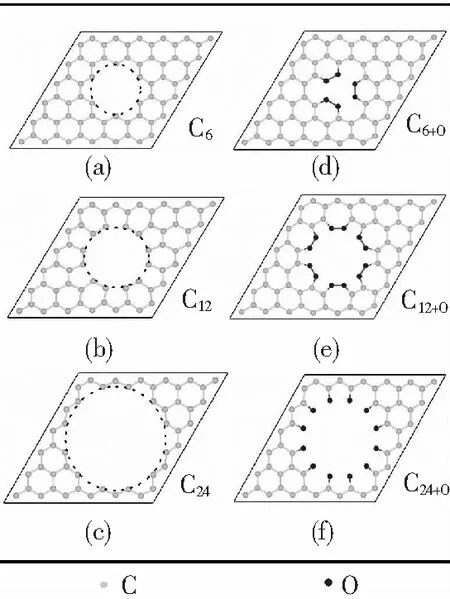
图1 圆形孔缺陷石墨烯及氧钝化的圆形孔缺陷石墨烯结构的俯视图
2 结果和讨论
弛豫的结果显示 C6与 C24结构的孔洞边缘形状呈锯齿型,如图 1 中(a)(b)所示,而且内部的碳原子结构及晶格常数只有轻微的改变.相对而言,C12结构的晶格常数大概收缩了14%,内部碳原子的位置也发生了较大的改变,孔洞边缘大体上呈现出扶手椅形状,上述计算结果与Ahin等[7]的计算结果相符.
在图 1 中可以看出 C6与 C24结构中的碳原子和石墨烯中的碳原子一样在周围有3个最近邻的碳原子,然而孔洞边缘处的碳原子仅有2个最近邻碳原子.这说明边缘处的碳原子有一个悬挂的σ轨道,这个轨道将会在能带图中给出一条平滑的能带.由于 C6结构中有6个边缘碳原子,因此在能带图中可以看到6个平滑的能带,如图 2(a)所示.其中有一半的能带将被边缘处悬挂的6个σ电子所占据而分布在费米能级以下,另一半能带分布在费米能级以上.然而,可以看出这6个能带有一半以上的能带被占据,部分空带越过了费米能级,这些附加的电子主要来源于π电子.可以看出π电子的成键轨道亦有部分空余,导致了满占据的π电子成键轨道越过费米能级,这些空出的电子转移到了悬挂的 σ 轨道上,呈现出图中所示的能带结构.通过投影态密度能够更明显的看出这种电子转移现象,这种电子转移现象同样出现在 C24结构中,而相似的电子转移现象在石墨烯纳米带的计算中也可以看到[10].

图2 顺磁态和反铁磁态的C6结构,C12结构的能带图和投影态密度图
在考虑自旋效应之后,可以看到 C6的能带结构发生了变化,如图 2(b)所示.由图可以明显看出平滑能带的变化,悬挂的 σ 电子的占据态和未占据态的能量间隔变大,而且占据态轨道明显远离费米能级.由投影态密度图中可以看出费米能级附近的轨道主要被π电子占据,而且由π电子向悬挂的σ轨道的电子转移现象消失,使得 C6呈现出半导体性质.这种由于磁性而产生的带隙同样出现在锯齿型石墨烯纳米带的相关计算中[2]. C24结构的孔洞边缘形状与 C6相似,亦展现出了相似的导电性质.
C12结构的孔洞边缘形状呈现出扶手椅型,具有顺磁性基态.图 2(c)中给出了 C12结构的能带图和投影态密度图,由图中可以看出 C12的能带中并没有出现平滑的σ电子轨道,费米能级附近的能带都被π电子占据.图3 中给出了 C12结构的差分电荷密度,由图中可以看出孔洞边缘处的碳原子除了和最近邻的2个碳原子成键,还和邻近的边缘处的碳原子轻微成键,这种成键的结果导致悬挂的 σ 电子消失.而且,在悬挂的 σ 电子消失后,C24结构没有 C6和 C24结构顺磁态中的电子转移现象,因此体系呈现出了半导体性质,上述导电性计算结果与Ahin等人[7]的计算结果一致.磁性和导电性等相关计算结果如表1所示.

图3 C12结构的差分电荷密度
表1所有结构的计算结果
Tab.1 Calculation results of all the structure

结构磁性带隙/eV总能/eVRC—O/nmEb/O/eV C6反铁磁0.72-591.842∗∗ C6+O顺磁0.73-631.0340.1335.00 C6+O(非)顺磁0.98-640.8170.1236.63 C12反铁磁1.34-528.376∗∗ C12+O顺磁0.59-578.3300.1332.64 C12+O(非)顺磁0.42-616.9360.1225.85 C24反铁磁0.13-408.492∗∗ C24+O顺磁0.64-503.6040.1276.39 C24+O(非)顺磁0-504.5650.1236.48
为了保证石墨烯缺陷体系的稳定性或对其电子结构进行调节,通常使用其他元素钝化悬挂的σ键,多数情况下会使用氢元素钝化[7,17].此外,氧元素也多用于钝化悬挂的 σ 键[10,11],氧原子除了可以和悬挂的 σ 电子成键,其pz轨道的电子还可以与边界的碳原子形成π键,因此碳原子与氧原子将会形成稳定的双键结构,由此可以改变体系的磁性及电子结构.
图 1 (d) (e) (f) 中给出了氧钝化的圆形孔缺陷石墨烯的结构图,根据移除的碳原子数目标记为 Cn+O.在图 1(d)(e)中可以看出由于氧原子的密度较大,导致碳原子和氧原子与期望中形成的碳氧双键不同,氧原子除了和孔洞边缘处的碳原子成键,还与邻近的氧原子相互成键.由图 4(a)给出的 C6+O的投影态密度可以进一步分析这种复杂的成键特点.氧原子(O1)的pz轨道和期望中一样与孔洞边缘处的碳原子(C1)形成了π键.然而,和石墨烯纳米带计算中不同,氧原子并没有出现孤对电子轨道[10,11],而是氧原子的px与py轨道关联形成了2个新的未满轨道,这2个轨道分别与孔洞边缘处的碳原子(C1)和邻近的氧原子(O2)成键,这种成键和 σ 键相似,因此其成键轨道的能量范围要低于π键能量,由图 4(a)中可以看出π点的成键轨道分布在费米能级附近,而这种类 σ 成键轨道能量在-3 eV以下.此外,还可以在态密度图中找到对应的碳氧键和氧氧键的反键轨道,进而证明这种复杂成键的存在.
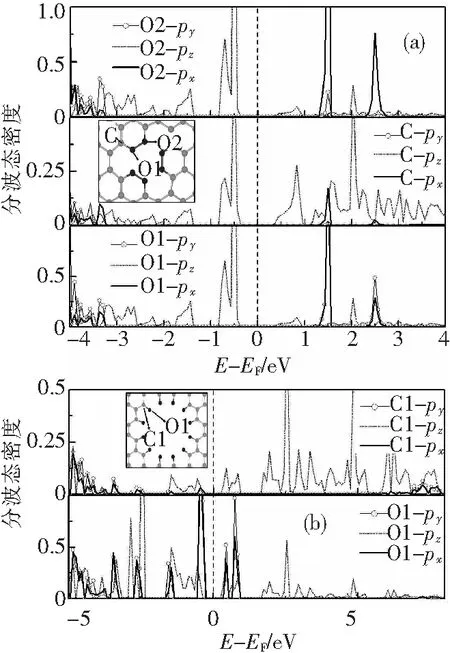
图4 C6+O和C24+O结构的投影态密度图
C24+O结构中,由于氧原子的密度较大,氧原子与氧原子之间并未成键,在表1中给出了氧原子与孔边缘处碳原子的键长RC—O.由表1可以看出 C24+O的碳氧键长度小于 C6+O与 C12+O的碳氧键长度,碳原子与氧原子之间的成键特性也不同于前述2种结构.由图 4(b)中可以看出碳氧之间的成键与期望中仍然不一致,氧原子的px与py轨道之间的关联效应在 C24+O结构中依然存在.氧原子(O1)的pz与孔洞边缘处的碳原子(C1)形成了π键,px与py轨道关联形成的新轨道与碳原子形成类 σ 键,但是 C24+O与 C6+O和 C12+O结构中成键不同的是氧原子与氧原子之间没有成键,px与py关联形成的2个轨道中有一个满占据的轨道,这个轨道与纳米带计算中氧原子的孤对电子轨道相似[10-11],具有较强的局域性,且能量高于碳与氧之间的类 σ 成键轨道,并与π电子轨道能量相近,如图 4(b)所示.
氧原子钝化后的孔缺陷石墨烯的磁性和导电性都发生了变化,首先由于悬挂的 σ 轨道被钝化,体系的磁性消失变成的顺磁性基态.其次,由图 5 中的能带图可以看出,由于氧原子对悬挂的 σ 电子的钝化效应,能带中的平滑轨道全部消失,费米能级附近的轨道只被π电子占据,进而导致体系产生带隙.与钝化前不同的是费米能附近的能带主要来源于碳碳π键和碳氧π键的贡献,这使得体系的能隙发生的变化.如表 1 所示,C6结构的带隙变化不大,但是 C12和 C24结构由于受碳氧π键的影响,带隙变小.

图5 C6+O, C12+O, C24+O结构的能带图
表1中还给出了各个结构平均到每个氧原子的结合能Eb/O(单位eV),其计算公式为
Eb/O=(ECn+EO-ECn+O)/nO,
其中:ECn为圆形孔缺陷石墨烯的能量,EO为单个氧原子的能量,ECn+O为氧钝化的孔缺陷石墨烯的能量,nO为原胞参与钝化的氧原子的个数.可以看出随着氧原子之间的间隙变小,Eb/O变大,这让我们有理由相信,较小的氧原子密度可以得到更稳定的结构.而且在石墨烯纳米带相关计算中,氧原子钝化的石墨烯纳米带存在着非平面的边界结构[10-11].我们可以推测氧钝化的圆形孔缺陷石墨烯结构中,可能也存在更稳定的非平面吸附结构.
图6给出了氧钝化圆形孔缺陷石墨烯的非平面结构图,其中黑色(灰色)圆点代表位于石墨烯平面之上(下)的氧原子,从图6可以看出,氧原子交替的分布在石墨烯平面的上方和下方,而且边缘处的碳原子也有轻微的起伏.由表1中的总能(单位eV)计算可知这种非平面吸附结构比平面吸附结构具有更低的总能,而且平均到每个氧原子上得结合能Eb/O更大,这说明非平面吸附结构更加稳定.

图6 非平面C6+O、C12+O、C24+O结构的俯视图
C6和 C24的孔洞边缘因为具有相同的锯齿型排列,它们的Eb/O值相差不大,而C12孔洞边缘为扶手椅型,其Eb/O值相对较小,这说明锯齿形边缘结构更容易和氧结合.由图6中可看出,由于氧原子之间的间隔变大,3种结构中氧与氧之间都不再成键,碳氧键的长度相近,碳氧成键具有相似的特性.通过投影态密度可以对这种非平面结构的成键特点进行分析,图7给出了C6+O的分波态密度图.和平面结构相比,非平面结构中的p轨道之间的关联性更强,具有和sp3杂化相似的特性,这说明当氧原子和碳原子离开石墨烯平面后获得了更有效的杂化,这种类sp3杂化使得非平面吸附结构比平面吸附结构中的类sp2杂化结构具有更大的稳定性.

图7 非平面C6+O结构的投影态密度图
非平面结构具有顺磁性基态,而且与平面结构相比,其电子结构发生了显著的改变,如图8所示.非平面 C6+O和 C12+O结构依然为半导体,但是和平面结构相比,其带隙发生了改变,如表1所示.值得注意的是非平面结构的 C24+O由平面结构中的半导体变成了导体,C24+O的导体性质起源于氧原子有较大的电负性,由图9给出的非平面C24+O结构的分波态密度图中可以看出,氧原子除了和边缘处的碳原子成键,其pz轨道电子与次近邻的碳原子的pz轨道在-1.5 eV 附近亦发生了关联.这是由于具有较大电负性的氧原子(O)在与边缘处的碳原子(C1)成键时破坏了边缘碳原子(C1)与内层电子(C2)之间的π键,内层电子出现了未成键的pz轨道电子,这部分pz电子和氧原子的pz轨道电子发生关联.但是氧原子的pz轨道电子已经和 C1 的pz轨道电子成键,因此需要额外的电子填充氧原子pz轨道,这部分额外的电子由氧原子的px轨道电子提供,如图9所示,氧原子的px轨道电子部分转移到了氧的pz轨道上,导致了px轨道和pz轨道都穿过了费米能级,使得C24+O呈现出导体性质.在C24+O平面结构中,边缘处的碳原子和邻近的碳原子有较强的关联性,这使得氧原子的电负性影响较小,并未发生这种电子转移现象.而在C24+O非平面结构中,由于 C1 原子偏离了石墨烯平面,它和邻近的碳原子之间的关联性变弱,氧原子的电负性产生了较大的影响.即是说C24+O的导体性质是氧的电负性和纳米孔中碳原子之间的关联作用共同影响的结果.同理,其他的吸附结构中由于 C1 受其他碳原子的关联影响较大,并未变成导体,只有C24+O结构在由平面吸附结构变为非平面吸附结构时导电性发生了改变.这种半导体-金属的转变可用于石墨烯电子器件的设计.

图8 非平面C6+O,C12+O,C24+O结构的能带图

图9 非平面C24+O结构的分波态密度图
3 结 论
利用第一性原理方法计算了氧钝化圆形孔缺陷石墨烯的电学与磁学特性.结果表明氧钝化的孔缺陷石墨烯存在非平面的钝化结构,而且氧原子对圆形孔缺陷石墨烯的电子结构和磁学性质产生了影响.氧钝化圆形孔缺陷石墨烯均具有顺磁性基态,且根据缺陷的碳原子数目的不同,氧原子对缺陷石墨烯的导电性影响也不相同.其中C6+O和C12+O缺陷构的带隙和钝化之前相比产生明显的变化,而非平面的C24+O结构由于受氧原子的电负性和边界处碳原子关联性的影响,展现出导体性质.本文研究为缺陷石墨烯的电学调制方法提供了一定的参考, 有助于推动石墨烯在电子器件中的应用.
参考文献:
[1]Zhang Yuanbo, Tan Yanwen, Stormer H L, et al. Experimental observation of the quantum Hall effect and Berry phase in graphene[J]. Nature, 2005, 438: 201-204.
[2]Son Y W, Cohen M L, Louie S G. Energy gaps in graphene nanoribbons[J]. Phys Rev B, 2006, 97: 216803(1-4).
[3]Panchakarla L S, Subrahmanyam K S, Saha S K, et al. Synthesis, structure, and properties of boron-and nitrogen-doped graphene[J]. Adv Mater, 2009, 21(46): 4726-4730.
[4]Ahin H S, Senger R T. First-principles calculations of spin-dependent conductance of graphene flakes[J]. Phys Rev B, 2008, 78: 205423 (1-8).
[5]Ahin H S, Senger R T, Ciraci S. Spintronic properties of zigzag-edged triangular graphene flakes[J]. J Appl Phys, 108: 074301(1-5).
[6]Xiao Jin, Yang Zhixiong, Xie Weitao, et al. Electronic properties of graphene nanoribbon doped by boron/nitrogen pair: a first-principles study[J]. Chin Phys B, 2012, 21(2): 027102 (1-7).
[7]Ahin H S, Ciraci S. Structural, mechanical, and electronic properties of defect-patterned grapheme nanomeshes from first principles [J]. Phys Rev B, 2011, 84: 035452 (1-7).
[8]Oswald W, Wu Zhigang. Energy gaps in graphene nanomeshes [J]. Phys Rev B, 2012, 85: 115431(1-5).
[9]张振江,胡小会,孙立涛. 单空位缺陷诱导的扶手椅型石墨烯纳米带电学性能的转变[J].物理学报, 2013, 62(17):177101(6).
[10]Lee G, Cho K. Electronic structures of zigzag graphene nanoribbons with edge hydrogenation and oxidation[J]. Phys Rev B, 2009, 79: 165440 (1-12).
[11]Simbeck A J, Kharche N, et al. Electronic structure of oxygen-functionalized armchair graphene nanoribbons[J]. Phys Rev B, 2013, 88: 035413 (1-10).
[12]Yang Hongxin, Chshiev M. Inducing and optimizing magnetism in graphene nanomeshes [J]. Phys Rev B, 2011, 84: 214404 (1-7).
[13]Kresse G, Hafner J. Ab initio molecular dynamics simulation of the liquid metal amorphous semiconductor transition in germanium[J]. Phys Rev B,1994, 49: 14251-14269.
[14]Blochl P E. Projector augmented-wave method[J]. Phys Rev B, 1994, 50(24): 17953-17979.
[15]Perdew J P, Chevary J A, Vosko S H. Atoms, molecules, solids, and surfaces: Applications of the generalized gradient approximation for exchange and correlation[J]. Phys Rev B, 1992, 46(11): 6671-6687.
[16]魏晓林, 陈元平, 王如志, 等. 含孔缺陷石墨烯纳米条带的电学特性研究[J]. 物理学报, 2013, 62(5): 057101(1-5).
[17]Jippo H, Ohfuchi M, Kaneta C. Theoretical study on electron transport properties of graphene sheets with two-and one-dimensional periodic nanoholes [J]. Phys Rev B, 2011, 84, 075467 (1-8).
