基于胃镜图像的病灶区域检测方法研究*
2014-07-25邢永吉
关 沫,邢永吉
(沈阳工业大学 信息科学与工程学院,辽宁 沈阳 110023)
随着人类生活方式和日常饮食的改变,加之现代生活快节奏性与不规律性,胃肠道疾病的发病率越来越高。目前,胃部疾病的检测主要借助于电子胃镜。医学电子胃镜主要由内窥镜、视频处理器和视频显示器组成。应用电子胃镜可以采集到高分辨率的医学图像,如图1所示。临床医生可以灵活地操控电子胃镜来实时地观察胃镜的病变区域。尽管如此,由于诊断过程主要凭借临床医生的主观性,加之病理特征的多样性和胃部环境的复杂性,胃病诊断的误诊率和漏诊率仍居高不下。因此,研究与设计一种基于胃镜图像的计算机辅助检测系统十分必要。
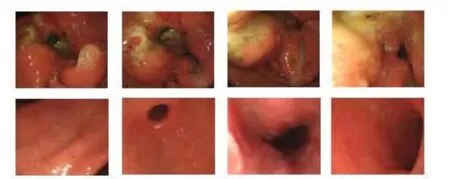
图1 胃镜图像样例
就目前来看,此方面的研究主要集中在无线胶囊内窥镜图像上,其研究的焦点主要集中于小肠和结肠的病灶区域检测。而针对于传统胃镜图像的研究尚处于起步阶段,对于胃部病变的检测尚未形成一种有效的方法。纵观前人的工作,虽然检测方法多种多样,但可以粗略概括为图像预处理、特征提取和用分类器进行识别3个步骤。在图像预处理阶段,图像通常会被分割成小矩形块[1]或相互重叠的圆形区域[2];接下来,从分割后得到的区域提取各种不同特征,包括颜色直方图、局部二进制模式(LBP)和小波域共生矩阵特征等。在最近几年中,机器学习被广泛地应用到医学图像的病灶检测领域当中,例如支持向量机(SVM)[3]、贝叶斯推理和神经网络等。
前人方法的主要缺陷在于过少地考虑了干扰因素的影响,提取特征相对单一。针对以上问题,本文提出了一种新的基于胃镜图像的病灶方法。首先,运用超像素的思想将图像进行分割;然后,针对每一个分割后的区域,分别提取适合于排除干扰和识别病灶的组合特征;最后,采用二级串联分类器进行干扰区域的去除和病灶区域的识别。
1 本方法中的相关技术
胃肠道不同于人体其他器官,作为消化系统的一部分,它的生理环境十分复杂,其表面经常会被粘液、气泡和食物残渣等覆盖。除此之外,胃镜的光照条件也极大地影响了图像的质量。综合前人工作的分析可知,过多的噪声极大地影响了病灶区域的识别准确率。针对此种情况,本文方法在图像分割、特征提取以及分类器的设计上进行了相应改进。
1.1 基于超像素的区域划分
超像素在计算机视觉中得到了广泛应用,但是在病灶检测领域尚未得到应用。参考文献[4]提出了一种简单线性迭代聚集算法(SLIC)来减少计算量。相比较于归一化分割算法和快速漂移算法,该算法具有耗时短、超像素的尺寸和矩形度可调节的特点。
SLIC 分割算法作 用于图 像的 5 维[l,a,b,x,y]空间上,l、a、b分别为 CIELAB 颜色空间的 3 个分量,x、y是像素在图像的二维坐标平面的位置坐标。因此,每一个像素可 以表示为[li,ai,bi,xi,yi]T。
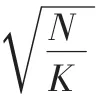
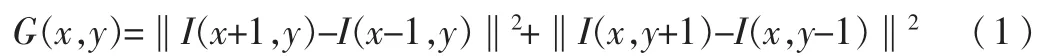
I(x,y)表示在 CIELAB 颜色 空 间内 坐标 为 (x,y)的 像素点的值,‖…‖表示欧式距离,每个超像素的中心点表示为[lk,ak,bk,xk,yk]T。
当期望的超像素的大小近似为S×S时,则相似像素的搜索范围将扩展至以中心像素为中心点的2S×2S大小的区域。为了将更相似的像素聚集到聚类中心,参考文献[4]提出了一种新颖的计算距离的方法,即:
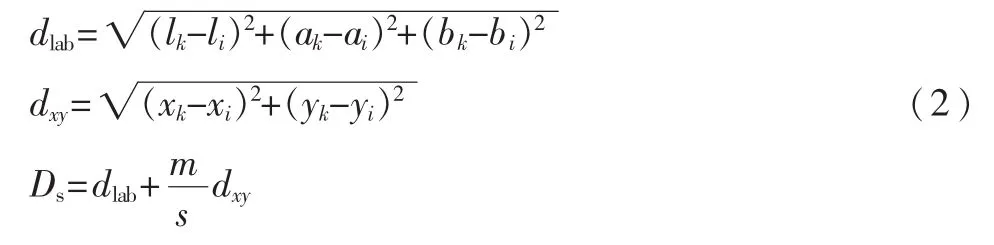
Ds是CIELAB颜色空间内有颜色距离和二维相平面的欧式距离之和。设置m的大小可以控制超像素的矩形度。
1.2 特征提取
基于胃镜图像的特点,应该选取一些具有光照不变性、旋转及平移不变性的颜色和纹理特征,例如HIS_I、HSV_HV、RGB、Norm RGB、RG、Opponent、HUE 颜色直方图特征,以及局部二进制模式(LBP)纹理特征。为找出分别适用于干扰区域和病灶区域的特征,本文人工提取了30×30大小的样本9 000个 (干扰-非干扰样本45 00个、病灶-非病灶样本4 500个),之后分别提取各特征,并放入分类器进行训练与识别,实验结果如表1和表2所示。
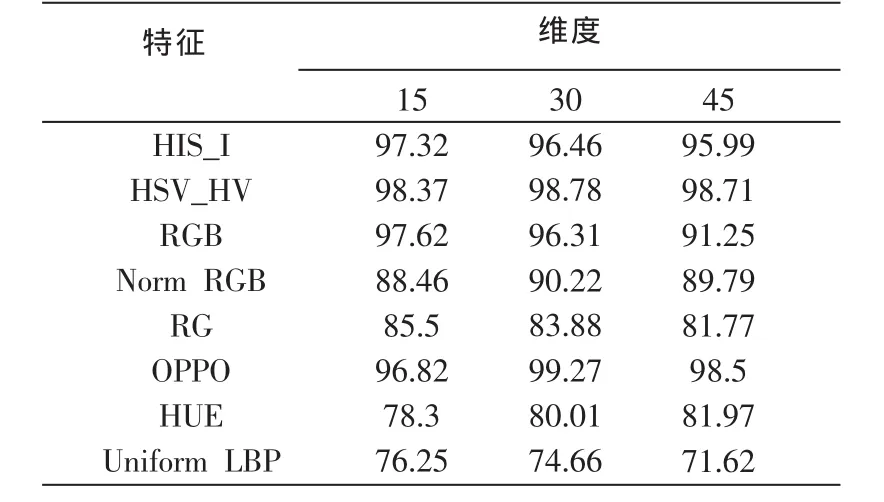
表1 各特征在识别干扰区域时的正确率(AUC/%)
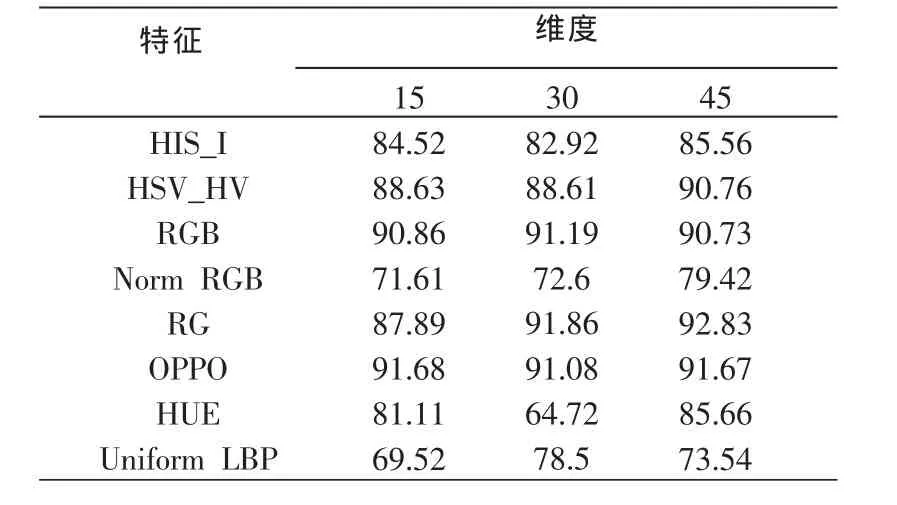
表2 各特征在识别病灶区域中的正确率(AUC/%)
从实验结果可以看出,对于干扰区域,15维的HIS_I、30维的 HSV_HV、15维的 NormalizedRGB 和 15维的Opponent颜色特征表现出色,其受试者工作特征曲线 (ROC曲线)下面积均可达到97.32%、98.78%、97.62%和 99.27%。对于病灶区域,45维的 HSV_HV、30维的RGB、45维的 RG、15维的 Opponent特征表现良好,其ROC曲线下面积均可达到 90.76%、91.19%、92.83%和91.68%。然而单一的特征其代表性也比较单一,在实际复杂的应用环境中仍达不到理想的效果,因此本文方法将多种特征进行融合,通过多种特征的叠加来加强特征的鲁棒性,从而可以应对复杂多变的应用环境,其实验结果如图 2和图 3所示。图 2中,(1)表示 HIS_I(15维)+HSV_HV (30 维),NormRGB (45 维)+OPPO (30 维)+RGB(30 维);(2)表示OPPO(30 维)+LBP(15 维);(3)表示OPPO(30 维)+HUE(45 维);(4)表示OPPO(30 维)+HUE(45 维)+LBP(15 维);(5)表示所有单个特征表现最好的组合。图 3 中,(1)表示 HIS_I(45 维)+LBP(30 维)+NormRGB (45 维)+HUE (45 维);(2) 表示 LBP (30 维),NormRGB (15 维)+RG (30 维);(3) 表示LBP (30 维)+NormRGB(45-d)+RG(45 维)+OPPO(15维);(4)表示 LBP(30 维)+RG(30 维);(5)表示LBP(30 维)+RG(45 维)+OPPO(45 维);(6)表示 RG(45 维)+OPPO(15 维)+RGB(30维);(7)表示RG(45 维)+OPPO(15 维)+RGB(30 维)+LBP(30维);(8)表示所有单个特征表现最好的组合。
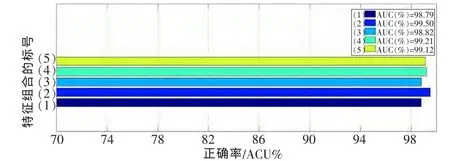
图2 组合特征在识别干扰区域时的正确率
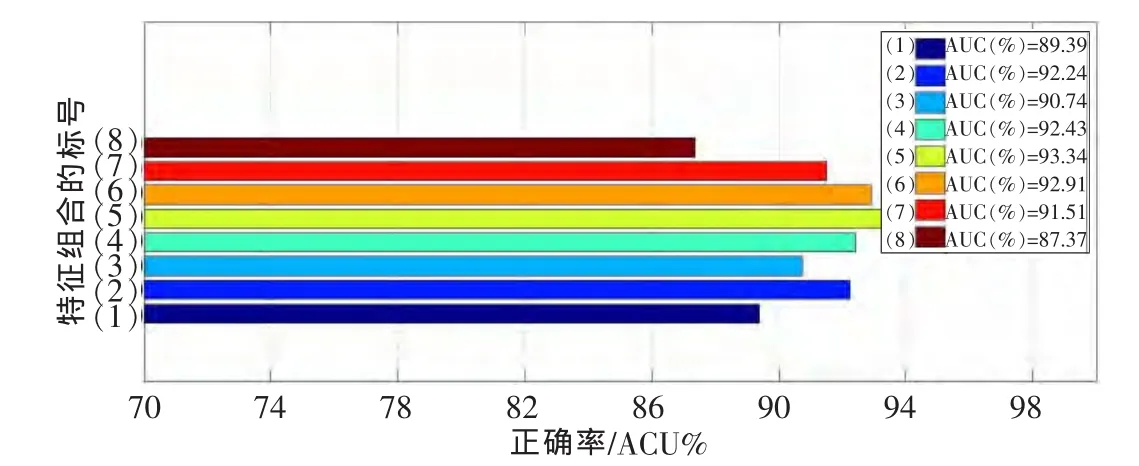
图3 组合特征在识别干扰区域时的正确率
实验结果证明,其组合后的特征性能平均高于任何一个单一特征,达到了预期效果。在干扰区域排除阶段,特征组合 (2)(30维的 Opponent颜色直方图串联 15维的LBP纹理特征)表现最为突出,AUC达到99.50%。在病灶区域识别阶段,特征组合(5)(30维 LBP纹理特征串联45维的RG和45维的Opponent颜色特征)表现出色,AUC达到93.34%。本方法最终采用以上两种最优特征组合方式,为后续的去除干扰和病灶识别工作奠定了基础。
1.3 分类器设计
Adaboost衍生于 Boosting算法,自从 Schapire提出以来得到了广泛的应用。Adaboost属于一种迭代算法,其核心思想是将多个弱分类器组合成一个强分类器。本文选取决策树作为子分类器,为避免过度学习的情况发生,本文将树的深度设置为2。其次需要确定算法迭代的次数,综合考虑算法的识别率及分类器的训练时间,最终确定迭代次数为60最为合适。
为减少胃镜图像中噪声对检测结果的影响,本文方法将两个Adaboost分类器串联起来,形成一个三分类器,通过此分类器,待检测区域将被识别为正常区域、干扰区域或病灶区域3类。其工作流程如图4所示。
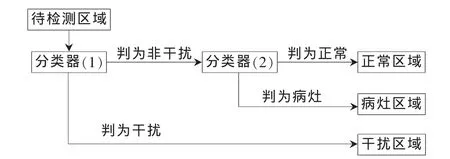
图4 二级串联分类器工作流程
2 方法实现
首先,采用超像素的思想将图像分割成像素相对紧凑一致的区域;其次,通过实验分别找出适用于干扰区域和病灶区域的特征的组合;最后,采用二级分类器完成干扰区域的去除以及病灶区域的识别工作。本文方法的整个流程下。
算法:
(1)设置期望的分割块数K及区域的矩形度m。
(2)在边长为S的区域内随机初始化起始聚集中心CK=[lk,ak,bk,xk,yk]T。
(3)采用3×3大小的邻域寻找梯度最小的点作为聚集中心点。
(4)repeat
(5)for对于每一个中心点CKdo
(6)利用式(2),在中心点周围 2S×2S范围内寻找与中心点最匹配的像素点。
(7)end for
(8)重新计算中心点的位置,并计算新中心点与前中心点位置坐标的欧式距离E。
(9)untilE≤threshold
(10)将孤立存在的小区域强制划分到相邻的最大区域。
(11)for每一个分割后的区域 do
(12)if区域内像素个数≥Nthen
(13)提取适合于干扰区域识别的特征组合。
(14)利用第一级分类器进行识别。
(15)if该区域被识别为干扰区域then
(16)提取适合于病灶区域识别的特征组合。
(17)利用第二级分类器进行识别。
(18)end if
(19)end if
(20)end for
3 实验与结果分析
3.1 实验设计
本实验的数据来源于120个临床病例,共计3 000张医学胃镜图像,其中包含1 500张含有病灶区域的图像和1 500张完全健康的图像。图像的大小为489像素×409像素,存储格式为JPEG。每一幅含有病灶区域的图像都配有专业医师标注的标注图,在实验中作为地面真值。
在实验中,规定对于完全健康的图像,只要有一个区域被识别为病灶区域,则认为检测失败;反之,则认为检测成功。对于含有病灶区域的图像,只要有识别为病灶的区域与医生标注区域有重叠,则认为检测成功;否则,认为检测失败。
在实验中,采用4种不同的方法对相同一批图像进行检测,用来进行检测效果的分析对比。方法1,SLIC分割+组合特征+二级串联分类器;方法 2,SLIC分割+组合特征+单级分类器;方法 3:按 30×30矩形分割图像+组合特征+二级串联分类器;方法 4:按30×30矩形分割图像+组合特征+单级分类器。
3.2 实验结果与分析
本文采用ROC曲线对实验进行分析。ROC曲线将灵敏度与特异性以图示方法结合在一起,可以准确反映分析方法中特异性和敏感性的关系,是试验准确性的综合代表。在ROC曲线图表中,X轴表示假阳性率FPR(False Positive Rate),Y 轴表示真阳性率 TPR(True Positive Rate)。ROC曲线展示了当评判标准变化时这两个变量之间的相互关系。ROC曲线下方的面积可以用来评判一个系统性能的好坏[5]。
实验结果如图5所示,本文所提出的方法(方法1)的检测效果远好于其他方法,其正确率远好于其他3种方法,正确率(AUC)达到91.588%。方法2、方法3和方法4的正确率(AUC)分别为86.058%、76.458%和70.727%。
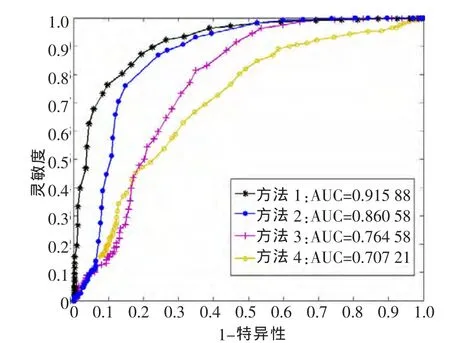
图5 实验ROC曲线图
部分实验效果如图6所示,其中第1排为含有病灶区域的胃镜图像;第2排为临床医师给出的地面真值图;第3排为本文方法检测后的结果图。
医疗器械的限制以及胃部特殊生理环境的影响,使得有些病灶区域很难用肉眼识别。考虑到胃镜图像的成像质量受多方面因素的影响,图像噪声多的特点,本文方法在预处理阶段采用SLIC分割算法,将图像分割成大小均匀的超像素,相较于简单的人工划分区域,具有区域内像素更加统一和紧凑的特点。此外,本文方法还采用了多种特征组合的形式替代了单一特征。最后通过使用二级串联分类器将去干扰和病灶检测步骤串联进行。实验表明,本文方法的病灶检测正确率优于传统方法。
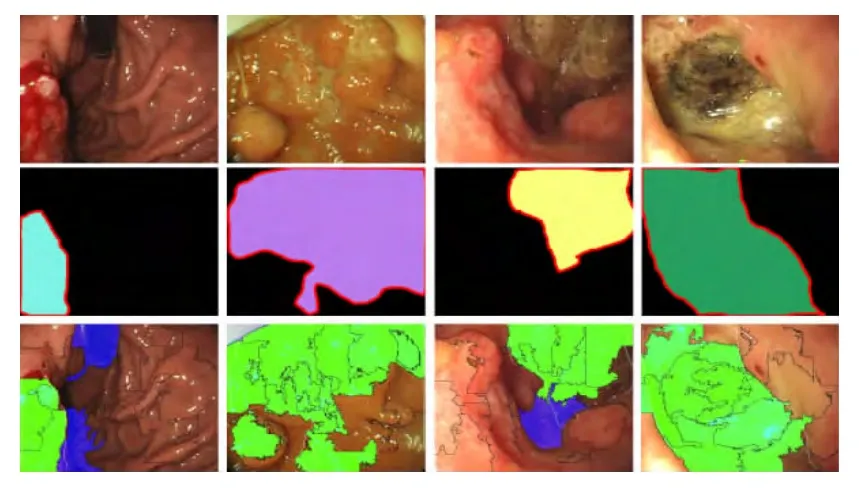
图6 实验效果图
[1]Liang Pan, Cong Yang, Guan Mo.A computer-aided lesion diagnose method based on gastroscope image[C].2012 IEEE InternationalConference on Information and Automation,ICIA 2012, Washington, DC.IEEE ComputerSociety,2012:871-875.
[2]SZCZYPINSKI P, KLEPACZKO A, PAZUREK M, et al.Texture and color based image segmentation and pathology detection in capsule endoscopy videos[J].Computer Methods and Programs in Biomedicine, 2014,13(1):396-411.
[3]LI B,MENG M Q H.Tumor CE image classification using SVM-based feature selection[C].IntelligentRobots and Systems (IROS), 2010: 1322-1327.
[4]ACHANTA R,SHAJI A,SMITH K,et al.Slic superpixels[J].Ecole Polytechnique Federal de Lausssanne (EPFL),Technical Report, 2010: 149300.
[5]SWETS J A,DAWES R M,MONAHAN J.Psychological science can improve diagnostic decisions[J].Psychological Science in the Public Interest, 2000, 1(1): 1-26.
