腐殖质的光化学降解及其对环境污染物环境行为的影响
2014-07-16楼涛汪学军何昆鹏杨臻
楼涛,汪学军,何昆鹏,杨臻
青岛大学化学科学与工程学院,山东 青岛 266071
腐殖质是动植物残体在自然水体和土壤中经过长期的物理、化学和生物作用形成的一种褐色或黑色无定形胶态复合物,它是地表环境中最重要的有机组分, 对生态系统的物理、化学和生物性质起着重要的作用(GOUVÊA 等,2008;MOSTOFA 等,2013;POLUBESOVA 和 CHEFETZ,2014)。腐殖质也是地表自然系统最主要的吸光物质之一,其本身的光化学降解是影响其结构组成和环境特性的一个重要因素(VAHATALO 和 ZEPP,2005;郭卫东等,2008)对环境污染物的形态、迁移、毒性和生物可利用性有着重要的影响(BITTNER等,2012;TANG 等,2013;陈蕾等,2013)。近年来,环境污染日益加剧,臭氧空洞增加,腐殖质的光化学降解及其对环境污染物环境行为影响的研究已成为相关领域的研究热点,本文拟就腐殖质的光化学降解及其对环境污染物环境行为的影响作评述。
1 腐殖质的结构特征
腐殖质根据其在酸碱性溶液中的溶解性可分为以下3类:溶于碱液又能用酸(pH<2)沉淀下来的组分称为腐殖酸(humic acid),溶于酸同时也溶于水的低分子量组分称为黄腐酸(fulvic acid),不溶于酸碱的残留大分子称为腐黑物(humin)。腐殖质结构相对稳定,具有不易被进一步化学、微生物降解和高度非均一化的特征(ALUWIHAREA等,2002)。其主要构成元素有碳、氢、氧、氮和少量硫、磷等,如土壤中腐殖酸含碳 50%~60%,含氢 1.5%~6%,含氮1.5%~6%,其余大部分是氧,以及1%以下的磷和硫。腐殖质相对分子量在300~106之间,其中黄腐酸相对分子量约在300~2000之间,腐殖酸在2×103~2×104之间,腐黑物约在 104~106之间(曾宪成和成绍鑫,2002;CHEN等,2004;MAO等,2007;MUSCOLO 等,2013)。
腐殖质结构十分复杂,随来源和产地的不同有很大的变化。土壤腐殖质分子量较高、低羧基和高酚基含量;水体腐殖质含有较多的酸性基团,与陆源腐殖质相比,其分子量较低,具有较低的芳香基团、酚基、甲氧基和C/N比,但包含较多的羧基和糖等结构组分。大多数的研究认为腐殖质是以多元酚和醌为芳香核心的多聚物,其中芳香核心上有羧基、酚基、羰基、糖、肽等成分,核心之间通过多种桥键如-O-,-CH2-,=CH-,-NH-,-S-S-等连接起来;也有研究者认为腐殖质不存在完整固定的分子结构,而是芳香核心随机聚集的化学结构(GIGLIOTTI等,2002;ROSSEL 等,2013)。
尽管不同来源的腐殖质结构有较大的差异,但都含有苯环和共扼羰基等众多可吸收太阳光的显色基团,在自然系统中易于发生各种光化学降解反应,导致其本身结构和环境物理化学性质的变化。
2 腐殖质的光化学降解
腐殖质的光降解过程分成3类:第一类称为直接光解,这是腐殖质本身直接吸收了太阳能而进行分解反应;第二类称为光敏化反应或间接光解过程,这是腐殖质被太阳光激发,然后将激发态的能量转移给化合物而导致的分解反应;第三类是氧化反应,这是腐殖质被太阳光辐射而产生了各种氧自由基中间体,这些中间体又与化合物作用而生成其它的产物(FAN,2008;PAGE 等,2011;SHINDE 等,2012)。
腐殖质的光化学降解过程通常是在铁或铜等金属的催化作用下进行氧化反应,其主要矿化产物是二氧化碳(CARLOS 等,2012)。Xie等提出光降解机理如下式:
(1)光降解氧化脱羧基/羧基再生过程
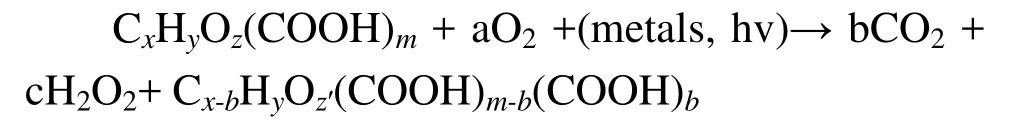
(2)光降解氧化非脱羧基过程
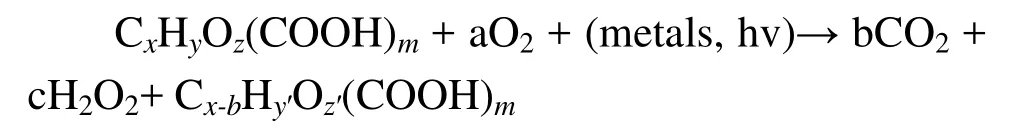
以铁的催化过程为例,其催化过程的机理为:催化过程涉及到三价铁还原为二价铁,然后二价铁又被氧或羟基自由基氧化为三价铁的过程。此机理解释了含有大量有机物水体表层缺氧的现象(水体中氧气的消耗主要为微生物的消耗)。在铁的存在下,反应途径主要有以下2类:(1)通过配位体和铁之间的电荷转移,直接裂解铁与有机物羧基之间的复合物,三价铁还原为二价铁,形成聚羧酸盐自由基,聚羧酸盐自由基脱去羧酸,形成自由基中间体;(2)自由基中间体和铁复合物之间的反应可进一步还原三价铁,使反应性较低的氧类自由基转化为羟基自由基。光解过程中,氧生成反应性氧类中间体(reactive oxygen species),如单线态氧、过氧、羟基自由基和过氧化氢(GARG等,2011)。自由基具有高反应活性,在氧化腐殖质和环境污染物的过程中起到重要的作用,其最终降解产物为二氧化碳和水(MOLOT等,2005;LOISELLE等,2012)。
光化学降解腐殖质产生其它一系列小分子量的物质(LOU和XIE,2006),减弱了对紫外线的吸收(SWAN 等,2012)。小分子量产物大致可分为 4类: 低分子量有机化合物(碳水化合物,MW<200);一氧化碳和二氧化碳;未知褪色有机质;含氮磷化合物(NH4+,PO4--)。代表性低分子量有机化合物主要有甲醇、甲醛、乙醛、乙二醛、丙酮等,这些低分子量的有机物更容易被生物体所利用(DE BRUYN 等,2011;REMINGTON 等,2011)。因此,光化学降解反应对腐殖质的生物可利用率有重要的影响。
Schmitt-Kopplin等(1998)研究了在紫外和可见光照射下,氮气和氧气饱和的条件下对腐殖质结构的影响。结果表明在氮气饱和条件下,腐殖酸结构和分子量保持相对稳定;在氧气饱和条件下,加速了腐殖酸的光化学降解反应,并发现酚基的大量减少以及羧基的生成。照射后腐殖酸的分子量降低、水溶液酸性增强,结构表征的结果表明木质素和类脂结构最易被光降解,而烷烃、氮杂环和烷基苯结构则相对稳定。楼涛等对 Suwannee河腐殖酸和黄腐酸等腐殖质的光化学降解研究表明:UV-B、UV-A和可见光部分分别占无机碳产量的 31.8%、32.6%和25.6%,表明了紫外线和可见光区域都有较大的贡献(楼涛等,2007,2008)。在天然水体中,紫外线易被表层水体吸收,而由于可见光部分较大的贡献,光化学反应仍可发生在紫外光无法到达的水体较深区域。光化学降解腐殖质使其紫外和可见光区域的吸收率降低,对美国东南部Satilla和Altamaha富含腐殖质的河水照射研究表明,紫外吸光系数a320的降低和光化学照射时间有显著的指数下降关系。研究还表明铁、铜和锰等离子能促使氧形成自由基,从而加速腐殖质的光化学降解(FAN,2008;楼涛等,2008)。另外腐殖质的质量浓度、pH和氧气含量以及入射光的强度、波长等都对光化学降解过程有着重要的影响(WINTER等,2007;DALZELL等,2009)。光化学降解过程被认为是影响腐殖质中难降解部分结构的主要因素,季节、纬度、质量浓度和水体的混合程度等环境因素也会影响其反应活性和产物分布(韩宇超和郭卫东,2008;LI 等,2009;HANCKE 等,2014)。
综上所述,光化学降解过程增强了自然体系的酸度、降低了腐殖质的分子量、破坏其芳环结构、改变了其紫外和可见光区域的吸收等,这些水体酸碱性质的变化以及腐殖质结构性质的变化对其结合环境污染物的能力有重要的影响。
3 腐殖质的光化学降解对环境污染物环境行为的影响
腐殖质在自然环境中通过氢键、p键、范德华力等物理化学作用形成巨大的聚集体,呈现多孔疏松海绵结构,有很大的比表面,高达300~340 m2·g-1,呈现胶体性质(LOISELLE等,2012;MUSCOLO等,2013)。腐殖质可与水体、土壤和底泥中的金属离子、氧化物、矿物质和有机污染物通过离子交换、吸附、络合、螯合、絮凝和沉淀等一系列物理化学过程发生结合作用,其结合能力与腐殖质的分子量、疏水性、芳环含量以及环境酸度、温度等密切相关(许中坚等,2003;GAO等,2007;YANG等,2014),而腐殖质本身光化学降解导致的结构特性和环境特性的变化将对环境污染物的环境行为产生重要的影响,其影响主要体现在以下方面。
3.1 腐殖质的光敏化反应对环境污染物降解和转化的影响
王新颖等(2012)研究发现单独日光辐射阿特拉津几乎不降解,而在分别加入3、5和10 mg·L-1的腐殖酸时,阿特拉津的降解率分别为 34.36%、40.74%和15.66%,腐殖酸的存在可促进阿特拉津的降解。Zeng等对拮抗药阿替洛尔的光化学降解研究表明,在腐殖酸和黄腐酸的存在下其降解速率加快,如有三价铁离子的存在则可进一步加速光降解速率,但加入硝酸盐则抑制光化学降解。其机理为腐殖酸和黄腐酸在光化学过程中可产生大量的羟基自由基,从而加速阿替洛尔的光化学降解,铁离子的存在起到协同效应,硝酸盐的存在则起到屏蔽效应。Martínez-Zapata课题组(2013)对内分泌干扰物 4n-壬基酚和三氯苯氧氯酚的光化学降解研究表明,腐殖酸的存在降低了三氯苯氧氯酚的光降解速率,而在腐殖酸(1 mg·L-1)和铁(2 mg·L-1)共存的条件下,产生了协同效应,促进了 4n-壬基酚的光化学降解。Jia等(2013)采用可见光对菲进行光降解,发现土壤腐殖质中的溶解有机物组分降低了菲的降解速率,原因可能为溶解有机物对反应性氧自由基的竞争作用;而土壤腐殖质的腐殖酸和黄腐酸组分在临界质量浓度下,由于光敏化作用加速了菲的光化学降解,但高于临界质量浓度则产生抑制作用,主要是因为腐殖质本身是吸光类物质,其大量存在会起到屏蔽效应。李恭臣等以氙灯作为模拟光源,对水相中5种不同来源、不同质量浓度的黄腐酸对 5种不同多环芳烃的光解作用进行了实验研究,结果表明不同来源的黄腐酸对多环芳烃光解的影响具有较高的一致性。在低质量浓度(1.25 mg·L-1)体系中,黄腐酸对二氢苊、菲和芴的光解表现出不同程度的抑制作用, 而对荧蒽和芘的光化学降解则表现出一定的促进作用,但质量浓度升高后对多环芳烃的光解总体上呈抑制趋势(李恭臣等,2008)。
总的来说,腐殖质的光敏化作用对环境污染物的影响是非常复杂的,一方面腐殖质本身是吸光物质,而且也可与自由基发生反应,与环境污染物的氧化反应形成竞争,尤其在高质量浓度下,大多数的研究表明是抑制其光敏化作用的;但腐殖质本身可强化单线态氧和羟基自由基的生成,尤其在铁等催化剂的作用下可产生协同效应,又可促进有机污染物的降解。而且在腐殖质和污染物共存的条件下,腐殖质与污染物还可形成复合物,其光降解过程的机理更为复杂(AIKEN等,2011)。
3.2 腐殖质的光化学降解对絮凝和吸附环境污染物的影响
Gao和 Zepp(1998)对美国 Satilla河经0.22 μm滤膜过滤后及氧气饱和的水样进行3 d的模拟太阳光照射,发现了黑色的颗粒状物质,元素分析表明形成颗粒中铁和有机碳的质量分数分别为原水体的45%和13%。Hemls等(2013)观察到了同样的现象,对美国弗吉尼亚Great Dismal沼泽水样经30 d的光化学照射后,其中75%的腐殖质矿化为二氧化碳,7%的有机碳和 87%的铁絮凝为颗粒物。推测的机理可能为光化学过程中腐殖酸的脱羧基反应不仅降低了腐殖酸的溶解度,而且释放出部分吸附的铁,铁被水中的氧气和光化学反应产生的高活性氧自由基氧化成三价铁离子,最终通过双电层的排斥作用和范德华力形成腐殖质和氧化铁的颗粒复合物(POERSCHMANN 等,2008;THORN 等,2010;FU和WANG,2011)。
Brooks(2006)研究了湿地和河流的腐殖质经72 h光化学照射后,其与铜离子的结合能力减弱,游离的铜离子质量浓度增加了1.5倍,结构分析表明,腐殖质与铜离子结合能力的减弱与腐殖质芳环和羰基结构的减少显著相关。相似的现象也同样在铅离子中发现,腐植酸经48 h的模拟太阳光照射后,其与铅的结合系数下降了67.8%(汪学军等,2010)。楼涛等(2007)对腐殖酸、黄腐酸进行了模拟太阳光照射,并采用平衡渗析法测定了其与苯并芘、五氯苯酚的结合系数,发现随照射时间的增加,结合系数呈指数下降趋势,结构表征的结果表明结合系数的下降与腐殖酸和黄腐酸的分子量、270 nm下的紫外吸光系数有良好的关联关系,并指出可测定腐殖酸或黄腐酸的结构特性来预测腐殖质在光化学降解过程中与环境污染物结合系数的变化(LOU等,2006;汪学军等,2009)。
综上,腐殖质本身的光化学降解通常导致其与重金属离子和有机污染物结合能力的下降,造成水体或颗粒态中游离的污染物质量浓度增加,这通常代表着环境污染物毒性的增强,对生态系统将造成更大的危害。
4 研究展望
腐殖质的光化学降解过程改变了环境的物理化学特性、降低了腐殖质的分子量、破坏了其芳环结构、改变了其疏水性和亲水性组分的比例和紫外和可见光区域的吸收等。上述环境物理化学特性的变化以及腐殖质结构性质的变化必将对环境污染物的环境行为有重要的影响,从而影响环境污染物的归宿。虽然目前对腐殖质和环境污染物本身的光化学降解机理已经有了很多的研究,但对于腐殖质的光敏化作用以及腐殖质在光化学降解后对环境污染物结合能力的研究还不够深入。笔者认为今后需重点关注:自然水体或土壤系统中腐殖质光化学降解的影响因素;腐殖质光化学降解过程中结构特性的变化机理;以及腐殖质的结构特性与环境污染物结合性质之间的构效关系。特别是随着平流层臭氧空洞的增加,增强了到达地球表面的紫外线强度,由此可能造成对腐殖质和有机污染物的降解以及对生态系统的影响更是一个关键和迫切的科学问题。
AIKEN G R, HSU-KIM H, RYAN J N. 2011. Influence of dissolved organic matter on the environmental fate of metals, nanoparticles, and colloids[J]. Environmental Science & Technology, 45:3196-3201.
ALUWIHAREA L I, REPETAB D J, CHEN R F. 2002. Chemical composition and cycling of dissolved organic matter in the Mid-Atlanic Bight [J]. Deep Sea Research II, 49:4421-4437.
BITTNER M, SAUL N, STEINBERG C E. 2012. Antiandrogenic activity of humic substances [J]. Science Total Environment, 432:93-96.
BROOKS M L, MEYER J S, MCKNIGHT D M. 2006. Photooxidation of wetland and riverine dissolved organic matter: altered copper complexation and organic composition [J]. Hydrobiologia, 579:95-113.
CARLOS L, CIPOLLONE M, SORIA D B, et al. 2012. The effect of humic acid binding to magnetite nanoparticles on the photogeneration of reactive oxygen species [J]. Separation and Purification Technology,91:23-29.
CHEN R F, BISSETT P, COBLE P, et al. 2004. Chromophoric dissolved organic matter (CDOM) source characterization in the Louisiana Bight[J]. Marine Chemistry, 89:257-272.
DALZELL B J, MINOR E C, MOPPER K M. 2009. Photodegradation of estuarine dissolved organic matter: a multi-method assessment of DOM transformation [J]. Organic Geochemistry, 40:243-257.
DE BRUYN W J, CLARK C D, PAGEL L, et al. 2011. Photochemical production of formaldehyde, acetaldehyde and acetone from chromophoric dissolved organic matter in coastal waters [J]. Journal of Photochemistry and Photobiology A: Chemistry, 226:16-22.
FAN S M. 2008. Photochemical and biochemical controls on reactive oxygen and iron speciation in the pelagic surface ocean [J]. Marine Chemistry, 109:152-164.
FU F, WANG Q. 2011. Removal of heavy metal ions from wastewaters: a review [J]. Journal of Environmental Manage, 92:407-418.
GAO H, ZEPP R G. 1998. Factors influencing photoreactions of dissolved organic matter in a coastal river of the southeastern United States [J].Environmental Science & Technology, 32:2940-2946.
GAO Y, XIONG W, LING W, et al. 2007. Impact of exotic and inherent dissolved organic matter on sorption of phenanthrene by soils [J].Journal of Hazardous Materials, 140:138-144.
GARG S, ROSE AL, WAITE TD. 2011. Photochemical production of superoxide and hydrogen peroxide from natural organic matter [J].Geochimica et Cosmochimica Acta, 75:4310-4320.
GIGLIOTTI G, KAISER K, GUGGENBERGER G, et al. 2002. Differences in the chemical composition of dissolved organic matter from waste material of different sources [J]. Biology and Fertility of Soils,36:321-329.
GOUVÊA S P, BOYER G L, TWISS M R. 2008. Influence of ultraviolet radiation, copper, and zinc on microcystin content in Microcystis aeruginosa (Cyanobacteria) [J]. Harmful Algae, 7:194-205.
HANCKE K, HOVLAND E K, VOLENT Z, et al. 2014. Optical properties of CDOM across the Polar Front in the Barents Sea: Origin,distribution and significance [J]. Journal of Marine Systems,130:219-227.
HELMS J R, MAO J, SCHMIDT-ROHR K, et al. 2013. Photochemical flocculation of terrestrial dissolved organic matter and iron [J].Geochimica et Cosmochimica Acta, 121:398-413.
JIA H, LI L, FAN X, et al. 2013. Visible light photodegradation of phenanthrene catalyzed by Fe(III)-smectite: role of soil organic matter[J]. Journal of Hazardous Materials, 256-257:16-23.
LI S X, ZHENG F Y, HONG H S, et al. 2009. Influence of marine phytoplankton, transition metals and sunlight on the species distribution of chromium in surface seawater [J]. Marine Environmental Research, 67:199-206.
LOISELLE S, VIONE D, MINERO C, et al. 2012. Chemical and optical phototransformation of dissolved organic matter [J]. Water Research,46:3197-3207.
LOU T, XIE H, CHEN G, et al. 2006. Effects of photodegradation of dissolved organic matter on the binding of benzo(a)pyrene [J].Chemosphere, 64:1204-1211.
LOU T, XIE H. 2006. Photochemical alteration of the molecular weight of dissolved organic matter [J]. Chemosphere, 65:2333-2342.
MAO J, FANG X, SCHMIDT-ROHR K, et al. 2007. Molecular-scale heterogeneity of humic acid in particle-size fractions of two Iowa soils[J]. Geoderma, 140:17-29.
MART NEZ-ZAPATA M, ARISTIZ BAL C, PE UELA G. 2013.Photodegradation of the endocrine-disrupting chemicals 4n-nonylphenol and triclosan by simulated solar UV irradiation in aqueous solutions with Fe(III) and in the absence/presence of humic acids [J]. Journal of Photochemistry and Photobiology A: Chemistry,251: 41-49.
MOLOT L A, HUDSON J J, DILLON P J, et al. 2005. Effect of pH on photo-oxidation of dissolved organic carbon by hydroxyl radicals in a coloured, softwater stream [J]. Aquatic Sciences, 67:189-195.
MOSTOFA K M, LIU C Q, VIONE D, et al. 2013. Sources, factors,mechanisms and possible solutions to pollutants in marine ecosystems[J]. Environmental Pollution, 182:461-478.
MUSCOLO A, SIDARI M, NARDI S. 2013. Humic substance: Relationship between structure and activity. Deeper information suggests univocal findings [J]. Journal of Geochemical Exploration, 129:57-63.
PAGE S E, ARNOLD W A, MCNEILL K. 2011. Assessing the contribution of free hydroxyl radical in organic matter-sensitized photohydroxylation reactions [J]. Environmental Science &Technology, 45: 2818-2825.
POERSCHMANN J, TROMMLER U, NYPLOVA P, et al. 2008.Complexation-flocculation of organic contaminants by the application of oxyhumolite-based humic organic matter [J]. Chemosphere, 70:1228-1237.
POLUBESOVA T, CHEFETZ B. 2014. DOM-Affected Transformation of Contaminants on Mineral Surfaces: A Review [J]. Critical Reviews in Environmental Science & Technology, 44:223-254.
REMINGTON S, KRUSCHE A, RICHEY J. 2011. Effects of DOM photochemistry on bacterial metabolism and CO2 evasion during falling water in a humic and a whitewater river in the Brazilian Amazon [J]. Biogeochemistry, 105:185-200.
ROSSEL PE, VOHATALO A V, WITT M, et al. 2013. Molecular composition of dissolved organic matter from a wetland plant (Juncus effusus) after photochemical and microbial decomposition (1.25 yr):Common features with deep sea dissolved organic matter [J]. Organic Geochemistry, 60:62-71.
SCHMITT-KOPPLIN P, HERTKORN N, SCHULTEN H R, et al. 1998.Structure changes in a Dissolved Soil Humic Acid during Photochemical Degradation Processes under O2and N2Atmosphere [J].Environmental Science & Technology, 32:2531-2541.
SHINDE S S, BHOSALE C H, RAJPURE K Y. 2012. Hydroxyl radical’s role in the remediation of wastewater [J]. Journal of Photochemistry Photobiology B, 116:66-74.
SWAN C M, NELSON N B, SIEGEL D A, et al. 2012. The effect of surface irradiance on the absorption spectrum of chromophoric dissolved organic matter in the global ocean [J]. Deep Sea Research Part I:Oceanographic Research Papers, 63:52-64.
TANG W W, ZENG G M, GONG J L, et al. 2013. Impact of humic/fulvic acid on the removal of heavy metals from aqueous solutions using nanomaterials: A review [J]. Science Total Environment,468-469C:1014-1027.
THORN K A, YOUNGER S J, COX L G. 2010. Order of functionality loss during photodegradation of aquatic humic substances [J]. Journal of environmental quality, 39:1416-1428.
VAHATALO A, ZEPP R G. 2005. Photochemical mineralization of dissolved organic nitrogen to ammonium in the Baltic Sea [J].Environmental Science & Technology, 39:6985-6992.
WINTER A R, FISH T A, PLAYLE R C, et al. 2007. Photodegradation of natural organic matter from diverse freshwater sources [J]. Aquatic Toxicology, 84:215-222.
YANG C, ZENG Q, YANG Y, et al. 2014. The synthesis of humic acids graft copolymer and its adsorption for organic pesticides [J]. Journal of Industrial and Engineering Chemistry, 20:1133-1139.
曾宪成, 成绍鑫. 2002. 腐殖酸的主要类别 [J]. 腐殖酸, 4(2) :4-10.
陈蕾, 超峰, 王郑, 等. 2013. 天然有机质对环境污染物的转化过程的介导作用 [J]. 生态环境学报, 22(7):1244-1249.
郭卫东, 程远月. 2008. 天然日光辐照下河口区 CDOM 的光化学降解[J]. 环境科学, 29(6):1463-1468.
韩宇超, 郭卫东. 2008. 河口区有色溶解有机物(CDOM)三维荧光光谱的影响因素 [J]. 环境科学学报, 28(8):1646-1653.
李恭臣, 夏星辉, 周追, 等. 2008. 富里酸在水体多环芳烃光化学降解中的作用 [J]. 环境科学学报, 28(8):1604-1611.
楼涛, 汪学军, 王士财. 2007. 光化学降解黄腐酸及其对黄腐酸-苯并芘结合性质的影响 [J]. 地球化学, 36(4):363-367.
楼涛, 汪学军, 徐绍辉, 等. 2007. Suwannee河腐植酸光化学生成溶解无机碳的研究 [J]. 感光科学与光化学, 25(6):431-434.
楼涛, 汪学军, 徐绍辉, 等. 2008. Suwannee河黄腐酸光化学生成溶解无机碳的研究 [J]. 安全与环境学报, 8(1):15-17.
汪学军, 楼涛, 徐绍辉. 2009. 土壤中胡敏酸的光化学降解及其对苯并芘结合性质的影响 [J]. 土壤, 41(2):269-273.
汪学军, 楼涛, 徐绍辉. 2010. 腐殖酸的光化学降解及对铅结合性质的影响 [J]. 环境科学与技术, 33(12F):119-121.
王新颖, 孙霞, 张耀斌, 等. 2012. 腐殖酸和铁对阿特拉津光降解影响的研究 [J]. 环境工程学报, 6(1):81-86.
许中坚, 刘广深, 刘维屏. 2003. 土壤中溶解性有机质的环境特性与行为 [J]. 环境化学, 22(5):427-433.
