不同酸掺杂聚吡咯对酸性红G的吸附性能
2014-07-05张瑜苏翔周远涛李晶晶冯江涛延卫
张瑜,苏翔,周远涛,李晶晶,冯江涛,延卫
(1西安交通大学能源与动力工程学院,陕西 西安 710049;2西安创业水务有限公司,陕西 西安 710068)
不同酸掺杂聚吡咯对酸性红G的吸附性能
张瑜1,苏翔1,周远涛2,李晶晶1,冯江涛1,延卫1
(1西安交通大学能源与动力工程学院,陕西 西安 710049;2西安创业水务有限公司,陕西 西安 710068)
由于掺杂态的聚吡咯导电性能有大幅度的提高,通过质子酸掺杂机制,不同酸掺杂的聚吡咯吸附性可能会有所改善。本文首先用化学氧化法合成了不同酸(盐酸、硝酸、硫酸)掺杂的聚吡咯和未掺杂的聚吡咯,并对制得样品特性进行了扫描电子显微镜(SEM)、傅里叶转换红外光谱(FT-IR)、比表面积分析(BET)、Zeta电位测试,对测定结果进行比较分析;同时考察不同酸掺杂对聚吡咯吸附酸性红G的影响,在最适宜的pH值条件下进行了吸附动力学研究,结果表明吸附过程符合准二级动力学方程;并在同样pH值条件下进行了热力学实验,结果表明吸附过程更倾向于Langmuir吸附等温式,且线性相关系数均在0.99以上,热力学实验参数计算表明样品对酸性红G的吸附是一个自发过程。
聚吡咯;吸附;掺杂;酸性红G
吸附作为一种常用的化工操作单元,在处理环境污染物的过程中也经常被用到,并且选择适当的吸附剂往往可以得到意想不到的处理效果[1-2]。随着环境标准的不断提高,常规吸附剂逐渐难以满足处理的要求。目前不断有新型的吸附剂被开发和应用到水体或大气污染物的吸附处理中,并得到了较好的效果[3-5]。导电聚合物可以通过自身掺杂和脱掺杂的可逆性实现吸附和脱附过程的快速可逆进行,这为导电聚合物在吸附领域的应用提供了便利。例如,聚吡咯与二氧化钛复合吸附剂不仅对水中的有机染料具有良好的吸附去除性能[6-8],而且表现出非常好的再生性能。
研究表明,通过掺杂可以提高导电聚合物的理化性能。通过从导电聚合物分子链上移除(氧化)或添加(还原)一些电子使其性能得到提高的过程称为掺杂。在导电聚合物的掺杂中,质子酸掺杂较为常见。在质子酸掺杂过程中,掺杂剂与聚合物链间没有电荷的移动,掺杂剂的阴离子进入高分子链中,掺杂剂质子则靠近高分子链中的碳原子,并且在一定范围内电荷可以在共轭链上延展,从而导致高分子链的电荷分布改变,相当于失去电子被氧化。聚吡咯的酸掺杂一般是在吡咯单元的β位碳上发生质子化,带正电荷的质子转移到聚吡咯分子链上并延展开来,同时带负电的阴离子与聚合物分子链结合进行掺杂[9],见图1。

图1 质子酸掺杂聚吡咯结构示意图
本工作拟单独考察聚吡咯的吸附性能。通过以不同质子酸HNO3、HCl、H2SO4对聚吡咯的掺杂,来研究其吸附性能。通过样品的FTIR、BET、Zeta电位、SEM等测试手段的表征,以及所制得样品的吸附热力学和吸附动力学的初步研究,来探讨不同质子酸掺杂聚吡咯的吸附性能的优劣。
1 实验部分
1.1 实验试剂与仪器
吡咯单体(浙江台州清泉医药化工有限公司,分析纯)重蒸后充氮气置于冰箱内冷藏备用;硝酸、盐酸、硫酸均为分析纯购自北京化工厂;酸性红 G (Acid Red G,ARG),市售,工业级,使用前经重结晶;FeCl3分析纯,天津市耀华化学试剂有限责任公司。
产物的形貌采用 SEM (FESEM,Jeol,JSM-6700F,日本电子株式会社);产物的结构采用傅里叶红外光谱(FTIR,Nicolet,FT-IR6000,德国布鲁克仪器公司)进行表征;以BET比表面积测试仪(Builder SSA-4200,彼奥德电子(北京)有限公司)对所得样品的孔径和比表面积进行分析;以Malvern Zetasizer Nano ZS90型电位分析仪(英国马尔文仪器公司)对样品的Zeta电位进行表征。以紫外-可见分光光度计(Agilent 8453,美国安捷伦科技有限公司)对吸附实验过程中溶液中的染料浓度进行定性和定量测试。
1.2 实验方法
1.2.1 不同酸掺杂聚吡咯的制备
在三口烧瓶内分别加入0.1mol/L无机酸溶液30mL(未掺杂对照组,用30mL蒸馏水代替),置于5℃的恒温水浴锅中搅拌30min,再加入1.37mL吡咯(Py)单体至上述溶液,搅拌30min;接着用恒流泵以8r/min的恒速缓慢加入1.0mol/L的FeCl3溶液,反应12h以上,对反应液用真空抽滤,经多次用水反复洗涤,并将产物置于50℃恒温箱中干燥24h,研磨成粉状装袋标记备用。
1.2.2 吸附动力学研究方法
通过设计预吸附实验,确定吸附过程的最适pH值,由于在pH=4时样品吸附率较pH=2有明显上升,且酸性红G溶液的原有pH值在4~5之间,因此选择pH=4作为接下来吸附动力学和热力学实验的pH值条件。 在此基础上进行4种样品的动力学实验,并对他们的动力学过程进行相应的动力学方程拟合。拟合方程如表1所示。

表1 吸附动力学模型表达式
精确称量80mg所制得的不同酸掺杂的聚吡咯样品于大试管中,加入40mL质量浓度为10mg/L的酸性红G溶液。在室温条件下磁力搅拌,进行吸附动力学实验。于1min、3min、5min、10min、20min、40min、60min分别取样,并对样品离心,取上清液测定其吸光度,并计算吸附剂的吸附量,直至吸附反应达到平衡,以时间(t)-吸附量(qt)作图,绘制吸附动力学曲线。再分别对质量浓度为30mg/L、50mg/L的酸性红G进行相同实验。对4种样品进行了动力学实验,并对其动力学过程进行相应的动力学方程拟合。
1.2.3 吸附热力学研究方法
进行吸附热力学的实验,对其吸附的热力学过程进行两种吸附等温式模型的拟合,并根据拟合结果,确定其热力学参数。两种吸附等温式模型如表2所示。

表2 吸附等温式模型
各称取30mg某一种样品于6个大试管中,同时于6个试管中分别加入浓度分别为5mg/L、10mg/L、20mg/L、30mg/L、40mg/L、50mg/L的酸性红G溶液各15mL,然后将试管于15℃恒温条件下振荡2h,使其达到吸附平衡,随后离心取上清液,测其吸光度并记录。分别再于25℃、35℃重复上述实验。
2 结果与讨论
2.1 不同酸掺杂聚吡咯的表征
2.1.1 微观形貌
图2是3种酸掺杂与未掺杂聚吡咯的扫描电镜图(SEM)。由图2可见,4种样品都呈颗粒状堆积在一起,表现为经典的菜花状形貌。其中未掺杂样、HCl掺杂、HNO3掺杂的样品聚集在一起,并且十分紧密,只有H2SO4掺杂的聚吡咯颗粒比较分散,并且硫酸掺杂的聚吡咯样品颗粒要小一些,颗粒直径在0.5μm左右,其他3种样品的粒径都在1μm左右。显示出硫酸掺杂得到的聚吡咯与其他样品具有不同的聚集形态。
2.1.2 结构组成
不同酸掺杂聚吡咯的红外光谱如图3所示。聚吡咯的特征吸收峰都出现在光谱中。在1570cm-1和1480cm-1为吡咯环骨架的振动吸收峰[11];1295cm-1、1093和1038cm-1为=C—H面内弯曲振动吸收峰;3429cm-1为N—H伸缩振动吸收峰。1550cm-1为—NO2的振动吸收峰[12];1130cm-1为砜的振动吸收峰[12]。上述吸收峰证明合成的样品中含有少量的掺杂剂,即制得了4种不同酸掺杂的聚吡咯材料。

图2 不同酸掺杂聚吡咯SEM图
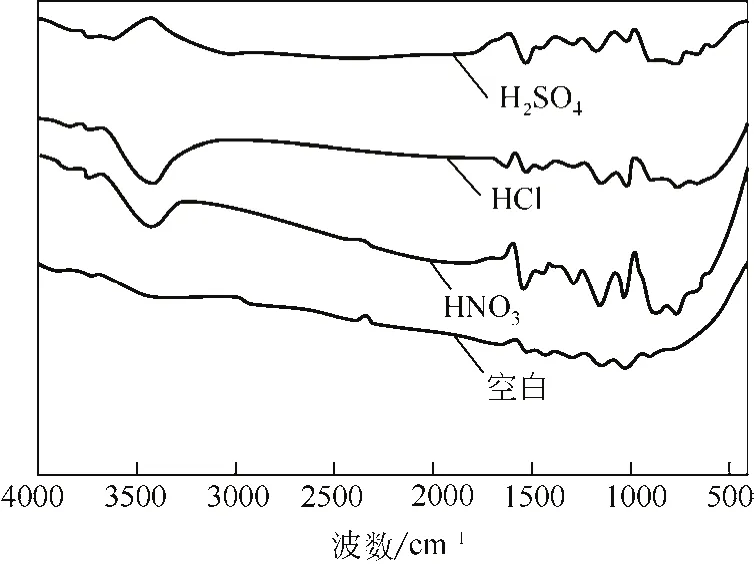
图3 不同酸掺杂聚吡咯的FT-IR图
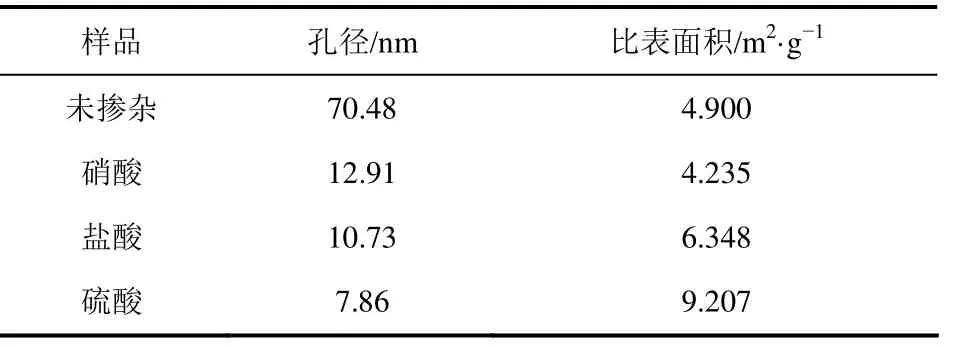
表3 不同酸掺杂聚吡咯样品的BET分析
2.1.3 孔径与比表面积
在不同酸掺杂后,样品的孔径都有所下降,由表3可知,未掺杂样的孔径为70.48nm,其他3种酸掺杂的样品孔径都明显低于未掺杂样,说明在不同酸掺杂后,样品的孔径由于质子酸掺杂导致分子空间结构上的分枝较多较密,使得原先的孔径在掺杂后减小。而比表面积里,不同酸掺杂后,除了硝酸掺杂聚吡咯比表面积有所减少外(4.235m2/g),其他样品的比表面积都有所增加,比表面积的增大说明样品在分子空间结构中的空隙更多更小,这同时验证了孔径的减小。而硝酸掺杂聚吡咯样品的孔径相较于未掺杂样减小了,比表面积同时也减小了,原因可能是硝酸掺杂后导致聚吡咯分子表面有所凸起,比较紧密,空隙较少,导致体积有所增加而表面积增加不大,最终导致比表面减小,而同时这些突起将导致原有的孔径减小。综上所述,不同酸掺杂聚吡咯都会导致聚吡咯孔径的大幅度减小,比表面积除了硝酸掺杂样品降低外,其他两种酸掺杂的样品都有所提高,其中硫酸掺杂聚吡咯的比表面积最大,达到9.207m2/g。
2.1.4 Zeta电位分析
由图4可知,在pH值小于10时,4种样品的Zeta电位均为正值,说明4种样品颗粒表面均带正电。且3种酸掺杂的聚吡咯样品相比于未掺杂样的正电荷数要高一些,而在pH值大于10之后,所有样品的Zeta电位都变成了负值。就颗粒表面所带电荷来说,在pH值达到12后,所有样品的表面电荷数绝对值都在增加,且在pH=12时达到电荷数负值绝对值的最大值,而且3种酸掺杂的聚吡咯样品颗粒表面电荷数绝对值要高于未掺杂样,在3种酸掺杂的聚吡咯样品中,又以盐酸掺杂聚吡咯样品的电荷数负值绝对值最高。
2.2 不同酸掺杂聚吡咯吸附酸性红G的动力学
2.2.1 吸附动力学过程
通过吸附动力学实验表明样品对于酸性红G的吸附可分为两个阶段。由图5可知,在刚开始与酸性红G接触的10min左右为一个快速吸附过程,这时吸附剂表面上的吸附位点较多,所以染料可以快速吸附到吸附剂表面;随后是一个缓慢达到吸附平衡的过程。随着吸附时间的延长,一是吸附剂表面的有效吸附位点减少,其次是染料的浓度也逐渐降低,染料分子的传质速率受到这两个因素的影响而降低;另外被吸附的染料分子与溶液中游离的染料分子由于所带电荷相同而相互排斥,导致后期的吸附速度减慢,最终达到平衡吸附过程。达到吸附平衡时,未掺杂样的平衡吸附量在3种浓度的酸性红G里都是最高的,原因是质子酸掺杂聚吡咯时与聚吡咯上的一些活性吸附位点结合,致使掺杂后的聚吡咯吸附位点有所减少,从而导致了最终平衡吸附量的减少。

图4 不同酸掺杂聚吡咯样品的Zeta电位测试
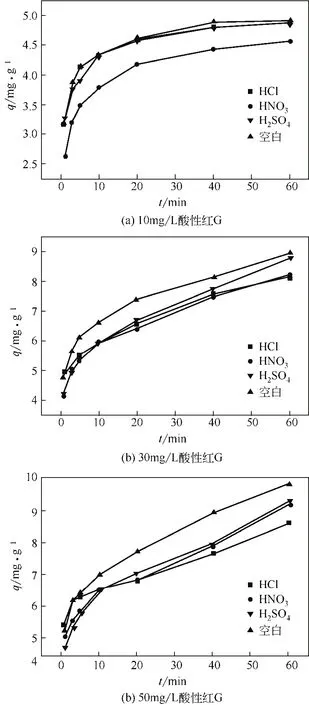
图5 不同酸掺杂聚吡咯的吸附量与时间的关系
2.2.2 吸附动力学线性拟合
在酸性红G染料浓度不同的情况下,不同吸附剂的平衡吸附量qe也是不尽相同的。由拟合结果计算出相关参数列于表4中,在酸性红G染料浓度为10mg/L时,测得的不同样品的平衡吸附量值都比较接近,当酸性红G染料的浓度变为30mg/L时,所有样品的平衡吸附量都有了一定的增大,且平衡吸附量的大小排序并没有因为所用染料浓度的增加而明显改变,依然是未掺杂样吸附量最大,达到9.124 mg/g,其他3种样品依旧与10mg/L条件下得到的大小顺序基本一致,从硫酸、盐酸到硝酸依次减小,只有盐酸与硝酸样品的平衡吸附量改变使其排序互换。当酸性红G浓度升到50mg/L时,4种样品的平衡吸附量相较于从10mg/L和30mg/L平衡吸附量有所增加,但并没有明显的变化,平衡吸附量只增加了0.44~1.60mg/g,依旧是未掺杂样的平衡吸附量最大。
而对于两种动力学方程的拟合相关性来说,在酸性红G染料浓度为10mg/L时,准二级方程的拟合相关性系数R2均大于0.99,说明在该浓度下的吸附动力学过程更符合准二级动力学方程。而未掺杂样的准二级反应k2值也是4种样品里最大的,说明未掺杂样在吸附过程中的吸附速度是最快的,其次依序是硝酸、硫酸、盐酸掺杂的样品。当酸性红G染料的浓度变为30mg/L时,依然是准二级反应更适合此浓度下的吸附动力学过程,相关系数均在0.99以上,表现出良好的相关性。对于准二级反应参数k2可以看出,未掺杂样的吸附速率依然是最快的。当酸性红G浓度升到50mg/L时,除盐酸的拟合相关性系数R2为0.9832外,其余样品的拟合相关性系数R2均在0.99以上,而对于准一级方程的拟合,相关性系数R2均未达到0.99。参看准二级反应参数k2的值发现,硝酸掺杂样品的k2值在4种样品里是最大的,为0.0507,这表明硝酸掺杂样品在吸附过程中吸附速率最快,但是其平衡吸附量在4种样品里却是最差的;未掺杂样虽然没能继续作为吸附速率最快的样品,只有0.0411,但其平衡吸附量最高。其他两种样品吸附速率要低于上述的硝酸掺杂样品和未掺杂样。在拟合方程里,准二级方程的拟合相关性要优于准一级方程的拟合相关性。
2.3 不同酸掺杂聚吡咯吸附的热力学研究
2.3.1 吸附热力学过程
不同酸掺杂聚吡咯吸附过程中酸性红G平衡浓度与平衡吸附量之间的关系如图6所示。
2.3.2 吸附热力学线性拟合
通过热力学Langmuir拟合与Freundlich拟合得出表5,3种制备的样品对于Langmuir吸附等温式拟合结果较好,相关性系数R2均在0.99以上。因此可以判断出吸附过程是一种单层吸附过程。而所制得不同酸掺杂聚吡咯样品在温度升高时吸附量都有所上升,此规律可以通过接下来对吸附过程热力学参数ΔG、ΔH、ΔS的计算来解释。
2.3.3 吸附过程热力学参数的确定
考查了288K、298K、308K 三个温度下,不同酸掺杂聚吡咯吸附的过程。热力学参数的计算见式(1)、式(2)。
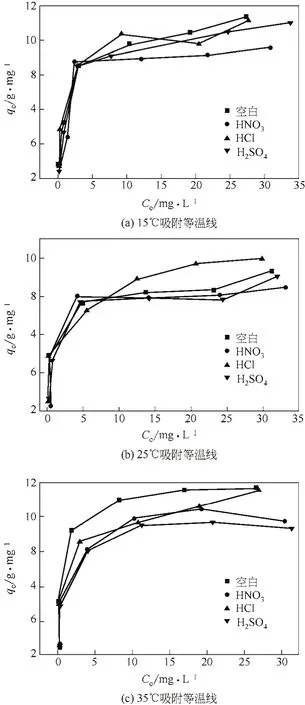
图6 不同酸掺杂聚吡咯吸附热力学关系
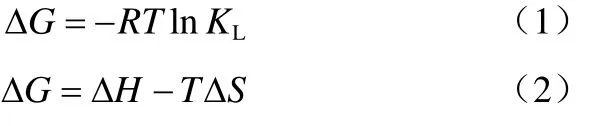
联立式(1)与式(2)得:


表4 酸性红G吸附动力学拟合参数表
由于吸附等温线符合Langmuir等温方程,按式(3)由lnKL与1000/T做线性回归计算得到ΔH的值,然后根据式(1)和式(2)求得ΔG和ΔS,如表6所示。
ΔG值表征的是反应过程中自发进行的推动力大小,其负值绝对值越大,推动力越大。一般来说,物理吸附的ΔG绝对值小于化学吸附的ΔG绝对值,前者大致在-20~0kJ/mol,后者一般在-400~-80 kJ/mol[13]。在本实验中,所有样品的ΔG值均为负值,表明所有的吸附过程都是自发进行的。且同一种样品的ΔG的绝对值随着温度的增加都在增大,说明升温可以使所有样品吸附过程的推动力增大。而且ΔG值均处于-16~-10kJ/mol内,因此属于物理吸附。ΔS为负值,说明所有样品的吸附过程均为熵减过程。这是因为在固液吸附体系中同时存在着溶质的吸附和溶剂的解吸,溶质分子的吸附是一个熵减小的过程,自由度减小,而溶剂分子的解吸是一个熵增加的过程[14]。因此,吸附过程的熵变是两者的总和。由溶剂置换理论可知水分子的解吸过程需要吸热,而溶质的吸附过程则需要放热[15]。实验中样品吸附过程的熵变为负值,可以判断出酸性红G的吸附数目要高于水分子的解吸数目,且水分子解吸吸收的热量必定大于酸性红G吸附释放的热量,最终该过程表现为吸热。这与计算得出的焓变值以及吸附等温线中平衡吸附量随温度升高而升高的趋势是一致的。通过以上热力学实验及研究表明,不同酸掺杂聚吡咯的吸附热力学过程是一个吸热、熵减和自发的过程。

表6 不同酸掺杂聚吡咯吸附热力学参数
3 结 论
以盐酸、硝酸、硫酸作为掺杂剂,以化学氧化合成法合成掺杂态的聚吡咯,并分析了制得样品的微观形貌、红外光谱、比表面积、等电点等特性。然后对所得样品吸附酸性红G进行吸附动力学和吸附热力学实验,并进行了动力学方程拟合和吸附等温式拟合,并分析了吸附过程的热力学参数。主要得出以下结论。
(1)不同酸掺杂聚吡咯的微观形貌都为经典的菜花状;掺杂后聚吡咯的孔径有所减小,但比表面积除HNO3掺杂外都有所增大,由4.900m2/g增大到硫酸掺杂样的9.207m2/g;所有样品在pH值小于10时Zeta电位都为正值,其表面均带有正电荷,pH值大于10以后均带负电荷。
(2)吸附动力学实验表明聚吡咯样品吸附过程符合准二级动力学过程。
(3)吸附热力学实验表明不同酸掺杂聚吡咯的吸附过程更符合Langmuir吸附等温式,线性相关系数均在0.99以上,而对热力学参数的计算得出不同酸掺杂聚吡咯的吸附是一个吸热、熵减和自发过程,并且酸掺杂使吸附过程的推动力有所增加。
[1] Chandra V,Kim K S. Highly selective adsorption of Hg2+by a polypyrrole–reduced graphene oxide composite[J].Chem. Commun.,2011(47):3942-3944.
[2] Zhao Z Q,Chen X,Yang Q,et al. Selective adsorption toward toxic metal ions results in selective response:Electrochemical studies on a polupyrrole/reduced graphene oxide nanocomposite[J].Chem. Commun.,2012(48):2180-2182.
[3] 高如琴,郑水林,刘月,等. 硅藻土基多孔陶瓷的制备及其对孔雀石绿的吸附和降解[J].硅酸盐学报,2008,36(1):21-25.
[4] 二乙烯三胺改性多壁碳纳米管对溶液中Au(Ⅲ)和Pb(Ⅱ)的吸附[J]. 高等学校化学学报,2012,33(3):586-590.
[5] Seo H O,Kim D H,Kim K D,et al. Adsorption and desorption of toluene on nanoporous TiO2/SiO2prepared by atomic layer deposition (AlD):Influence of TiO2thin film thickness and humidity[J].Adsorption,2013,19(6):1181-1187.
[6] Li J J,Feng J T,Yan W. Synthesis of polypyrrole-modified TiO2composite adsorbent and its adsorption performance on acid Red G[J].Journal of Applied Polymer Science, 2013,128(5):3231-3239.
[7] Li J J,Feng J T,Yan W. Excellent adsorption and desorption characteristics of polypyrrole/TiO2composite for Methylene Blue[J].Applied Surface Science,2013,279:400-408.
[8] Li J J,Zhang Q,Feng J T,et al. Synthesis of PPy-modified TiO2composite in H2SO4solution and its novel adsorption characteristics for organic dyes[J].Chemical Engineering Journal,2013,225:766-775.
[9] 冯江涛,延卫,常青,等. 掺杂剂存在对聚吡咯性能和微观形貌的影响评述[J]. 化工进展,2010,29(6):1080-1085.
[10] Ho Y S,Mckay G. Sorption of dye from aqueous solution by peat[J].Chemical Engineering Journal,1998,70:115-124.
[11] Liang W,Lei J,Martin C R. Effect of synthesis temperature on the structure,doping level and charge-transport properties of polypyrrole[J].Synth. Met.,1992,52(2):227-239.
[12] Theo K J,Wharton D,Leisel H,et al. Infrared and Raman study of interlayer anions,,andin Mg/Alhadrotalcite[J].American Mineralogist,2002,87(5-6):623-629.
[13] Lu L,He J,Wei M,et al. Uptake of chloride ion from aqueous solution by calcined layered double hydroxides:Equilibrium and kinetic studies[J].Water Research,2006,40(4):735-743.
[14] 李燕,施利文,刘志山,等.邻甲酚在类水滑石,焙烧及改性类水滑石上的吸附[J].化学学报,2012,70(6):683-690.
[15] 张莎莎.淀粉及其衍生物对一水硬铝石的抑制作用研究[D].长沙:中南大学,2011.
Adsorption properties of Acid Red G onto polypyrrole doped by various acids
ZHANG Yu1,SU Xiang1,ZHOU Yuantao2,LI Jingjing1,FENG Jiangtao1,YAN Wei1
(1School of Energy and Power Engineering,Xian Jiaotong University,Xi’an 710049,Shaanxi,China;2Xi’ an Capital Water Company Limited,Xi’an 710068,Shaanxi,China)
The conductivity of polypyrrole(PPy)will be greatly improved by doping. In addition,doping with various protonic acids may have a positive impact on the adsorption of PPy with the protonic acid doping mechanism. PPy doped with various acids(HCl,HNO3,H2SO4) and undoped PPy were synthesized by chemical polymerization. The structure and characteristics of the prepared samples were tested by scanning electron microscopy (SEM),Fourier transform infrared spectrum (FT-IR),specific surface area analysis (BET) and Zeta potential analysis. Then,the effects on the adsorption of Acid Red G onto the samples were studied. Kinetic experiments were conducted at suitable pH. The adsorption process followed the pseudo second-order kinetic equation. Also at this pH,thermodynamic experiments were conducted and data fitting indicated that the adsorption process tended to obey the Langmuir isotherm,with linear correlation coefficients more than 0.99. Thermodynamic parameters indicated that Acid Red G adsorption onto the samples was an endothermic entropy-driven spontaneous process.
polypyrrole;adsorption;doping;Acid Red G
TQ 317
A
1000-6613(2014)09-2286-07
10.3969/j.issn.1000-6613.2014.09.009
2014-01-13;修改稿日期:2014-01-28。
国家自然科学基金青年基金(21307098)及中国博士后科学基金(2013M532053)项目。
张瑜(1984—),女,硕士,助理工程师。联系人:冯江涛,博士,讲师,研究方向为环境吸附材料及导电聚合物材料。E-mail fjtes@mail.xjtu.edu.cn。
