掺杂NaCl水溶液结晶形貌的分形研究
2014-07-03李淑红欧建文
李淑红,欧建文
(1.天津工业大学,天津 300387;2.云南师范大学,云南 昆明 650500)
平衡态是指一种完全不受外界影响,内部各宏观量达到稳定的理想物理状态。现实系统绝大多数情况下会与外界有物质或能量交换,这就是非平衡态系统。自然界中,水气凝固而自发形成的雪花,流水中耗散结构形成的湍流,叶脉的自组织生长等等都是非平衡态系统。分形理论的提出,为揭示这一类复杂系统提供了有力的工具,它所描述的就是在非平衡态下形成的极其破碎而复杂,但有其自相似性或自仿射性的体系[1]。该理论提出后,人们从这个新的角度进一步了解自然界的各类复杂行为,包括自然科学和社会科学的各个领域[2-5]。
水溶液结晶因其实验装置简单,操作方便,宏观参数易于控制,对不同的实验条件能获得形态各异的分形结构,因而成为被研究较多的实验系统。赵珊茸等[6]利用快速冷却结晶,形成在远离平衡态条件下的b-石英晶体形貌,找到一种具有Sierpinski铺垫分形图案的形态。薛其彬等[7]研究含能材料NTO晶体在玻璃基片上的结晶行为,发现随着浓度升高,晶体形貌从分形结构转变为立方结构。
曾有文献单独就NaCl和Na2SO4结晶行为进行研究[8-9],指出NaCl结晶符合随机Koch曲线,是远离平衡态下的自组织现象,Na2SO4结晶的微观形貌具有分形特征,并用一维随机成核生长模型对形成机理进行探讨。NaCl和Na2SO4是两种常见的生产和生活资料,对它们水溶液结晶形貌的研究不仅能够推广人们对分形理论的理解,而且还能从分形理论中更加深刻理解水溶液的结晶行为。
本文通过改变水溶液结晶实验的浓度、溶质组分和温度等宏观参数,用偏光显微镜观察玻璃基片下溶液的结晶形貌,由分形维数分析,定量考察各宏观参数对溶液结晶形貌的影响。
1 实 验
1.1 实验样品的制备
讨论浓度对结晶形貌的影响,配制0.1、0.3、0.7和1.0 mol/L浓度的 NaCl溶液,蒸发温度设定为50℃,在烘箱中烘干结晶。讨论溶质组分的影响,保持溶液总浓度为0.1 mol/L,在NaCl溶液中按 0、1、3、5、7、9 组分添加 Na2SO4作为杂质引入,蒸发温度100℃。最后讨论温度对结晶形貌的影响,按上一实验条件在3组分的Na2SO4溶液中,改变蒸发温度25、50、80和135℃。
1.2 分形维数分析
分形维数是描述分形的主要参量,它可以定量描述分形结构的自相似程度、不规则程度或破碎程度,反映了复杂形体的不规则性[10]。随着分形理论发展起来的分形维数分析软件有很多,本文主要运用Fractalyse软件分析实验图像的分维。
2 实验结果与讨论
2.1 浓度对结晶形貌的影响
结晶形貌见图1(a)~(d)分别是 0.1、0.3、0.7和1.0 mol/L浓度下的NaCl结晶图片。从图中可以看到溶液浓度对NaCl结晶形貌影响显著。在低浓度情况下(0.1和 0.3 mol/L),NaCl结晶呈生长凌乱的束状晶体或颗粒状小晶粒,部分束状晶体在局部相互连接,小晶粒则相对独立的凝聚在某个区域。高浓度下(0.7和1.0 mol/L),NaCl呈现出明显的晶体形状,图1(c)此即为典型的NaCl立方晶体,随着浓度增加立方晶体结构遭到破坏而形成饱和的圆形颗粒。

图1 不同浓度的NaCl结晶形貌(×100)
运用Fractalyse软件分析不同浓度下NaCl结晶的分形维数,变化趋势见图2。

图2 浓度对NaCl晶体分维的影响
在0.1和0.3 mol/L 浓度下,NaCl晶体分形维数分别是1.631和1.639,从图1(a)和(b)看尽管宏观上看它们有所区别,但它们的分形维数相近,也就是说0.1和0.3 mol/L浓度下NaCl结晶的不规则程度或破碎程度相似,意味着低浓度下晶体的结晶现象有相似的动力学过程。在较高浓度的0.7和1.0 mol/L下,NaCl呈现出明显的晶体形状,甚至达到了典型的立方晶体。理论认为,在非线性非平衡态下晶体结晶是分形结构[1],而在平衡态下晶体总是得到完美结晶。由此,我们可以推断,随着蒸发的进行,低浓度下由于NaCl小晶粒远未达到结晶平衡态所需的浓度,故是一个远离平衡态的结晶行为,所以晶体结构呈现出分形特征;在较高浓度下,有足够的NaCl小晶粒团聚凝结在一起,不存在由于小晶粒不足而造成的结晶缺陷的局面,因此总能达到平衡态结晶出完整的NaCl立方晶体,但随着浓度曾高完整的NaCl立方晶体遭到破坏,成为饱和圆鼓的形状。
2.2 杂质对结晶形貌的影响
图3(a)~(f)分别是Na2SO4杂质组分占0、1、3、5、7、9 时的 NaCl结晶图像。
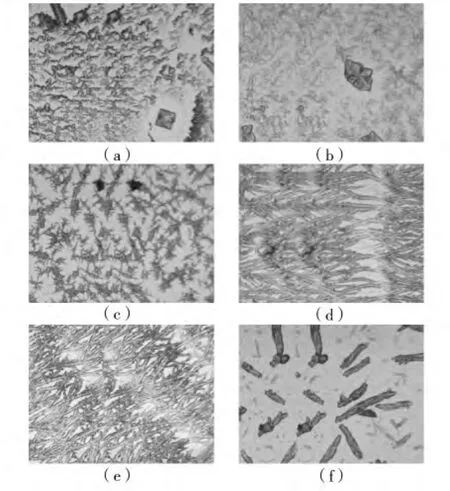
图3 不同杂质组分的NaCl结晶形貌(×100)
从图3中可以看到随着杂质组分改变,NaCl晶体的形貌发生了巨大变化,呈现出一定渐变趋势,从一开始的以NaCl晶体为主导的云雾状结晶形貌[8]渐变为NaCl晶体和Na2SO4晶体相互作用的树状结晶形貌,最后变为以Na2SO4晶体起主要作用的束状形貌[9]。
对结晶形貌进行分维分析,以分维做纵坐标,杂质Na2SO4所占组分做横坐标,绘制分维变化曲线图,见图4。
图4可以直观地看到,纯NaCl晶体的分维是1.817,加入Na2SO4杂质后晶体形貌的分维轻微下降,这是由于纯NaCl结晶过程受外来杂质Na2SO4影响,两种结晶过程叠加,导致纯NaCl结晶作用减小,分形维数降低。另外,我们实验还给出纯Na2SO4结晶分维1.858,此时可以反过来思考,视NaCl为杂质,纯Na2SO4结晶受到杂质影响,在掺杂1组分NaCl后导致纯Na2SO4结晶作用减小,分形维数降低。在横坐标组分为1和9的时候,分维值分别处于两个极小值,证明了以上推导。

图4 杂质对晶体分形维数的影响
在组分的中间过程,两种物质的结晶作用力相持不下、相互争执,达到了最大的混乱度。正如两个人打拳一样,若其中一个人特别强那么另一个人很容易就被打倒,但是,当两个人的力量相当,则可能形成拉锯战,甚至难分胜负的复杂状态[10]。从一开始的以NaCl结晶团聚生长为主导的形貌逐渐变为以Na2SO4结晶延续生长为主导的形貌。而当NaCl和Na2SO4结晶生长作用力相近时,即 Na2SO4杂质占 3、5、7组分时,晶体形貌最为混乱复杂,分维也达到最大1.935。由此得出,晶体的生长作用力是影响晶体形貌的主要因素。
2.3 温度对结晶形貌的影响
在上节我们看到图3(c)形貌最为精彩,并且近年来有研究人员用改进的DLA模型[12]对此图像进行了模拟,有理论支持,因此促使我们对这种形态进一步研究。本小节通过改变实验温度,考察温度结晶形貌的影响,其他条件仍按上节所述。拍得结晶图见图5。
图5(a)~(d)温度分别是25、50、80和135℃,其中100℃图片见图3(c)。受温度影响,结晶体形貌从一开始的 flower-like形状[13]逐渐延展,在80℃连成片后随着温度升高最终又断裂开来。值得强调的是25℃下的结晶,该结晶在纳米粉体材料的制备中常常出现,例如纳米镁铝水滑石的制备就观测到这种结晶,它们类似于菊花状,研究人员称其为flower-like结晶。由于它结构奇特,在化学催化、传感器元件、复合纳米材料等诸多领域都有应用研究[14-16]。

图5 不同温度的结晶形貌(×100)
分维随温度的变化趋势如图6,随着温度的增加,分形维数先增大后减小,在80℃时达到最大。
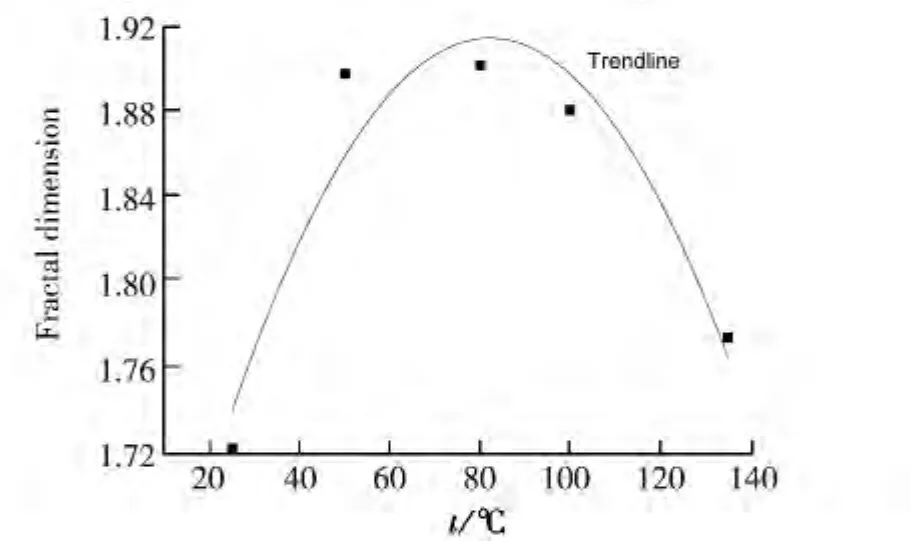
图6 温度对结晶体分形维数的影响
上节分析可知,NaCl结晶总是偏向于团聚生长,Na2SO4结晶则偏向于延续生长。
在温度较低时,不论是NaCl晶体还是Na2SO4晶体分子的热运动都比较小,没有大量的活跃分子存在,因此结晶后,NaCl仍保持着原有的团聚生长,Na2SO4保持着原有的延续生长,从图5(a)可以看到NaCl晶体团聚在一起构成了花核,Na2SO4向往延续构成了花瓣,构成了flower-like结晶。随着温度升高,NaCl晶体和Na2SO4晶体的分子热运动剧烈起来,两种粒子有很大的动能破坏原有的flower-like形状,但还不足以挣脱其束缚,因此晶体还相对独立地存在于某个区域,但晶体边缘已经开始相互连接。当温度达到135℃时,分子热运动更加剧烈,粒子有足够动能挣脱flower-like晶体的束缚,从而断裂成不规则束状晶体,随机遍布于整个显微镜视场。
3 结 论
分析浓度对NaCl结晶形貌的影响,指出在非平衡态下的结晶形貌是分形结构,而平衡态下能得到完美的结晶。浓度低,提供的小晶粒不足,远未达到结晶平衡态所需的浓度,晶体结构呈分形特征;浓度过高,完整晶体遭破坏,形成饱和圆鼓状;达到平衡态时,得到完整的立方晶体。
逐步改变杂质组分,指出晶体的生长作用力是影响结晶形貌的主要因素。从以NaCl结晶团聚生长为主导的形貌逐渐转化为以Na2SO4结晶延续生长为主导的形貌;在结晶生长作用力相近时,晶体形貌最为复杂混乱,分维达到最大。
通过改变实验温度,指出温度较低时,分子的热运动较小,结晶后NaCl保持着原有的团聚生长Na2SO4保持着延续生长,构成flower-like结晶。随着温度升高,分子热运动剧烈,两种粒子均有很大的动能破坏低温时的flower-like形状,最终随机覆盖于载玻片上。
[1] 张济忠.分形[M].北京:清华大学出版社,1995.
[2] 员美娟,郁伯铭,郑伟,等.多孔介质中卡森流体的分形分析[J].物理学报,2011(2):410-415.
[3] 欧建文,姚金波,李淑红,等.分形理论在羊毛纱线定形中的应用[J].纺织学报,2011(5):33-37.
[4] 杨妮.汇率时间序列非线性动力学特征及组合预测研究[D].湖南大学,2008.
[5] 梁坚生,陈乐.非线性聚集生长理论的研究及其应用[J].大学物理实验,2013(1):32-35.
[6] Zhao Shan-rong,,Tan Jin,Wang Ji-yang.A den-drite with sierpinski gasket fractal morphology in matt glaze of Li AlSi O4-Si O2system.Fractals.2003.
[7] 薛其彬,黄辉,康彬,等.NTO晶体生长:从分形结构到立方结构[J].含能材料,2009(4):381-384.
[8] 欧建文,李淑红,梁小平,等.NaCl稀溶液结晶的分形形态研究[J].物理实验,2010(3):39-41.
[9] 欧建文,李淑红,李淑英,等.Na2SO4水溶液结晶形貌的分形研究[OL].中国科技论文在线,./paper.edu.cn/releasepaper/content/200909-250.
[10]辛厚文.分形理论及其应用[M].合肥:中国科学技术大学出版社,1993.
[11]刘适式,刘适达.物理学中的非线性方程[M].北京:北京大学出版社,2000.
[12]谢国锋,王德武,应纯同.改进的DLA方法模拟薄膜二维生长[J].物理学报,2005,54(5).
[13]李芳,杜雪岩,徐凯,等.花状自组装FePt纳米颗粒的制备[J].稀有金属材料与工程,2012(4):707-710.
[14]向全军,余家国.暴露{001}面TiO2纳米片分等级花状结构的制备及其光催化活性[J].催化学报,2011(4):525-531.
[15]杨永强,杜高辉,许并社.花状ZnO纳米结构的液相合成和光学性能[J].发光学报,2010(2):248-252.
[16]付乌有,曹静,李伊荇,等.类花状 ZnO-CoFe2O4复合纳米管束的制备及其电磁波吸收特性[J].物理学报,2011(6):683-690.
[17]蒋智强.二维云母界面对晶体定向生长的诱导作用研究[J].大学物理实验,2013(4):1-2.
