限进材料的制备及其应用*
——介绍一个仪器分析综合实验
2014-07-02王超展李溟卫引茂
王超展李溟 卫引茂
(西北大学合成与天然功能分子化学教育部重点实验室化学与材料科学学院 陕西西安710069)
限进材料的制备及其应用*
——介绍一个仪器分析综合实验
王超展**李溟 卫引茂
(西北大学合成与天然功能分子化学教育部重点实验室化学与材料科学学院 陕西西安710069)
介绍一个仪器分析综合实验,利用原子转移自由基聚合技术制备反相限进材料;以该材料为基础,建立牛奶中4种塑化剂的固相萃取-高效液相色谱分析方法。
仪器分析实验 限进材料 高效液相色谱 牛奶 塑化剂
随着生命科学、食品科学和环境科学等领域的发展,相关样品分析已成为分析化学非常重要的任务。目前,色谱法是复杂样品分析中最常用的方法,在生物、食品和环境分析中得到了非常广泛的应用。然而,在分析上述样品之前,必须对样品进行前处理。首先,这些样品一般都含蛋白质、核酸、腐殖酸等物质,它们会吸附在固定相表面,造成色谱柱污染甚至堵塞,严重影响分离效率和色谱柱使用寿命;其次,对于痕量和超痕量分析而言,待分析物含量可能远低于仪器检测水平,必须对其进行富集;另外,这些样品中的基质非常复杂,很容易对分析造成干扰,因此需要对样品进行净化。简单、快速、高效、绿色的样品前处理方法对于提高样品分析的准确度、精密度和分析效率具有重要意义[1]。下面结合我们的科研工作介绍一个仪器分析综合实验,该实验涉及吸附分离材料制备、生物样品前处理、高效液相色谱分析方法建立等方面的内容。整个实验过程需要130小时。
1 实验目的
(1)了解生物样品的特殊性并掌握生物样品分析的全过程。
(2)认识生物样品前处理的重要性,熟悉限进材料的原理。
(3)了解限进材料的制备方法和应用。
2 实验原理
固相萃取(SPE)技术是一种由柱色谱和液固萃取技术相结合的样品前处理技术。其基本原理与液相色谱相似,根据待分析物在溶液和吸附剂两相间的作用强度或分配能力不同,与吸附剂作用力强的或者分配系数大的物质会被优先吸附,作用力很弱的或者分配系数很小的物质作为不保留组分流出,从而实现对目标物的分离、纯化和富集。与液液萃取相比,固相萃取具有以下优点:(1)溶剂耗费小;(2)操作简单、快速;(3)易于收集目标组分;(4)可处理微量试样;(5)可在线或离线操作,可与其他仪器联用。然而,在处理生物样品时,蛋白质、腐植酸和核酸等会与待分析物同时吸附在固相萃取柱上,从而造成干扰。
限进材料是近年来生物分析中广泛采用的一类样品前处理材料,它能有效吸附小分子化合物,而排除(不吸附)蛋白质,因此能够有效去除或降低蛋白质对小分子分析的干扰。限进材料的出现极大地提高了生物样品分析的速度、准确度和重现性,并有利于分析过程自动化[1]。限进材料一般具有双层结构:内层为小分子结合层;外层为亲水性的大分子屏蔽层,多为具有抗蛋白吸附性能的二醇基亲水性聚合物[2]或蛋白质[3]。限进材料对蛋白质的排除作用就是通过亲水层的化学扩散屏障或化学扩散屏障与孔径限制的物理屏障相结合来实现的。
原子转移自由基聚合(ATRP)是近年发展起来的一种高分子合成技术,它在吸附分离材料制备方面的应用也逐渐引起了广泛关注。本实验采用ATRP技术制备反相限进材料,并用于牛奶中4种塑化剂的分析。
3 仪器与试剂
3.1 仪器
傅立叶变换红外光谱仪(布鲁克,德国),紫外-可见分光光度计(岛津,日本),高效液相色谱仪(岛津,日本),固相萃取装置(Sigma-Aldrich,美国),SinoChrome ODS-BP色谱柱(4.6mm×200mm,5μm,依利特,大连)。
3.2 试剂
HF254型薄层硅胶(青岛海洋化工厂),甲基丙烯酸环氧丙酯(上海晶纯试剂有限公司),(对-氯甲基)-苯基三氯硅烷(百灵威科技有限公司),十八烷基三氯硅烷(百灵威科技有限公司);牛血清白蛋白和溶菌酶购自西安沃尔森生物技术有限公司,葛根素(安康市天源植物提取有限公司)、对羟基苯甲醛(阿拉丁试剂)、氯雷他定、硝苯地平和地西泮购自中国药品生物制品检定所,吡啶、溴化亚铜、2,2-联二吡啶、甲苯、邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丙酯(DPrP)和邻苯二甲酸二异丁酯(DiBP)购自国药集团化学试剂有限公司,脱脂牛奶购自本地超市(使用前分别用滤纸和滤膜过滤)。
4 实验内容
4.1 反相限进材料的制备
4.1.1 硅胶活化
将薄层硅胶分别过200目和320目筛,取中间粒径硅胶。取2.0g筛分后的硅胶,加入到50mL圆底烧瓶,再加入30mL 6mol/L盐酸,超声10min。搅拌下110℃回流4h。用砂芯漏斗抽滤,并用蒸馏水洗涤至中性。120℃下真空干燥8h。
4.1.2 硅胶硅烷化
称取1.0g活化硅胶,置于50mL三颈烧瓶中,加入20mL无水甲苯,超声15min。将0.1mL对-氯甲基-苯基三氯硅烷和0.4mL十八烷基三氯硅烷溶解在5mL无水甲苯中,用滴液漏斗缓慢滴加。120℃回流搅拌24h。抽滤,依次用甲苯、甲醇、丙酮洗涤改性硅胶。60℃真空干燥8h。
4.1.3 在硅胶表面接枝聚甲基丙烯酸缩水甘油酯(pGMA)
称取0.2g硅烷化硅胶,置于50mL三口烧瓶中,加入10mL异丙醇,再加入1mL甲基丙烯酸缩水甘油酯(GMA),超声3min。通氮气30min,冷冻—抽真空—解冻—通氮气循环3次,迅速加入40mg溴化亚铜和128mg 2,2-联二吡啶。再次冷冻—抽真空—解冻—通氮气。在氮气保护下,40℃下反应24h,通入空气终止反应。抽滤,依次用异丙醇、甲醇、水、丙酮洗涤产物。将改性硅胶转移至50mL圆底烧瓶中,加入20mL 0.2mol/L EDTA溶液,60℃下络合4h,以去除吸附的铜离子。再依次用水、甲醇洗涤。60℃真空干燥8h。
4.1.4 环氧基水解
将表面接枝pGMA的改性硅胶置于50mL圆底烧瓶中,加入20mL 30%四氢呋喃水溶液,再加入2mL 0.25mol/L硫酸,60℃水解8h。依次用水、甲醇洗涤,40℃真空干燥8h,即得到反相限进材料。
4.1.5 限进材料的红外光谱表征
采用KBr压片法分别测定活化硅胶、硅烷化硅胶和反相限进材料的红外光谱图,分析并对比谱图,推断材料制备是否成功。
4.2 分析方法的建立与验证
4.2.1 HPLC条件
色谱条件如下:色谱柱:SinoChrome ODS-BP色谱柱(4.6mm×200mm,5μm);流动相:65%乙腈水溶液;流速:1mL/min;检测波长:240nm;进样体积:20μL。
4.2.2 固相萃取条件
称取200mg反相限进材料,装填于10mL空柱管中,制成固相萃取小柱。将待处理样品上样至用50mmol/L PBS(pH7.4)平衡过的固相萃取柱,用2mL 30%甲醇淋洗,再用3mL甲醇洗脱,用氮气吹干洗脱组分,将残留物溶于0.20mL 65%乙腈。图1是牛奶加标样在固相萃取前后的色谱图。可以看出,经过固相萃取后,牛奶样品中的蛋白和其他基质对塑化剂分析的干扰大大降低,同时塑化剂得到了富集,大大提高了检测灵敏度。
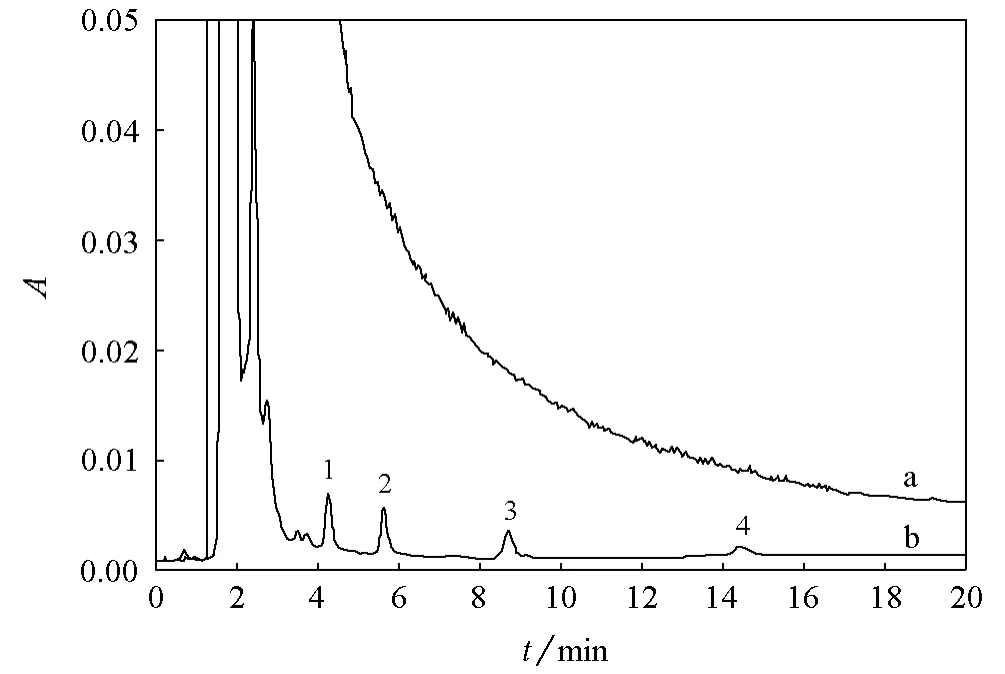
图1 反相限进材料对牛奶加标样的处理效果牛奶加标样中各种塑化剂均为15μg/L。a.固相萃取前;b.固相萃取后1.邻苯二甲酸二甲酯;2.邻苯二甲酸二乙酯;3.邻苯二甲酸二丙酯;4.邻苯二甲酸二丁酯
4.2.3 制作标准曲线
将一定体积的塑化剂混合溶液(含DMP、DEP、DPrP和DiBP质量浓度均为100mg/L)加入到70mL牛奶中,分别配制含各种塑化剂质量浓度为0.3、1.0、3.0、10.0、30.0、100和300μg/L的标准工作溶液;每个标准工作溶液经固相萃取处理后进行HPLC分析,每次测定重复3次,以质量浓度对峰面积平均值作图,分别得到DMP、DEP、DPrP和DiBP的线性方程和线性范围(表1)。

表1 分析方法的线性关系及线性范围
4.2.4 回收率和重现性
取20mL牛奶3份,分别加入20μL(样品1)、60μL(样品2)、120μL(样品3)塑化剂混合液(DMP、DEP、DPrP和DiBP的质量浓度均为100mg/L),经固相萃取处理后进行HPLC分析,每次测定重复3~6次,计算加标质量回收率和相对标准偏差(RSD),结果见表2。
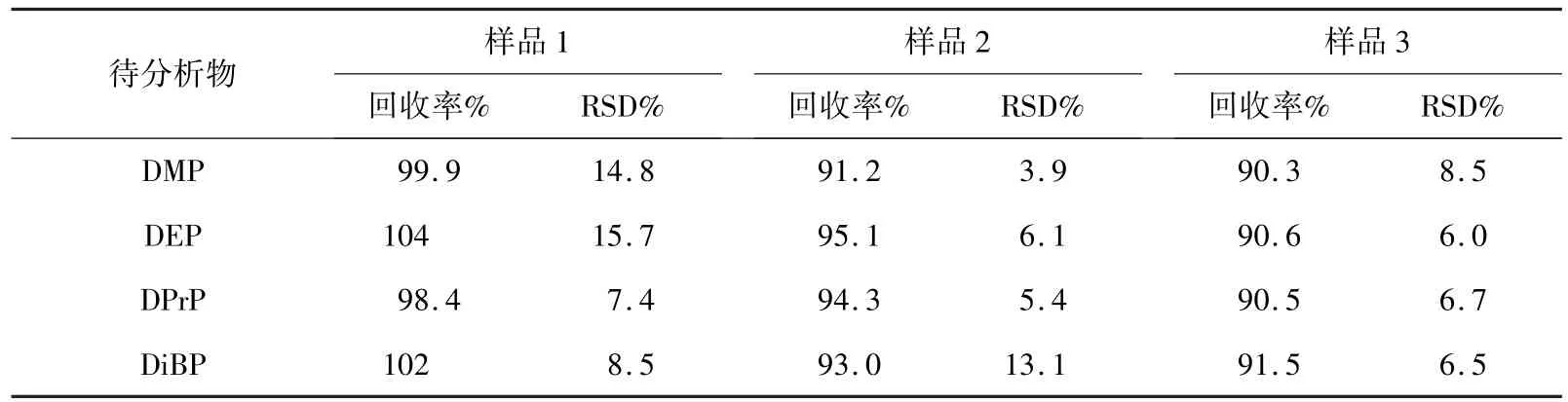
表2 分析方法的回收率和相对标准偏差(n=6)
4.2.5 最低检测限和最低定量限
最低检测限(LOD)定义为3.3(Sy/b),最低定量限(LOQ)定义为10(Sy/b)。Sy是将含各种塑化剂浓度均为10μg/L的牛奶样品平行进行6次SPE-HPLC分析后,所得峰面积的标准偏差,b是标准曲线的斜率。表3是所得各物质的检测限和定量限。

表3 检测限和定量限
5 数据处理
(1)以质量浓度对峰面积平均值作图,分别得到DMP、DEP、DPrP和DiBP的标准工作曲线,包括线性范围、线性相关系数、标准偏差。
(2)计算4种塑化剂的回收率和相对标准偏差。
(3)计算LOD和LOQ。
6 实验注意事项
(1)ATRP反应中要充分除氧。
(2)硅烷化反应中要采用无水甲苯。
(3)用液氮冷冻过程中要注意安全。
(4)实验中应采用满环进样以提高进样精密度。
(5)实验结束后要对色谱柱和色谱仪进行清洗。
7 总结
随着生命科学发展以及人们对食品安全和环境保护的关注,生物分析、食品分析和环境分析已成为分析化学中的主要任务。“限进材料的制备及其应用”作为化学相关专业的仪器分析综合实验,能够使学生通过吸附分离材料制备、样品前处理、分析条件优化、样品分析测定以及数据分析处理等环节的学习和实践,掌握复杂生物样品分析的全过程。本实验对学生进一步消化、吸收和运用课堂所学理论知识具有重要作用,有利于提高学生解决复杂问题的能力。而且,实验中的样品是与人们生活密切相关的,待分析物也是近年来各方颇为关注的污染物和非法添加物,可增强学生参与实验的积极性和主动性,调动学生的学习兴趣。
[1] Gil G C,Brennan J,Throckmorton D J,et al.JChromatog B,2011,879:1112
[2] Xu W,Su S,Jiang P,et al.JChromatog A,2010,1217(46):7198
[3] Wa C,Mallik R,Hage D S.Anal Chem,2008,80(22):8751
陕西省科技厅社发攻关项目(No.2013K13-02-10,2013-2014);西安市科技计划项目(No.CXY1344(1));西北大学本科教学质量与教学改革工程项目(No.JX12020,2013-2014)
**通讯联系人,E-mail:czwang@nwu.edu.cn
