盐酸西那卡塞固体分散体片的制备及溶出度评价
2014-06-15杨文涛姜伟化吴影琪王东凯
杨文涛,杨 磊,姜伟化,吴影琪,王 鹏,王东凯
(沈阳药科大学 药学院,辽宁 沈阳 110016)
盐酸西那卡塞固体分散体片的制备及溶出度评价
杨文涛,杨 磊,姜伟化,吴影琪,王 鹏,王东凯*
(沈阳药科大学 药学院,辽宁 沈阳 110016)
目的采用溶剂法制备盐酸西那卡塞固体分散体片并对其溶出度进行测定。方法 以PVP K30作为载体,选用微晶纤维素(MCC)进行流化床制粒,将制得的固体分散体进行压片;采用差示扫描量热法(DSC)、X-射线衍射(XRD)、红外光谱法(FTIR)以及扫描电镜(SEM)对固体分散体进行表征,并对所制备的片剂进行溶出度测定。结果 盐酸西那卡塞与PVP K30以氢键结合,药物以无定形状态高度分散于MCC表面;固体分散体片4种溶出介质中的溶出速度明显高于普通片;与市售制剂比较,相似因子f2值均大于50。结论 盐酸西那卡塞与PVP K30、MCC制备的固体分散体片有效地提高了药物的溶出速度,且方法简单,易于实现产业化。
药剂学;盐酸西那卡塞;片剂;固体分散体;溶出度
盐酸西那卡塞(cinacalcet hydrochloride)是第二代拟钙剂中第一个获FDA批准上市的药物,用于治疗进行透析的慢性肾病(chronic kidney disease)患者的继发性甲状旁腺功能亢进症[1]。美国和日本分别于2004年3月和2008年1月批准盐酸西那卡塞片上市,目前该药还没有在国内上市。文献对于盐酸西那卡塞的报道中主要集中于药物合成[2-3]、新药述评和药代动力学研究[4-6],还未见对盐酸西那卡塞制剂研究方面的报道。本试验以协和发酵麒麟株式会社生产的REGPARA®(盐酸西那卡塞片)为参比制剂,制备盐酸西那卡塞固体分散体片以获得满足溶出度要求的仿制制剂。本课题将盐酸西那卡塞与载体PVP K30共同溶于体积分数80%的乙醇溶液中,采用流化床制粒,使药物以非晶态形式吸附分散到辅料(MCC)上,达到药物在辅料中的最大分散,从而提高药物的溶出速度。盐酸西那卡塞属于BCSⅡ类药物,药物的溶出是吸收的限速过程。因此通过此方法制备的盐酸西那卡塞固体分散体片可以有效地提高药物的溶出速度,以期提高药物的生物利用度。
1 仪器与材料
赛多利斯BS 100 S电子分析天平、DPL-Ⅱ流化床多功能制粒制丸包衣机(重庆精工制药机械有限公司),754CP紫外可见分光光度计(上海光谱仪器有限公司),岛津 DSC-60自动差示扫描量热仪(日本岛津公司),布鲁克IFs 55红外光谱仪(瑞士布鲁克公司),X-射线衍射仪(日本理学株式会社),S-3400N扫描电镜 (日本日立公司),DP30A单冲压片机(北京国药龙立科技有限公司),CJY-2C片剂脆碎硬度测定仪(上海黄海药检仪器有限公司),RC-6溶出度测定仪(天津国铭医药设备有限公司)。
盐酸西那卡塞对照品(含量质量分数为99.9%,Assia Chemical Industries Ltd. Teva Tech Site,批号6969ST01-00312),盐酸西那卡塞原料药(含量质量分数为99.8%,Assia Chemical Industries Ltd. Teva Tech Site,批号696900113),盐酸西那卡塞片(规格:以西那卡塞计25 mg,协和发酵麒麟株式会社,批号CM22)。甲醇(色谱纯,天津康科德科技有限公司),其余试剂(分析纯,市售),水为去离子水。
2 方法与结果
2.1 盐酸西那卡塞溶出度测定方法的建立
2.1.1 最大吸收波长的确定
取盐酸西那卡塞对照品约10 mg,置100 mL量瓶中,加甲醇2 mL溶解后,用pH值1.2盐酸溶液稀释至刻度,所得溶液作为盐酸西那卡塞对照储备液;移取盐酸西那卡塞对照储备液1.0 mL,置10 mL量瓶中,用pH值1.2的盐酸溶液稀释至刻度。按处方比例,配制相应质量浓度的空白辅料溶液。分别进行紫外-可见光扫描。
结果表明,盐酸西那卡塞在波长221 nm有最大吸收,辅料溶液在波长221 nm处无干扰。因此,选择221 nm为盐酸西那卡塞在溶出介质中的测定波长。
2.1.2 标准曲线的建立
分别精密移取“2.1.1”条的盐酸西那卡塞对照储备液0.4、1.0、1.5、2.0和2.2 mL置于50 mL量瓶中,用pH值1.2的盐酸溶液稀释至刻度,摇匀,配制成不同质量浓度的系列标准溶液。在波长221 nm处测定吸光度,以吸光度(A)对质量浓度(ρ)进行线性回归,回归方程:A=0.159ρ+7.3×10-2,r=0.999 5,线性范围为:0.80~4.42 mg·L-1。
2.1.3 精密度试验
精密移取“2.1.1”条的盐酸西那卡塞对照储备液1.5 mL,置于50 mL量瓶中,用pH值1.2的盐酸溶液稀释至刻度,摇匀,作为供试溶液。连续测定6次,RSD为0.20%(n=6),表明仪器精密度良好。
2.1.4 溶液稳定性试验
取“2.1.3”条的供试溶液,室温放置,于0、1、2、4、6和8 h测定吸光度,供试溶液在室温放置8 h后测得吸光度均值为0.606,RSD为0.23%,表明供试溶液稳定性良好。
2.2 固体分散体片的制备
精密称取PVP K30 4.0 g、盐酸西那卡塞27.55 g,依次溶于90 mL体积分数80%的乙醇溶液中,继续搅拌30 min,作为黏合剂。精密称取MCC 155.45 g,置于流化床内;按如下工艺参数:物料温度40~45 ℃,进风温度45~50 ℃,雾化压力15 000~20 000 Pa,料液流速3.0~4.0 g·min-1,进行流化制粒、干燥。整粒后,得到固体分散体产物。向产物中加入交联羧甲基纤维素钠(CCNa)12.0 g、硬脂酸镁 1 g,混合均匀,压片。片质量为0.2 g,每片含盐酸西那卡塞27.55 mg(以西那卡塞计25 mg)。
2.3 普通片的制备
精密称取PVP K30 4.0 g,搅拌溶解于100 mL体积分数80%的乙醇溶液中,继续搅拌30 min,作为黏合剂溶液。精密称取MCC 155.45 g和盐酸西那卡塞27.55 g,置于流化床内,混合均匀。按如下工艺参数:物料温度40~45 ℃,进风温度45~50 ℃,雾化压力15 000~20 000 Pa,料液流速3.0~ 4.0 g·min-1,进行流化制粒、干燥,整粒。向上述干颗粒中加入CCNa 12.0 g、硬脂酸镁1 g,混合均匀,压片。片质量为0.2 g,每片含盐酸西那卡塞27.55 mg(以西那卡塞计25 mg)。
2.4 固体分散体的表征
2.4.1 红外光谱法(FTIR)
采用KBr压片法,在400~4 000 cm-1内对盐酸西那卡塞、MCC、PVP K30、固体分散体和处方比例的物理混合物的红外吸收光谱进行测定,结果见图1。

图 1 红外光谱图Fig. 1 Infrared spectra
由图1可知,物理混合物图谱基本为盐酸西那卡塞、PVP K30和MCC图谱的简单叠加;固体分散体中盐酸西那卡塞的仲胺NH引起的伸缩振动峰向低波数发生位移,由3 429 cm-1移向3 302 cm-1,并且仲胺NH引起的弯曲振动峰1 517 cm-1在固体分散体中消失,PVP K30在1 658 cm-1处的—C=O峰在固体分散体中强度明显减弱,并且移向1 608 cm-1。结合以上结果分析可知,固体分散体中峰强度的减弱以及峰位的红移可能是由于盐酸西那卡塞的仲胺NH与PVP K30的—C=O发生氢键结合所致。
2.4.2 X-射线衍射法(XRD)
测试条件:铜靶,加速电压:40 kV,加速电流:40 mA,以衍射角(2θ)4°·min-1,扫描范围:0~50°,将盐酸西那卡塞、固体分散体和处方比例的物理混合物分别进行X-射线衍射分析,结果见图2。

图 2 X-射线衍射图Fig. 2 X-ray diffraction spectra
由图2可知,盐酸西那卡塞在2θ为13°~25°内都有明显的晶体衍射峰,物理混合物衍射峰强度有所减弱,但特征衍射峰依然存在;固体分散体在2θ为13.9°、15.0°、15.5°、16.0°、17.9°和19°的特征衍射峰都消失。X-射线衍射结果表明,盐酸西那卡塞在固体分散体中可能以无定形状态存在。
2.4.3 差示扫描量热法(differential scanning calorimetry,DSC)
测试条件:以空铝钳锅为参比物,另一铝锅中放入约3 mg样品,升温速率10 ℃·min-1,扫描范围30~250 ℃。分别测定盐酸西那卡塞、MCC、PVP K30、固体分散体和处方比例的物理混合物的DSC图谱,结果见图3。

图 3 DSC图谱Fig. 3 DSC thermograms
由图3可知,物理混合物中的吸热峰与盐酸西那卡塞图谱中的吸热峰相比,强度与位置并未发生明显的变化,说明在物理混合物中盐酸西那卡塞与PVP K30和MCC并未发生本质上的作用,盐酸西那卡塞仍以晶体形式存在;而固体分散体中的盐酸西那卡塞的吸热峰几乎消失,由此进一步说明盐酸西那卡塞主要以无定形状态存在于固体分散体中。
2.4.4 扫描电镜法(SEM)
分别取盐酸西那卡塞、固体分散体和处方比例的物理混合物,置于S-3400N扫描电镜下观察,加速电压为5 kV,观察并记录样品图谱,结果见图4。

图 4 SE M图Fig. 4 Scanning electron micrographs
由图4可知,物理混合物中大多数盐酸西那卡塞都被包埋在辅料MCC中,而固体分散体中多数的盐酸西那卡塞都高度分散于MCC表面。
2.5 片剂在不同介质中的溶出度测定
按照《中华人民共和国药典》2010版二部附录ⅩC第二法[7],取本品,分别以pH值1.2盐酸、pH值4.5磷酸盐缓冲液、pH值6.8磷酸盐缓冲液、纯化水900 mL为溶出介质,转速为50 r·min-1,选择221 nm作为测定波长,分别于5、15、20、30、45和60 min取样10 mL,并补充等量溶出介质,样品过0.45 μm滤膜,取续滤液,分别测定市售片、固体分散体片和自制普通片在各取样点的累积溶出量。采用相似因子(f2)比较自制片与市售片的溶出曲线相似度。表1~4为市售片、固体分散体片和自制普通片在各时间点的累积溶出度数据,图5为溶出曲线图。
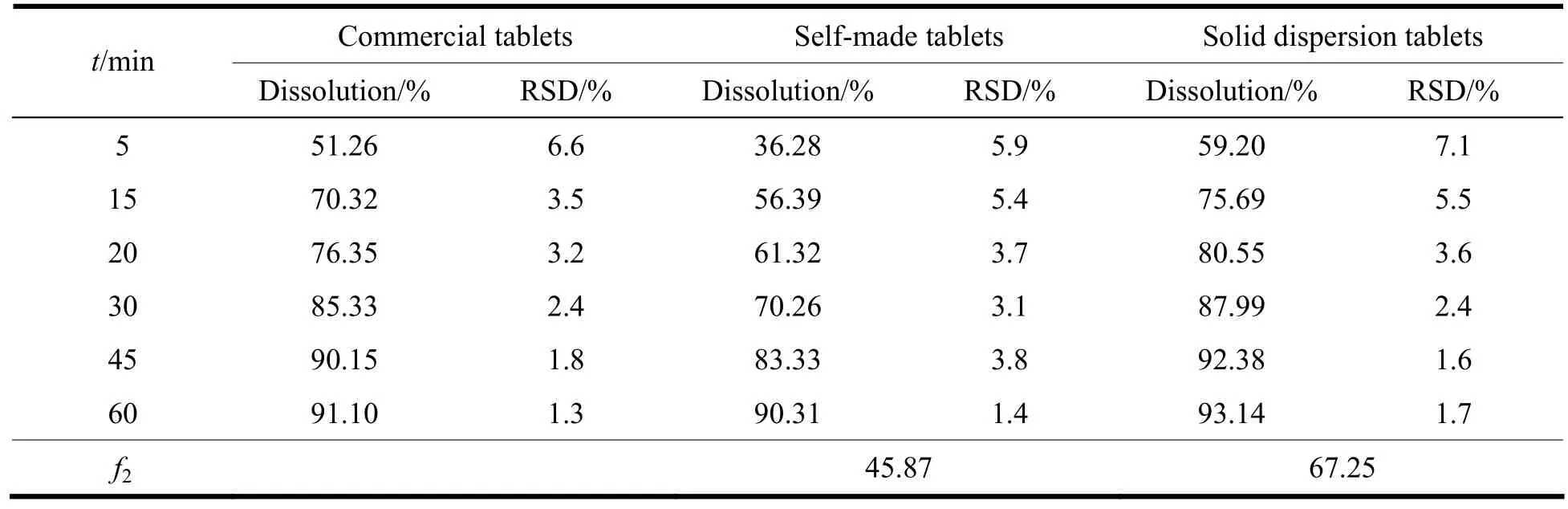
表 1 盐酸西那卡塞片在pH值1.2盐酸介质中的溶出数据Table 1 Dissolution data of cinacalcet hydrochloride tablets in pH1.2 hydrochloric acid

表 2 盐酸西那卡塞片在pH值4.5磷酸盐缓冲液中的溶出数据Table 2 Dissolution data of cinacalcet hydrochloride tablets in pH4.5 PBS

表 3 盐酸西那卡塞片在pH值6.8磷酸盐缓冲液中的溶出数据Table 3 Dissolution data of cinacalcet hydrochloride tablets in pH6.8 PBS
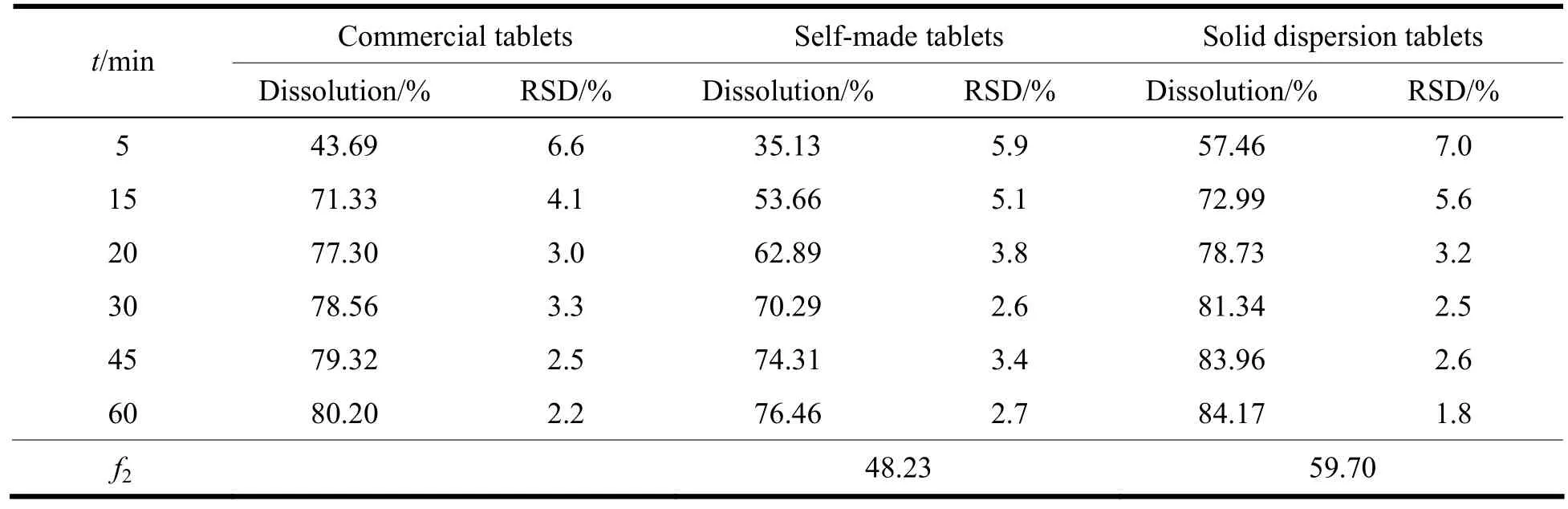
表 4 盐酸西那卡塞片在水中的溶出数据Table 4 Dissolution data of cinacalcet hydrochloride tablets in purified water
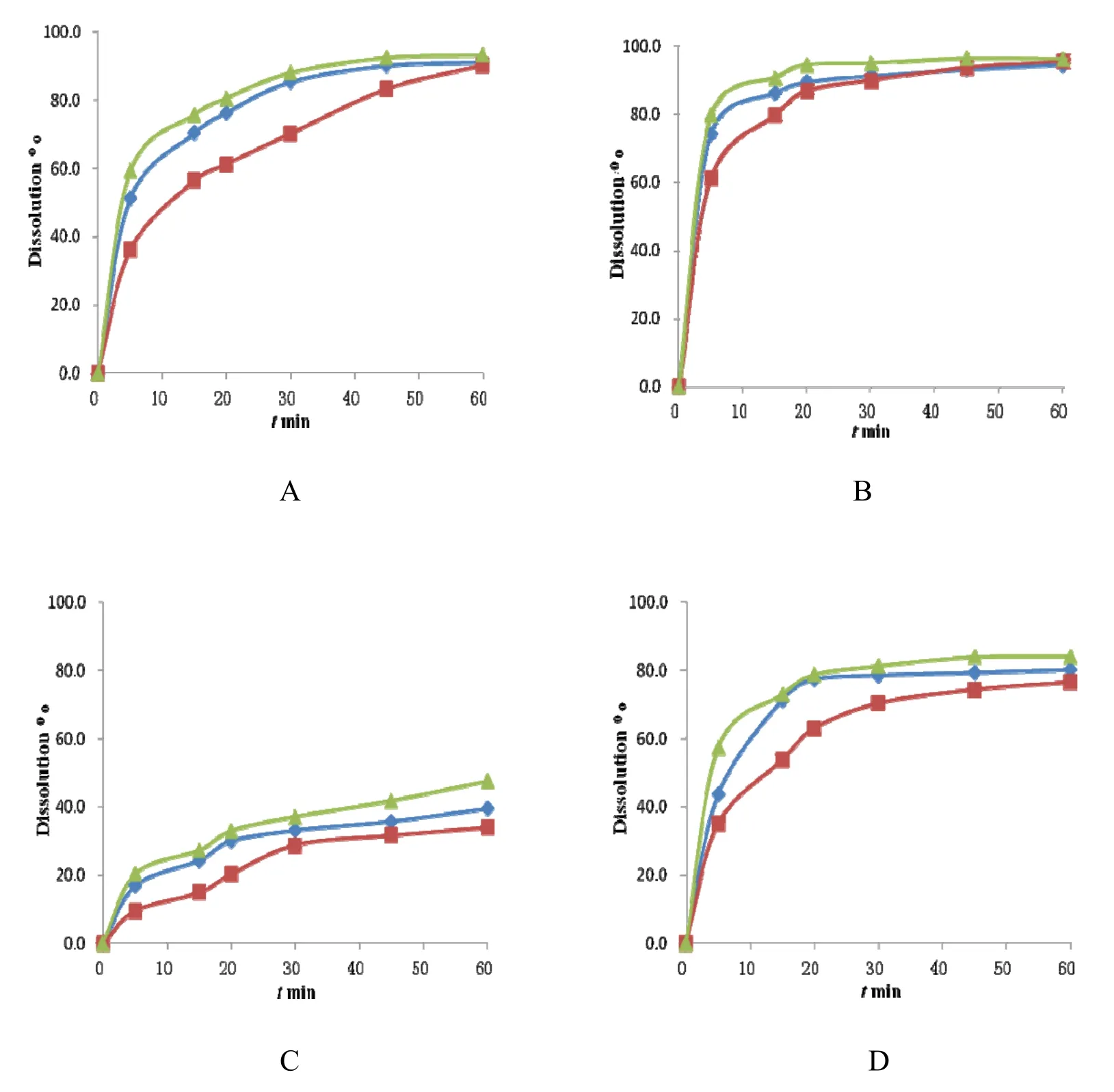
图 5 盐酸西那卡塞片溶出曲线图Fig. 5 Dissolution profiles of cinacalcet hydrochloride tablets in different pH solutions
由图5可知,固体分散体片在4种溶出介质中的溶出速度都明显高于自制普通片;固体分散体片的溶出速度也快于市售片,并且在4种介质中的溶出效果都能与市售制剂达到相似。本课题所制备的盐酸西那卡塞固体分散体片有效地提高了盐酸西那卡塞的溶出速度。
3 讨论
a. 盐酸西那卡塞为白色至类白色结晶性粉末,易溶于甲醇和乙醇。在水中的溶解度随pH值发生变化,当pH为3~5时,盐酸西那卡塞的溶解度可以达到约1.6 g·L-1;然而,在中性pH值下的溶解度低于1 mg·L-1,当pH约为1时,溶解度减小至约0.1 g·L-1。盐酸西那卡塞在水性介质中溶解度低,药物的溶出是吸收的限速过程。因此,本试验通过制备盐酸西那卡塞固体分散体片以提高药物的溶出速度,以期提高其生物利用度。
b. 药物在制剂中的存在形式会影响药物的溶解度、溶出速率及生物利用度,对于药物的溶出速率而言,无定形>结晶形。本实验将盐酸西那卡塞制成固体分散体片可以提高药物的溶出速率。从DSC和XRD的结果可知,固体分散体片中盐酸西那卡塞以无定形形式存在,提高了药物的溶出速度;SEM图则表明药物高度分散于MCC表面,使得药物溶出时的表面积增大,固体分散体片中的药物可以迅速的与溶出介质接触,从而提高药物的溶出速度。而物理混合物中大多数盐酸西那卡塞被MCC所包埋,限制了药物的溶出,因此溶出速度要远远低于固体分散体片。
c. 本课题采用溶剂法,流化床制粒制备固体分散体片,相对于传统的利用微粉化技术增加药物的溶出速度,此方法避免了在工业规模生产期间微粉化产生的健康风险,且该方法简便易行,更易于实现产业化。
[1] KOMABA H, MORIWAKI K, GOTO S, et al. Cost-effectiveness of cinacalcet hydrochloride for hemodialysis patients with severe secondary hyperparathyroidism in Japan[J]. American Journal of Kidney Diseases, 2012, 60(2): 262-271.
[2] 李林羚, 胡雪峰, 杨玉雷, 等. 盐酸西那卡塞的工艺研究[J]. 中国新药杂志, 2013, 22(7): 834-836.
[3] 胡键, 董菁, 施小新. 盐酸西那卡塞的合成[J]. 中国医药工业杂志, 2010, 41(7): 488-490.
[4] 燕宇. 西那卡塞的临床应用以及研究进展[J]. 中国血液净化, 2012, 11(8): 460-463.
[5] YANG Fen, WANG Hong-yun, ZHAO Qian, et al. Determination of cinacalcet hydrochloride in human plasma by liquid chromatography-tandem mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2012, 61: 237-241.
[6] SAIMA S C, SINGER F R, JEROME M. Cinacalcet for the treatment of primary hyperparathyroidism[J]. Metabolism Clinical and Experimental, 2008, 57(4): 517-521.
[7] 中华人民共和国药典委员会. 中华人民共和国药典:二部[M]. 北京: 化学工业出版社, 2010: 附录XC86.
Preparation of cinacalcet hydrochloride solid dispersion tablets and evaluation of the dissolution
YANG Wen-tao, YANG Lei, JIANG Wei-hua, WU Ying-qi, WANG Peng, WANG Dong-kai*
(School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110016, China)
ObjectiveTo prepare cinacalcet hydrochloride solid dispersion tablets by solvent method and evaluate the dissolution behaviors of the tablets. Method PVP K30 was used as the carrier of solid dispersion. The solution containing cinacalcet hydrochloride and PVP K30 was sprayed to the surface of MCC using fluid bed granulation method, and then this preformed solid dispersion was used to prepare cinacalcet hydrochloride tablets . Fourier transform infrared spectroscopy(FTIR), X-ray diffraction(XRD), differential scanning calorimetry(DSC) and scanning electron microscopy(SEM) were employed to characterize solid dispersion. The dissolution behavior in vitro of cinacalcet hydrochloride solid dispersion tablets was also studied. Results Cinacalcet hydrochloride interacted with PVP K30 through hydrogen bonds and cinacalcet hydrochloride was highly dispersed on the surface of MCC in the form of amorphous. Cinacalcet hydrochloride solid dispersion tablets exhibited better dissolution which was similar with that of commercial tablets. Conclusion The solid dispersion tablets of cinacalcet hydrochloride based on PVP K30 and MCC effectively improved the dissolution of cinacalcet hydrochloride and this simple method is easy to realize industrial production.
pharmaceutics; cinacalcet hydrochloride; tablet; solid dispersion; dissolution
R 94
A
(2014)02–0053–09
(本篇责任编辑:马丽丽)
2014–03–10
杨文涛(1985-),男(汉族),河北石家庄人,硕士研究生,E-mail ywtao2011@126.com;*通讯作者:王东凯(1962-),男(汉族),辽宁沈阳人,教授,博士,博士生导师,主要从事多功能纳米给药传递系统及临床药学研究,Tel. 024-23986310, E-mail wangdksy@126.com。
