益肾通络方对大鼠长期毒性研究*
2014-06-11邹晨曦
金 一,杨 智△,金 红,凌 晓,马 征,邹晨曦,蒋 娜
(1.湖南师范大学医学院,长沙 410013;2.湖南省疾病预防控制中心,长沙 410005)
益肾通络方由黄芪、制首乌、当归等中药组成,具有补肾化瘀的作用。临床及实验研究表明,对肾病综合征肾虚夹瘀证有较好的治疗效果[1~3]。为给临床用药提供安全依据,根据国家新药相关法规和技术规范[4,5],笔者对益肾通络方进行了长期毒理作用研究,现将结果报告如下。
1 材料与方法
1.1 材料
1.1.1 实验动物 SPF级Sprague Dawley(SD)大鼠由长沙市开福区东创实验动物科技服务部提供(生产许可证号SCXK(湘)2009-0012)。6~9周龄SD大鼠80只,体质量150±20 g,雌雄各半。
1.1.2 药物 益肾通络方组成药材均购自湖南中医药大学第一附属医院。采用益肾通络方流浸膏:将上述药材按比例混合后加入85℃左右的水浸没,热浸0.5 h后煎煮1 h,过滤,药渣再加85℃左右的水浸没,煎煮30 min,过滤并合并煎液。将上述煎液在65℃下浓缩至2.5 g/mL,即得到益肾通络方流浸膏。
根据《中药新药研究指南》用药量以成人的临床用量推算动物用量,根据人与大鼠用药剂量换算法计算,并根据前期药效学实验结果。具体如下:(1)益肾通络方高剂量(50 g/kg);(2)益肾通络方中剂量(25 g/kg);(3)益肾通络方低剂量(12.5 g/kg)。
1.1.3 主要仪器及试剂 瑞士Büchi R-220旋转蒸发仪,日本Olympus AU400全自动生化分析仪,美国雅培CD3700全自动血球计数仪,英国珊顿Finesse325旋转石蜡切片机,日本Olympus BX41TF系统显微镜等。Cr(Creatinine,Cr)试剂盒购自上海申能-德赛诊断技术有限公司,其他试剂盒购自上海复星长征医学科学有限公司。
1.2 方法
1.2.1 试验分组及给药 将80只SD大鼠按随机数字表法分为益肾通络方高剂量组(50.0 g/kg)、中剂量组(25.0 g/kg)、低剂量组(12.5 g/kg)和空白对照组,每组20只。单笼饲养,先于实验室饲育1周,观察各组动物体征、体质量、毛发、进食、粪便无异常后,分组按剂量每日经口灌胃给药。益肾通络方高剂量组灌服50 g/kg益肾通络方浸膏水溶液,中剂量组灌服25 g/kg浸膏水溶液,低剂量组灌服12.5 g/kg浸膏水溶液,按2 ml/100 g灌胃给药1次;空白对照组灌服等体积蒸馏水。大鼠每周称体质量1次,根据体质量情况调整药量,连续观察13周。
1.2.2 指标检测 (1)一般情况观察:单笼饲养,自由摄食饮水,试验期间观察动物的活动和生长情况,每周加食2~3次,记录给食量和剩食量,每周称1次体质量,计算食物利用率。每日观察记录精神状态、活动情况、饮食、二便、毛发光泽度、体质量等;(2)血液学指标:13周末次给药后,每组取14只,雌雄各半,12 h禁食不禁水,乙醚麻醉后舌下采血至抗凝管和非抗凝管,采集的血样于血细胞分析仪上检测红细胞或网织红细胞计数(RBC)、血红蛋白(HGB)、白细胞计数(WBC)血小板(PLT)、白细胞分类等血液学指标;(3)血液生化学指标:采集的血样于非抗凝管血分离血清后,于生化自动分析仪上测定血清中的门冬氨酸氨基转换酶(AST)、丙氨酸氨基转换酶(ALT)、碱性磷酸酶(ALP)、总蛋白(TP)、白蛋白 (ALB)、血糖 (GLU)、总胆红素(TBIL)、尿素氮 (BUN)、肌酐 (Gr)、总胆固醇(CHOL)等生化学指标;(4)病理组织学检查:采血后颈椎脱臼处死动物,对主要脏器进行全面尸检,取肝、脾、肾、睾丸等脏器称重并计算脏器系数;然后对上述主要脏器及胃、小肠、子宫、卵巢、睾丸、脑等脏器用10%甲醛固定进行常规病理学检查;(5)各组余下大鼠停药观察2周后同样处理,并检测上述指标。在对益肾通络方各剂量组动物作大体检查未发现明显病变和生化指标改变时,只进行高剂量组及空白对照组动物主要脏器的组织病理学检查,发现病变后再对较低剂量组相应器官及组织进行检查。
1.2.3 统计学方法 采用SPSS 17.0软件进行统计分析,各组数据以均数±标准差(s)表示,组间比较用t检验。
2 结果
2.1 一般情况
各组动物在灌胃给药后,由于灌胃刺激出现轻度不适,但很快恢复正常。试验期间各组大鼠无死亡,益肾通络方中、高剂量组动物出现不同程度的排便量增多,高剂量组表现明显,粪便稀软,呈大颗粒或条状,试验后期出现腹泻症状。
2.2 生长状况、进食量及食物利用率
表1、2显示,益肾通络方各剂量组动物体质量增长缓慢,从第7周开始高剂量组动物体质量与空白对照组比较,差异有统计学意义(P<0.05)。试验末高剂量组动物增重减少,总摄食量和食物利用率降低,与空白对照组比较,差异有统计学意义(P<0.05)。

表1 益肾通络方对大鼠体质量的影响
2.3 血液学和血生化检查
表3~5显示,各剂量组动物的血液学检查和各项临床血生化指标均在实验室正常范围内,给药期和恢复期与空白对照组比较,差异无统计学意义(P>0.05)。
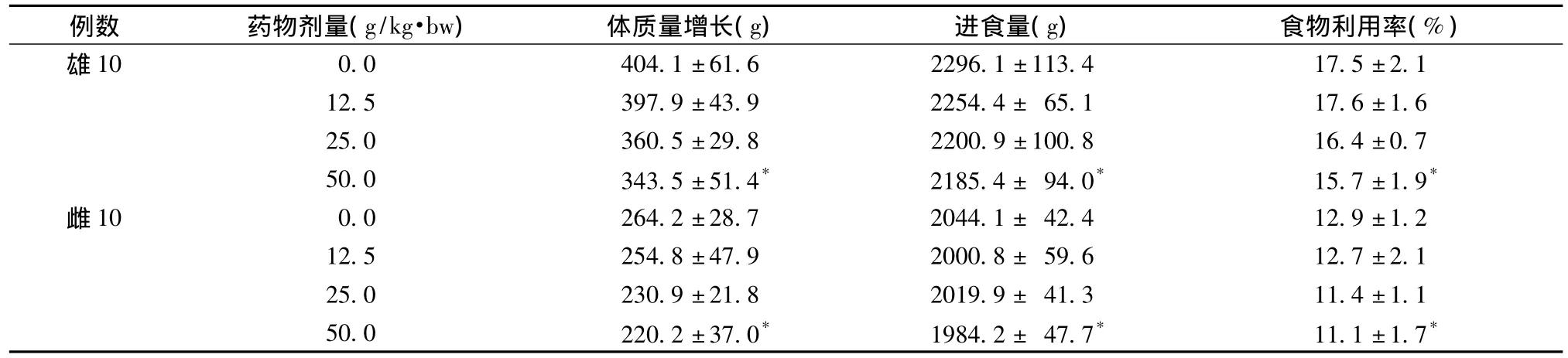
表2 益肾通络方对大鼠体质量、进食量、食物利用率的影响
2.4 脏器系数
表6显示,试验末尸检肉眼观察各脏器无明显异常并未见病变,益肾通络方各剂量组肝/体、脾/体、肾/体和睾丸/体比值给药期和恢复期与空白对照组比较,差异无统计学意义(P>0.05),所有变化在正常范围内。
2.5 病理组织学检查
大体观察:各组大鼠胸腺、心、肝、脾、肺、肾、胃、十二指肠、回肠、直肠、睾丸(或卵巢)未见异常,也未见膀胱、肝总管结石。组织学观察:对益肾通络方高剂量和空白对照组进行组织病理学检查,动物肝脏被膜完整,肝小叶结构清楚,肝细胞索排列整齐;肾脏被膜完整,肾小球、肾小管结构正常、肾间质无异常;胃肠壁各层结构清楚,黏膜上皮完整,黏膜下各层未见充血、水肿、炎性细胞浸润;脾脏被膜完整,脾小梁结构正常,红、白髓比例正常,无炎性细胞浸润及色素沉着;睾丸曲精管内各级生精细胞发育良好,间质未见水肿、出血、炎性细胞浸润;卵巢上皮与白膜正常,各级卵泡发育良好,间质未见瘀血和炎性细胞浸润。

表3 益肾通络方对大鼠血常规的影响
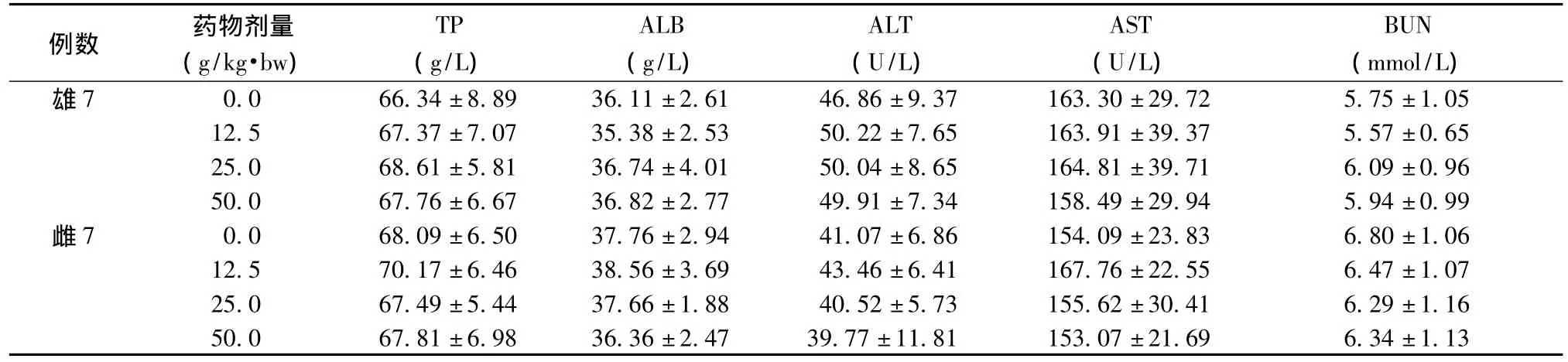
表4-1 给药期益肾通络方对大鼠生化指标的影响

表4-2 给药期益肾通络方对大鼠生化指标的影响

表5-1 第15周末益肾通络方对大鼠生化指标的影响

表5-2 第15周末益肾通络方对大鼠生化指标的影响
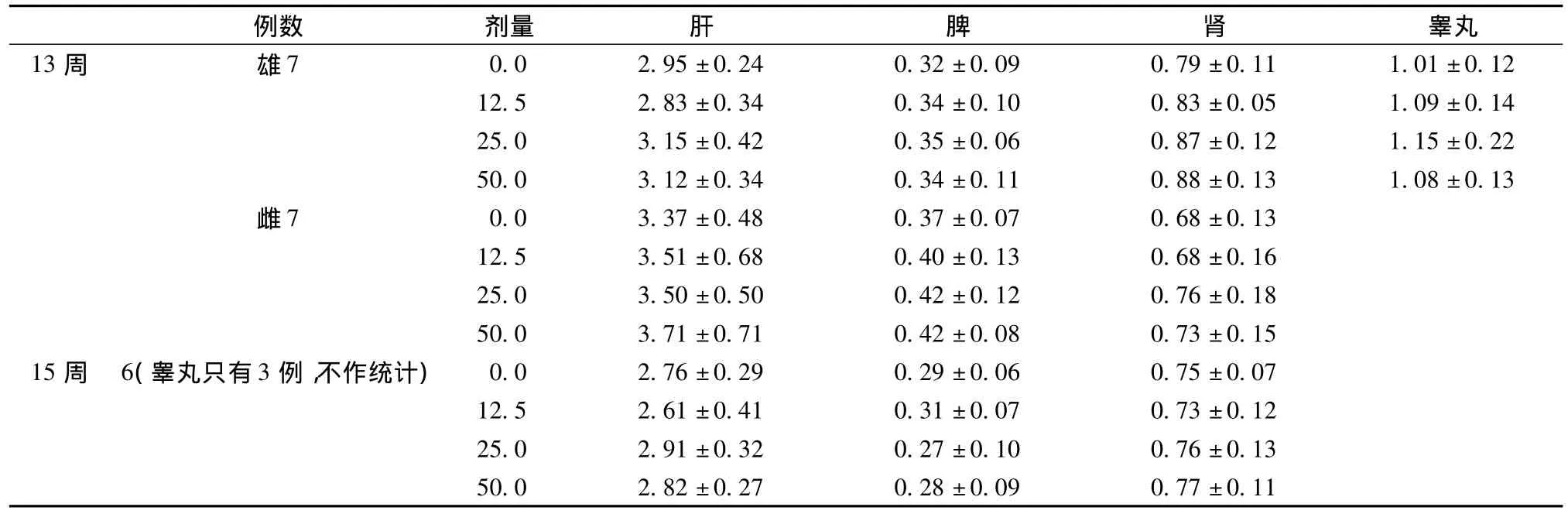
表6 益肾通络方对大鼠器官/身体质量量比影响
3 讨论
益肾通络方经临床多年运用及前期药效学研究均证实,对肾病综合征肾虚夹瘀证有明显疗效。前期实验研究还显示,该复方对脂多糖诱导的大鼠肾小球细膜增殖有明显的抑制作用[6]。本试验以益肾通络方的高、中、低3个灌胃剂量50.0、25.0、12.5 g/kg均远远高于推荐的临床给药剂量2.35 g/kg,其中高剂量组达到临床给药量的20倍,给药时间90 d,也长于临床给药时间15~30 d。
本实验显示,连续给药90 d后,益肾通络方50.0 g/kg剂量组大鼠的体质量从第7周开始与空白对照组比较显著下降,而各剂量组大鼠的血常规及血清生化指标与空白对照组比较差异无统计学意义,说明益肾通络方对大鼠的生长及各项生理指标无明显病理影响。本试验中,剖检和病理组织学观察心、肝、脾、肺、肾、胃和肠功能均正常,说明益肾通络方对大鼠脏器无明显损伤。
以上结果表明,益肾通络方按照推荐的给药剂量和给药疗程服用,其长期毒性不明显,临床应用安全。
[1]卢岳华,陈小光,金红,等.补肾通络方治疗肾病综合征的临床观察[J].湖南中医药大学学报,2007,27(6):47-49.
[2]金红,杨智,刘慧萍,等.益肾通络方对C-BSA肾病综合征大鼠模型的整体治疗作用[J].辽宁中医杂志,2008,35(10):1597-1600.
[3]金红,李雅,凌晓,等.健康大鼠服用益肾通络方后血清中阿魏酸的RP-HPLC测定[J].湖南师范大学学报(医学版),2007,4(4):9-10,13.
[4]国家食品药品监督管理局.中药、天然药物长期毒性试验技术指导原则[S].2005.
[5]陈奇.中药药理研究方法学[M].2版.北京:人民卫生出版社,2006:107-113
[6]金红,易宇新,卢岳华,等.益肾通络方对体外大鼠肾小球系膜细胞增殖的抑制作用[J].中国中医基础医学杂志,2008,14(7):505-506.
