细胞定量国际比对CCQM-P102及流式细胞技术的不确定度评定
2014-06-07陈大舟隋志伟刘新海
张 玲, 王 晶, 陈大舟, 隋志伟, 刘新海
(1.中国计量科学研究院,北京 100013; 2.中国医学科学院整形外科医院,北京 100022)
细胞定量国际比对CCQM-P102及流式细胞技术的不确定度评定
张 玲1, 王 晶1, 陈大舟1, 隋志伟1, 刘新海2
(1.中国计量科学研究院,北京 100013; 2.中国医学科学院整形外科医院,北京 100022)
对中国计量科学研究院应邀参加2010年CCQM-P102“具有特定表型的细胞定量测量比对”的测量过程、数据分析及不确定度评定进行了阐述。比对结果表明,中国计量科学研究院CD4+细胞计数测量结果与各参加国达到等效一致,成绩良好;其测量细胞平均CD4抗原值的细胞荧光强度值在经过对数转换及线性回归后,计算结果在国际比对不确定度范围内,并作为该比对提交测量不确定度的3个国家之一。对流式细胞术的测量不确定度评定进行了探讨。
计量学;流式细胞术;CD4+细胞计数;国际比对;不确定度
1 前 言
表面抗原分化簇4(CD4+)是一类位于辅助性T细胞、单核细胞、巨噬细胞和树突状细胞表面的糖蛋白。对CD4+T细胞的测量是艾滋病毒感染患者的实验室监测的重要工具[1]。2007年世卫组织公布,CD4细胞数小于200个/μL的血液细胞即诊断为获得性免疫缺陷综合症(AIDS)[2]。2005年世卫组织对CD4 T细胞测量公开声明,所有的CD4+T细胞的计数技术需要与外部质控和评估程序相一致[3]。启动和切换治疗方案的决定主要基于CD4细胞计数和临床研究结果,因此,可靠的CD4测量结果是治疗艾滋病患者的前提。
2010年CCQM生物工作组针对流式细胞法测量CD4细胞计数及人外周血单核细胞表面的CD4抗原测量的准确性和可比性,进行了代号为P102的国际比对。该比对由英国国家生物标准与控制研究所(NIBSC)、德国物理技术研究院(PTB),美国国家技术和标准研究院(NIST)联合主导,8个国家的15个实验室参加,在12种不同的仪器、平台和3种不同的计数技术上实施了该比对。
2 实验部分
2.1 仪器与试剂
试剂:Na2HPO4、NaH2PO4,分析纯,北京毅力精细化工有限公司;磷酸,MOS级,北京化学试剂公司;高纯去离子水,密理博公司MilliQ纯水仪制备,用于制备细胞悬液的缓冲液。
仪器:FC500流式细胞仪(Beckman Coulter,美国);CP324S天平(量程320 g,精度0.1 mg,Sartorius,德国),用于溶液的配制及移液器的校准;MS3型漩涡振荡器(IKA,德国),用于细胞混匀。移液器(200μL、1 000μL,Eppendorf,德国),用于移取样品,配制溶液。
比对样品:2010年5月收到样品,包括4管预标记的冻干细胞,8管细胞数量校准微球,1管荧光彩虹校准微球。按比对要求存放温度为4°C。
2.2 标准品
比对主办方提供的细胞数量校准微球(TruCount Tube),出自BD(Becton,Dickinson and Company)公司;荧光彩虹校准微球(rainbow),出自NIST。均未提供不确定度。
2.3 样品前处理
细胞冻干粉溶于1mL灭菌去离子水中,温和漩涡混匀10~30 min。该细胞已预先由异硫氰酸荧光素(FITC)标记的抗体与细胞表面CD4抗原蛋白结合、固定后冻干。该比对以FITC荧光强度代表CD4细胞表面抗原含量的多少。
3管1∶5稀释样品:取200μL溶解的细胞悬液于TruCount Tube微球校准管中,加入800 μL磷酸盐缓冲液(PBS pH 7.2~7.4),温和混匀并保证细胞和微球冻干粉充分悬浮、均匀分散于溶液中。
3管1∶20稀释样品:取50μL溶解的细胞悬液于TruCount Tube微球校准管中,加入950μL磷酸盐缓冲液(PBS pH 7.2~7.4),温和混匀并保证细胞和微球冻干粉充分悬浮、均匀分散于溶液中。
上述悬液存放于4°C,并在2h内分析。
2.4 测量方法
加2~3滴空白颗粒和荧光彩虹校准颗粒到0.5 mL磷酸缓冲液PBS中,在流式细胞仪上以图1中圈门P1的方式确保荧光最强的那群细胞都圈在检测窗里,获取至少20 000个颗粒检测事件。并按图2分析该群颗粒,FITC为异硫氰酸荧光素,将5种不同荧光强度的颗粒区分开来(P2~P6),记录每一群颗粒的荧光的几何平均值作为其等量荧光强度值E[4~6]。图中散射光和荧光信号强度均为仪器光电倍增管返回的信号强度数值,单位为1,下同。
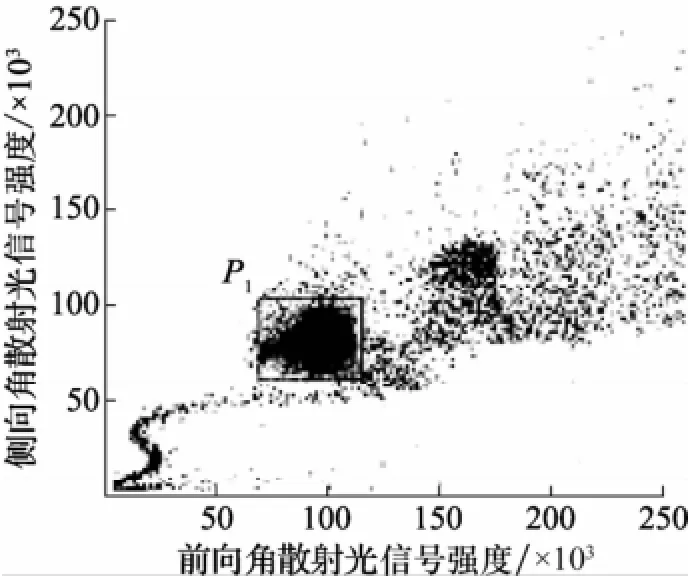
图1 荧光校准颗粒的圈门
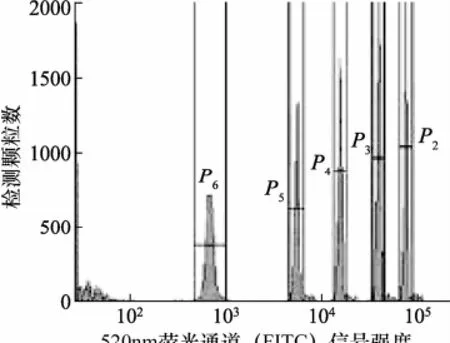
图2 荧光校准颗粒分群记录其荧光强度值
对于本文实验部分第2.3节中制备的外周血细胞样品,图3用侧向角散射光的观察方式圈出CD4+细胞P1。图4用荧光检测的方式圈出校准颗粒P2,PE为藻红蛋白荧光素。1次测量中至少获得10 000个颗粒检测事件。图5记录CD4+细胞P1的荧光强度值E(P3)。
2.5 数据分析


图3 CD4+细胞的圈门

图4 细胞数量校准颗粒的圈门
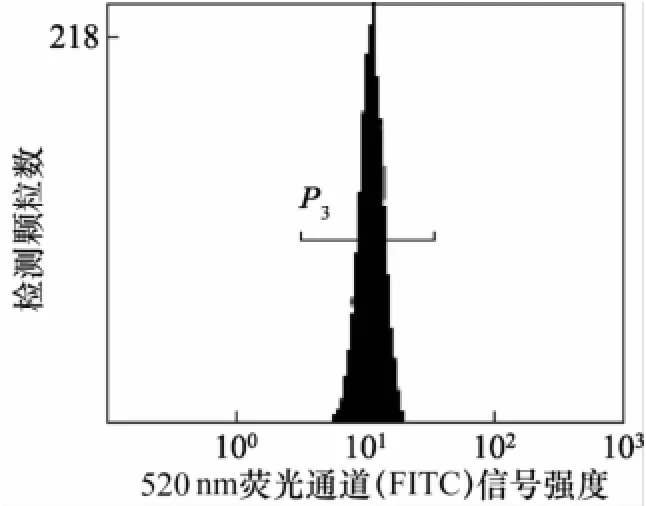
图5 CD4+细胞的荧光强度
CD4+细胞计数的计算式为式中,P1为细胞检测数;P2为颗粒检测数;B为比对主导方提供的细胞数量校准颗粒,其值为51511个/管;V为测量体积,其值为1 mL;F为稀释因子,实验中为稀释5倍。
CD4+细胞所带的CD4抗原以等量荧光素荧光值E表示,用荧光校准颗粒所得荧光值做标准曲线,在该曲线上得到CD4+细胞的E值。
3 结果与讨论
3.1 CD4+细胞计数
根据实验步骤,共分析3瓶样品,每个样品平行测量3次。并用式(1)计算细胞个数,表1为中国计量科学研究院测量结果。

表1 NIM CD4+细胞计数结果个/μL
参加比对实验室测量结果见图6,图中上下2条虚线分别为95%置信区间不确定度范围,椭圆形圈出的实验室J为中国计量科学研究院的测量结果。CCQM公布的CD4+细胞计数结果的平均值为307.3个/μL,扩展不确定度为246.7~356.8个/μL(p=95%)。中国计量科学研究院给出的测量结果为(320±28)/μL(k=2),接近中心值,且数据分散性小。
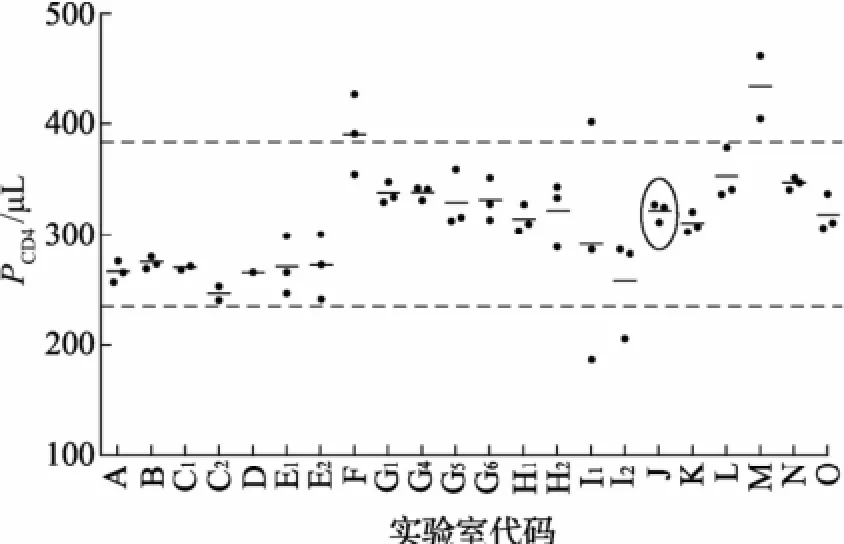
图6 CCQM-P102 CD4+细胞计数比对结果分布图
3.2 CD4+表面荧光测量
用比对主导方提供的荧光彩虹校准微球制作校准曲线,测量结果见表2。由于流式细胞仪FC500的检测器是根据荧光强度指数倍增,因此制作标准曲线应对荧光强度和测量荧光值选择指数回归,见图7(a)。为了计算方便,将该曲线进行对数变换,变成对荧光强度和测量荧光值的对数值进行线性回归,见图7(b)。

表2 荧光彩虹校准微球的测量结果

图7 荧光彩虹微球校准曲线
比对样品测量结果见表3,测量的荧光值Ec根据校准曲线计算等量荧光素荧光值E。
CCQM公布的CD4+抗原数测量结果(以荧光值E表示)为19 363,扩展不确定度为15 916~22675(p=95%)。中国计量科学研究院给出的测量结果是18372±2100(k=2),接近中心值。
4 不确定度评定
本文分别对CD4细胞计数和CD4表面抗原测量的不确定度进行了评定[7~10]。
4.1 CD4+细胞计数不确定度评定
A类不确定度:CD4+细胞计数结果见表1,根据贝塞尔公式

B类不确定度:根据第2.5节中的细胞计数计算式(1),B类不确定度有以下几个来源:(1)CD4+细胞检测数P1
测量平均值P1=12 699,厂家给出的测量重复性不大于2%,因此uB(P1)=2%。
(2)颗粒检测数P2
测量平均值P2=10 000,厂家给出的测量重复性不大于2%,因此uB(P2)=2%。
(3)校准颗粒浓度
主导实验室NIST提供的校准品浓度为51 511个/μL,但并未提供该标物的不确定度,因此uB(B)=0%。
(4)测量体积(移液器)
细胞溶液的体积200μL,根据移液器校准证书uB(V1)=1.5%,磷酸盐缓冲液PBS的体积800 μL,根据移液器校准证书uB(V2)=1.0%。
因此总测量体积为1 000μL,uB(V)=(200μL ×1.5%+800μL×1.0%)/1000μL=1.1%
(5)稀释倍数
由于采用移液器稀释,因此稀释倍数的不确定度来源于移液器,稀释倍数为1∶5的情况下,合并2次移液的不确定度为
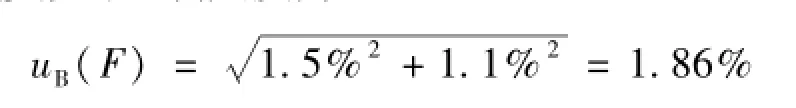
合成B类不确定度为
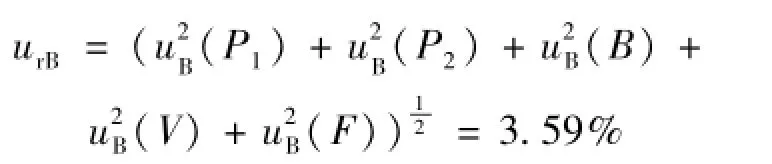
相对合成不确定度为

扩展不确定度为
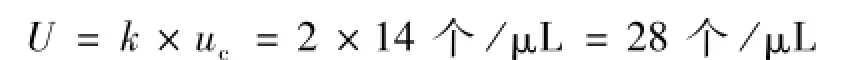
因此,CD4+细胞数为(320±28)个/μL(k=2)。
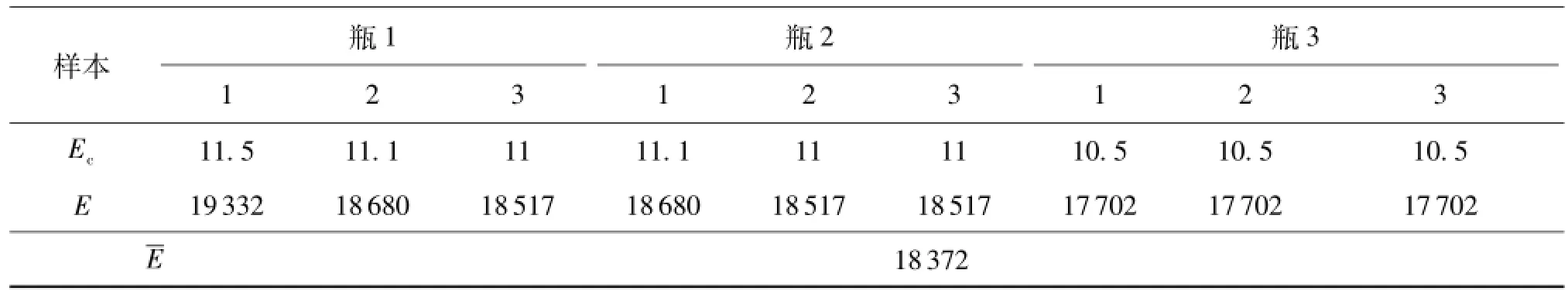
表3 CD4+表面抗原量(细胞表面等量荧光素值)
4.2 CD4抗原测量不确定度评定
A类不确定度:CD4+表面抗原量(细胞表面等量荧光素值E)的测量结果见表3,平均CD4抗原值为18 372。根据贝塞尔公式
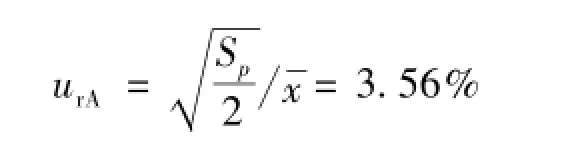
B类不确定度:
(1)校准颗粒:校准颗粒来自比对主导实验室NIST,未提供不确定度,因此ur1=0%。
(2)荧光强度:厂家给出的测量重复性不大于2%,ur2=2%。
(3)校准曲线线性回归引入的不确定度:在流式细胞仪中,荧光分子数x与测量的荧光信号强度y之间可以表示为

进行对数变换得到
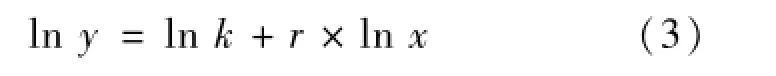
用x′表示lnx,y′表示lny,得到

评估式(4)线性拟合的不确定度[7],其中残差S为

式(4)中x′的不确定度为

根据式(6),计算u(x′)=0.041
取扩展因子k=2,U(x′)=0.041×2=0.082则 9.728≤x′≤9.892
再进行指数变换

假设x满足t分布,

校准曲线线性回归引入的相对不确定度

合成B类不确定度
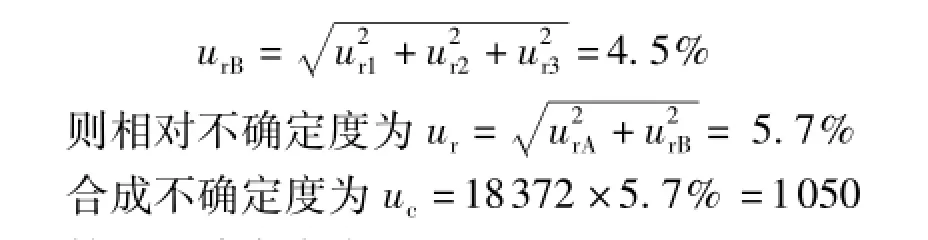
扩展不确定度为U=k×uc=2×1050=2100
每个细胞表面的CD4+抗原数量(以E表示)为18372±2100(k=2)。
5 结 论
在细胞表面荧光值的测量中,第一次测量是直接采用荧光测量值与荧光分子数的线性回归,得到的CD4表面抗原数量(E)明显偏低。通过考察该流式细胞仪器的荧光检测器相应方式,发现其检测器是指数倍增,因此改用荧光测量值与荧光分子数分别取对数后再进行线性回归,所得的测量结果接近国际比对平均值。
通过CCQM-P102具有特定表型的细胞测量比对,中国计量科学研究院验证了实际测量能力,得到较好的测量结果,参加比对的15个实验室中,仅3家实验室(包括中国NIM,英国NIBSC,美国NIST)提供了测量不确定度评定,进行了流式细胞技术测量不确定度的探索性研究。这些可为今后研制外周血细胞标准物质,将比对成果应用到量值溯源中,更好地促进临床检验标准化提供经验。
[1] Sherman G G,Galpin JS,Patel JM,etal.CD4+T cell enumeration in HIV infection with limited resources[J].JImmunolMethods,1999,222(1-2):209-217.
[2] WHO(2004).CD4+T-Cell Enumeration Technologies-Technical Information[EB].http://www.who.int/diagnostics_laboratory/publications/en/cd4_is_draft.pdf,2012-06-12.
[3] WHO(2007).WHO Case Definitions of HIV for Surveillance and Revised Clinical Staging and Immunological Classification of HIV-Related Disease in Adults and Children[EB].http://www.who.int/hiv/pub/guidelines/HIVstaging150307.pdf,2012-06-12.
[4] Pattanapanyasat K,Phuang-Ngern Y,Sukapirom K,et al.Comparison of 5 flow cytometric immunophenotyping systems for absolute CD4+T-lymphocyte counts in HIV-1-infected patients living in resource-limited settings[J].JAcquirImmuneDeficSyndr,2008,49(4):339-47.
[5] Pattanapanyasat K,Phuang-Ngern Y,Lerdwana S,etal. Evaluation of a single-platform microcapillary flow cytometer for enumeration of absolute CD4+T-lymphocyte counts in HIV-1 infected Thai patients[J].CytometryBClinCytom,2007,72(5):387-96.
[6] Dieye TN,Diaw PA,Daneau G,etal.Evaluation of a flow cytometry method for CD4 T cell enumeration based on volumetric primary CD4 gating using thermoresistant reagents[J].JImmunolMethods,2011,372(1-2):7-13.
[7] 全浩,韩永志.标准物质及其应用(第2版)[M].北京:中国标准出版社,2003.
[8] 中国实验室国家认可委员会.化学分析中的不确定度的评估指南[M].北京:中国计量出版社,2002.
[9] JJF 1059—1999测量不确定度评定与表示[S].
[10] 国家质量技术监督局计量司.测量不确定度评定与表示指南[M].北京:中国计量出版社,2000.
Research on CCQM-P102 Quantification of Cells with
Specific Phenotype and Uncertainty Evaluation in Flow Cytometry
ZHANG Ling1, WANG Jing1, CHEN Da-zhou1, SUIZhi-wei1, LIU Xin-hai2
(1.National Institute ofMetrology,Beijing 100013,China;
2.Plastic Surgery Hospital of Chinese Academy of Medical Science,Beijing100022,China)
National Institute of Metrology(NIM)was invited to participate in CCQM-P102 comparison“cells with specific phenotype quantitativemeasurement”in 2010.The results showed that,CD4+cell countmeasurements in NIM achieved equivalent consistent with the participating countries and got good results.Mean CD4 antigens per cell by fluorescence intensity values was measured by linear regression after logarithmic transformation,the value got in the uncertainties of the international comparisonm,and submitted flow cytometrymeasurement uncertainty assessment to CCQM as one of the three laboratories(NIM,China;NIBSC,UK and NIST U.S.),which was discussed.
Metrology;Flow cytometry;CD4+cell count;International comparison;Uncertainty
TB99
A
1000-1158(2014)01-0092-05
10.3969/j.issn.1000-1158.2014.01.19
2012-06-18;
2013-10-29
国家科技支撑项目(2008BAK41B03,2013BAK12B05);中国计量科学院基本业务费科研课题(AKY0915)
张玲(1980-),女,山东济南人,中国计量科学研究院助理研究员,主要从事生物化学和微生物计量标准研究。zhangling@nim.ac.cn刘新海为通讯作者。drlxh@126.com
