咸水环境下沉积物中镭的解吸特点
2014-06-07袁晓婕郭占荣马志勇
袁晓婕, 郭占荣, 刘 洁, 马志勇, 王 博
厦门大学海洋与地球学院, 福建厦门 361105
咸水环境下沉积物中镭的解吸特点
袁晓婕, 郭占荣*, 刘 洁, 马志勇, 王 博
厦门大学海洋与地球学院, 福建厦门 361105
海底沉积物向上覆水体扩散的镭是海洋水体中镭同位素的重要来源之一。为了研究沉积物中镭同位素的解吸和扩散特点, 进行了不同盐度和不同粒度条件下224Ra和226Ra解吸的模拟实验, 并通过多个时间段的沉积物培养实验获取224Ra和226Ra的扩散通量。实验结果表明: 随着水体盐度增大, 沉积物中224Ra、226Ra的解吸量随之增加, 在盐度为 25时, 解吸量基本达到最大值; 在同一咸水环境条件下, 4个粒级(2000~1000 μm、1000~500 μm、500~250 μm、250~125 μm)的沉积物的224Ra、226Ra解吸量比较接近, 粒级>2000 μm的224Ra、226Ra解吸量略高于上述4个粒级, 而粒级<125 μm的224Ra、226Ra解吸量远大于上述5个粒级; 胶州湾沉积物中224Ra和226Ra的平均扩散通量分别为0.85 Bq · m-2· d-1和0.022 Bq · m-2· d-1。
沉积物; 镭同位素; 解吸; 扩散; 咸水环境
自然界中存在4种镭同位素, 即223Ra、224Ra、226Ra和228Ra, 其半衰期分别为 11.4 d、3.6 d、 1600 a和5.7 a。它们分别属于3个天然放射系,226Ra 是238U放射系核素,224Ra和228Ra是232Th放射系核素,223Ra是235U放射系核素。镭同位素可以用来示踪海底地下水排泄(SGD)和研究不同时空尺度的海洋学过程, 诸如涡动扩散、混合速率、滞留时间, 以及用来研究N、C、P等生源要素的生物地球化学界面过程和通量等(Moore, 2000; Moore et al., 2008; Charette et al., 2001; 郭占荣等, 2008)。在许多大型的国际合作研究计划中, 如海岸带陆海相互作用(LOICZ)、全球大洋环流实验(WOCE)、海洋断面地球化学研究(GEOSECS)等计划, 同位素示踪技术均发挥了独特且重要的作用, 其中镭同位素是最具有代表性和应用非常广泛的海洋地球化学示踪剂。
海洋水体中的镭同位素来源主要有: (1)海底沉积物的输入, 包括海底沉积物中镭的扩散输入和近海表层沉积物再悬浮解吸释放的镭; (2)入海河流输入的镭, 包括河流中溶解态的镭和河流颗粒物在河口解吸释出的镭; (3)海底地下水排泄输入的镭(郭占荣等, 2011)。Moore(1981)在研究美国Chesapeake Bay的镭同位素时, 发现湾内水体中高含量的226Ra 和228Ra主要来源于海底表层沉积物的扩散及河流输入到河口的颗粒物的解吸。Beck等(2007)研究发现, 在美国纽约Jamaica Bay水体中的镭有4%~11%来源于海底沉积物的扩散输入。由此可见, 海底沉积物中的镭向上覆水体的扩散是海洋水体中镭同位素的重要来源之一, 对沉积物中镭的解吸和扩散机理进行研究能为今后更好的开展其它海洋学过程的研究提供科学依据。
镭的一个重要特性是它在水相和固相物质之间存在着可逆吸附行为, 在淡水环境吸附在固相颗粒表面上, 当固相颗粒遇到咸水时解吸到水体中(李开培等, 2011)。Gonneea等(2008)在美国马萨诸塞州Waquoit Bay进行了镭同位素吸附/解吸机制的实验研究, 结果表明: 沉积物从淡水中吸附镭的能力都很大; 延长沉积物与水接触时间不能增加镭的解吸数量, 证实了Langmuir等(1985)关于镭的吸附/解吸反应在几秒到几小时的时间内就完成的结论;升高水的盐度, 镭的解吸量也增加, 但增加的幅度取决于沉积物的化学特性; 低pH有利于镭的解吸;沉积物中Fe和Mn氧化物的存在会抑制镭的解吸。Beck等(2013)实验研究表明, 孔隙水的 pH对镭的吸附/解吸有重要影响, 其影响可以与盐度对镭的吸附/解吸影响相提并论, 在pH值2~10范围内, 镭的固液分配系数可以变化1~2个数量级。在众多控制镭解吸的因素中, 粒度大小也是一个不可忽视的因素, Webster等(1995)在数学模型中考虑了粒度(<63 μm和125~500 μm)对镭解吸的作用, Beck等(2013)采用美国弗吉尼亚海滩沙研究镭的固液分配系数(Kd), 得出粒度<63 μm和710 μm的分配系数分别是20.0 L · kg-1和0.95 L · kg-1, 从侧面反映出粒度小, 吸附力强, 被解吸的可能性就小。Gonneea 等(2008)采用沉积物表面束缚的226Ra确定3个盐度条件下的固液分配系数, 发现盐度为 5时分配系数为270~475 L · kg-1, 盐度为15时分配系数为210~445 L · kg-1,盐度为25时分配系数为210~420 L · kg-1, 也从侧面反映当盐度升高时, 镭的解吸量增大。但是, 目前还没有专门针对不同粒度以及不同盐度开展镭同位素解吸实验的报道。
镭解吸到海底沉积物的孔隙水中后, 如果忽略其它海洋驱动力(潮汐泵、波浪等)的存在, 孔隙水中的镭则主要在密度差(密度梯度)的作用下扩散到上覆海水中。Beck等(2007)将Jamaica Bay潮间带的沉积物取回实验室进行不同时间段的镭扩散培养实验, 实验结果显示沉积物中223Ra和224Ra的扩散通量分别为0.02 Bq · m-2· d-1和0.47 Bq · m-2· d-1。类似地, Garcia-Solsona等(2008)采集意大利Venice瀉湖北部盐沼的沉积物在室内进行不同时间段的培养实验, 获得沉积物中223Ra、224Ra、226Ra和228Ra的扩散通量分别为0.02 Bq · m-2· d-1、0.53 Bq · m-2· d-1、0.28 Bq · m-2· d-1和0.45 Bq · m-2· d-1。郭占荣等(2011)采集福建省九龙江河口沉积物也进行了类似的培养实验, 获得沉积物中224Ra和226Ra的扩散通量分别为0.38 Bq · m-2· d-1和0.04 Bq · m-2· d-1。以上扩散实验都是将沉积物取回实验室后放置一段时间后再开始扩散实验, 虽然放置一段时间可以消除取样过程对沉积物的扰动, 但是放置时间较长可能引起沉积物内部 pH、Eh等条件发生变化, 反过来影响镭的解吸/扩散效果。故本文在 Beck等(2007)扩散实验的基础上进行改进, 沉积物取回实验室,紧接着就开展扩散实验, 无需静置一段时间。
1 研究方法
1.1 取样
2011年 10月, 于青岛胶州湾采集了 3个沉积物样, 岩性均为粘土质粉砂, 在青岛大学实验室进行了沉积物孔隙水中镭的扩散实验。2011年12月,在厦门白城海滩低潮线附近采集了沉积物样, 用来进行不同盐度和不同粒度条件下沉积物颗粒上镭的解吸实验。
1.2 实验方法
根据前人的研究成果, 沉积物颗粒上镭的解吸受多个因素(pH、Eh、盐度、粒度、岩性、铁/锰氧化物等)控制, 所以, 本文的实验只针对盐度或粒度单一因素而设计, 实验过程中最大限度地保证其它因素是不变的, 否则, 其它因素叠加进来, 就很难分析单一因素的影响机理。
(1)镭的富集采用 MnO2纤维吸附水体中的镭,即利用虹吸方式让水体以小于 300 mL/min的流速通过MnO2纤维富集筒来富集镭(门武等, 2010)。富集完成后, 挤去锰纤维上的水分, 然后装入扩散管内, 随后进行224Ra活度测量。
(2)镭放射性活度的测量测量镭活度的仪器为中核(北京)核仪器厂生产的FD-125型氡钍仪。224Ra活度的测量采用220Rn连续射气闪烁计数法(黄奕普等, 2001)。224Ra测量完毕, 将装有MnO2纤维的扩散管两端密封起来, 放置7 d以上, 然后测量226Ra的活度。226Ra活度的测量采用222Rn直接射气闪烁计数法(谢永臻等, 1994)。
(3)不同盐度条件下镭的解吸实验沉积物样品运回实验室后放入塑料桶中, 首先将去离子水加入沉积物中搅拌, 静置 1 d后倒去上覆水, 再加入去离子水浸泡, 反复洗盐直到水中的盐度小于0.5。然后将沉积物等分为 6份, 分装在 6个塑料圆桶中,充填直径约35 cm、高度约20 cm(下同)。取盐度30左右的海水流过装有MnO2纤维的富集筒制成无镭海水, 通过往无镭海水中加去离子水配置成盐度分别为5、10、15、20、25、30的6种水样。取6个水样各15 L, 分别加入到6个桶中, 放置2 h后, 按照前面的方法用虹吸方式让沉积物上覆水缓慢流过MnO2纤维富集筒来富集镭, 并测量镭的活度。第一组实验完成后, 为了检验实验的效果, 又重复第一组实验的方法和步骤进行了第二组平行实验。
(4)不同粒度条件下镭的解吸实验沉积物样品运回实验室后, 放入烘箱内烘干。烘干后充分将胶结的颗粒打散, 用标准筛进行筛分, 将沉积物划分成 6个粒级: >2000 μm、2000~1000 μm、1000~500 μm、500~250 μm、250~125 μm以及<125 μm,然后分别放入6个塑料桶中, 加入盐度为28的无镭海水15 L, 放置2 h后, 利用前面的方法富集和测量镭。第一组实验完成后, 为了检验实验的效果,又重复第一组实验的方法和步骤进行了第二组平行实验。
(5)沉积物中镭的扩散实验3个沉积物样品运回实验室后, 分别放置于3个塑料桶中。每个沉积物样品进行6个时间段的培养, 分别是24 h、48 h、72 h、120 h、168 h、216 h。每个时段的培养过程是: 首先, 沿着桶壁缓慢加入盐度为28的无镭海水15 L, 尽量不扰动沉积物, 放置培养。当达到培养时间后, 利用前面的方法富集和测量镭。接下来, 再加入无镭海水按照上述步骤进行下一个时间段的扩散培养。
2 结果与讨论
2.1 不同盐度条件下224Ra和226Ra的解吸特点
同一种沉积物在不同盐度条件下的224Ra、226Ra的解吸实验测量结果见表1。对于224Ra, 不同盐度(5、10、15、20、25、30)所对应的沉积物镭解吸活度(平均值)分别为5.17 Bq · m-3、8.23 Bq · m-3、9.93 Bq · m-3、11.08 Bq · m-3、15.48 Bq · m-3、16.28 Bq · m-3; 对于226Ra, 不同盐度(5、10、15、20、25、30)所对应的沉积物镭解吸活度(平均值)分别为1.31 Bq · m-3、1.36 Bq · m-3、1.82 Bq · m-3、1.94 Bq · m-3、3.15 Bq · m-3、3.34 Bq · m-3。224Ra的解吸活度均高于对应的226Ra的解吸活度, 这与厦门沿海地区沉积物和岩层中富钍贫铀, 且224Ra再生速率快有关(224Ra母体228Th的半衰期为1.91 a, 而226Ra母体230Th的半衰期长达7.5×104a)。

表1 不同盐度条件下224Ra和226Ra的解吸活度Table 1 224Ra and226Ra desorption activities in water of different salinities
镭的解吸活度与盐度的关系见图1。从图1可以看出, 第一组实验和第二组实验的变化规律相似,随着盐度的逐渐增加,224Ra和226Ra解吸活度呈增加趋势, 说明盐度越高, 沉积物颗粒上解吸下来的Ra越多。其原因是随着盐度的增加, 水体的离子强度增大, 离子交换作用加强, 例如与镭属于同族的Ca2+离子可能将镭从沉积物颗粒表面上置换下来。图1还显示出, 盐度从5增加到20时,224Ra和26Ra的解吸数量增加较为缓慢, 每增加 1个盐度分别增加0.39 Bq · m-3和0.04 Bq · m-3, 但在盐度由20增加到 25时,224Ra和226Ra的解吸量增加特别明显, 每增加 1个盐度分别增加 0.88 Bq · m-3和0.24 Bq · m-3, 这与Cable等(2009)认为在盐度18左右镭的解吸最强烈的观点基本是一致的, 可是盐度由 25增加到 30时, 解吸量增幅又明显缓慢下来,每增加 1个盐度分别仅增加 0.16 Bq·m-3和
0.04 Bq·m-3, 似乎盐度达到25时, 镭同位素的解吸量达到了最大值。从理论上分析, 镭的解吸量不可能无限制地增加。从图1的发展趋势看, 初步可以判断在盐度25附近时224Ra和226Ra的解吸程度达到了最大。当然, 该结论只是针对本文的沉积物样品而言, 如果换成其它地方的沉积物, 那么镭解吸量随盐度的变化可能有所不同, 但是解吸量随盐度升高而增加的规律是确信无疑的。
如果选取两组实验的224Ra、226Ra解吸活度的平均值进行盐度与活度的相关性分析, 发现224Ra、226Ra活度与盐度之间具有很强的线性关系(224Ra: r2=0.9553;226Ra: r2=0.8216, 显著性水平P<0.01)(图2), 说明沉积物中镭同位素的解吸确实与水体的盐度存在很密切的关系, 随着盐度的增大, 镭同位素解吸量也随之增大。
2.2 不同粒度条件下224Ra和226Ra的解吸特点
通过6个粒级的沉积物在同一盐度(盐度28)水体中的培养实验, 测得224Ra和226Ra的解吸活度结果见表2。对于224Ra, 不同粒级(>2000 μm、2000~ 1000 μm、1000~500 μm、500~250 μm、250~ 125 μm以及<125 μm)所对应的沉积物颗粒上镭解吸活度(平均值)分别为 4.31 Bq·m-3、3.50 Bq·m-3、3.84 Bq·m-3、2.97 Bq·m-3、3.62 Bq·m-3、10.77 Bq·m-3;对于226Ra, 不同粒级所对应的沉积物颗粒上镭解吸活度(平均值)分别为0.75 Bq·m-3、0.39 Bq·m-3、0.51 Bq·m-3、0.56 Bq·m-3、0.66 Bq·m-3、1.49 Bq·m-3。
图3为沉积物解吸到咸水中的224Ra、226Ra活度与颗粒粒径的关系图。由图3看出,224Ra和226Ra解吸量与粒度的关系十分相似, 均呈现一定规律: 4个粒级(2000~1000 μm、1000~500 μm、500~250 μm、250~125 μm)的224Ra、226Ra解吸量非常接近; 粒级>2000 μm的224Ra、226Ra解吸量略高于上述 4个粒级, 可能是这个粒级的沉积物孔隙较大,孔隙水向上覆水体扩散通道比较通畅, 可以使较多的镭短时间内扩散到水体中; 粒级<125 μm 的224Ra、226Ra解吸活度远大于上述5个粒级, 其原因是沉积物颗粒越小, 其比表面积越大, 吸附的镭同位素越多, 因而遇到咸水解吸出来的镭同位素也越多。Beck等(2013)发现3种沉积物的比表面积与镭的固液分配系数(Kd)存在非常强的正线性相关关系(R2=0.94), 完全支持沉积物比表面积大, 其吸附镭同位素能力强的观点。

图1 224Ra、226Ra解吸活度与盐度的关系Fig. 1 Relationship between224Ra,226Ra activities and salinity

图2 224Ra、226Ra平均解吸活度与盐度的相关性Fig. 2 Correlation of224Ra,226Ra mean activities with salinity
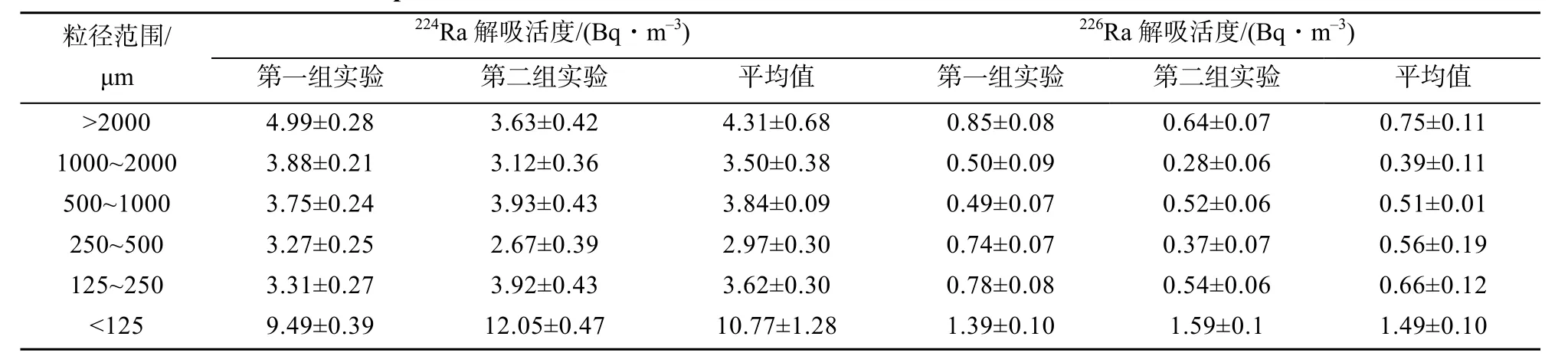
表2 不同粒级沉积物的224Ra和226Ra解吸活度Table 2 Desorption activities of224Ra and226Ra from the sediments of different size fractions
通过上述分析可知, 沉积物颗粒大小这种内因决定了镭的解吸数量的多少, 其中粒径 125 μm是一个关键的界限, 小于该界限, 沉积物解吸到咸水中的224Ra、226Ra数量明显增加(图 3)。粒级大于125 μm时, 沉积物解吸到咸水中的224Ra活度小于4.31 Bq · m-3, 解吸到咸水中的226Ra活度小于0.75 Bq · m-3; 但粒级小于125 μm时, 沉积物解吸到咸水中的224Ra活度可高达11.77 Bq · m-3, 解吸到咸水中的226Ra活度可达1.49 Bq · m-3。

图3 224Ra和226Ra解吸活度与粒径的关系Fig. 3 Relationship between224Ra,226Ra activities and particle sizes
根据沉积物的粒级划分, 小于 125 μm的颗粒还包括极细砂、粉砂(粗粉砂、细粉砂)、粘土等粒级, 由于筛分条件的限制, 没有做更小粒级沉积物的224Ra和226Ra解吸实验。在更小粒级下, 沉积物是否依然表现为粒级越小,224Ra和226Ra解吸量越大呢?从理论上分析, 粒级越小, 比表面积越大,但同时颗粒间空隙就越小, 不利于Ra的释出, 二者的综合作用结果尚不清楚, 有待于进一步的实验研究。

图4 沉积物扩散到水体中的224Ra、226Ra活度与培养时段的关系Fig. 4 224Ra and226Ra diffusive activities of sediments in relation to different incubation periods of time
2.3 沉积物中224Ra和226Ra的扩散通量
镭的吸附/解吸反应在几秒到几小时的时间内就完成(Langmuir et al., 1985; Gonneea et al., 2008),所以, 第一时段加入无镭海水进行培养, 这个时段主要表现为沉积物中原有镭同位素的解吸作用, 扩散作用不明显, 第二时段开始后, 沉积物孔隙水中镭同位素的扩散作用增强, 因为经过前一个时段的积累, 孔隙水中镭同位素浓度有所增大。沉积物样品中的镭同位素通过其母体(Th)的自然衰变而生成,生成后解吸到沉积物孔隙水中, 然后在密度差的作用下向上覆水体扩散。224Ra的再生速率快, 在2~3个半衰期内(170~260 h), 添加到上覆水体中的224Ra与水体中224Ra的衰变损失基本达到平衡, 散点连线趋近于水平。由于226Ra再生速率很慢, 致使上覆水体中的226Ra的添加十分缓慢, 在图上的反映就是散点基本上呈下降趋势(图 4), 个别散点例外, 原因尚不清楚。

表3 沉积物孔隙水中224Ra和226Ra的扩散通量Table 3 Diffusive fluxes of224Ra and226Ra from sediment samples

图5 沉积物粒度频率直方图Fig. 5 Grain size distribution of sediment samples
如果只考虑培养样上覆水体中的镭同位素的扩散添加和镭同位素的衰变损失, 那么上覆水体中的镭同位素的活度随时间的变化可以表达成如下公式(Garcia-Solsona et al., 2008):

式中, I0和It是初始时刻和t时刻上覆水体中镭的库存量(Bq), Jdiff是镭的扩散通量(Bq · m-2· d-1),λ是镭的衰变常数(h-1), Adiff是培养样品的面积(m2)。
将第一个培养时段的镭解吸活度作为初始时刻的镭库存I0, 根据理论公式(1)用拟合法来确定每个培养样的Jdiff值, 3个沉积物样品的224Ra和226Ra扩散通量见表3。3个沉积物的224Ra扩散通量相差不大, 平均值是0.85 Bq · m-2· d-1,226Ra扩散通量几乎是一样的, 平均值为0.022 Bq · m-2· d-1,226Ra的扩散通量比224Ra小一个数量级, 是由于226Ra再生速率很慢, 上覆水体中226Ra的添加十分缓慢而造成的。由此可见, 镭同位素的再生速率大小是影响其扩散通量的一个重要因素。
本文实验结果与Beck等(2007)、Garcia-Solsona 等(2008)和郭占荣等(2011)的实验结果相比较(表3),224Ra 扩散通量在一个数量级范围, 但是Garcia-Solsona等(2008)的226Ra扩散通量明显偏大, 从226Ra很慢的再生速率分析, 其扩散通量不可能和224Ra扩散通量在一个数量级上。
根据 3个沉积物样品的粒度分析(Mastersizer 2000型激光粒度分析仪测量结果), 粒度均以细粒组分为主, 定名为粘土质粉砂(图5)。3个沉积物样品粒度组成略有差异, 这是导致三者扩散通量略有不同的主要原因。
3 结论
水体盐度对沉积物中镭同位素的解吸有重要影响,224Ra和226Ra的解吸程度与水体盐度成正相关关系。针对厦门白城海滩的沉积物来说, 盐度从5增加到20,224Ra和226Ra的解吸量增幅较为缓慢,盐度从20增加到25,224Ra和226Ra的解吸量增幅有所增大, 在盐度25附近,224Ra和226Ra的解吸量基本达到最大值。
粒度大小对沉积物中镭同位素的解吸也有重要影响, 总体趋势是随着沉积物粒度变小,224Ra和226Ra的解吸量则增加, 但不是线性关系。以厦门白城海滩的沉积物为例, 在同一水环境条件下, 4个粒级(2000~1000 μm、1000~500 μm、500~250 μm、250~125 μm)的沉积物的224Ra、226Ra解吸活度比较接近; 粒级>2000 μm的224Ra、226Ra解吸活度略高于上述4个粒级, 而粒级<125 μm的224Ra、226Ra解吸活度远大于上述5个粒级。
镭同位素的再生速率大小是影响其扩散通量的一个主要因素。本文采用的3个胶州湾海底沉积物, 都属于粘土质粉砂, 粒度组成非常相似, 所以镭的扩散通量也很接近。224Ra和226Ra的扩散通量平均值分别是0.85 Bq · m-2· d-1和0.022 Bq · m-2· d-1,224Ra的扩散通量比226Ra大一个数量级。
参考文献:
郭占荣, 黄磊, 刘花台, 袁晓婕. 2008. 镭同位素示踪隆教湾的海底地下水排泄[J]. 地球学报, 29: 647-652
郭占荣, 黄磊, 袁晓婕, 刘花台, 李开培. 2011. 用镭同位素评价九龙江河口区的地下水输入[J]. 水科学进展, 22: 118-125.
黄奕普, 谢永臻, 陈性保, 陈敏, 邱雨生. 2001. 海水中224Ra快速富集和测定的新方法[J]. 厦门大学学报: 自然科学版, 40: 699-705.
李开培, 郭占荣, 袁晓婕, 章斌, 马志勇. 2011. 氡和镭同位素在沿岸海底地下水研究中的应用[J]. 勘察科学技术, 173(5): 30-36.
门武, 刘广山, 陈志刚, 何建华, 尹明端, 余雯. 2010. 镭同位素在海洋学研究中的应用及进展[J]. 地球科学进展, 25(1): 33-42.
谢永臻, 黄奕普, 施文远, 邱雨生. 1994. 天然水体中226Ra、228Ra的联合富集与测定[J]. 厦门大学学报: 自然科学版, 33: 86-90.
BECK A J, COCHRAN M A. 2013. Controls on solid-solution partitioning of radium in saturated marine sands[J]. Marine Chemistry, 156: 38-48.
BECK A J, RAPAGLIA J P, COCHRAN J K. 2007. Radium mass-balance in Jamaica Bay, NY: Evidence for a substantial flux of submarine groundwater[J]. Marine Chemistry, 106: 419-441.
CABLE J E, SMITH C G, BLANFORD W J. 2009. Dispersivity and distribution coefficients in marine sediments using tritium and radium-226[J]. Radioprotection, 44(5): 185-190.
CHARETTE M A, BUESSELER K O, ANDREWS J E. 2001. Utility of radium isotopes for evaluating the input and transport of groundwater-derived nitrogen to a Cape Cod estuary[J]. Limnol. Oceanogr, 46: 465-470.
GARCIA-SOLSONA E, MASQUE P, GARCIA-ORELLANA J, RAPAGLIA J, BECK A J, COCHRAN J K, BOKUNIEWICZ H J, ZAGGIA L, COLLACINI F. 2008. Estimating submarine groundwater discharge around Isola La Cura, northern Venice Lagoon (Italy), by using the radium quartet[J]. Marine Chemistry, 109: 292-306.
GONNEEA M E, MORRIS P J, DULAIOYA H, CHARETTE M A. 2008. New perspectives on radium behavior within a subterranean estuary[J]. Marine Chemistry, 109: 250-267.
GUO Zhan-rong, HUANG Lei, LIU Hua-tai, YUAN Xiao-jie. 2008. Estimating submarine inputs of groundwater to a coastal bay using radium isotopes[J]. Acta Geoscientica Sinica, 29: 647-652(in Chinese with English abstract).
GUO Zhan-rong, HUANG Lei, YUAN Xiao-jie, LIU Hua-tai, LI Kai-pei. 2011. Estimating submarine groundwater discharge to the Jiulong River estuary using Ra isotopes[J]. Advances in Water Science, 22: 118-125(in Chinese with English abstract).
HUANG Yi-pu, XIE Yong-zhen, CHEN Xing-bao, CHEN Min, QIU Yu-sheng. 2001. A new method for rapid concentration and determination of224Ra in seawater[J]. Journal of Xiamen University: Natural Science, 40: 699-705(in Chinese with English abstract).
LANGMUIR D, RIESE A C. 1985. The thermodynamic properties of radium[J]. Geochim. Cosmochim. Acta, 49: 1593-1601.
LI Kai-pei, GUO Zhan-rong, YUAN Xiao-jie, ZHANG Bing, MA Zhi-yong. 2011. The application of Radon and Radium isotopes in estimating submarine groundwater discharge in coastal areas[J]. Site Investigation Science and Technology, 173(5): 30-36(in Chinese with English abstract).
MENG Wu, LIU Guang-shan, CHEN Zhi-gang, HE Jian-hua, YIN Ming-duan, YU Wen. 2010. Progresses of Radium isotopes applications to oceanography research[J]. Advances in Earth Science, 25(1): 33-42(in Chinese with English abstract).
MOORE W S, OLIVEIRA J D. 2008. Determination of residence time and mixing processes of the Ubatuba, Brazil, inner shelf waters using natural Ra isotopes[J]. Estuarine, Coastal and Shelf Science, 76: 512-521.
MOORE W S. 1981. Radium isotopes in the Chesapeake Bay[J]. Estuarine Coastal and Shelf Science, 12: 713-723.
MOORE W S. 2000. Ages of continental shelf water determined from223Ra and224Ra[J]. Journal of Geophysical Research, 105(22): 117-122.
WEBSTER I T, HANCOCK G J, MURRAY A S. 1995. Modeling the effect of salinity on radium desorption from sediments[J]. Geochimica et Cosmochimica Acta, 59(12): 469-2476.
XIE Yong-zhen, HUANG Yi-pu, SHI Wen-yuan, QIU Yu-sheng. 1994. Simultaneous concentration and determination of226Ra,228Ra in natural waters[J]. Journal of Xiamen University: Natural Science, 33: 86-90(in Chinese with English abstract).
Characteristics of Radium Desorption from Sediments in the Salt Water Environment
YUAN Xiao-jie, GUO Zhan-rong*, LIU Jie, MA Zhi-yong, WANG Bo
College of Ocean and Earth Sciences, Xiamen University, Xiamen, Fujian 361005
Radium diffusion from sediments to overlying water is one of the important sources of radium isotopes in ocean water. A series of laboratory desorption/diffusion experiments were conducted to help elucidate the characteristics of sediments on224Ra and226Ra desorption and diffusion, which included 1)224Ra and226Ra desorption from sediments in water of different salinities, 2)224Ra and226Ra desorption from sediments of different grain sizes in water of the same salinity, 3)224Ra and226Ra diffusive fluxes by observing Ra enrichment with time in the overlying water of incubated sediments. The experimental results show that there is an increase in the amount of224Ra and226Ra with the increase of salinity from 5 to 30, and Ra desorption is strongest at the salinity of 25. Under the same salt water condition,224Ra and226Ra desorption activities of the four grain sizes (2000~1000 μm, 1000~500 μm, 500~250 μm and 250~125 μm) of sediments are very close to each other. When the grain sizes of sediments are larger than 2000μm, the224Ra and226Ra desorption activities are slightly higher than those of the sediments of the above-mentioned four grain sizes. When the grain sizes of sediments are less than 125 μm, the224Ra and226Ra desorption activities are much larger than those of the above-mentioned five grain sizes. The average diffusive fluxes of224Ra and226Ra of sediments from Jiaozhou Bay are
0.85 Bq·m-2·d-1and 0.022 Bq·m-2·d-1, respectively.
sediments; radium isotopes; desorption; diffusion; salt water
O614.234; O647.3
A
10.3975/cagsb.2014.05.08
本文由国家自然科学基金项目(编号: 41072174)资助。
2014-01-12; 改回日期: 2014-04-03。责任编辑: 魏乐军。
袁晓婕, 女, 1985年生。博士研究生。研究方向为镭同位素示踪海底地下水排泄。通讯地址: 361102, 厦门大学翔安校区希平楼C3-123室。E-mail: jieer17@163.com。
*通讯作者: 郭占荣, 男, 1965年生。教授。主要从事海岸带水文地质学和海洋地质的教学与研究工作。通讯地址: 361102, 厦门大学翔安校区希平楼C3-123室。E-mail: gzr@xmu.edu.cn。
