硫酸氢铵焙烧高钛渣提取TiO2
2014-06-04隋丽丽翟玉春
隋丽丽 ,翟玉春
(1. 东北大学 材料与冶金学院,沈阳 110819;2. 沈阳医学院 基础医学院化学系,沈阳 110034)
TiO2是一种重要的无机化工产品,广泛应用于涂料、油墨、塑料和橡胶等行业[1−5]。工业生产二氧化钛的方法主要有硫酸法和氯化法。硫酸法技术比较成熟,设备简单,操作容易掌握,投资成本低。但硫酸法工序多、流程长,水的耗量大,副产物多,硫酸酸雾等对环境污染很大[6−9]。氯化法对环境污染程度只有硫酸法的十分之一,生产能力易于扩大,连续化自动化程度高,劳动生产率高。但是氯化法需要使用富钛料,投资成本高,工艺难度大,设备材料难以维修,这些均影响氯化法的发展与推广[10−15]。因此,探索制备二氧化钛的新技术具有重要的现实意义。
我国四川攀西地区含有丰富的钒钛磁铁矿资源,经过高炉冶炼得到生铁,而钛则排放到渣中,攀钢每年要排放300万t该种高钛渣,堆积如山,污染环境,所以高钛渣的堆积问题亟待解决[16−18]。利用高钛渣生产钛白(TiO2),可以减少或者消除副产物绿矾,省去结晶分离工序,降低能耗和时间,同时解决了环境污染的问题。
本文作者提出硫酸氢铵法焙烧高钛渣的工艺,探讨原料粒度、硫酸氢铵与钛渣质量比、焙烧温度和焙烧时间对TiO2提取率的影响,确定了最佳工艺参数。利用硫酸氢铵焙烧高钛渣原料成本低,生产设备腐蚀程度低,环境污染小,硫酸氢铵可以循环使用。而且溶液中富集了铝、镁等有价组元,为后续铝、镁提取创造了有利条件,是实现高钛渣资源综合利用的第一步。
1 实验
1.1 实验原料
采用四川某地高钛渣,经过破碎、球磨后用于实验,其化学组成见表1。高钛渣的主要成分是TiO2,其含量为48.65%。高钛渣的XRD谱如图1所示。主要物相为固溶镁和铁的黑钛石(Mg0.5Fe0.5)Ti2O5和复杂的硅酸盐相Al2Ca(SiO4)2。

表1 高钛渣的主要化学组成Table 1 Chemical composition of high titanium slag (mass fraction, %)
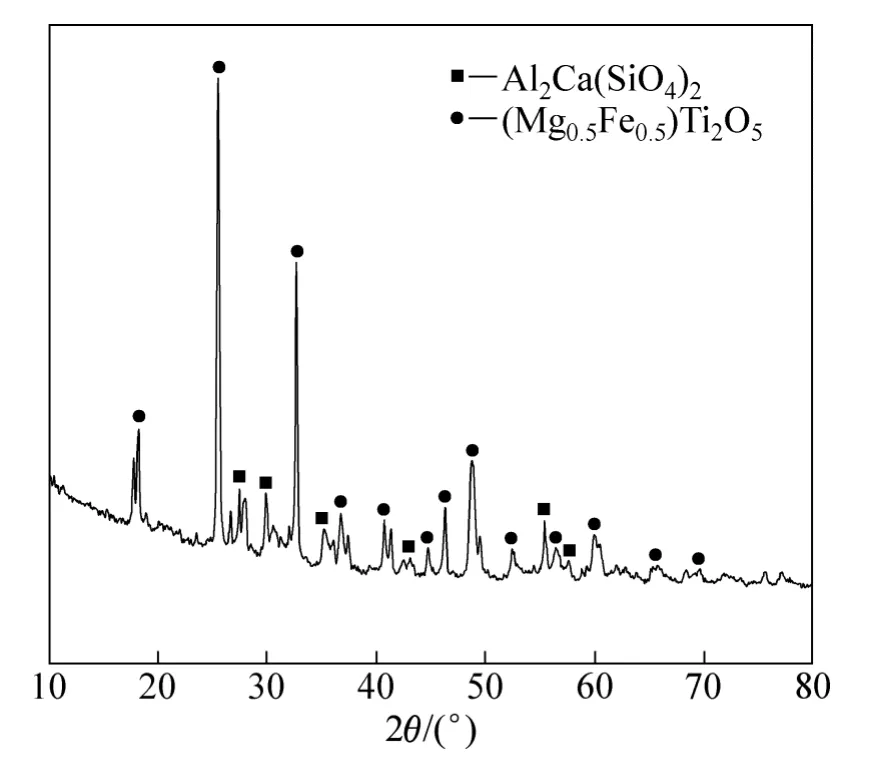
图1 高钛渣的XRD谱Fig. 1 XRD pattern of high titanium slag
1.2 实验原理
高钛渣与硫酸氢铵在焙烧过程中发生的主要化学反应[19]如下:

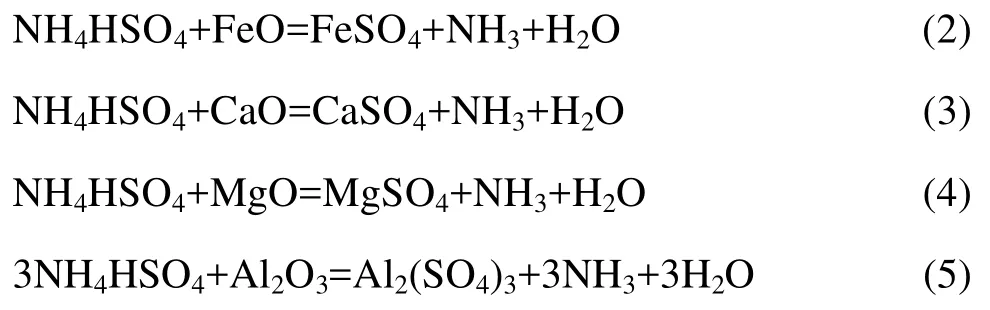
硫酸氢铵与TiO2、FeO、MgO和Al2O3反应,经过溶出进入溶液中;硫酸氢铵与CaO反应得到不溶产物CaSO4,与SiO2一起残留在渣相中。
1.3 实验过程
将高钛渣和硫酸氢铵混合均匀放入坩埚后置于电阻丝加热炉中,加热至实验所需温度,保温一定时间后取出,冷却至室温,向熟料中加入一定量的蒸馏水溶出,溶出温度为70 ℃,固液质量比为1:4,搅拌速率为400 r/min,溶出60 min后,抽滤得到钛液和滤渣,烘干滤渣。溶液中TiO2的含量采用硫酸高铁铵滴定法测定,并按式(6)计算TiO2的提取率:

式中:α(TiO2)为 TiO2的提取率;m′(TiO2)为滤液中 TiO2的质量;m(TiO2)为高钛渣中TiO2的总质量。
2 结果与讨论
2.1 单因素试验
2.1.1 原料粒度对TiO2提取率的影响
在硫酸氢铵与钛渣质量比为6:1、焙烧温度为500℃、焙烧时间为2 h的实验条件下,考察原料粒度与TiO2提取率的关系,结果如图2所示。
从图2可知,随着钛渣粒度的逐渐减小,其提取率逐渐提高,所以钛渣粒度对 TiO2提取率的影响很大。化学反应速率和颗粒的比表面积成正比,钛渣变细后,增加了反应的接触面积,加速了分子之间的有效碰撞,提高了反应速度。当钛渣粒度为 45~53 µm时,TiO2提取率可达到80.75%,所以钛渣粒度控制在45~53 µm 最佳。
2.1.2 硫酸氢铵与高钛渣质量比对 TiO2提取率的影响
在原料粒度为45~53 µm、焙烧温度为500 ℃、焙烧时间为2 h的实验条件下,考察硫酸氢铵与高钛渣质量比与TiO2提取率的关系,结果如图3所示。硫酸氢铵与高钛渣质量比的选择与高钛渣的化学成分密切相关,在反应过程中,硫酸氢铵可与高钛渣中的钛、镁、铁、铝和钙等反应,溶出后大部分物质进入溶液中,所以实际反应过程很复杂,除了根据计算来推断其硫酸氢铵用量,还应通过实验进行验证。

图2 原料粒度对TiO2提取率的影响Fig. 2 Effect of particle size of materials on extracting rate of TiO2

图3 硫酸氢铵与高钛渣质量比对TiO2提取率的影响Fig. 3 Effect of mass ratio of ammonium bisulfate to high titanium slag on extracting rate of TiO2
从图3可知,随着硫酸氢铵与高钛渣质量比的增加,TiO2提取率是逐渐提高的,当硫酸氢铵与高钛渣的质量比为5:1时,TiO2提取率最高,达到83.35%,再增加质量比,其提取率基本不再提高,综合考虑原料成本,此质量比控制在5:1为宜。
2.1.3 焙烧温度对TiO2提取率的影响
在原料粒度为45~53 µm、硫酸氢铵与钛渣质量比为5:1、焙烧时间为2 h的实验条件下,考察焙烧温度与TiO2提取率的关系,结果如图4所示。
从图4可知,随着焙烧温度的提高,TiO2提取率不断增大,说明焙烧温度对TiO2提取率影响很大。焙烧温度在350 ℃时基本不发生反应;当焙烧温度升高到480 ℃时,提取率最高,达到83.75%,考虑到能耗,选取480 ℃为最佳焙烧温度。
2.1.4 焙烧时间对TiO2提取率的影响
在原料粒度为45~53 µm、硫酸氢铵与高钛渣质量比为5:1、焙烧温度为480 ℃的实验条件下,考察焙烧时间与TiO2提取率的关系,结果如图5所示。
从图5可以看出,随着焙烧时间的延长,TiO2的提取率不断提高。当焙烧时间为60 min时,TiO2提取率达到84%,继续时间延长,提取率基本保持不变,在保证较高提取率的前提下尽可能缩短反应时间,所以焙烧时间控制在60 min为宜。
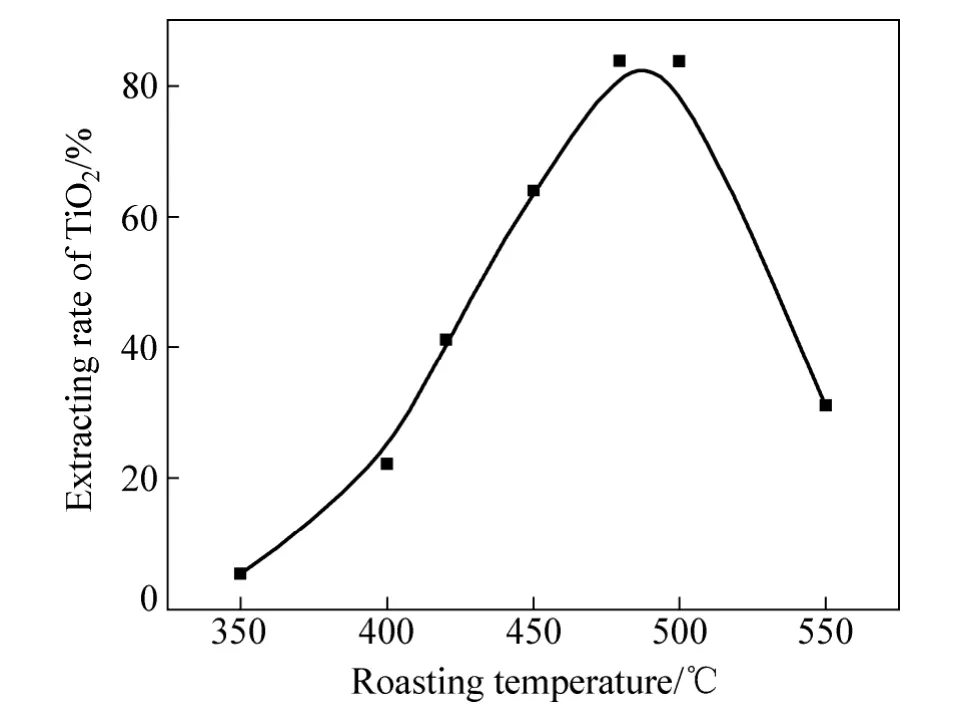
图4 焙烧温度对TiO2提取率的影响Fig. 4 Effect of roasting temperature on extracting rate of TiO2
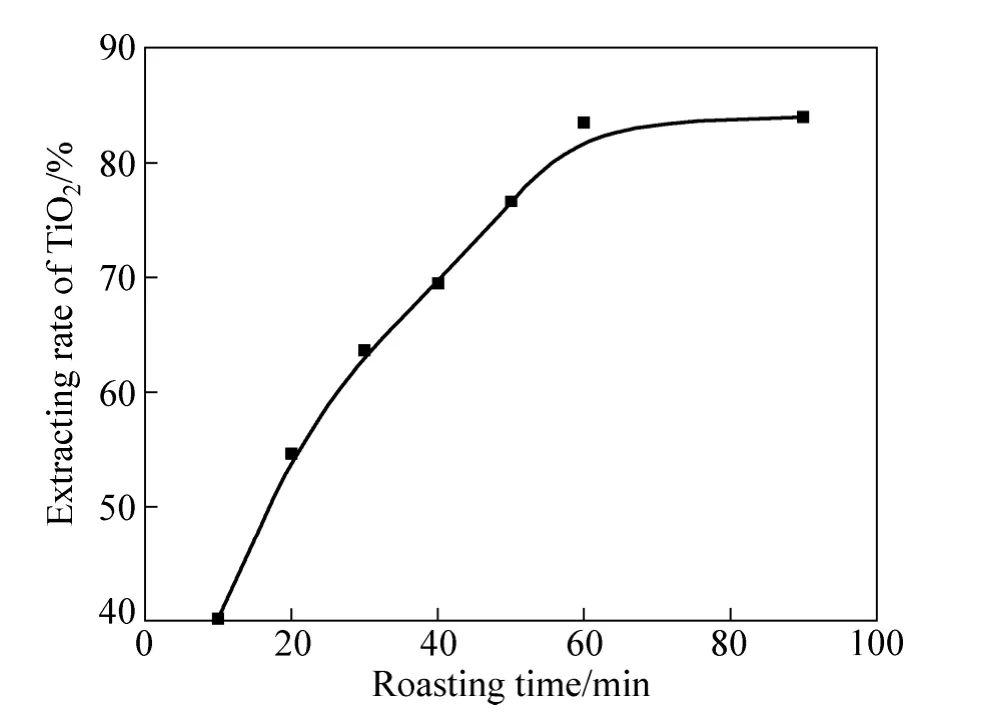
图5 焙烧时间对TiO2提取率的影响Fig. 5 Effect of roasting time on extracting rate of TiO2
2.2 正交实验结果与分析
影响TiO2提取率的因素较多,采用正交设计可确定相关因素对TiO2提取率的影响,从而寻找最佳的工艺参数。根据高钛渣提取率的探索性实验,选择硫酸氢铵与钛渣质量比、焙烧时间和焙烧温度3个因子进行3水平正交实验。固定实验条件:原料粒度45~53µm、溶出固液质量比1:4、溶出温度70 ℃、搅拌速率400 r/min、溶出时间为60 min,以TiO2提取率为评价指标进行正交实验,实验结果如表2所列。
采用极差法对正交实验结果进行统计分析,由极差R的大小可知:1) 在各因素选择的范围内,影响TiO2提取率各因素由大到小的顺序为焙烧温度、焙烧时间、硫酸氢铵与高钛渣质量比,即焙烧温度的影响最显著,其次是焙烧时间和硫酸氢铵与高钛渣质量比;2) 用硫酸氢铵焙烧高钛渣提取 TiO2的最佳实验条件如下:硫酸氢铵与钛渣质量比4:1、焙烧时间60 min、焙烧温度480 ℃。在此最佳实验条件下进行稳定性实验,TiO2的提取率达到85%。

表2 从高钛渣中提取TiO2正交实验结果与分析Table 2 Results and analysis of orthogonal test for extracting TiO2 from high titanium slag
2.3 滤渣的成分分析
滤渣经洗涤至中性,取样进行成分分析,结果如表3 所列。由表3可知,滤渣的主要成分是SiO2,TiO2含量很低。滤渣通过 X射线衍射分析(见图 6),主要物相为 SiO2、Al2Ca(SiO4)2和 Ca(Mg,Al)(Si,Al)2O6,含钛矿物峰消失,这说明高钛渣经硫酸氢铵处理后,含钛矿物几乎反应完全,剩余硅酸盐相残留在渣中。
图7所示为高钛渣和滤渣经过喷金处理后的SEM像。由图 7(a)可以看出,高钛渣的表观结构致密,表面粗糙,形状不规则。由图7(b)可知,经过硫酸氢铵反应后,滤渣表面凸凹不平,高钛渣的形貌被破坏,硅酸盐相大部分以 SiO2形式存在,这为后续 SiO2的提取奠定了基础。

表3 滤渣的主要化学组成Table 3 Chemical composition of residue (mass fraction, %)

图6 滤渣的XRD 谱Fig. 6 XRD pattern of residue

图7 高钛渣和滤渣的SEM像Fig. 7 SEM image of high titanium slag (a) and residue (b)
3 结论
1) 综合单因素实验和正交实验得到硫酸氢铵法焙烧高钛渣提取TiO2的最佳实验条件如下:硫酸氢铵与高钛渣质量比4:1、焙烧温度480 ℃、焙烧时间60 min、原料粒度45~53 µm。按照最佳条件进行稳定性实验,TiO2的提取率达到85%。
2) 焙烧后的渣中富集了 SiO2和硫酸钙,在钛液中获得铝和镁,为后续硅、钙、铝和镁的提取创造了有利条件。
[1]ZHANG Wen-sheng, ZHU Zhao-wu, CHENG Chu-yong. A literature review of titanium metallurgical processes[J].Hydrometallurgy, 2011, 108(3): 177−188.
[2]LIU Shui-shi, GUO Yu-feng, QIU Guan-zhou, JIANG Tao,CHEN feng. Preparation of Ti-rich material from titanium slag by activation roasting followed by acid leaching[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(4): 1174−1178.
[3]张树立. 酸溶性钛渣制取钛白工业试验[J]. 钢铁钒钛, 2005,26(3): 33−36.ZHANG Shu-li. Industrial experiment of producing titanium white by acid dissolved titanium slag[J]. Iron Steel Vanadium Titanium, 2005, 26(3): 33−36.
[4]刘晓华, 隋智通. 含 Ti高炉渣加压酸解[J]. 中国有色金属学报, 2002, 12(6): 1281−1284.LIU Xiao-hua, SUI Zhi-tong. Leaching of Ti bearing blast furnace slag by pressuring[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(6): 1281−1284.
[5]ZHANG Yong-jie, QI Tao, ZHANG Yi. A novel preparation of titanium dioxide from titanium slag[J].Hydrometallurgy, 2009, 96(1): 52−56.
[6]GRZMIL B U, GRELA D, KIC B. Hydrolysis of titanium sulphate compounds[J]. Chemical Papers, 2008, 62(1): 18−25.
[7]王 斌, 程晓哲, 韩可喜, 秦兴华, 马 勇. 酸溶性钛渣酸解性能研究[J]. 钢铁钒钛, 2009, 30(2): 6−11.WANG Bin, CHENG Xiao-zhe, HAN Ke-xi, QIN Xing-hua,MA Yong. Research of acidolysis performance of acid soluble titanium slag[J]. Iron Steel Vanadium Titanium, 2009, 30(2):6−11.
[8]李 亮. 攀枝花钒钛磁铁矿深还原渣酸解工艺研究[J]. 无机盐工业, 2010, 42(6): 52−54.LI Liang. Study on acid hydrolysis process of deep reduction slag of Panzhihua V−timagnetite[J].Inorganic Chemicals Industry, 2010, 42(6): 52−54.
[9]ZHANG S C, NICOL M J. Kinetics of the dissolution of ilmenite in sulfuric acid solutions under reducing conditions[J].Hydrometallurgy, 2010, 103(1/4): 196−204.
[10]景建林, 张全忠, 邱礼有, 梁 斌. 硫酸法钛白生产中钛铁矿液相酸解反应的实验研究[J]. 化学反应工程与工艺, 2003,19(4): 337−343.JING Jian-lin, ZHANG Quan-zhong, QIU Li-you, LIANG Bin.An investigation on the liquid phase digestion of ilmenite in sulfate process TiO2pigment production[J]. Chemical Reaction Engineering and Technology, 2003, 19(4): 337−343.
[11]ZHOU Zhong-cheng, RUAN Jian-ming, ZOU Jian-peng, LI Song-lin, FU Nai-ke. Preparation of nanosized rutile TiO2powders by direct hydrolysis of TiCl4[J]. Chinese Journal of Rare Metals, 2006, 30(5): 653−656.
[12]AKHGAR B N, PAZOUKI M, RANIBAR M, HOSSEINNIA A,KEYANPOUR-RAD M. Preparetion of nanosized synthetic rutile from ilmenite concentrate[J]. Minerals Engineering, 2010,23(7): 587−589.
[13]LI Chun, LIANG Bin, WANG Hai-Yu. Preparation of synthetic rutile by hydrochloric acid leaching of mechanically activated Panzhihua ilmenite[J]. Hydrometallurgy, 2008, 91(1/4):121−129.
[14]华一新. 冶金过程动力学导论[M]. 北京: 冶金工业出版社,2004: 9.HUA Yi-xin. Metallurgical process kinetics introduction[M].Beijing: Metallurgical Industry Press, 2004: 9.
[15]张树立, 程晓哲, 胡鸿飞. 酸溶性钛渣酸解工艺研究[J]. 钢铁钒钛, 2003, 24(1): 39−45.ZHANG Shu-li, CHENG Xiao-zhe, HU Hong-fei. Study on digestion technology of acid-dissolved titanium slag[J]. Iron Steel Vanadium Titanium, 2003, 24(1): 39−45.
[16]LIU Xiao-hua, SUI Zhi-tong. Kinetics of leaching Ti-bearing slag by dilute sulphuric acid[J]. Acta Metallurgica Sinica, 2003,39(3): 293−296.
[17]刘晓华, 隋智通. 含钛高炉渣制取富钛料新工艺[J]. 内蒙古工业大学学报, 2005, 24(4): 268−271.LIU Xiao-hua, SUI Zhi-tong. A new method for preparing rich TiO2materials from Ti-bearing slag[J]. Journal of Inner Mongolia University of Technology, 2005, 24(4): 268−271.
[18]DONG Hai-gang, TAO Jiang, GUO Yu-feng, CHEN Jia-lin,FAN Xing-xiang. Upgrading a Ti-slag by a roast-leach process[J].Hydrometallurgy, 2012, 113/114: 119−121.
[19]隋丽丽, 翟玉春. 硫酸氢铵焙烧高钛渣反应动力学[J]. 中国有色金属学报, 2014, 24(2): 542−546.SUI Li-li, ZHAI Yu-chun. Kinetics on reaction of roasting high titanium slag with ammonium bisulfate[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 542−546.
