壳聚糖的溶解行为及其纤维研究进展
2014-06-01杨俊杰胡广敏相恒学毛宇辰张君妍朱美芳
杨俊杰,胡广敏,相恒学,毛宇辰,张君妍,朱美芳
(1.东华大学材料科学与工程学院纤维材料改性国家重点实验室,上海201620)(2.山东海斯摩尔生物科技有限公司,泰安271400)
壳聚糖的溶解行为及其纤维研究进展
杨俊杰1,胡广敏2,相恒学1,毛宇辰1,张君妍1,朱美芳1
(1.东华大学材料科学与工程学院纤维材料改性国家重点实验室,上海201620)(2.山东海斯摩尔生物科技有限公司,泰安271400)
近年来,随着天然大分子多糖在材料领域的不断研究应用,纤维素、壳聚糖等逐渐引起了人们的广泛关注。由于其自身优异的生物相容性、抗菌性以及可降解性,壳聚糖吸引了众多研究者的高度重视,在医疗、食品、环境工程等领域的研究和应用均取得了可观的进展。首先从壳聚糖的溶液性质研究出发,分别介绍了脱乙酰度、温度、分子量等因素对壳聚糖溶液的溶解行为的影响,重点介绍了醋酸和离子液体体系下的溶液性质,其次对壳聚糖的湿法纺丝研究进行了综述,同时对纤维性能的提高方法以及长丝的实现可能性进行了总结,最后对壳聚糖及其纤维制品的未来发展前景进行了展望。
溶液性质;壳聚糖纤维;力学性能
1 前 言
壳聚糖,学名聚-(1,4)-2-乙酰氨基-2-脱氧-D-葡萄糖,又被称为甲壳胺、几丁质,是一种白色或淡黄色略带珍珠光泽的半透明固体,广泛存在于虾壳、蟹壳、昆虫外壳及各种天然菌类和藻类的细胞壁中,是迄今发现的自然界中唯一的碱性多糖,其化学结构与纤维素非常相似[1]。壳聚糖是一种重要的生命物质,在自然界中,其含量仅次于纤维素,被誉为自然界的“第六生命元素”[2-3]。图1是壳聚糖分子的结构,图2是壳聚糖单体和纤维素单体的结构。

图1 壳聚糖分子的结构Fig.1 Structure of chitosan molecule
工业上,壳聚糖通常由甲壳素在浓碱中加热脱乙酰化得到。由于来源的不同,壳聚糖的相对分子质量从几万、数十万到数百万不等。壳聚糖通常不溶于水、也不溶于碱液、有机溶剂、稀硫酸等,但可溶于乙酸等有机酸和盐酸等无机酸。

图2 氨基葡萄糖(壳聚糖单体)(a)与葡萄糖(纤维素单体)(b)的结构[15]Fig.2 Structure of glucosamine(monomer of chitosan)(a)and glucose(monomer of cellulose)(b)[15]
壳聚糖作为一种潜力巨大的多糖资源已经引起了人们的广泛关注[4]。壳聚糖具有优异的广谱抗菌性,其抗菌效率高并且无毒副作用,在达到材料良好抗菌性的同时,又具有可降解性和吸附螯合金属离子的能力,这使得其在功能材料领域有着巨大的发展空间[5],但是对壳聚糖的开发应用远落后于纤维素。近年来,由于壳聚糖纤维良好的成纤性以及优异的生物相容性,相关研究不断发展,壳聚糖纤维在医用纺织品、保健服装等方面均得到了广泛的应用[6]。
壳聚糖及其功能型衍生物已经得到了广泛的研究,但是少有专门涉及壳聚糖溶解性问题的研究工作,而研究壳聚糖的溶液性质,对于指导壳聚糖纤维纺丝过程以及新材料的开发都具有重要意义。为此,本文从壳聚糖的溶解角度出发,对壳聚糖的溶液行为以及纤维成形进行了综述。
2 壳聚糖溶液性质研究
有关壳聚糖水解的研究,在生物医学、药剂学等方面均有着较多的应用,这些应用与相应壳聚糖溶液的粘度、稳定性有着密切关系,而粘度的变化是大分子链的降解和高分子溶液的稳定性中最显著的标志,因此,研究多糖溶液粘度变化具有非常积极的意义。同时在壳聚糖纤维的湿法纺丝中,纺丝液的溶液性质对于壳聚糖纤维的成形过程以及最终的性能有着重要影响,为此,也需要对其溶液的溶解行为及相应的溶液性质进行研究。
壳聚糖是一种半刚性高分子,由于其分子内和分子间强烈的氢键作用,壳聚糖不溶于二甲基甲酰胺和二甲基亚砜等有机溶剂。通常情况下,壳聚糖可以溶解于pH低于6的稀酸溶液中,甲酸、醋酸、离子液体等均可作为其良溶剂,下面以醋酸体系和离子液体体系等为例,具体阐述对应体系下壳聚糖的溶液性质研究。
2.1 醋酸体系
醋酸很早就被研究者发现是一种溶解壳聚糖的有效溶剂,因此相关溶液性质研究最早也是集中于醋酸体系,围绕这一溶液体系,研究者们建立了壳聚糖溶液流变性质的一系列理论,脱乙酰度、温度、分子量等性质,均会对壳聚糖溶解行为产生影响。
脱乙酰度是影响壳聚糖性质的重要因素。壳聚糖中的氨基基团决定了壳聚糖的带电性质随着pH值的变化而变化[7]。当pH值较低时,氨基发生质子化而带正电荷,使得壳聚糖成为水溶性阳离子聚电解质。而当pH值达到6时,壳聚糖中的氨基开始去质子化并失去正电荷,这时壳聚糖变得不溶。壳聚糖这种可溶-不溶的转变发生在pH值为6~6.5范围内,与pKa值有关。由于pKa值高度依赖于脱乙酰化程度,因此,壳聚糖的溶解行为与其脱乙酰度及脱乙酰的方法密切相关[8]。
其溶解常数K a由下式表达和计算:
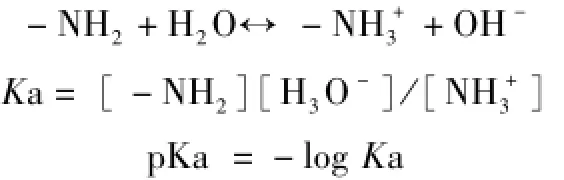
在壳聚糖的研究中,温度、脱乙酰反应的时间,脱乙酰所用碱液浓度,碱液中甲壳素所占比重等都会影响所得壳聚糖的性质,并对最终的溶解性能产生影响[15]。除此以外,壳聚糖溶液的性质,还与主链上乙酰基沿主链的分布有关[9]。
温度及分子量也会对壳聚糖溶液性质产生重要影响。江南大学李星科等[10]研究发现,在0~80℃范围内,温度对壳聚糖溶液的粘度的影响符合Arrhenius模型,如图3所示壳聚糖溶液的粘度随分子量的增大而增大(图3a),随温度的升高逐渐下降(图3b)。研究结果对于调控壳聚糖纺丝液的流变性质,以及纺丝过程的进行具有直接的指导意义。
通过在壳聚糖溶液中添加盐类也可以达到调控其溶液流变性质的目的,同时,溶液的存放时间也会对溶液性质产生影响。华南理工大学吴国杰等[11]通过对不同环境条件下壳聚糖的醋酸溶液的粘度变化情况进行研究发现,壳聚糖醋酸溶液粘度与温度、溶液的存放时间、外加盐量呈负相关,并进一步说明壳聚糖醋酸溶液为非牛顿假塑性流体,结果与李星科等人的研究相符。
壳聚糖的来源对其流变性质也会造成影响,从不同原料得到的壳聚糖之间性质有着明显差异。浙江工业大学韩怀芬等[12]发现在其他条件相同的情况下,虾壳聚糖溶液的粘度要比蟹壳聚糖溶液的粘度大,同时从降解速率的角度来看,从蟹壳中提取的壳聚糖比从虾壳中提取的壳聚糖的降解速度要快。这是因为从不同原料中得到的壳聚糖分子量、分子量分布及分子间作用力不同。研究证实,虾甲壳素中-O…H-N-型氢键数量要比蟹甲壳素中多,因此,虾甲壳素产生的壳聚糖中分子间作用力要比从蟹甲壳素得到的壳聚糖中的作用力大,进而使得虾壳聚糖溶液粘度大于蟹壳聚糖溶液粘度,并产生不同的降解速率。
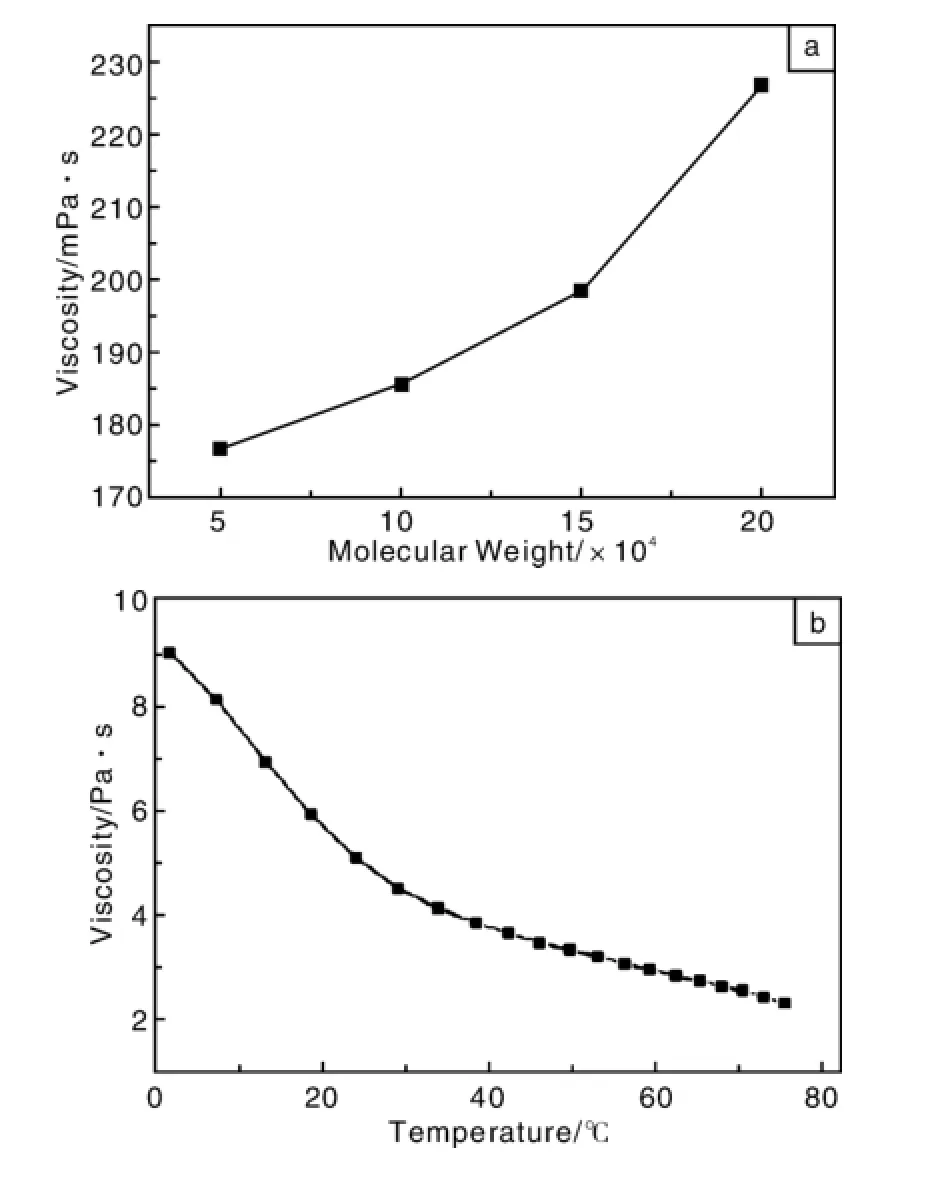
图3 分子量(a)和温度(b)对壳聚糖溶液粘度的影响[10]Fig.3 Effect of molecular weight(a)and temperature(b)on viscosity of chitosan solution[10]
在酸性水溶液中,壳聚糖以电解质的形式存在。这时,壳聚糖通过酸中的质子与壳聚糖上的胺基作用形成铵盐,从而破坏壳聚糖分子间的氢键进而实现溶解过程。余木火等[13]在研究壳聚糖醋酸水溶液粘度行为的基础上,提出了一套较为合理的常数确定方法,据此提出了一个新的经验式,用以描述聚电解质溶液粘度与浓度经验关系,并且其适用范围较宽,对聚电解质溶液体系同样适用。
醋酸是溶解壳聚糖最常用的溶剂,除此以外,壳聚糖也溶于稀盐酸和稀硝酸,但不溶于硫酸和磷酸。需要注意的是,壳聚糖在浓酸中溶解时,较高的温度会导致壳聚糖的降解[14],后续的研究需要进一步对溶解机理进行研究以改进溶解体系,以使壳聚糖得到更好的溶解。
2.2 离子液体体系
壳聚糖由于优良的生物特性,在生物医药等领域取得了广泛的应用。但其分子内和分子间强烈氢键作用的存在,使得壳聚糖难以溶解在普通溶剂中进行生产加工,实际应用中可用于壳聚糖溶解加工的溶剂比较少,这也在一定程度上限制了其研究与应用[15]。
离子液体(Ionic Liquid)具有极性强且可调控[16]、热稳定性高[17]等特性,其对许多无机和有机物具有良好的溶解性,因此,近年来离子液体引起了人们的广泛关注[18-19]。离子液体最开始用于溶解多糖的实例是纤维素。自2002年Swatloski等[20]利用离子液体溶解纤维素以后,越来越多采用离子液体溶解纤维素并进行加工和改性的研究工作不断开展[21-22]。如前所述(图1,2),壳聚糖的分子结构与纤维素相似,因此,有研究工作采用离子液体对壳聚糖进行溶解。
离子液体通常由阴阳离子组成,离子液体的结构对壳聚糖的溶解有着重要影响。与离子液体对纤维素的作用相比,离子液体对壳聚糖有着相似的溶解机理。郑州大学孙璠等[23]发现在离子液体对壳聚糖的溶解过程中,在阳离子相同的情况下,具有Cl-、HCOO-、Ac-等容易接受氢键阴离子的离子液体,更容易破坏壳聚糖分子内和分子间的氢键作用,对壳聚糖的溶解效果更好;而当阴离子相同时,体积小、极性强的阳离子更容易与壳聚糖中-OH和-NH2产生氢键作用,从而破坏壳聚糖本身的氢键作用,进一步促进壳聚糖的溶解。表1中列出了不同温度下壳聚糖在不同离子液体中的溶解浓度。

表1 不同温度下壳聚糖在不同离子液体中的溶解浓度(w/%)[24]Table 1 Dissolution concentration of chitosan in different ionic liquids at various tem peratures(w/%)[24]
离子液体对壳聚糖的溶解机理可以解释为,在加热条件下,离子液体中的离子对发生解离,形成游离的阳离子和阴离子,其中游离的阴离子既可以和壳聚糖大分子链羟基中的氢原子形成氢键,也可以同大分子链中氨基中的氢原子形成氢键,而游离的阳离子和壳聚糖大分子中失去氢原子的氧作用,从而破坏了壳聚糖中原有的氢键,导致壳聚糖在离子液体中的溶解。段先泉等[25]以[EMIM]Ac为研究对象,在分析其溶解壳聚糖的机理,探究溶液流变性能的同时,也详细分析了不同分子质量壳聚糖在[EMIM]Ac中的溶解与再生特性,以及溶液的流变性能,为壳聚糖进行复合材料成膜以及后续成纤加工提供了理论基础。图4是壳聚糖在[EMIM]Ac中的溶解机理图示。
离子液体对于大多数的无机物、有机物和高分子材料而言,是一种优良溶剂,可以代替挥发性大的有机溶剂,减少废物的产生,从而降低对环境的污染,被人们看做是一种绿色溶剂。国内外众多学者对壳聚糖在离子溶液中的溶解进行了广泛的研究。但是对于其是否具有潜在的危害性,如毒性或稳定性等有待研究。因此,寻找能更有效溶解壳聚糖的绿色溶剂,以及如何降低生产成本,仍是目前壳聚糖功能材料制备过程中需要解决的问题。

图4 壳聚糖在[EMIM]Ac中的溶解机理图示[25]Fig.4 Graphic representation of dissolution mechanism of chitosan in[EMIM]Ac[25]
2.3 其他溶剂体系
2.3.1 碱-尿素低温体系
碱-尿素低温溶解体系是近年来发展起来的一种溶解天然大分子多糖的有效手段,由武汉大学张俐娜院士最先发现并应用于纤维素的溶解,取得了很好的效果[26-27]。由于壳聚糖的结构与纤维素有一定的相似之处,有研究者将这一原理应用到壳聚糖的溶解之中。
借鉴甲壳素在质量分数为8%NaOH与4%尿素的混合溶液中的溶解过程,首先甲壳素分子于室温下浸润于溶液中,充分溶胀,随后水分子进入经过NaOH活化过的甲壳素分子链,冰点下水分子冻结并膨胀,同时打破分子间和分子内氢键,最终促使了甲壳素分子的溶解,如图5所示。壳聚糖在碱-尿素体系下的溶解具有相似的机理。

图5 甲壳素溶解过程示意图[28]Fig.5 Schematic diagram of dissolution process of chitin[28]
与传统醋酸溶解体系相比,碱-尿素体系下的壳聚糖溶液也是切力变稀的液体,但与传统有机酸体系不同的是,两种体系下,壳聚糖溶液粘度随剪切速率的变化趋势不同。浙江大学李友良[29]研究了壳聚糖在碱性溶剂中的溶解情况,并与传统醋酸溶解体系进行了对比研究,实验发现,随着剪切速率升高,壳聚糖碱性溶液体系粘度下降较为平缓,而酸性溶液体系下曲线斜率更大。这是由于壳聚糖在不同的溶液环境下存在的形式不同造成的。在酸性溶液中,剪切变稀的内在原因是分子链的解缠结,而在碱性溶液中,壳聚糖的两种存在形式——单个包合络合物(Single IC)和包合络合物聚集体(ICs Aggregate)可以转化,包合络合物的解体引起了溶液粘度的下降。表2给出了甲壳素在碱-尿素体系中的溶解情况。
虽然碱-尿素体系在纤维素的溶解方面取得了一定的研究进展,但在壳聚糖的溶解方面还处于起步阶段,主要存在低温要求高、溶解效率低等问题[30],相关研究工作还需要继续完善。

表2 不同温度下,8%NaOH/4%尿素溶液(质量分数)中甲壳素的溶解度[28]Tab le 2 Solubility of chitin in 8%NaOH/4%urea aqueous solution(m ass fraction)at various temperatures[28]
2.3.2 其他有机酸体系
壳聚糖是一种结晶度较高的物质,其大分子具有较好的立构规整性和较强的氢键作用,因此,只有在稀酸中,而且当氢离子活度达到一定程度(至少与溶液中壳聚糖上的-NH2浓度相等)才可让氢离子和-NH2质子化成为-NH+3,破坏掉原来的氢键和晶格结构,最终全部溶解。不同的酸对于壳聚糖的溶解行为效果不同。陈雄等[31]研究了壳聚糖在不同酸介质中的特性粘度,分别研究了乙酸、甲酸、盐酸对壳聚糖的作用,结果发现,在温度相同的前提下,特性粘度最大的是盐酸,乙酸其次,甲酸粘度最小。
壳聚糖的溶解效果与所用酸的浓度以及溶液的pH直接相关。由于甲酸和乙酸进一步电离以维持电离平衡,但过多的酸根离子会屏蔽聚电解质分子间的静电斥力,因而造成分子链收缩,链与链之间的缠结减弱,最终使得壳聚糖在乙酸中的粘度低于在甲酸中的粘度。表3列出了不同酸介质条件下壳聚糖溶液的特性粘度值。

表3 不同酸介质(溶剂浓度2%)条件下壳聚糖溶液特性粘度(dl/g)[31]Tab le 3 Viscosity o f chitosan solution under different acidic medium s w ith solvent concentration of2%(d l/g)[31]
采用柠檬酸作为溶剂也可以很好地溶解壳聚糖,并且研究表明,随着柠檬酸酸浓度的增大、溶解温度的升高和溶解时间的延长,壳聚糖的溶解也相应提高。昆明理工大学李维艳等[32]以柠檬酸为溶剂,采用电位测试法和电导测试法研究了壳聚糖的溶解行为,结果发现对于柠檬酸体系,高浓度不一定有利于壳聚糖的溶解,在一定酸浓度范围内,可以使溶液中质子化程度达到最大,从而使得壳聚糖的溶解性问题得到更好的解决,满足其在生物医学工程领域的应用要求。
3 壳聚糖纤维
早在1942年,美国就首先成功研制出壳聚糖纤维。研究者们证实,壳聚糖纤维不但具有良好的物理机械性能,而且具有优良的生物相容性和生物活性。由于壳聚糖纤维对人体的免疫抗原性小、同时具有优异的生物活性,引起了医学界的广泛关注。高洸等[33]的研究表明壳聚糖纤维具有无毒、止血、消炎、与人体相容性好等优点,同时还具有优异的生物可降解性,既可以作为医用可吸收手术缝线、伤口敷料等,也可与其它纤维混纺做服装面料。但同时,壳聚糖纤维也存在纺丝过程连续性不好,纤维性能差等缺点,为此需要对纤维进行处理,以增强其力学性能。
3.1 壳聚糖湿法纺丝
用湿法纺丝进行壳聚糖纤维的纺制由来已久,早在1980年就有人用0.5%的乙酸溶液制成3%的壳聚糖纺丝液,第1次制备出壳聚糖纤维,其纤维强度为2.2 g/dtex[36]。
高洸等[33]研究了壳聚糖纤维的成形机理,并对纺丝液的配制以及纺丝过程中的相关参数进行了探究,确定了壳聚糖的质量分数为3.5%,乙酸的质量分数为2%,同时添加1%质量分数的脲素等进行纺丝可以取得较好的纺丝效果,所纺纤维力学性能较优。
壳聚糖纤维具有天然的抗菌性,其产品对常见菌种大肠杆菌和金黄色葡萄球菌有着良好的抗菌效果。山东海斯摩尔生物科技有限公司通过湿法纺丝,自主研发生产了海斯摩尔(Hismer)纤维并获得了国家发明专利,在解决壳聚糖纺丝液输送问题的同时使其干断裂强度达到1.6cN/dtex以上,干断裂伸长率大于13%[34]。所研制的这种纯壳聚糖纤维,不含添加剂成分,同时具有优异的抗菌性能,测试结果显示其对大肠杆菌和金黄色葡萄球菌均有90%以上的抑菌率[35]。
壳聚糖也可以与其他物质共同溶解进行纺丝改善力学性能。四川大学的华坚等[36]研究了胶原蛋白和壳聚糖的共混溶液,探究了其溶液的粘度,并利用湿法纺丝的方法进行纺丝,对温度、存放时间、浓度、剪切速率等可能影响溶液粘度的因素进行了研究,最终发现用Na2SO4作为凝固剂对于纤维的力学性能效果较好。
壳聚糖湿法纺丝是壳聚糖纤维最常用的纺丝方法,随着近些年的发展,壳聚糖湿纺技术已日臻成熟,后续的研究还需要综合考虑纺丝液流变性能和纺丝条件的控制,使纺丝过程更加平衡稳定。图6是壳聚糖湿法纺丝流程示意图。
3.2 壳聚糖纤维力学性能的提高
力学性能不高的一直是壳聚糖纤维亟待解决的一个问题,为此科研工作者们进行了多种尝试。吴清基[38]等人通过对湿法纺丝机理的研究,发现降低凝固浴中凝固剂与溶剂的扩散系数对于形成结构均匀、具有良好拉伸性能好的初生纤维有利。由于无水乙醇的扩散系数为0.87×10-6cm2/s,远小于水的扩散系数(5.2×10-4cm2/s),因此可以在NaOH水溶液中添加适量乙醇,以减小扩散系数,进而得到力学性能好的壳聚糖纤维[39]。

图6 壳聚糖湿法纺丝流程示意图[37]:(1)压缩空气,(2)纺丝罐,(3)过滤装置,(4)凝固浴,(5,6)水洗浴Fig.6 Flow diagram of chitosan wet spinning[37]:(1)compressed air,(2)spinning pot,(3)filtering apparatus,(4)coagulation bath,and(5,6)washing bath
王载利等[3]从纺丝液的脱泡角度出发,针对壳聚糖溶液脱泡困难、效率低等问题,提出了动态脱泡与静态脱泡相结合的方法,大大缩短了纺丝原液的脱泡时间,并取得了良好的脱泡效果,为高力学性能壳聚糖纤维的纺制提出了一种新的思路。
有研究认为,壳聚糖纺丝液从喷丝孔流出后凝固成初生纤维时,不是脱水过多而是脱水过少。据此,提高拉伸前和拉伸时冻胶纤维中聚合体大分子含量应该是实现纤维强度增强的有效方法之一。郯志清等[39]则选择NaCl溶液代替水溶液作为拉伸浴组分,以提高壳聚糖纤维的取向度。
吉亚丽等[40]将甲壳素纳米晶体添加到壳聚糖溶液中,通过湿纺制得壳聚糖/甲壳素纳米复合纤维中,结果发现,一定量甲壳素晶体的加入不仅可以使得壳聚糖纤维的截面形貌得到改善,同时也提高了纤维的力学性能。Vladimir等[41]也采用了相同方法,通过在壳聚糖溶液中添加0~20%含量的甲壳素纳米晶体,获得强度提高的壳聚糖纤维。图7是带有不同含量甲壳素纳米晶的壳聚糖纤维的表面和横截面的SEM照片。图8是含有甲壳素纳米原纤的壳聚糖复合纤维结构示意图[41]。

图7 带有不同含量甲壳素纳米晶的湿纺壳聚糖纤维表面及横截面的SEM照片[40]:(a)0%,表面,(b)0%,断面,(c)2.5%,表面,(d)2.5%,断面,(e)5%,表面,(f)5%,断面,(g)10%,表面,(h)10%,断面Fig.7 SEM micrographs of surface and cross-section of chitosan wet-spun fiberswith ChiNC of various contents[40]:(a)0%,surface,(b)0%,section,(c)2.5%,surface,(d)2.5%,section,(e)5%,surface,(f)5%,section,(g)10%,surface and(h)10%,section
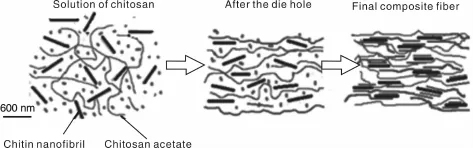
图8 含有甲壳素纳米原纤(黑色)的壳聚糖(灰色)复合纤维结构示意图[41]Fig.8 Schematic diagram of formation of the chitosan(grey)composite fiber structure containing chitin nanofibrils(black)[41]
壳聚糖材料在骨修复领域的潜力巨大,壳聚糖类材料不但可以促进细胞的分化,加速组织的形成,而且能够促进成骨细胞和软骨细胞的表型表达[42]。近年来,壳聚糖的静电纺丝得到了广泛的关注,利用静电纺丝得到的生物相容性好、细胞粘附性佳、力学性能好的壳聚糖纳米纤维在纤维支架及骨工程领域应用广泛。但纯的壳聚糖纳米纤维的力学强度很弱,不利于成骨细胞的粘附和增殖。将聚己内酯与壳聚糖和复合,利用静电纺丝得到纳米纤维的弹性模量得到很大提高,细胞粘附能力也很好[43]。
有关壳聚糖纤维力学性能提高的方法还有很多,后期可以围绕提高壳聚糖溶液浓度的提高,以及发展更合适的溶剂体系进行研究。同时将溶液性质与后期纺丝、后整理等结合,也是未来研究的重要方向。
3.3 长丝的探索
壳聚糖纤维研究开展以来,壳聚糖长丝的实现是个一直困扰科研工作者的难题。目前壳聚糖纤维仍局限于小量生产,无法生产长丝束,这不利于扩展壳聚糖纤维的应用。
目前多数壳聚糖纤维是用湿法纺丝或干湿法纺丝制得的,具体的过程为先将壳聚糖溶解在溶剂中,随后过滤、脱泡得到符合条件的纺丝液,经喷丝头挤出,随后在凝固浴中成型,拉伸浴中进行拉伸、洗涤,最终得到原丝。总结来看,壳聚糖长丝工业化面临的问题主要是纺丝液的制备工序复杂费时,纺丝效率不高[3]。为此,需要进行相关针对性工作。在纺丝方面,传统的纺丝方法(湿法纺丝或干湿法纺丝)生产的壳聚糖纤维可纺性差,存在着强度低、细度高、纤维易粘连、易产生短绒等缺陷,这对壳聚糖纤维的性能和外观造成了严重影响,同样也限制了纤维的应用。而水洗不充分、脱水困难、干燥较慢等生产过程中普遍存在的缺点也限制了壳聚糖长丝的实现。
有关壳聚糖长丝的研究工作目前还处在探索阶段,虽然冯淑芹等[44]采用离子液体溶剂溶解壳聚糖并进行纺丝,得到了一种力学性能较高的壳聚糖纤维,但壳聚糖长丝距离真正实现工业化还有很长一段路要走,这需要科研工作者们更进一步的探究。
4 结 语
现阶段,醋酸、离子液体均可较好地溶解壳聚糖,从溶解效果来看,两者各有利弊,为此需要在原有溶解体系的基础上进行改进工作,与此同时也可以寻求新型溶解体系,以促进壳聚糖溶解。壳聚糖材料的使用可以加快伤口的愈合,壳聚糖良好的生物相容性、生物可降解性、无毒、以及吸附螯合重金属的能力,使得其在组织工程支架、载药、伤口敷料、分离膜、支架涂层以及传感器等方面有着潜在应用。
壳聚糖长丝的研究目前仍处于起步阶段,距离工业化还有很长的一段路要走。作为一种具有优异性能的新材料,随着研究的深化和应用领域的拓展,相信纤维力学性能差的问题将得到解决,可以预见,壳聚糖将会发挥其巨大的应用潜力,但这些都还需要研究者付出艰辛的努力。
Re ferences
[1] Jeon Y J,ShahidiF,KIM SEK.Preparation of Chitin and Chitosan Oligomersand Their Applications in Physiological Functional Foods[J].Food Reviews International,2000,16(2):159-176.
[2] Jiang Tingda(蒋挺大).Chitosan(壳聚糖)[M].Beijing:Chemical Industry Press,2006.12:19.
[3] Wang Zaili(王载利).Key Production Technology to the Research and Development of Chitosan Filament(壳聚糖长丝束关键生产技术的研究开发)[D].Qingdao:Qingdao University,2011.
[4] Wanjun T,Cunxin W,Donghua C.Kinetic Studies on the Pyrolysis ofChitin and Chitosan[J].Polymer Degradation and Stability,2005,87(3):389-394.
[5] Peng Geng(彭 耿),Wang Jing(王 靖),Liu Changsheng(刘昌胜).葡聚糖/壳聚糖水凝胶的制备及其作为生长因子载体的研究[J].Materials China(中国材料进展),2013,10:599-604.
[6] Agboh O C,Qin Y.Chitin and Chitosan Fibers[J].Polymers for Advanced Technologies,1997,8(6):355-365.
[7] Yi H,Wu LQ,BentleyW E,etal.Biofabrication with Chitosan[J].Biomacromolecules,2005(6):2 881-2 894.
[8] Cho YW,Jang J,Park CR,et al.Preparation and Solubility in Acid and Water of Partially Deacetylated Chitins[J].Biomacromolecules,2000(1):609-614.
[9] Peniche C,Argüelles-Monal W.Overview on Structural Characterization of Chitosan Molecules in Relation with Their Behavior in Solution[J].Macromol Symp,2001,168:1-20.
[10] Li Xingke(李星科),Jiang Qixing(姜启兴),Xia Wenshui(夏文水).Study on Properties and Application of Rheology of Chitosan Solution Study(壳聚糖溶液的流变学性质及应用研究)[J].Scienceand Technology of Food Industry(食品工业科技),2011(02):65-68.
[11] Wu Guojie(吴国杰),Yao Ruhua(姚汝华).Study on the Rheological Properties of Chitosan Solution(壳聚糖溶液流变学性质的研究)[J].Journal of South China University of Technology(Natural Science)(华南理工大学学报(自然科学版)),1997(10):62-66.
[12] Han Huaifen(韩怀芬),Qian Junqing(钱俊青).Study on the Viscosity Changes of Shrimp,Crab Chitosan Solution(虾、蟹壳聚糖溶液粘度变化的研究)[J].Bulletin of Science and Technology(科技通报),1998(06):441-445.
[13] Yu Muhuo(余木火),Zhou Zhenglong(周征龙),Wu Xiuge(武秀阁),et al.Study on Viscosity Behavior of Chitosan Acetic Acid Solution(壳聚糖醋酸水溶液粘度行为的研究)[J]. Polymer Materials Science and Engineering(高分子材料科学与工程),1991(06):97-101.
[14] Rinaudo M,Pavlov G,Desbrieres J.Influence of Acetic AcidConcentration on the Solubilization of Chitosan[J].Polymer,1999,40:7 029-7 032.
[15] Pillai C K S,PaulW,Sharma C P.Chitin and Chitosan Polymers:Chemistry,Solubility and Fiber Formation[J].Progress in Polymer Science,2009,34(7):641-678.
[16] Zhang Suojiang(张锁江),Lv Xingmei(吕兴梅).Ionic Liquids:From Basic Research to Industry Application[M].Beijing:Beijing Scientific Press,2006:60-83.
[17] Domanska U,Bogel-Lukasik R.Physicochemical Properties and Solubility of Alkyl-(2-hydroxyethyl)-Dimethylammoniumbromide[J].The Journal of Physical Chemistry B,2005,109(24):12 124-12 132.
[18] Zhang Puyu(张普玉),Liu Yang(刘 洋),Peng Lichao(彭李超).RAFT法合成两亲性嵌段共聚物PSt-b-PAA-b-PSt及其在离子液体[BMIM][PF6]中的自组装[J].Acta Polymerica Sinica(高分子学报),2010(1):59-64.
[19] Zhu Ning(朱 宁),Ling Jun(凌 君),Xiao Kun(肖琨).ε-己内酯在咪唑型离子液体中开环聚合[J].Acta Polymerica Sinica(高分子学报),2009(8):838-840.
[20] Swatloski R P,Spear S K,Holbrey JD,et al.Dissolution of Cellose with Ionic Liquids[J].Journal of the American Chemical Society,2002,124(18):4 974-4 975.
[21] Hermanutz F,Gähr F,Uerdingen E,et al.New Developments in Dissolving and Processing of Cellulose in Ionic Liquids[C]//Proceedings of Macromolecular Symposia.2008,262(1):23-27.
[22] Kosan B,Michels C,Meister F.Dissolution and Forming of Cellulose with Ionic Liquids[J].Cellulose,2008,15(1):59-66.
[23] Sun Fan(孙 璠),Xu Ming(徐 民),Li Kerang(李克让),etal.甲壳素和壳聚糖在离子液体中的溶解与改性[J].Progress in Chemistry(化学进展),2013(05):832-837.
[24] Zhu Qingsong(朱庆松),Han Xiaojin(韩小进),Chen Chunzu(程春祖),et al.壳聚糖在4种咪唑型离子液体中溶解性的研究[J].Acta Polymerica Sinica(高分子学报),2011(10):1 173-1 179.
[25] DuanXianquan(段先泉),Xu Jigang(徐纪刚),Li Xiaojun(李晓俊),et al.离子液体在壳聚糖研究中的应用进展[J].Polymer Bulletin(高分子通报),2013(03):12-17.
[26] Cai Jie,Zhang Lina.Rapid Dissolution of Cellulose in LiOH/U-rea and NaOH/Urea Aqueous Solutions[J].Macromolecular Bioscience,2005,5(6):539-548.
[27] Qi H,Yang Q,Zhang L,et al.The Dissolution of Cellulose in NaOH-Based Aqueous System by Two-Step Process[J].Cellulose,2011,18(2):237-245.
[28] Hu X,Du Y,Tang Y,et al.Solubility and Property of Chitin in NaOH/Urea Aqueous Solution[J].Carbohydrate Polymers,2007,70(4):451-458.
[29] LiYouliang(李友良).Study on Novel Chitosan Materials Based on Alkali Solvent(基于碱性溶剂体系制备壳聚糖新材料的研究)[D].Hangzhou:Zhejiang University,2012.
[30] Zhou Junyu(周俊宇),Nie Jingyi(聂景怡),Li Youliang(李友良),et al.LiOH/尿素溶剂体系制备高强度壳聚糖水凝胶膜[J].Journal of Materials Science and Engineering(材料科学与工程学报),2013(04):525-528.
[31] Chen Xiong(陈 雄).Study of Chitosan Solution Behavior(壳聚糖溶液行为研究)[D].Beijing:Beijing Institute of Fashion Technology,2008.
[32] Li Weiyan(李维艳),Huang Lin(黄 林),Yang Peng(杨 朋),et al.壳聚糖在柠檬酸溶液中溶解行为研究[J].New Chemical Materials(化工新型材料),2011(11):121-123.
[33] Gao Guang(高 洸),Lin Minyi(林敏怡),Wu Guoming(邬国铭).壳聚糖纤维的成型[J].Journal of Textile(纺织学报),2005(02):41-43.
[34] Zhou Jiacun(周家村),Hu Guangmin(胡广敏).A Method of Industrial Preparation of Spinning Solution for Pure Chitosan Fiber(一种工业化生产纯壳聚糖纤维的纺丝液制备方法):China,ZL 2010 1 0166861.9[P].2010-05-10.
[35] Zhou Jiacun(周家村),Ma Jianwei(马建伟).Medical Chitosan Fiber and Its Preparation Method(医用壳聚糖纤维及其制备方法):China,ZL 2008 1 0015053.5[P].2010-05-10.
[36] Du Yuping(杜玉平).Research on High Performance Chitosan Fiber Key Preparation Technology(高性能壳聚糖纤维关键制备工艺的研究)[D].Qingdao:Qingdao University,2012.
[37] Ma B,Zhang M,He C,etal.New Binary Ionic Liquid System for the Preparation of Chitosan/Cellulose Composite Fibers[J]. Carbohydrate Polymers,2012,88(1):347-351.
[38] Wu Qingji(吴清基),Qi Bofu(祁波夫),Zhu Jiemin(朱介民).高强高模聚乙烯醇纤维的研制[J].Journal of Chinese Textile University(中国纺织大学学报),1993,19(06):37-46.
[39] Tan Zhiqing(郯志清),Shen Xinyuan(沈新元),Zhao Jiongxin(赵炯心),et al.壳聚糖纤维的制备及应用[J].Knitting Industry(针织工业),2002(4):44-46.
[40] Yan W,Shen L,Ji Y,et al.Chitin Nanocrystal Reinforced Wet-Spun Chitosan Fibers[J].Journal of Applied Polymer Science,2014,131(19).
[41] Yudin V E,Dobrovolskaya IP,Neelov IM,et al.Wet Spinning of Fibers Made of Chitosan and Chitin Nanofibrils[J]. Carbohydrate Polymers,2014,108:176-182.
[42] Jiao Yanpeng(焦延鹏),Li Lihua(李立华),Luo Binghong(罗丙红),et al.壳聚糖对骨组织工程中组织修复的影响[J]. Materials China(中国材料进展),2012(09):35-39.
[43] Lei Bo(雷 波),Ma Xiaolong(马晓龙).仿生纳米纤维支架促进骨组织再生[J].Materials China(中国材料进展),2013,10:583-590.
[44] Feng Shuqin(冯淑芹),Miao Hangen(缪汉根),Tang Junsong(唐俊松),et al.A Kind of Chitosan Filament and Its Preparation(一种壳聚糖长丝及其制备方法):China,CN 103409850[P].2013-11-27.
Progress in the Research of Chitosan Dissolution Behavior and Its Fibers
Y
ANG Junjie1,HU Guangmin2,XIANG Hengxue1,MAO Yuchen1,ZHANG Junyan1,ZHU Meifang1
(1.College of Materials Science and Engineering,State Key Laboratory for Modification of Chemical Fibers&Polymer Materials,Donghua University,Shanghai201620,China)(2.Shandong Hismer Biological Technology Co.,Ltd.,Tai’an 271400,China)
In recent years,with the developmentof natural polysaccharide in the field ofmaterial,cellulose and chitosan have attracted wide attention.Because of its excellent biocompatibility,biodegradability and antibacterial properties,chitosan has attracted attention ofmany researchers,great progress has beenmade in themedical,food,environmental engineering and many other fields.This paper starts from the solution properties of chitosan,introducing the influence of deacetylation degree,molecularweight,temperature and other factors on chitosan solution behavior respectively,focusing on the introduction of chitosan dissolution using acetic acidandionic liquid,summarizing the wet spinning of chitosan,as well as themethods to improve the performance of fiber and the possibility of filament realizing.Finally,the future development of chitosan and its fiber products are prospected.
solution property;chitosan fibers;mechanical properties
O631
A
1674-3962(2014)11-0641-08
2014-10-20
长江学者和创新团队发展计划(IRT1221,T2011079)
杨俊杰,男,1993年生,博士生
朱美芳,女,1965年生,教授,博士生导师,Email:zm f@dhu.edu.cn
10.7502/j.issn.1674-3962.2014.11.01
