混合溶液中硫酸根离子浓度测定方法的改进
2014-05-10冯瑞
冯 瑞
( 河南南阳医学高等专科学校,河南 南阳 473058)
混合溶液中硫酸根离子浓度测定方法的改进
冯 瑞
( 河南南阳医学高等专科学校,河南 南阳 473058)
采用一种改进的乙二胺四乙酸(EDTA)滴定方法检测硫酸根离子浓度,可以同时消除钙、镁及碳酸根离子、磷酸根离子等的干扰。该方法操作简单,适用范围较广,分析结果准确度高,是一种经典的容量分析法。
乙二胺四乙酸(EDTA);硫酸根离子;滴定法;容量分析法
由于硫酸及其可溶性盐在工业上的广泛应用,使得SO42-浓度的准确测定成为一个经常需要解决的问题。通过查阅相关文献可知,目前测定SO42-的方法主要有硫酸钡重量法[2]、吸光比浊法[3]、分光光度法[4]。由于这些分析方法操作步骤繁琐,干扰因素多,可行性差,因此不能广泛应用于对混合物溶液中的SO42-浓度进行定量分析,传统的EDTA(乙二胺四乙酸)滴定法[5]也有很多弊端。本文采用的是一种改进的EDTA滴定法,优点在于测定中不受其它共存离子如Ca2+、Mg2+、 CO32-、PO43-等的影响,可以对含有多种离子的混合溶液中的硫酸根离子浓度进行测定。
1 实验部分
1.1 仪器
20.00mL移液管,250mL的锥形瓶,加热和过滤装置,25mL的滴定管,1000mL容量瓶。
1.2 试剂及配制
待测溶液(SO42-约为0.02mol·L-1);1∶1的乙醇、浓盐酸混合液;氨性缓冲溶液(pH=10)。
氯化钡溶液(0.5mol·L-1):将122g BaCl2·2H2O溶于600mL水中,加热,冷却,然后将溶液稀释到1L,贮存备用。
EDTA标准溶液(浓度约为0.05mol·L-1):称取18.6125g EDTA, 溶于少量的水中,转入1000mL的容量瓶中,再加蒸馏水稀释至标线。
铬黑T指示剂:称取0.5g的铬黑T,加100g固体氯化钠,研磨均匀后贮存于棕色瓶中,装塞备用。
氯化镁溶液(0.05mol·L-1):将10.1500g的MgCl2·6H2O,先加适量的水溶解,冷却,然后将溶液稀释到1L,贮存备用。
1.3 基本原理
依据容量分析法的基本原理,利用配位滴定中的返滴定法[6],用适当过量的Ba2+完全沉淀待测的混合物溶液中的SO42-,使SO42-完全转化为BaSO4沉淀;将硫酸钡沉淀分离、净化后,用已知过量的EDTA标准溶液定量地络合硫酸钡沉淀中的钡离子,使硫酸钡沉淀完全溶解;再用MgCl2标准溶液返滴定过量的EDTA,用铬黑T作指示剂,可计算出待测的混合物溶液中硫酸根离子的浓度及含量。
1.4 实验步骤
用移液管准确移取20.00mL配制好的、硫酸根离子浓度约为0.02mol·L-1的待测溶液,置于250mL的锥形瓶中,加适量的蒸馏水稀释。
若待测溶液中含有六价铬、七价锰等氧化性的有色离子,为了减少它们对随后硫酸钡沉淀净化时的干扰以及对返滴定时指示剂显色的影响,可加入理论量约5倍的乙醇(1∶1的乙醇、浓盐酸混合液),在80~90℃左右保温约10~15min,以将它们还原。
乙醇在酸性条件下还原六价铬的反应为:
3CH3CH2OH+Cr2O72-+8H+→3CH3CHO+2Cr3++7H2O
整个还原过程应尽量避免乙醇和氯化氢气体的挥发。
往待测溶液中加入2mL的盐酸溶液,加热到60~80℃左右,在不断搅拌下,慢慢地加入浓度为0.5mol·L-1的氯化钡溶液10mL,放置1h,使硫酸钡沉淀充分陈化,用紧密型滤纸过滤沉淀,并用经过盐酸酸化的热水,将锥形瓶及沉淀洗涤至无钡离子(用稀硫酸检测滤液,滤液中加稀硫酸无白色沉淀出现)为止。
将洗净的沉淀和滤纸一起放回原锥形瓶中,准确地加入浓度为0.05mol·L-1左右的EDTA标准溶液25.00mL及适量的蒸馏水,用氨水将溶液的pH值调整到10左右(可以用氨水和稀盐酸进行调节);慢慢加热到60~80℃,搅拌至沉淀完全溶解;冷却后,再用氨水将溶液的pH值调整到10左右,以铬黑T为指示剂,用浓度为0.05mol·L-1的氯化镁标准溶液(先用EDTA标准溶液进行标定),滴定至溶液颜色由蓝色变为红色为终点。
2 实验结果讨论
2.1 结果计算
硫酸根离子浓度按下式计算:待测溶液中硫酸根离子的浓度/(g·L-1)=(M1V1-M2V2)× 4.8式中:M1为EDTA标准溶液的浓度,mol·L-1;V1为加入EDTA标准溶液的体积,mL;M2为氯化镁标准溶液的浓度,mol·L-1;V2为加入氯化镁标准溶液的体积,mL。
根据所得到的待测溶液中硫酸根离子的浓度,可以进一步换算出待测物中硫酸根离子的含量。
2.2 讨论
2.2.1 待测溶液的取样量
本实验要求待测溶液中硫酸根离子的浓度为0.02mol·L-1,并取20.00mL待测溶液进行分析,是为了使整个分析过程符合定量分析的要求,减小分析误差,否则硫酸钡沉淀在氨性EDTA中溶解不完全,会使硫酸根离子测定的结果偏低。取样的多少用氯化钡溶液来略测待测溶液中硫酸根离子的含量,若开始滴加时出现少量浑浊(硫酸根离子浓度小于5×10-4mol·L-1),要增加待测溶液取样量。如果开始滴加就出现沉淀,则应该减少待测溶液的取样量。
2.2.2 影响沉淀物纯度的因素
影响沉淀物纯度的因素有很多,主要有待测溶液的浓度、温度、搅拌、陈化的时间等,具体影响[7]见表1。

表1 沉淀条件对沉淀物纯度的影响
从表1可以看到,本实验中需要注意的问题:
1) 在适当稀的热溶液中,在不断搅拌的条件下,缓慢地加入稀的沉淀剂,使沉淀缓慢、均匀地产生,这样可以避免产生局部过饱和的问题,可以得到粗大纯净的晶形沉淀。
2) 为了防止继沉淀现象的发生,缩短陈化时间,本实验陈化的时间约为1h,沉淀后稍搅拌一定时间就立即分离。
3) 本实验沉淀时加热温度控制在60~80℃,沉淀后经过盐酸酸化的热水洗涤沉淀是减少表面吸附的有效方法,可以减少共沉淀现象,提高沉淀物的纯度。
3 改进后的实际检验
取5种分别含有2~6种不同离子的混合液,5种样品中的ρSO42-=1920.00mg·L-1(CSO42-=0.02mol·L-1)用本方法进行实际检验,结果见表2。
从表2可见,不同离子在SO42-相同的混合溶
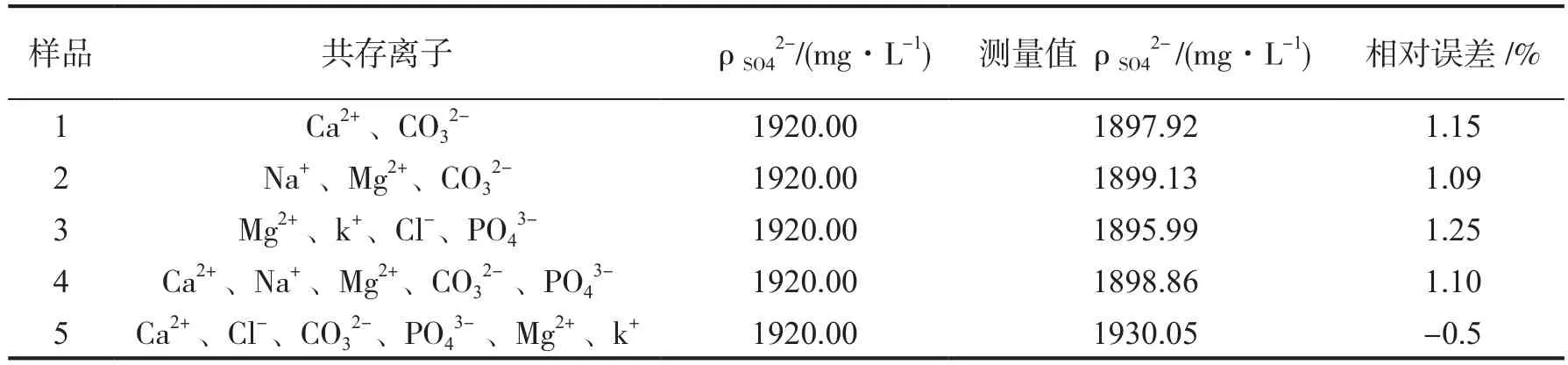
表2 用改进的EDTA滴定法测定含有不同离子溶液中的SO2-4
液中,采用上述改进的EDTA滴定法,方法可行,并且相对误差在-0.5%~1.25%之间,准确度高,符合实际需要。
4 结语
改进后的EDTA滴定法在不受其它共存离子的影响下,可以有效地对含有多种离子混合溶液中的硫酸根离子浓度进行测定。方法简单,适用范围较广,准确度高,是一种较好的分析方法。
[1] 王晋强.水分析方法实验汇编[M].北京:地质出版社,1985.
[2] GB 11899-89,水质 硫酸盐的测定 重量法[S].
[3] 宋金如,刘淑娟,朱霞萍.测定水中硫酸根方法的概述[J].华东地质学院学报,2002,25(2):64-67.
[4] 李源流,李军,张永福,等.分光光度法测定油田水样中的硫酸根离子[J].应用化工,2008,37(5):579-581.
[5] 叶向红,张彩云.EDTA测定法测定草酸中硫酸根[J].光谱实验室,2005,22(4):750-752.
[6] 华中师范学院,等.分析化学[M].北京:人民教育出版社,1981.
[7] 武汉大学,等.分析化学[M].北京:人民教育出版社,1986.
Improved Method for Determination of Sulfate Ion in Mixed Solution
FENG Rui
(Nanyang Medical College , Nanyang 473058, China)
EDTA titration method had been improved to determine ssulfate ion, the interference of Ca2+、Mg2+and CO2-and PO3-34could be eliminated.
ethylenediamine tetraacetic acid; sulfate ion; titration method; volumetric analysis
O 655.2
A
1671 -9905(2014)08-0044-02
冯瑞(1975-),女,讲师,硕士,主要有机合成及应用方面的研究,电话:13525107689,E-mail:fengrui20032006@163.com
2014-07-04
