薄层色谱法用于确定维生素B6合成过程反应终点
2014-05-10黎丹娜丘天凤
韦 勤,卢 红,黎丹娜,梁 飞,丘天凤,陆 欣
(广西化工研究院,广西 南宁 530001)
实验室与分析
薄层色谱法用于确定维生素B6合成过程反应终点
韦 勤,卢 红,黎丹娜,梁 飞,丘天凤,陆 欣
(广西化工研究院,广西 南宁 530001)
以硅胶加烧石膏(占15%)作为吸附剂,正丁醇∶醋酸∶水(60∶15∶25)为展开剂,3%茚三酮乙醇溶液为显色剂,采用薄层色谱法确定合成维生素B6中酯化和酰化反应的终点。结果表明,该方法设备、操作简单,速度快,受温度影响小,灵敏度高,用于确定合成维生素B6酯化反应和酰化反应终点明显,可操作性强。
维生素B6;酯化反应;酰化反应;终点;薄层色谱法
维生素B6具有广泛的生理作用,是人体必需的维生素之一[1-3]。维生素B6又称吡哆素,是一种水溶性维生素,遇光或碱易破坏,不耐高温。通常其分析方法有色谱法[4-5]、聚硫堇/亚铁氰根修饰碳糊电极法[6]、分光光度法[7]、荧光法[8]、微生物法[9]等。
维生素B6的合成工艺有 唑法和吡啶酮法等,本实验采用 唑法生产。工艺流程大致为:将氨基丙酸和盐酸投入成盐锅,在一定的温度下保温,减压蒸去酸水至锅内物呈乳白色固状;稍冷加入乙醇溶解固状物,用泵打到酯化锅然后加入定量的苯、乙醇进行三元共沸脱水酯化反应,当分水器有水分出时,开始滴加定量的苯、乙醇混合物,滴加速度大致与分水器速度相等,乙醇滴加完毕,继续回流一定时间(根据分析结果确定),加入催化剂磷酸,继续带水至锅内酯化液水分≤0.5%(W/V),然后常压加收苯醇至锅温90℃停止。将上述所得的酯化液抽入干燥的草酰化锅,加入草酸二乙酯,分次加入小苏打,然后升温至50℃保温反应一定时间(根据分析结果确定),得到N-草酰物。薄层色谱法[10-12]常用于中药材的薄层鉴别,具有设备简单,操作方便,分析速度快,灵敏度高,选择性好,固体相和流动相的选择范围大等优点。我们在合成维生素B6中,酯草工序难以确定酯化反应和酰化反应的终点。酯草工序有成盐反应、酯化反应和酰化反应,成盐反应很快就完成,但酯化反应和酰化反应的终点则难以确定。本文通过大量的实验,筛选出一种简易的薄层色谱法,并将该法用于化学药品合成过程中的分析。结果表明,薄层色谱法比用高效液相法分析速度快,投入成品低,且该方法设备、操作简单,灵敏度高,可用于维生素B6合成过程反应终点的确定。
1 仪器和试剂
载玻片、研钵、展开槽、干燥烘箱。
酯化液、酰化液、中性氧化铝、硅胶、烧石膏、正丁醇、醋酸、茚三酮、乙醇。
2 实验部分
2.1 吸附剂(载体)的选择
选择载体,必须同时兼顾所用展开剂与分离物质三者的关系。针对被分离物的性质,在众多的吸附剂中,分别选用中性氧化铝和硅胶作吸附剂加入烧石膏(占吸附剂的15%)为粘合剂制成薄层板,活化条件为105℃,30min。实验结果见表1。从表1可看出,活性为Ⅳ级的硅胶分离效果最好。
2.2 展开剂的选择
选用合适的展开剂,可使各成分恰当地分离,方便对各成分进行定量,确定反应的终点。要将吸附剂的活性,被分离化合物的极性和溶解性,以及展开剂的极性三方面的因素结合起来考虑。被分离化合物有丙氨酸盐酸盐和酯化物等,综合各因素,选用了正丁醇、醋酸和水3种溶剂按一定比例组成的溶剂系统作为展开剂,实验结果见表2。从表2可看出,展开剂为正丁醇∶醋酸∶水=60∶15∶25时,斑点显色效果最佳。
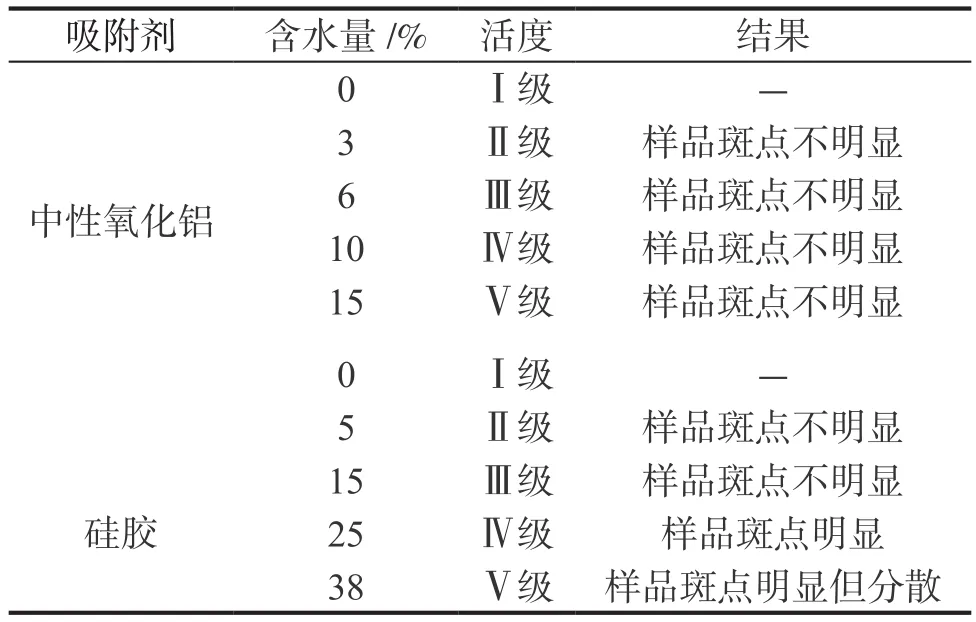
表1 吸附剂的选择

表2 展开剂的选择
2.3 显色剂的选择
生物碱指示剂中,选择麻黄生物碱类常使用的3%茚三酮乙醇溶液作指示剂,经过与2.1和2.2同步试验,结果显色明显。
2.4 实验样品测定
采用自制薄层硅胶G板(15cm×20cm玻璃棉板),课题组自制样品,按表3所列时间取样,用毛细管在离边缘1.5cm处点样,放入展开槽中约10min后展开,取出,放在干燥箱烘干,然后用3%的茚三酮乙醇溶液显色,在105℃加热约5 min,观察显色斑点。Rf=0.5处为丙氨酸盐酸盐斑点,Rf=0.7处为酯化物斑点,均显紫红色。
3 实验结果与讨论
采用薄层色谱法分析,以硅胶加烧石膏(占 15%)作为吸附剂,正丁醇∶醋酸∶水(60∶15∶25)为展开剂,3%茚三酮乙醇溶液为显色剂,在维生素B6合成中,在乙醇滴加完后第4h,Rf=0.5处无斑点,Rf=0.7处斑点明显,表明酯化反应结束;最后一次加入小苏打后第9h,Rf=0.5处无斑点,Rf=0.7处几乎看不见斑点,表明酰化反应结束。
4 结论
1)以硅胶加烧石膏(占15%)作为吸附剂,正丁醇∶醋酸∶水(60∶15∶25)为展开剂,3%茚三酮乙醇溶液为显色剂,进行薄层色谱分析,所显的斑点位置和颜色最佳。
2)采用薄层色谱分析法确定合成维生素B6中酯草工序酯化和酰化反应的终点方法可行,该方法设备、操作简单,速度快,受温度影响小,灵敏度高,可操作性强。
[1] 鲁昌盛.维生素B6的临床应用[J].检验医学与临床,2008(6):374-375.
[2] 杨军,侯雨梅.维生素B6的临床应用[J].中华现代临床医学杂志,2007(3):260.
[3] 白海青,王净华,王大博,等.维生素B1和B6对低血糖导致视网膜神经元损伤的保护作用[J].眼科研究,2008,26(5):373-376.
[4] 孙清,巴晓革,史磊. HPLC法同时测定更年安软胶囊中维生素B1、维生素B6的含量[J].药物分析杂志,2011,31(4):725-727.
[5] 贺霞,史朝晖,刘慧,等.反相离子对色谱法测定复方维生素片中3种水溶性维生素的含量[J].中国新药杂志,2012,21(22):2697-2700.
[6] 顾玲,张苗,贺亚梅.聚硫堇/亚铁氰根修饰碳糊电极的研制及其在维生素B6测定中的应用[J]. 理化检验-化学分册,2013(5):521-525.
[7] 张银梅,乌日汗.分光光度法测定维生素B6软膏的含量[J].内蒙古医学杂志, 2013,45(10):1171-1172.
[8] 谢秀娟,张振新.离子液体双水相萃取荧光法测定维生素B6[J].分析科学学报, 2011,27(4):513-515.
[9] 陈亚波,周敏,杨彤.微生物法测定维生素饮料中的维生素B6[J].安徽农业科学, 2013,41(12):5502-5503.
[10] 唐延国.中成药薄层色谱[M].北京:人民卫生出版社,1995:435-436.
[11] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010.
[12] 李俊锁,等.兽药残留分析[M].上海:上海科学技术出版社,2002:140-141.
Determination of Reaction End Point of Vitamin B6 Synthesis by Thin-layer Chromatography
WEI qin, LU hong, LI Dan-na, LIAN Fei, QIU Tian-feng, LU Xin
(Guangxi Research Institute of Chemical Industry,Nanning 530001,China)
Used silica gel and bassanite (15%) as absorbent, n-butyl alcohol : acetic acid : water(60:15:25) as developing solvent, 3% ninhydrin ethanol solution as color-developing agent,the end point of esterification and acylation reaction in synthesis of vitamine B6 was determined by thin-layer chromatography. The test result showed that this method was easy, rapid, simple equipment, little temperature influence, high sensitive and operability. The esterification and acylation reaction endpoint was clear.
vitamine B6; esterification; acylation reaction; end point; thin-layer chromatography
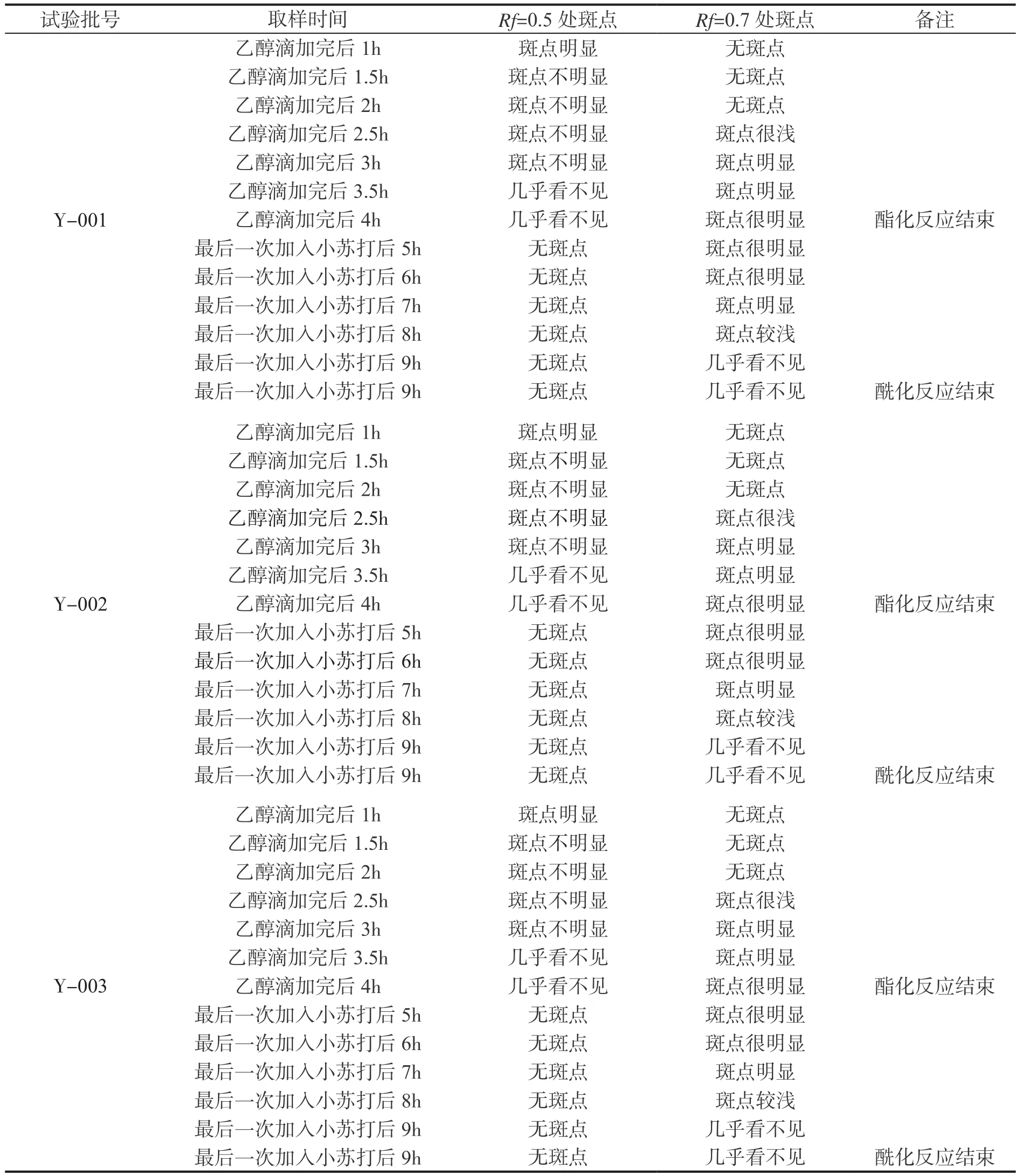
表3 样品测定结果
O 657.7
A
1671-9905(2014)08-0041-03
韦勤(1964-),女,高级工程师,主要从事原料药工艺和检测研究。E-mail: 952849588@. qq .com
2014-07-03
