模拟地下水中重碳酸盐浓度对零价铁还原硝基苯的影响
2014-05-09张海涛
张 娜,陈 日,张海涛,洪 梅
(吉林大学,地下水资源与环境教育部重点实验室,吉林 长春130021)
模拟地下水中重碳酸盐浓度对零价铁还原硝基苯的影响
张 娜,陈 日,张海涛,洪 梅*
(吉林大学,地下水资源与环境教育部重点实验室,吉林 长春130021)
通过静态试验研究了重碳酸盐浓度在0,100,300,500,800mg/L时对零价铁还原硝基苯的影响,检测反应过程中硝基苯和苯胺的浓度变化,同时检测溶液中pH值、Eh、Fe2+、CO32-的变化,结果表明,重碳酸盐浓度较低(100~500mg/L)时对零价铁还原硝基苯有促进作用,且促进作用随着重碳酸盐浓度的升高而增强.重碳酸盐浓度为500mg/L的反应体系中硝基苯去除率及苯胺生成率最高分别为88%,173mg/L,且在该体系中重碳酸盐对pH值的缓冲能力最强、Eh下降幅度最大,Fe2+浓度最高.重碳酸盐浓度为800mg/L的体系不利于硝基苯的还原.
重碳酸盐;零价铁;硝基苯
零价铁渗透反应墙(Fe0-PRB)技术已经成为处理地下水有机污染的研究热点[1-3].目前对Fe0-PRB的研究多侧重于零价铁粒径、介质类型、污染物的浓度、与微生物的协同作用等因素的影响[4-16],但是对于地下水中的阴阳离子对零价铁的活性影响研究比较少.
在Fe0-PRB长期运行过程中,零价铁的腐蚀会导致地下水的 pH值升高,在碳酸盐存在的条件下,易在铁表面形成各种沉淀物,这些沉淀物有可能会影响Fe0的活性,从而影响PRB的运行性能.重碳酸根作为地下水中主要的阴离子,其对Fe0-PRB 的活性的影响比较复杂[17-26].Liu等[27]对地下水中无机阴离子(Cl-、SO42-和HCO3-)对零价铁还原有机污染物的研究中,发现当 pH值为8.9~10.2时,重碳酸根对零价铁的抑制作用最强.Devlin等[3]报道了pH值为10时,离子强度为8mmol/L的 SO2-、Cl-、ClO-、NO-和 HCO-4433对零价铁还原四氯硝基苯的影响,SO42-和 Cl-促进反应的进行,ClO-对反应影响不大,而 NO-和43HCO3-抑制零价铁还原四氯硝基苯.Su等[28]研究地下水中含氧阴离子对零价铁去除砷酸盐的影响,认为碳酸盐类沉淀物会覆盖零价铁表面,阻碍电子的传递.Dong等[29]考查了地下水化学组分对零价铁还原硝基苯的影响发现,发现重碳酸盐在低浓度时可以促进零价铁的反应活性,高浓度时会抑制零价铁还原硝基苯.也有研究提及若体系中存在大量的重碳酸盐时,会在零价铁表面产生某种氧化还原活性相物质,且该物质不会降低零价铁的反应活性,可以在污染物与零价铁之间传递电子[30-31].
本文通过研究不同浓度的重碳酸盐对零价铁还原硝基苯的影响,分析反应过程中产生的化学变化,以期对Fe0-PRB的长期运行性能的评估提供理论依据.
1 材料与方法
1.1 材料
零价铁(铁含量为99.98%,粒径1~2mm)、NaHCO3(分析纯)、硝基苯(分析纯)、纯净水
1.2 实验步骤
取5份相同体积的去离子水于密闭容器中,曝气20~30min,使水中的溶解氧≤0.5mg/L,然后在绝氧(通 N2)的条件下加入等量的硝基苯溶液,使各个密闭容器中的硝基苯溶液的浓度为400mg/L左右,密封好,然后将密闭容器放置于恒温(25℃)厌氧摇床,使硝基苯溶于去离子水中,24h后取出,测量硝基苯的初始浓度C0,投加相同量的零价铁,重碳酸盐的浓度为0,100,300,500,800mg/L,具体方法如表1所示.定时取样分析体系中的 Eh、pH值的变化、Fe2+浓度的变化、CO32-、硝基苯和苯胺的浓度.

表1 不同反应体系中重碳酸盐的浓度Table1 The concentrations of bicarbonate in different systems
1.3 分析方法
硝基苯、苯胺的浓度采用岛津GC-2010气相色谱仪分析.色谱分析条件:DB-1毛细管柱(30m×0.25μm×0.25mm).进样口温度200℃;载气:氮气;FID检测器,检测器温度220℃.升温程序:初始温度60℃,保持2min,以5℃/min的速度升温至105℃,保持1min;进样量为1μL;分流进样,分流比为2:1.
pH值、Eh用便携式pH-Eh仪检测; CO32-采用酸标准溶液滴定法测定.
反应后的沉淀产物采用 D/MAX2500PC型X射线粉末衍射仪分析,其主要参数:18KW旋转阳极 铜靶 石墨单色器;500mg/L体系沉淀物的2θ角测试范围10~60°,扫描速度为5°/min;800mg/L体系沉淀物的2θ角测试范围20~100°,扫描速度为20°/min.测角仪半径285mm、测角仪测角精度优于0.01°2θ,最大分辨率0.06°2θ.
2 结果与讨论
2.1 溶液的硝基苯和苯胺随时间的变化
在厌氧条件下,在含有重碳酸盐及硝基苯的体系中,零价铁还原硝基苯的反应基本原理如下所示:
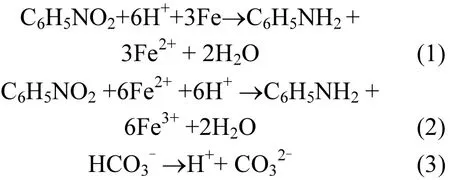
图1为硝基苯浓度变化曲线,各个反应体系中的硝基苯得到还原,反应进行600h时,0,100,300,500,800mg/L的重碳酸盐体系中硝基苯的去除率分别为65%、75%、88%、97%和45%,由此可见体系中重碳酸盐浓度低于500mg/L时,对硝基苯的还原有促进作用,促进作用大小为500mg/ L>300mg/L>100mg/L.体系中加入重碳酸盐后,首先发生反应(3),HCO3-电离产生H+,促进反应(1)和反应(2)的进行,从而促进硝基苯的还原.重碳酸盐浓度为800mg/L时,硝基苯的去除率低于未加入重碳酸盐的体系,说明800mg/L的重碳酸盐对硝基苯的还原具有抑制作用,这可能是由于体系中生成了过多的CO32-,与Fe2+生成了较多的碳酸盐沉淀,覆盖了零价铁的活性位点,抑制了反应(1),致使硝基苯的去除受到限制.
由图1可见,在反应前期120h内,硝基苯的浓度下降明显,120h后硝基苯下降速度明显变缓,出现这种现象的原因可能是由于零价铁表面反应位点的饱和以及零价铁表面沉淀物的覆盖造成的.因此为了更好的描述还原反应过程中,硝基苯还原速率与重碳酸盐质量浓度之间的关系,选择具有代表性的前120h的数据进行拟合.拟合结果见表2.
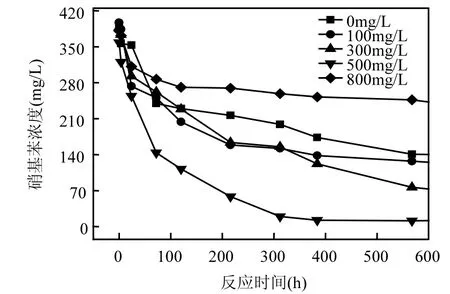
图1 溶液中硝基苯浓度的变化曲线Fig.1 Changes of nitrobenzene concentration in the solution with the time change
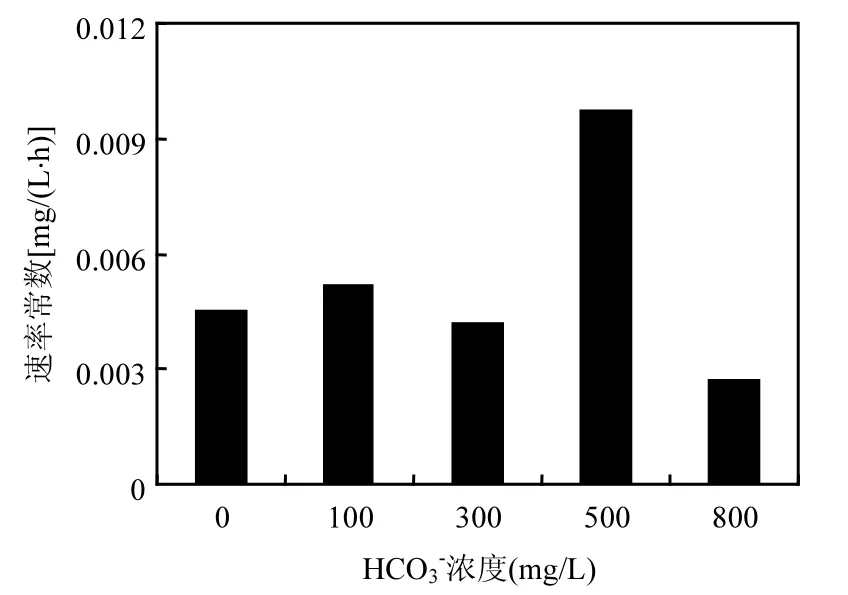
图2 反应速率与重碳酸盐浓度的关系Fig.2 Relationship between reaction rate and bicarbonate concentrations
由表2可以看出,反应体系中硝基苯还原过程均符合一级动力学方程.在不同反应体系中,硝基苯还原反应速率常数依次为0.0045,0.0052,0.0042,0.0097,0.0027mg/(L⋅h),可见重碳酸盐质量浓度为500mg/L的体系硝基苯还原速率最大,为0.0097mg/(L⋅h).由图2可以看出,当重碳酸盐浓度<500mg/L 时,反应速率常数随着重碳酸盐浓度的增加而增加,重碳酸盐浓度为800mg/L时,反应速率常数最小,还原反应速率变慢,所以当重碳酸盐浓度较大时,不利于硝基苯的还原.

表2 重碳酸盐浓度对硝基苯还原动力学的影响Table2 Effects of bicarbonate concentrations on the reduction kinetics of nitrobenzene
图3为反应体系苯胺浓度随时间的变化曲线.随反应的进行,各反应体系中苯胺的浓度逐渐升高,反应进行到856h,0,100,300,500,800mg/L的体系中苯胺的浓度分别为62.7,74,94.8,173.5,34.4mg/L,苯胺的生成反映了硝基苯的去除效果,重碳酸盐浓度≤500mg/L时,苯胺的生成速度随 HCO3-的浓度增加而升高,硝基苯的去除率也随之增强.

图3 溶液中苯胺浓度的变化曲线Fig.3 Changes of the concentration of aniline in the solution
由图1和图3可以看出苯胺的浓度增加变化与硝基苯的浓度减少变化趋势相符.根据Scherer[33]的研究在 Fe0还原硝基苯过程中,根据反应机理:

在体系中可能会产生中间产物亚硝基苯和硝基苯胺,但这两种物质存在时间短,在反应过程中未检测到这两种物质.
2.2 体系中pH值和Eh的变化曲线
图4为反应体系中pH值的变化情况,5个反应体系中pH值在反应开始100h内升高,当反应进行200h后,pH 值基本保持平稳.0,100,300,500,800mg/L的体系在反应1400h后,pH值分别达到10.5、10.35、9.5、9.05、9.0,pH值升高主要是由于硝基苯在还原过程中需要消耗大量H+.500,800mg/L的反应体系pH值变化幅度相较于其他体系偏小,pH值由6.67上升到9.0左右,这主要是由于高浓度的 HCO3-电离产生较多的H+,具有较强的缓冲作用,使体系的pH值升高幅度较小.
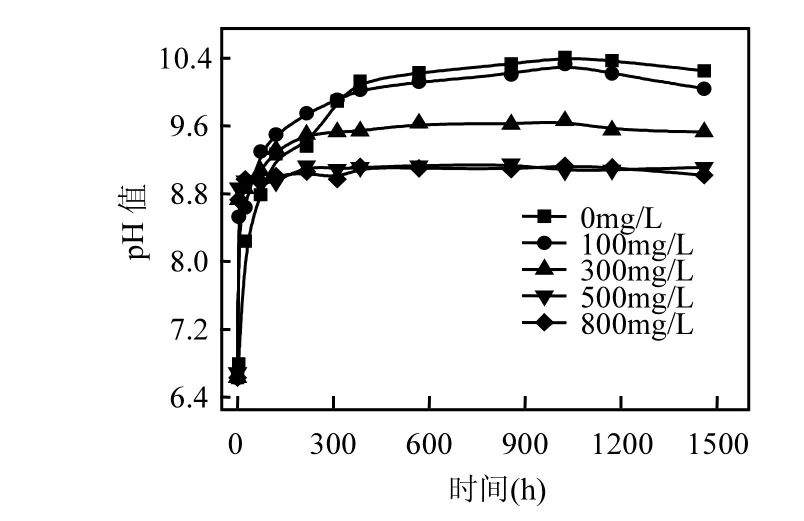
图4 重碳酸盐浓度对溶液pH值的影响Fig.4 Effects of bicarbonate concentrations on the pH of solutions
图5为反应体系中Eh的变化曲线,由图5可知,各体系的氧化还原电位在反应50~70h时降到最低,100~200h内Eh又逐渐升高,200h以后氧化还原电位趋于平稳.体系中加入零价铁后,立即发生反应(1),硝基苯被还原,氧化性物质减少,所以 Eh降低.在0~50h,500mg/L体系Eh最低,硝基苯还原速率也最大;0、100、300、800mg/L体系Eh变化规律相近,硝基苯的还原速率也相近.50~800h,500mg/L体系Eh的波动范围为-20~-50mV,为所有体系中的最低值,硝基苯的还原相较于其它体系也保持着较高的速率.800mg/L体系中 Eh一直保持着较高值,在27 ~54mV之间波动,其硝基苯的去除率也最低,可能是由于在零价铁表面的沉淀物,覆盖了零价铁表面的反应活性位点,阻碍了零价铁与硝基苯之间的电子传递即反应(1),体系中硝基苯剩余的多,所以Eh值较其他体系偏高.
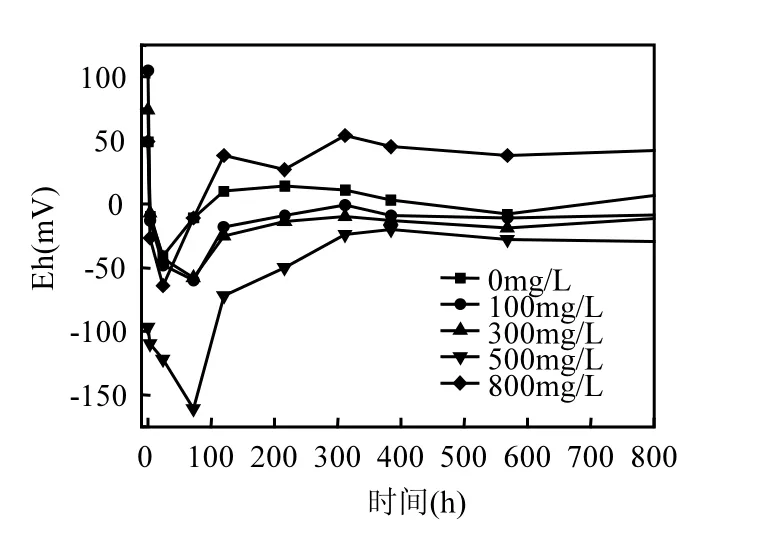
图5 重碳酸盐浓度对溶液Eh的影响Fig.5 Effects of bicarbonate concentrations on the Eh of solutions
2.3 体系中Fe2+浓度的变化
图6为体系中Fe2+的浓度变化曲线.反应开始12h内,各个体系中 Fe2+的浓度逐渐升高,500mg/L的体系中Fe2+生成的最多,浓度最高时达到2.18mg/L.12h后Fe2+浓度逐渐降低,反应进行到150h后趋于稳定.0~50h硝基苯维持了较高的还原速率,50h后还原速率降低,同时Eh开始升高, Fe2+的含量降低,说明体系中还原性物质Fe2+参与了反应(2),Fe2+被氧化为 Fe3+,同时 Fe2+与溶液中的CO32-及OH-离子结合形成铁的碳酸盐沉淀和氢氧化物沉淀,导致Fe2+浓度下降.因此可以推断在反应的0~50h以反应(1)为主,50h后以反应(2)为主.

图6 Fe2+浓度随时间的变化Fig.6 Changes of the concentrations of Fe2+in solution with the time change
2.4 体系中碳酸根的浓度变化
图7为碳酸根浓度的变化曲线,体系中HCO3的浓度越高,CO32-的浓度越高.0~25h是CO32-浓度快速上升时期,反应到25h后,CO32-浓度基本稳定.CO32-生成途径主要是反应(3), HCO3-发生电离反应,生成CO32-及H+,产生的H+参与硝基苯还原过程(1)(2),氢离子的消耗又促进反应(3)的进行,使溶液中的 CO32-不断增多,同时硝基苯得到还原.而800mg/L体系中 CO32-浓度最高,Fe2+可与 CO32-结合形成 FeCO3沉淀,覆盖零价铁表面的反应活性位点,不利于硝基苯的还原即反应(1).
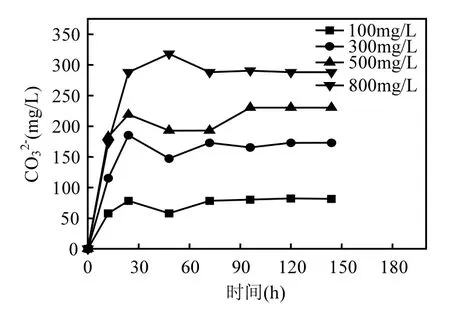
图7 溶液中碳酸根浓度变化曲线Fig.7 Changes of carbonate concentration variation in the solution
2.5 反应体系的沉淀产物进行X射线衍射分析
根据前述分析的反应过程,在体系中可能产生的沉淀物质为 FeCO3、Fe(OH)2、Fe(OH)3,在反应过程中,50h后观察到反应器内有黄褐色沉淀物产生,且以800mg/L的体系内产生的沉淀物最多.选取500,800mg/L体系产物进行XRD分析,沉淀产物制备时,首先将反应瓶放置于厌氧操作室中,用注射器将体系中剩余的上清液抽出,然后用滤纸过滤底部沉淀产物,同时用无水乙醇冲洗2~3次沉淀产物,静置干燥.
图8a为500mg/L的反应体系沉淀产物的XRD图谱,沉淀产物主要为 Fe3O4和 FeOOH, Fe3O4中含有Fe2+和Fe3+,为反式尖晶石结构,Fe2+与 Fe3+在八面体位置上基本上是无序排列的.通过 X射线衍射检测得到的 Fe3O4的原因可能是在沉淀产物制备过程中发生下列反应:
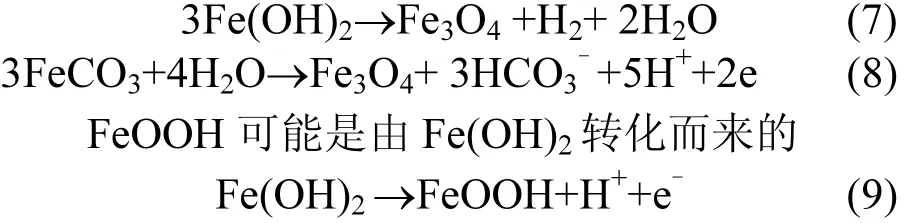
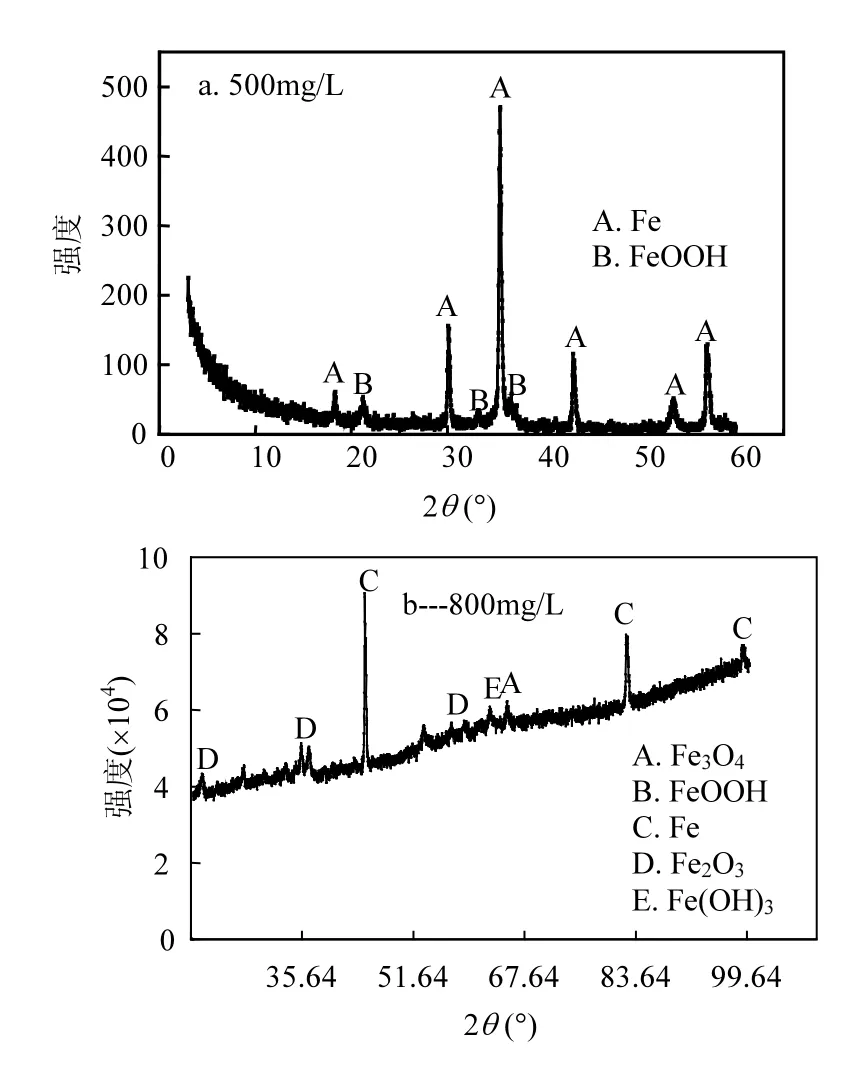
图8 反应产物X射线衍射分析图谱Fig.8 The X-ray differaction pattern of the reaction product
图8b为800mg/L的反应体系沉淀产物XRD图谱,沉淀产物有Fe3O4、Fe、Fe2O3和Fe(OH)3,结合实验观测到的沉淀物产生量,800mg/L体系沉淀物种类和数量均多于500mg/L体系.且800mg/L体系可观察到Fe0表面被褐色絮状沉淀物覆盖的现象,这些沉淀物阻碍了 Fe0继续与硝基苯发生还原反应.
3 结论
3.1 重碳酸盐浓度≤500mg/L时,硝基苯的去除率和苯胺的生成率均随着重碳酸盐浓度的增加而增加,当重碳酸盐浓度较高(800mg/L)时硝基苯的去除率和苯胺的生成率降低.
3.2 在各反应体系中,pH值均有不同程度的升高.随着重碳酸盐浓度的增加,体系中 pH值的增幅减小;重碳酸盐浓度≤500mg/L时,Eh随重碳酸盐浓度的升高而降低,同时溶液中 Fe2+的浓度随着重碳酸盐浓度的增加而升高.低浓度重碳酸盐(100~500mg/L)促进零价铁还原硝基苯,高浓度重碳酸盐(800mg/L)不利于硝基苯的还原.
3.3 对500mg/L重碳酸盐体系的沉淀物进行X射线衍射分析,得到沉淀物成分主要为 Fe3O4.推测其是由铁的氢氧化物和碳酸亚铁转化而成.而在800mg/L反应体系中检测到的成分有Fe3O4、Fe、Fe2O3和Fe(OH)3,沉淀产物中检测到未反应的 Fe0,说明重碳酸盐浓度高时,零价铁表面的沉淀物导致了零价铁与硝基苯之间的电子转移受阻,使得硝基苯还原效果最差.
[1] Lien Hsing-Lung, Wilkin Richard T. High-level arsenite removal from groundwater by zero-valent iron [J]. Chemosphere,2005,59(3):377-386.
[2] 吴双桃,陈少瑾,胡劲召,等.零价铁对土壤中硝基苯类化合物的还原作用 [J]. 中国环境科学,2005,25(2):188-191.
[3] Devlin J F, Allin K O. Major anion effects on the kinetics and reactivity of granular iron in glass-encased magnet batch reactor experiments [J]. Environmental Science and Technology,2005,39(6):1868-1874.
[4] 程 婷,戴友芝,刘智勇,等.零价铁对2,4-二氯酚生物还原脱氯的影响研究 [J]. 微生物学通报,2008,35(3):0332-0335.
[5] 李 雅,张增强,唐次来,等.Fe^0去除地下水中六价铬的研究[J]. 中国农业大学学报,2011,16(2):160-164.
[6] 吕国晓,尹 军,刘 蕾,周 璇,武海霞.pH值对零价铁还原降解模拟地下水中硝基苯的影响 [J]. 环境化学,2009,28(3):355-359.
[7] 董 军,赵勇胜,赵晓波,等.PRB技术处理污染地下水的影响因素分析 [J]. 吉林大学学报(地球科学版),2005,35(2):226-230.
[8] Orth W Scott, Gillham Robert W. Dechlorination of trichloroethene in aqueous solution using Fe0[J]. Environmental Science and Technology,1995,30(1):66-71.
[9] Navid Saleh, Kim Hye-Jin, Phenrat Tanapon, et al. Ionic strength and composition affect the mobility of surface-modified Fe0nanoparticles in water-saturated sand columns [J]. Environmental Science and Technology,2008,42(9):3349-3355.
[10] Liu Yueqiang, Lowry Gregory V. Effect of particle age (Fe0content) and solution pH on NZVI reactivity: H2evolution and TCE dechlorination [J]. Environmental Science and Technology,2006,40(19):6085-6090.
[11] Mantha R, Taylor K E, Biswas N,et al. A continuous system for Fe0reduction of nitrobenzene in synthetic wastewater [J]. Environmental Science and Technology,2001,35(15):3231-3236.
[12] Noubactep C. A critical review on the process of contaminant removal in Fe0-H2O systems [J]. Environmental Technology,2008,29(8):909-920.
[13] 樊金红,徐文英,高廷耀.零价铁体系预处理硝基苯废水机理的研究 [J]. 工业用水与废水,2004,35(6):53-56.
[14] 张国俊,孟 洪,薛 峰,等.TCE/PCE的DNAPL污染及零价铁墙防治技术 [J]. 环境污染治理技术与设备,2006,7(4):12-18.
[15] 张道勇,潘响亮,宋颖霞,等.零价铁去除水中锑(Sb)的研究 [J].地球与环境,2009,37(3):315-318.
[16] Aki S Ruhl, Jekel M. Impacts of Fe (0) grain sizes and grain size distributions in permeable reactive barriers [J]. Chemical Engineering Journal,2012,213:245-250.
[17] Klausen J, Vikesland Peter J, Kohn Tamar, et al. Longevity of cast iron in groundwater treatment processes: solution composition effects on reactivity towards organohalides and nitroaromatic compounds [J]. Environmental Science and Technology,2003,37(6):1208-1218.
[18] Valerio Zolla, Rajandrea Sethi, Antonio Di Molfetta. Performance Assessment and Monitoring of a Permeable Reactive Barrier for the Remediation of a Contaminated Site [J]. American Journal of Environmental Sciences,2007,3(3):158-165.
[19] Phillips D H, Gu B, WASTON D B, et al. Performance evaluation of a zerovalent iron reactive barrier: mineralogical characteristics [J]. Environmental Science and Technology,2000,34(19):4169-4176.
[20] Parbs Anika, Ebert Markus, Dahmake Andreas. Long-term effects of dissolved carbonate species on the degradation of trichloroethylene by zerovalent Iron [J]. Environmental Science and Technology,2007,41(1):291-296.
[21] 乐 晨,吴锦华,李 平,等.钙镁离子及重碳酸盐对零价铁还原对氯硝基苯的影响 [J]. 环境工程学报,2011,5(10)2177-2180.
[22] 时 琼.以零价铁为电子供体微生物协同去除地下水中高氯酸盐的研究 [D]. 济南:山东大学,2012.
[23] 乐 晨.对硝基苯污染地下水的零价铁修复研究 [D]. 广州:华南理工大学,2012.
[24] Zhou Chun Hui, Tong Dong Shen, Bao Man Hong, et al. Generation and characterization of catalytic nanocomposite materials of highly isolated iron nanoparticles dispersed in clays [J]. Topics in Catalysis,2006,39(3/4):213-219.
[25] Jia Hanzhong, Gu Cheng, Li Hui, et al. Effect of groundwater geochemistry on pentachlorophenol remediation by smectitetemplated nanosized Pd0/Fe0[J]. Environmental Science and Pollution Research,2012,8(19):3498-3505.
[26] Ralf Köber, Oliver Schlicker, Markus Ebert, et al. Degradation of chlorinated ethylenes by Fe0: inhibition processes and mineral precipitation [J]. Environmental Geology,2002,41(6):644-652.
[27] Liu Yueqiang, Phenrat Tanapon, Lowry Gregory V. Effect of TCE concentration and dissolved groundwater solutes on NZVI-promoted TCE dechlorination and H2evolution [J]. Environmental science & technology,2007,41(22):7881-7887.
[28] Su Chunming, Puls Robert W. Arsenate and Arsenite Removal by Zerovalent Iron: Effects of Phosphate, Silicate, Carbonate, Borate, Sulfate, Chromate, Molybdate, and Nitrate, Relative to Chloride. Environmental Science and Technology,2001,35(22):4562-4568.
[29] Dong Jun, Ding Linjie, Wen Chunyu,et.al. Effects of geochemical constituents on the zero-valent iron reductive removal of nitrobenzene in groundwater [J]. Water and Environment Journal,2012,27(1):20-28.
[30] Kohn Tamar, Roberts A Lynn. The effect of silica on the degradation of organohalides in granular iron columns [J]. Journal of Contaminant Hydrology,2006,83(1/2):70-88.
[31] Jeen Sung-Wook, Jambor John L, Blowes David W, et al. Precipitates on granular iron in solutions containing calcium carbonate with trichloroethene and hexavalent chromium [J]. Environmental Science and Technology,2007,41(6):1989-1994.
[32] Schultz Christopher A, Timothy J Grundl. pH dependence on reduction rate of4-Cl-nitrobenzene by Fe(Ⅱ)/montmorillonite system [J]. Environ. Sci.Technol.,2000,34(17):3641-3648.
[33] Scherer Michelle M,et al. Mass transport effects on the kinetics of nitrobenzene reduction by iron metal [J].Environmental Science and Technology,2001,35(13):2804-2811.
[34] Odziemkowski M S, Simpraga R P. Distribution of oxides on iron materials used for remediation of organic groundwater contaminants Implications for hydrogen evolution reactions [J]. Canadian Journal Chemistry,2004,82(10),1495-1506.
Effects of different bicarbonate concentrations on the reduction of nitrobenzene by zero-valent iron in simulated groundwater.
ZHANG Na, CHEN Ri, ZHANG Hai-tao, HONG Mei*
(Key Lab of Groundwater Resources and Environment, Ministry of Education, Jilin University, Changchun130021, China). China Environmental Science,2014,34(8):2010~2016
Batch experiments were designed to investigate the influence of different concentrations (0,100,300,500 and800mg/L) of bicarbonate on nitrobenzene degradation by zero valent iron in subsurface environment. The concentrations of nitrobenzene and aniline were monitored at interval time during the reaction progress, and the variations of pH, Eh, Fe2+, CO32-during the reaction were examined. The results indicated that bicarbonate can enhance the zero-valent iron activity at lower concentration (100~500 mg/L), and as the increasing of bicarbonate concentration, the promoting effect increases. in500 mg/L system, the highest nitrobenzene reduction was88% and aniline formation was173 mg/L, the buffering capacity for pH was the strongest, the decline range of Eh was the largest, and the concentration of Fe2+was the highest. The system of bicarbonate concentration of800 mg/L was not conducive to the reduction of nitrobenzene.
t:bicarbonate;zero-valent iron;nitrobenzene
X523
:A
:1000-6923(2014)08-2010-07
张 娜(1986-),女,河北保定人,硕士研究生,研究方向为污染场地控制与修复.
《中国环境科学》2011年度引证指标
《中国环境科学》编辑部
2013-12-20
国家自然科学基金项目(41102146)
* 责任作者, 教授, hongmei@jlu.edu.cn
根据《2012年版中国科技期刊引证报告(核心版)》,《中国环境科学》2011年度引证指标继续位居环境科学技术、安全科学技术类科技期刊前列,核心影响因子1.523,学科排名第1,综合评价总分79.2,学科排名第2;在被统计的1998种核心期刊中影响因子列第18位,综合评价总分列第52位.《中国科技期刊引证报告》每年由中国科学技术信息研究所编制,统计结果被科技管理部门和学术界广泛采用.
