小球藻热解特性及其液化制油实验分析
2014-05-08李桂菊段永梅赵茹玉何迎春
李桂菊,段永梅,赵茹玉,何迎春
(1. 天津市海洋资源与化学重点实验室,天津科技大学海洋科学与工程学院,天津 300457;2. 天津科技大学机械工程学院,天津 300222)
生物质能是一种极佳的可再生能源,与此同时, 由于生物通过光合作用利用 CO2,可减轻因大气中CO2增加造成的全球温室效应,所以生物质热解及其相关技术的研究已被世界各国所重视[1–3].与石油等化石能源相比,生物质能具有可再生、对环境污染小等优点.在众多的生物质中,藻类是低等的、放氧自养型植物,它生长和繁殖在水域中,不会引起与农业用地、牧业用地竞争的矛盾.同时,相对于其他植物,藻类脂类含量高,是采用热转化制造生物质燃料的良好材料.
热解是将生物质转化为气体和液体燃料的有效途径.藻类含有较多可溶性多糖和蛋白质等化学成分,易于热解,同时藻类具有光合作用效率高、环境适应能力强、生长周期短、生物产量高的特点[4–6],本身可以生化合成油脂,且油脂含量高,所以海洋藻类作为制备生物柴油的新原料展现出广阔的应用前景.因此,充分合理利用我国的特有海洋优势,高效、清洁、合理地利用丰富的藻类资源,必将推动我国海藻业的发展[7–9].常用的热解技术主要有催化热解技术和直接液化法热解技术.催化热解技术虽然无需很高的压力,常压即可,但所采用的微藻原料需经干燥脱水,使其干基含水率在 5%以下,此过程需要消耗大量的能量.直接液化法热解技术是在水中进行的,原料不需要干燥,由于藻类生物质通常具有高含水率,因此对藻类的转化反应是十分合适的[10–12].从能耗的角度来看,直接液化法是一种有前途的生物质转化方法.直接热化学液化的本质是热解,其中还发生各种复杂的变化,如低分子化的分解反应和分解物高分子化的聚合反应等,小球藻先生成水溶性中间体,在水中反复聚合、水解.液化制取油时,适度的聚合反应是主要的,抑制由油向焦炭聚合更加重要,而催化剂在此起着重要作用.
国外生物质热解制油所选用的原料大多数是木材,采用的催化剂[13–14]有碱金属盐及过渡金属盐等.本文选择钠盐作为催化剂,研究其对小球藻热解的影响.通过改变最佳催化剂用量,考察其对小球藻油化产物分布以及油产率的影响,并利用 GC/MS分析得到油产品中各成分的含量,为今后的产业化提供理论依据.
1 材料与方法
1.1 实验材料
本文所选的材料是在实验室自行培养的油脂含量较高的小球藻,其工业分析和元素分析结果见表1.由表 1可知,小球藻中水分质量分数为 89.09%,干基挥发分质量分数为 78.41%,这说明小球藻有机质含量较高.由于藻类热解的油产率与藻类中的挥发分含量直接相关,故小球藻是油化的好原料.由于Na元素质量分数较低,可忽略小球藻自身含有的钠元素对其热解的催化作用.
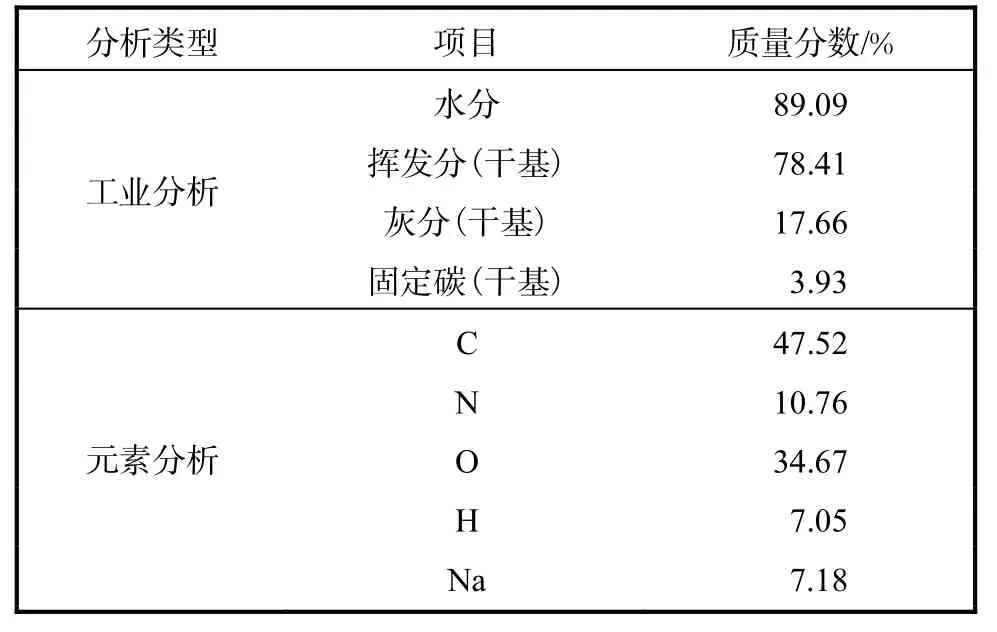
表1 小球藻的工业分析和元素分析结果Tab.1 Results of chlorella proximate analysis and ultimate analysis
1.2 实验装置
直接热化学液化藻类油化装置是自行设计的磁力驱动高压反应釜装置,其结构如图 1所示,主要包括热电偶、0.5,L高压釜、加热外套、磁力搅拌器、控制系统等.其中控制系统主要由冷凝器、冷凝液储罐、过滤器、回压控制器和一个气体储罐组成.反应系统利用回压控制器使反应釜中的工作压力恒定.

图1 高压反应釜装置图Fig.1 Schema of the high-pressure autoclave
1.3 实验方法
1.3.1 热重分析
本实验采用碳酸钠、硫酸钠、氯化钠 3种钠盐作为催化剂,通过热重分析证实这 3种物质在 373~1,023,K质量基本不发生变化,这说明在此温度范围内 3种物质均适合作催化剂.将干燥后的小球藻与每种催化剂分别按一定比例混合得到的混合样及小球藻空白样各取 10,mg,以升温速率 30,K/min,从室温加热到1,173,K,在美国TA公司的Q50TGA型热重分析仪上进行热解实验,得到相应升温速率下的TG-DTG曲线.依据不同种类催化剂及其用量对TGDTG曲线的影响,确定最佳催化剂种类及用量.
1.3.2 热解实验
在图 1所示反应装置中进行直接热化学藻类油化实验,分别选择最佳催化剂中钠离子质量占小球藻质量的 1%~5%为催化剂用量,考察催化剂用量对油产率的影响,验证与热重分析的结果是否吻合.实验主要分为 4个过程:对小球藻进行直接热化学液化、将液化后固相和液相过滤分离、用萃取法从液相分离出油产品,油和萃取剂用分馏法分离.实验流程如图2所示.前以 30倍体积乙醚为溶剂超声振荡 30,min,进行溶出预处理.产生的沉淀为沥青烯类,用 0.25,µm 的滤纸抽滤,滤液颜色为浅黄色.利用气质联用得到油产品成分的谱图,根据谱图来判断主要物质的含量.

图2 小球藻热解实验流程图Fig.2 Flowchart of chlorella pyrolysis experiment
2 结果与讨论
2.1 催化剂对小球藻TG-DTG曲线的影响
2.1.1 不同钠化合物对小球藻热解的催化作用
分别以 3种化合物 Na2CO3、Na2SO4、NaCl作为小球藻的催化剂[15],加入的钠离子的质量为小球藻质量的 5%,在热天平上进行热重分析,DTG曲线如图3所示、TG曲线如图4所示.

图3 加入钠盐催化剂的小球藻样品及空白样的DTG曲线Fig.3 DTG curves of chlorella with additives of sodium compounds and the blank sample
本文定义的油为 CH2Cl2萃取得到的溶质,油产率Y按式(1)进行计算.

1.3.3 油产品性能分析
取 1,mL经上述流程分离出的油产品,在检测之
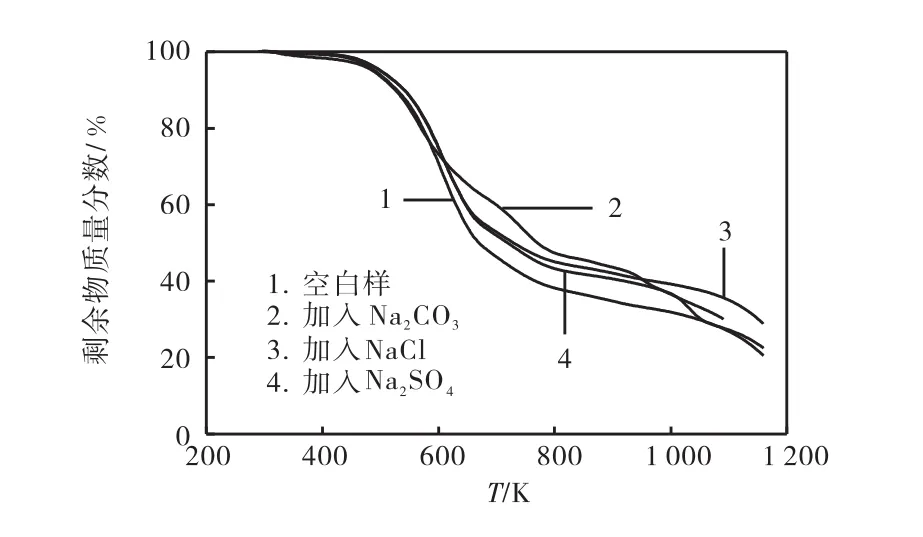
图4 加入钠催化剂的小球藻样品及空白样的TG曲线Fig.4 TG curves of chlorella with additives of sidium compounds and the blank sample
由图3可知:加入3种催化剂后,其最大失重速率对应的温度分别为603、595和565,K,均小于未加催化剂的空白样(607,K),说明加入钠盐催化剂后,在整体热解区间最大失重速率对应的热解温度向低温区移动,其中 Na2CO3向低温区移动最显著.除加入催化剂 Na2CO3后对应的最大失重率略有提高,其余两种催化剂略有降低,这是因为反应温度也是热解的重要影响因素.而加入 Na2CO3后温度不仅向低温区移动,而且最大失重速率略有升高,可能是由于碳酸根离子与蛋白质的羧基等反应生成二氧化碳等易挥发物质,使单位时间的失重量略有提高,而硫酸根离子和氯离子参与反应生成的磺酸盐和氯化合物挥发性不强的缘故.
由图4计算得到的转化率见表 2.由表 2可知:加入3种催化剂都能使得小球藻热解转化率升高,转化率大小的顺序为 Na2CO3>Na2SO4>NaCl.这个顺序与图 3的微分失重曲线中催化剂对小球藻热解最大失重速率影响大小顺序相一致,更进一步验证这 3种催化剂对小球藻的热解影响大小程度.3种催化剂中,碳酸钠对小球藻热解的催化效果最好.

表2 加入钠化合物后小球藻热解转化率的变化Tab.2 Variation of conversion rate of chlorella with additive of sodium compounds
2.1.2 催化剂用量对微藻热重的影响
以催化作用显著的碳酸钠为催化剂,将钠离子质量分别为小球藻质量 3%、5%和 10%的碳酸钠与小球藻粉混合后,进行热重实验,分析催化剂用量对小球藻热解的影响.不同样品的DTG曲线和TG曲线如图5和图6所示.
由图 5可知:随着碳酸钠用量的增加,第一个主要失重峰逐渐向低温区移动,达到最大失重速率对应温度分别为 588、565、551,K,最大失重率分别为0.368,3、0.373,4、0.386,3,%/K.随着催化剂加入量的增加峰值向低温区移动,说明加入量的增加促进了热解.由图6可知:加入量太大时,转化率却随之降低,因此综合考虑这两个方面来看(见表 3),选择 5%比例碳酸钠与小球藻混合,催化效果较为理想.

图5 不同样品的DTG曲线Fig.5 DTG curves of different samples

表3 加入不同比例碳酸钠后转化率、最大失重率及其对应温度变化Tab.3 Variation of the maximum weight loss rates ,correspondingtemperatures and the conversion rate with various proportion of Na2CO3
2.2 催化剂用量对油产率的影响
以碳酸钠为催化剂,将钠离子质量分别为小球藻质量 3%、5%、8%、10%的碳酸钠与小球藻粉混合后在自制的实验装置中进行实验,反应终温为 533,K,压力为对应温度的饱和蒸汽压,停留时间 0,min.实验结果见图7.

图7 催化剂用量对油产率影响Fig.7 Influence of catalyst dosage on oil yield

图6 不同样品的TG曲线Fig.6 TGcurves of different samples
从图7可知:油产率最初随着催化剂用量的增加而增加,在 5%时达到顶峰(62.58%),然后开始下降,最佳用量为碳酸钠中钠离子质量为小球藻质量的5%.这与催化剂对小球藻热重分析的影响研究结果基本吻合.随着催化剂用量的增加,使油化的起始温度降低,促进热解的发生,因此油产率随之增加,催化剂用量继续增加,促进了油品向焦炭的转化,进而使油产率下降.因此,适度的聚合反应,抑制由油向焦炭聚合至关重要,催化剂在此起着重要作用.
2.3 油产品组成分析
研究发现,不同条件下生成的热解油性状相近,颜色为深褐色,具有植物油和石油的混合气味,常温下为黏稠状液体.利用 GC/MS分析得到油品的总离子谱图,对其进行了化合物解析,方法是图谱库对照与保留值分析双重认定,GC/MS分析得到的产品油的组成见表 4.由表 4可知:产品油主要成分有苯系物、烃类、酚类、硬脂酸酯和酰胺.由缩聚等聚合反应形成的大分子不溶物(沥青烯)和糖类脱水环化的苯系产物被认为是纤维素热解的特征产物.大量的含碳(C7~C21)化合物表明脂肪族化合物是油产品的主要来源,油中大量的含氮化合物(主要是酰胺)则表明蛋白质广泛参与了热转化反应,主要机理是活性氢的作用下造成的肽键断裂和氨基酸的转化.含氮化合物在油产品中含量随反应温度增大是上升的,说明温度上升时蛋白质的转化反应增加.油产品组成可以说明热化学转化过程产油的主要机理是脂肪族化合物的蒸发和蛋白质肽键的断裂,同时还发生了脂肪酸的酯化、酰胺化等基团转移反应;在较高的温度段,糖类化合物通过支链断裂、缩聚等方式参与了转化反应.实验中将溶于二氯甲烷的组分定义为重油.

表4 产品油的组成Tab.4 Contents of chemicals in the oil product
2.4 能量衡算
本实验采用能量回收率和能量消耗率进行能量衡算.能量回收率是指藻样品中的挥发性固体能量转化为产品油能量的比率.

其中:小球藻固体热值为 20.3,MJ/kg;产品油的热值为32.4,MJ/kg.经计算,能量回收率为78.2%.
能量消耗率(energy consumption ratio,ECR)能反映实际生产过程的热衡算,ECR按照式(2)进行计算.ECR>1为能量消耗型,ECR<1为能量产出型.

式中:γ为热利用率,本文γ=0.7;Y为油的产率;Q为油的发热量;QΔ为原料由室温加热到反应温度所需的热量.

式中:w和 'V为初始物质中水分和挥发性固体的含量,分别为 0.890,9和 0.784,1;H为产生的重油的热值,32.4,MJ/kg;cpw和 cps分别是水的比定压热容(4.18,J/(g·K))和干燥小球藻样品的比定压热容(2.25,J/(g·K)).
经计算ECR=0.91,说明系统为能量产出型.
3 结 论
(1)通过热重分析可知:3种钠化合物对小球藻的热解均有催化作用,钠化合物的催化作用大小依次为 Na2CO3>Na2SO4>NaCl,其中 Na2CO3对小球藻热解的催化效果最显著;随着催化剂碳酸钠用量的增加,TG-DTG曲线的主要失重峰逐渐向低温区移动,最大失重率也随之增加,然而转化率随之减少.综合考虑,钠离子质量为小球藻质量的5%为相对理想用量.
(2)以 Na2CO3作为直接热化学小球藻油化实验的催化剂,油产率开始随着催化剂的增加而增加,达到顶峰后开始下降,钠离子质量为小球藻质量的 5%为最佳催化剂用量,与催化剂对藻类热解 TG-DTG曲线的影响研究结果基本吻合;通过 GC/MS对油产品化合物组成的分析可知:小球藻热化学转化过程的产油主要机理是脂肪族化合物的分解和蛋白质肽键的断裂,同时还发生了脂肪酸的酯化、酰胺化等基团转移反应,糖类化合物通过支链断裂、缩聚等方式参与了转化反应.产品油的主要成分包括苯系物、烃类物、沥青烯、酚类、酰胺等,将可溶于二氯甲烷的组分定义为重油.产品油的热值很高,为 32.4,MJ/kg.能量回收率也相当可观,为78.2%.
[1] Maggi R,Delmon B. Comparison between ‘slow’ and‘flash’ pyrolysis oils from biomass[J]. Fuel,1994 ,73(5):671–677.
[2] Maschio G,Koufopanos C,Lucchesi A. Pyrolysis,a promising route for biomass utilization[J]. Bioresource Technology,1992,42(3):219–231.
[3] Ferrero G L,Maniatis K,Buekens A,et al. Pyrolysis and gasification[M]. London:Elsevier Applied Science,1989.
[4] Milne T A,Evans R J,Nagle N. Catalytic conversion of microalgae and vegetable oils to premium gasoline,with shape-selective zeolites[J]. Biomass,1990,21(3):219–232.
[5] Minowa T,Yokoyama S,Kishimoto M,et al. Oil production from algal cells of Dunaliella tertiolecta by direct thermochemical liquefaction[J]. Fuel,1995,74(12):1735–1738.
[6] Miao X L,Wu Q Y. Biodiesel production from heterotrophic microalgal oil[J]. Bioresource Technology,2006,97(6):841–846.
[7] 黄知清,严兴洪. 海藻研究开发的发展概述[J]. 海洋技术,2002,21(3):22–25.
[8] 彭卫民,李祥书,吴庆余,等. 采用热解技术将湖泊浮游藻类用于燃料生产[J]. 环境污染治理技术与设备,2000,l(3):24–28.
[9] Peng W M,Wu Q Y,Tu P G,et al. Pyrolytic characteristics of microalgae as renewable energy source determined by thermogravimetric analysis[J]. Bioresource Technology,2001,80(1):1–7.
[10] 王子曦. 直接热化学法制革污泥制油技术[D]. 天津:天津科技大学,2009.
[11] Takagi M,Karseno,Yoshida T. Effect of salt concentration on intracellular accumulation of lipids and triacylglyceride in marine microalgae Dunaliella cells[J]. Journal of Bioscience and Bioengineering,2006,101(3):223–226.
[12] Yu G,Zhang T H,Schideman L,et al. Bio-crude oil production from microalgae through hydrothermal process[C]// Bioenergy Engineering Conference. Washington:ASABE,2009.
[13] Wang Jun,Zhang Mingxu,Chen Mingqiang,et al. Catalytic effects of six inorganic compounds on pyrolysis of three kinds of biomass[J]. Thermochimica Acta,2006,444(1):110–114.
[14] Aresta M,Dibenedetto A,Carone M,et al. Production of biodiesel from macroalgae by supercritical CO2,extraction and thermochemical liquefaction[J]. Environmental Chemistry Letters,2005,3(3):136-139.
[15] 李桂菊,白丽萍,王昶,等. 钠盐催化剂对制革污泥热解制油的影响[J]. 太阳能学报,2013,34(3):407–412.
