糯米淀粉水凝胶的制备及性质
2014-05-07王茂广
王茂广
(临沂大学,山东临沂276000)
淀粉是绿色植物根茎、果实的主要成分,在自然界中分布很广,是一种用之不竭的可再生天然资源[1]。由于天然淀粉不溶于冷水,易老化,机械性差等限制了其应用,对原淀粉运用物理、化学或酶的方法进行处理,使其具有适合某种特殊用途的性质,这一过程称为淀粉的变性[2]。吸水性凝胶材料是一种对水有特殊吸附作用的高分子功能材料,其内部带有强烈的亲水基团[3]。近年来,与水凝胶有关的研究已引起各界的高度关注[4-5]。淀粉水凝胶具有良好的生物可降解性,环境友好,污染性小的特点[6],直链淀粉所制得的淀粉水凝胶取代度较低,本研究选择的是含有几乎100%支链的糯米淀粉,探求由支链淀粉制备水凝胶的条件及性质,为后续糯米淀粉水凝胶综合开发利用提供了实验支持和理论依据。
1 材料与方法
1.1 材料与仪器
糯米淀粉:蚌埠市兄弟粮油食品科技有限公司;氢氧化钠、氯化氢、氯化钠:上海中式化工公司;4-二甲基氨基吡啶:天津凯通化学试剂有限公司;琥珀酸酐、乙醇:天津博迪化工有限公司。
精密电子天平:上海天平仪器厂;Thermo Nicolet FTIR200红外分光光度计:美国热电尼高力公司;增力电动搅拌器:江苏金坛市金城国胜实验仪器厂;THZ-9A气浴恒温震荡器:上海浦东物理光学仪器厂;DSC差热扫描量热仪:美国梅特勒-托利多公司。
1.2 方法
1.2.1 淀粉水凝胶的制备
将淀粉和蒸馏水以1∶100(g/mL)的比例配成100mL淀粉溶液,于95℃下加热,使淀粉完全糊化,然后冷却至室温,分别加入4-二甲基氨基吡啶和琥珀酸酐,放置24 h,加氢氧化钠水溶液,将溶液调至pH 7.0,加入1 000 mL乙醇析出产物后,过滤干燥。
1.2.2 淀粉水凝胶取代度测定
采用单因素实验法,分别加入与原淀粉不同比例的催化剂和琥珀酸酐,利用HCl与淀粉水凝胶中乙酰基的反应,同时用原淀粉的空白实验,计算乙酰基含量和淀粉水凝胶取代度,得出最佳反应条件[7]。
1.2.3 淀粉水凝胶吸水性测定
用茶袋法分别测定淀粉水凝胶在纯水中和在生理盐水中的吸水性[8]。
1.2.4 淀粉水凝胶透明度测定
称取1.00 g(干基)水凝胶样品置于锥形瓶中,加入蒸馏水100 mL,放入恒温加热磁力搅拌器中加热糊化并于糊化温度下保温 20 min,冷却至室温,波长选定范围600 nm~650 nm,以蒸馏水为空白,每隔10 nm测定不同波长下原淀粉与淀粉水凝胶溶液的透光度[9]。
1.2.5 淀粉水凝胶冻融稳定性测定[10]
制取30 mL浓度为3%的原淀粉溶液,沸水浴加热,使之充分糊化,冷却至室温。将原淀粉溶液和淀粉水凝胶置于-18℃冰箱,24 h后取出,在室温下自然解冻,观察其各自情况。重复多次,直至淀粉胶体结构破坏,有清水析出或变成海绵状为止,记录冻融次数。
1.2.6 淀粉水凝胶红外结构分析测定
采用KBr压片法对样品进行红外光谱仪进行全波段扫描[11]。
1.2.7 淀粉水凝胶DSC差示热量分析测定[12]
分别取原淀粉、水凝胶各3.0 mg,并加入10 μL的蒸馏水混合均匀,在铝坩埚中室温下平衡2 h,以空皿为参照,然后以10℃/min的速率升温,温度范围为30℃~200℃,通入30 mL/min的高纯氮,分别测定To(起始温度)、Tp(峰值温度)、Tc(终止温度)及焓值(△H)的变化情况。
2 结果与分析
2.1 不同物料比对淀粉水凝胶取代度的影响
制备淀粉水凝胶,催化剂与原淀粉羟基的为摩尔比1∶1,分别加入不同量的琥珀酸酐,其与原淀粉羟基的摩尔比分别为 1∶1、2.5∶1、5∶1、10∶1、20∶1。测定其取代度,结果如图1所示。
从图1可以看出,糯米淀粉水凝胶的取代度随琥珀酸酐的加入量增加而增加,在琥珀酸酐与淀粉羟基摩尔比为20时取代度达到最大值,但在实际操作过程中,加入的过量琥珀酸酐已无法完全溶解,形成沉淀与产物一起被过滤出,因此实际产物中含有大量未反应的琥珀酸酐,对取代度的测定产生了一定影响。所以采用18.6 g琥珀酸酐,即与原淀粉羟基摩尔比为10∶1为最佳用量。
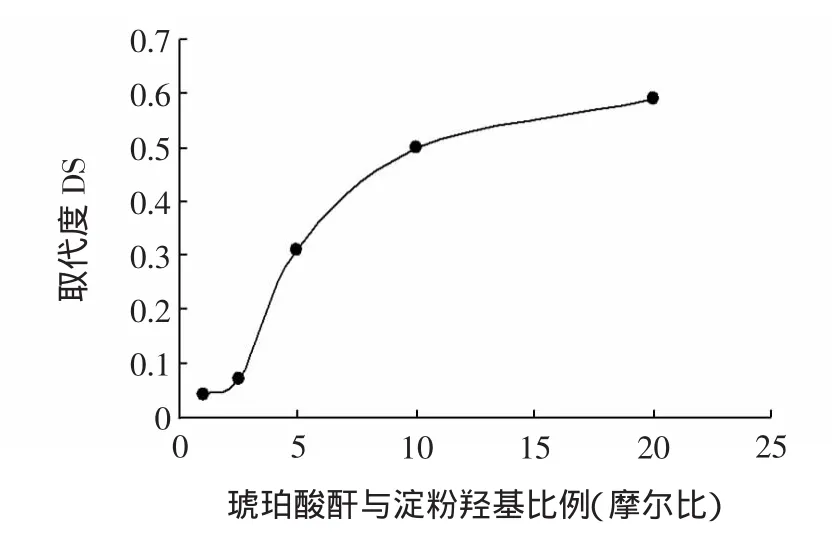
图1 不同物料比下产物的取代度Fig.1 Effect of succinic anhydride content on starches substitution degree
2.2 不同催化剂用量对淀粉水凝胶取代度的影响
制备淀粉水凝胶,分别加入催化剂与原淀粉羟基的为摩尔比 0.55∶1、0.80∶1、1.05∶1、1.30∶1、1.55∶1,待溶解后,加入琥珀酸酐35 mL(与淀粉羟基的摩尔比为10∶1),测定其取代度,结果如图2所示。
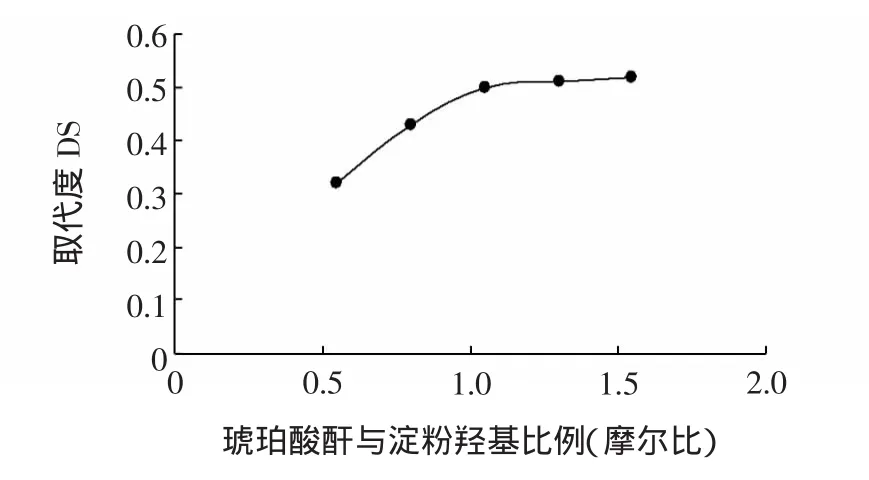
图2 不同催化剂用量下产物的取代度Fig.2 Effect of catalyst content on starches substitution degree
从图2可以看出,当催化剂用量与淀粉羟基摩尔比为1.05∶1时,产物取得较高取代度,之后再继续增加催化剂用量,产物取代度增长趋势趋于平稳。研究分析可知,当催化剂与淀粉羟基比例达到并超过1时,淀粉所含的羟基得到充分的活化,可以保证正向反应的最大化进行,再增加催化剂用量已无法影响反应程度,因此,最终确定催化剂用量为2.38 g(与原淀粉羟基摩尔比例为1.05∶1)为最佳用量。
2.3 淀粉水凝胶的吸水性
淀粉水凝胶在纯水中和在生理盐水中的吸水性研究结果如图3所示。
由图3可以看出,随着时间的增加,产物渐渐吸水,在3 h后产物吸水度都增加趋于平稳,表明产物已充分吸水。淀粉水凝胶在纯水中最大吸水度可以达到56 g水/g干胶,在生理盐水中可以达到17 g水/g干胶。但在盐水中的吸水能力远不如纯水,分析原因可能是盐水的中的离子浓度较纯净去离子水要高很多,因此阻碍了水凝胶的吸水能力。

图3 淀粉水凝胶的吸水性Fig.3 The water absorption of glutinous rice starch hydrogels
2.4 淀粉水凝胶的透明度
在不同波长下分别测定原淀粉与产物的水溶液透明度,所得结果如图4所示。

图4 淀粉水凝胶的透明度Fig.4 The transparency of s glutinous rice tarch hydrogels
从图4可以看出,淀粉水凝胶的透明度要明显远高于原淀粉,这主要是因为原淀粉亲水性不强,不能很好的结合水分子,糊化后容易形成淀粉团,阻碍光线透过,而淀粉水凝胶通过引入亲水基团,在制备成糊时,淀粉分子可以大量吸附水分子,形成质地均匀的凝胶,减少了光线的反射,大大增加了糊的透明度,且能长时间保持稳定。
2.5 淀粉水凝胶的冻融稳定性
淀粉水凝胶的冻融稳定性见表1。

表1 淀粉水凝胶的冻融稳定性Table 1 Stability of freeze thaw of glutinous rice starchhydrogels
由表1可知,通过酯化反应,糯米淀粉的冻融稳定性发生了很大的变化。原糯米淀粉对低温根本没有耐受力,只冻融一次就析出少量清水,而琥珀酸淀粉酯的糊液却能经反复冻融而保持原貌。分析原因,原糯米淀粉分子间主要靠氢键连接,低温下分子间氢键结合成束状结构而发生凝沉;经琥珀酸酯化后的糯米淀粉,琥珀酸基团的接入使得淀粉分子间的氢键减弱,因而在低温下也不容易析水分层。
2.6 淀粉水凝胶的红外结构分析
糯米淀粉水凝胶红外图谱结果如图5所示。
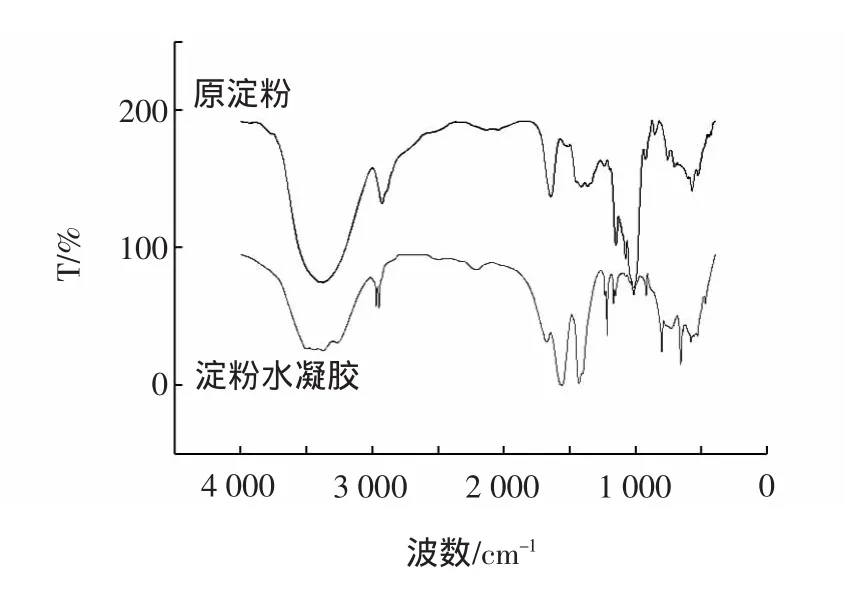
图5 淀粉水凝胶红外图谱Fig.5 IR of glutinous rice starch hydrogels
从图5可以看出,原糯米淀粉在3 100 cm-1~3 600 cm-1之间出现较强的—OH伸缩振动吸收峰,在1 645 cm-1处事烯醇式的C—O键伸缩振动吸收峰,1 155 cm-1、1 079 cm-1、1 019 cm-1处是非对称的C—O—C伸缩振动、C-0伸缩和骨架振动吸收峰。而糯米淀粉水凝胶除了以上特征吸收外,在1 681 cm-1处存在C=0伸缩振动吸收峰,在1 550~1 610 cm-1是RCOO的特征吸收,因此可以确定丁二酸基团已经成功地被引入淀粉分子。
2.7 淀粉水凝胶的DSC分析
测得原淀粉和淀粉水凝胶的DSC特征参数见表2所示。

表2 淀粉水凝胶的DSC的热力学特征参数值Table 2 DSC thermodynamics characteristic parameter value of starches
从表2可看出:淀粉水凝胶的初始温度、峰值温度、最终温度和热焓值均高于原淀粉。说明阳离子糯米淀粉分子间的氢键强度增强,淀粉颗粒的结构更紧固,受热难膨胀,糊化变难,因此阳离子糯米淀粉初始温度与峰值温度上升,热焓值增加。
3 结论
以糯米淀粉为原料,采用醇沉法工艺合成了糯米淀粉水凝胶,确定适宜的反应条件:羟基比比例为n(催化剂)∶n(原淀粉)=1.05∶1,n(琥珀酸酐)∶n(淀粉)=10∶1的条件下,所得产物的取代度为DS为0.513。制得的淀粉水凝胶吸水速度快,3 h就可以饱和,胶体吸水后质地柔软;糯米淀粉水凝胶透光率可以达到76%,远大于原糯米淀粉。通过红外分析与DSC表征证明了丁二酸基团被引入到糯米淀粉分子上。
[1] 蓝新宇.淀粉与变性淀粉[J].内蒙古科技与经济,2004,10:78-79
[2] 章毅鹏,廖建和,桂红星.浅析我国变性淀粉的应用现状[J].中国粮油学报,2007,22:179-184
[3] 蒲敏,王海霞,周根树.吸水性凝胶材料的研究现状与发展趋势[J].材料导报,1997,11(4)::43-45
[4] KimC J,LeeP J.Hydrophobic anionic gel beadso swelling controlled drug delivery[J].PharmRes,1992,9(2):195-199
[5] Kwon C,Bae Y,Kim S.Electrically erodible polymer gel for controlled release of drugs[J].Nature,1991,354(28):291-293
[6] 涂晓燕.淀粉类高吸水性树酯的研究及其应用[J].精细石油化工进展,2007,7(8):29-32
[7]钱大钧,杨光.醋酸酯淀粉制备及性质研究[J].中国粮油学报,2007(3):49-52
[8]何叶丽.高吸水性聚合物性能指标与测试方法[J].化工新型材料,1998,12(26):22-24
[9] 袁怀波,江力,曹树青,等.酯化红薯变性淀粉的制备及性质研质[J].食品科学,2006,10:245-247
[10]袁怀波,曹树青,王步强,等.交联-羧甲基木薯淀粉的合成及性质研究[J].中国粮油学报,2007,22(5):62-66
[11]何旭元,陈远斗,蔡湘雯,等.基于空白KBr压片的红外光谱制样方法[J].湖南文理学院学报,2006,18(2):31-33
[12]林丽菁.木薯淀粉磷酸酯的结构表征及理化性质研究[D].南宁:广西大学,2005
