夫西地酸钠乳膏的处方筛选及稳定性考察
2014-05-06杨丽珍杨柳余邦良
杨丽珍,杨柳,余邦良
(1.海南省人民医院药学部,海南海口571102;2.海南医学院药学院,海南 海口 571119)
夫西地酸钠乳膏的处方筛选及稳定性考察
杨丽珍1,杨柳2,余邦良2
(1.海南省人民医院药学部,海南海口571102;2.海南医学院药学院,海南 海口 571119)
目的筛选夫西地酸钠乳膏的最佳处方。方法采用L9(34)正交试验优选处方,以白凡士林用量(A)、液状石蜡用量(B)、羊毛脂用量(C)、十六醇用量(D)为考察因素,以外观性状、离心结果、耐寒、耐热四状态总评分和含量为质量评价指标。结果按评价指标确定最优处方组合为A1B3C1D3,用此处方制备3批夫西地酸钠乳膏样品,符合其质量标准和《中国药典》(2010年版)乳膏剂项下的各项规定,其稳定性考察的各项指标均符合要求。结论该处方设计方案合理,结果可靠。
夫西地酸钠;乳膏剂;正交试验;稳定性
夫西地酸钠是新型梭链孢酸类抗生素,有着良好的临床治疗效果。其主要用于由敏感细菌尤其是葡萄球菌引起的各种感染、败血症、心内膜炎、反复感染的囊性纤维化、肺炎、皮肤及软组织感染、尿路感染、生殖器疾病、脓疱病、疖肿、毛囊炎、甲沟炎、须疮、汗腺炎、红癣、寻常痤疮、创伤合并感染、湿疹合并感染、溃疡合并感染等,是美国《热病》手册推荐为抗葡萄球菌感染的首选抗生素[1]。夫西地酸钠具较高的安全性,无耳肾毒性和低耐药率,抗感染活力持久稳定,是一个非常理想的抗感染药[2]。国内外对于夫西地酸钠乳膏处方及工艺的研究报道较少,本文对夫西地酸钠乳膏处方进行正交筛选研究,并对该制剂进行质量和稳定性考察。
1 仪器与试剂
1.1 仪器BS-25型乳化均质机(上海贝而特流体设备有限公司);BW30实验型乳化搅拌机(上海贝而特流体设备有限公司);800型离心沉淀机(上海手术器械厂);AE100电子天平(梅特勒-托利多仪器(上海)有限公司);LC-15A高效液相色谱仪(日本岛津公司);SY21-Ni4型一列二孔电热恒温水浴锅(北京精科华瑞仪器有限公司)。
1.2 药品与试剂夫西地酸钠(四川海思科制药有限公司);白凡士林(南京长江江宇石化有限公司);十六醇(湖南尔康制药股份有限公司);液状石蜡(吉林吉化江城油脂化工有限公司);羊毛脂(上海大来化学试剂有限公司);纯化水(自制)。
2 方法与结果
2.1 处方组成及制备方法的初步确定处方组成:夫西地酸钠在水中不稳定,故考虑加入油溶性基质。参考相关文献[3-6],经采用多种辅料进行筛选比对试验,初步确定基质种类为:白凡士林、液状石蜡、羊毛脂和十六醇。制备方法:分别取十六醇、羊毛脂、白凡士林、液状石蜡适量,加热至80℃~85℃,再加入水相,采用高剪切乳化机进行混合,待形成乳液后保温灭菌30 min,滤过,在加热搅拌下按100 ml乳液中含夫西地酸钠2 g将夫西地酸钠逐渐加入乳液中,并搅拌均匀,放冷分装,即得。
2.2 正交设计法优化处方依据各基质的性质及用法用量,采用正交设计法确定最佳处方。以A:白凡士林用量;B:液状石蜡用量;C:羊毛脂用量;D:十六醇用量(A、B、C、D均用占处方总量的百分比表示)为考察因素,每个因素设定3个水平,采用L9(34)正交试验。因素与水平见表1。

表1 正交实验因素水平(%)
2.3 夫西地酸钠乳膏剂基质评价指标的测定
2.3.1 外观性状观察膏体的外观,并在50℃水浴中将样品重新加热至液态,观察乳液的性状。若出现分层,膏体外观粗糙不均匀,说明处方配比不合理;若乳液未分层,冷却后膏体外观符合要求,说明处方配比合理。通过评分的方法对正交试验后的各个处方结果进行评价。
2.3.2 离心试验按正交试验制分别备各处方乳膏(15 g/支),装入带刻度的离心管中,置于离心半径为8 cm,转速为3 000 r/min的离心机中离心30 min,观察有无油水分离现象。通过评分的方法对正交试验后的各个处方结果进行评价。
2.3.3 耐寒、耐热试验分别取正交试验制备的各处方乳膏,每个处方各10支,分别放入冰箱(-10℃)和烘箱内(50℃)进行试验。放置10 d后,将其还原到室温,观察样品的性状。通过评分的方法对正交试验后的各个处方结果进行评价。
2.3.4 含量测定参照夫西地酸乳膏剂的质量标准[7]中高效液相色谱法测定其含量。
2.3.4.1 色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;以0.05 mol/L磷酸-乙腈-甲醇(30:60:10)为流动相;检测波长为235 nm,理论板数按夫西地酸钠计算不低于2000,夫西地酸钠峰与杂质峰的分离度均应符合规定。
2.3.4.2 测定法取本品适量(约相当于夫西地酸钠30 mg),置50 ml分液漏斗中,加入10 ml正己烷和25 ml的流动相,剧烈振摇15 min,静置,取下层溶液,用流动相稀释至50 ml,过滤,即得。精密量取上述溶液10 μl注入液相色谱仪,记录色谱图;另取夫西地酸钠对照品适量,精密称定,加流动相溶解并稀释成每1 ml中含夫西地酸钠0.6 mg的溶液,同法测定。按外标法以峰面积计算,即得。
2.4 正交试验结果根据表1试验处方的设计,对就试验产品进行外观性状、离心、耐寒、耐热、含量等各个指标的测定,并将外观性状、离心、耐寒、耐热这几项进行评分,每一项最优得分分别为30分、30分、40分。各组处方根据优劣程度(外观无油水分离且膏体细腻、无粗糙为最优状态,经耐热、耐寒、离心试验后无明显变化为最优状态)依次降低减分。最后合计为状态总分,正交试验结果见表2,方差分析结果见表3。
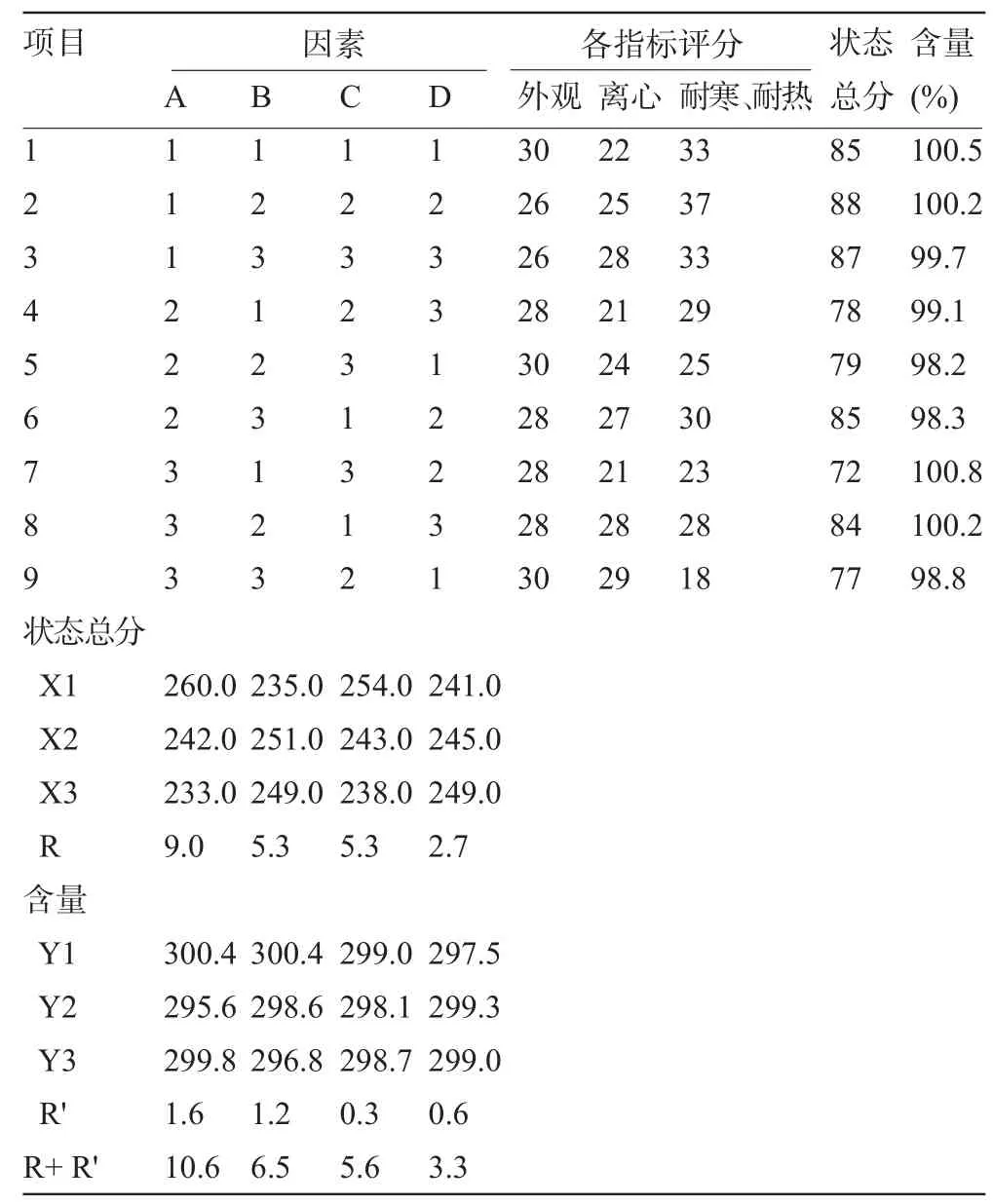
表2 处方正交试验结果(n=3)

表3 状态总分方差分析表
由直观极差分析可知:以状态总评分R为评价指标,各种因素的影响大小为A>B>D>C;以制剂含量极差R'为评价指标,各种因素的影响大小为A>B= C>D;综合极差R+R',各种因素的影响大小为A>B>C>D。依据表3状态总分方差分析结果表明,四因素均无显著性影响,制剂的状态总分最高以A1B2C1D3为宜。依据表4制剂的含量方差分析结果表明,A因素的影响差异具有统计学意义(P<0.05),A因素为1水平时,制剂的含量总分最高以A1B3C1D3为宜。综合考虑制剂状态总分和含量两项指标,确定最佳处方为A1B3C1D3,即白凡士林用量占总处方量的30%、液状石蜡用量占总处方量的15%、羊毛脂用量占总处方量的2%、十六醇用量占总处方量的13%。

表4 含量方差分析表
2.5 验证试验按照优选处方:白凡士林30%、液状石蜡15%、羊毛脂2%、十六醇13%;原料药夫西地酸钠均占总药量2%,加纯化水至30 kg。依2.1项的制备方法,以15 g/支的装样量进行分装,分别制得3批(2000支/批)夫西地酸钠乳膏,并按照夫西地酸钠乳膏的质量标准[7]和中国药典2010年乳膏剂的检查项[8]进行质量考察。试验结果表明各项检测指标均符合要求。
2.6 稳定性考察按照《中国药典》2010年版[8]中制剂稳定性考察方法,按照最优处方制得的3批夫西地酸钠乳膏,分别在温度(30±2)℃,相对湿度(65±5)%条件下进行加速试验,在温度(25±2)℃,相对湿度(60± 10)%条件下进行长期试验,定时取样,对其性状、鉴别、粒度、含量和微生物限度等项目进行考察。试验结果表明,在加速试验6个月和长期试验12个月后,各项指标均与新配乳膏数据差异无统计学意义,符合《中国药典》规定的各项指标,说明处方设计合理可行。
3 讨论
3.1 基质的调整笔者曾采用多种制备乳膏剂的辅料与夫西地酸钠混合乳化制成乳膏剂,在相同的制备工艺下,最后对这些辅料制得的乳膏剂进行质量研究发现:有的制剂出现油水分离情况;有的搽在皮肤上有砂粒感;有的甚至有开裂现象;有的影响原料的析出。说明选择的这些辅料制得夫西地酸钠乳膏剂不符合质量要求。笔者经多次试验筛选笔者选择:白凡士林、液状石蜡、羊毛脂、十六醇为夫西地酸钠乳膏的基质。
3.2 处方用量的筛选对于乳膏的配制有多种方法,但是由于夫西地酸钠在水和常用有机溶媒中的溶解度均较小,本文对这几种辅料的用量进行正交筛选,根据直观极差分析和方差分析结果,确定最佳的处方配比。处方正交筛选试验表明,直观极差分析和方差分析所得出的关键因素一致,说明该正交设计方案合理,结果可靠。经质量检测和稳定性考察结果表明,按照正交筛选处方制得的夫西地酸钠乳膏剂均匀、细腻、稳定且有适宜的粘稠度、粘着性、涂展性,涂布皮肤易软化、不溶化、无刺激性,对皮肤正常生理功能影响小,有适当的透皮性。该处方工艺可以用中试放大生产,为生产该制剂提供合理依据。
[1]陈卫东,刘雪芳.夫西地酸钠的药理研究及临床应用进展[J].中国当代医药,2012,19(34):24-25.
[2]Bauer CC,Apfalter P,Daxboeck F,et al.Prevalence of Panton-Valentine leukocidin genes in methicillin-resistant staphylococcus aureus isolates phenotypically consistent with community-acquired MRSA,1999-2007,Vienna General Hospital[J].European Journal of Clinical Microbiology&Infectious Diseases,2009,8:909-912.
[3]苏鲁·苏布拉马尼·瓦南加穆迪.一种制备夫西地酸乳膏的方法.中国,102325524A[P].2012-01-18.
[4]苏鲁·苏布拉马尼·瓦南加穆迪.使用夫西地酸钠制备的皮肤凝胶及其制备方法.中国,102325525A[P].2012-01-18.
[5]苏鲁·苏布拉马尼·瓦南加穆迪.使用夫西地酸钠和类固醇制备的新型皮肤用乳膏:中国,102292087A[P].2011-12-21.
[6]董娜.正交试验法优选新康松乳膏的制备工艺研究分析[J].黑龙江科技信息,2011,35:54.
[7]国家食品药品监督管局颁布.夫西地酸乳膏的质量标准JX20040002[S].北京:人民卫生出版社,2009.
[8]国家药典委员会.中华人民共和国药典:二部[S].北京:中国医药科技出版社,2010:附录IF、附录XIXC.
Study on stability and prescription screening of sodium fusidate cream.
YANG Li-zhen1,YANG Liu2,YU
Bang-liang2.
1.Department of Pharmacy,People's Hospital of Hainan Province,Haikou 571102,Hainan,CHINA; 2.Department of Pharmacy,Hainan Medical College,Haikou 571119,Hainan,CHINA
ObjectiveTo screen the best prescription of sodium fusidate cream.MethodsThe optimal prescription combination was determined by orthogonal experimental design L9(34)with the dosage of white Vaseline product(A),Liquid Paraffin(B),t lanolin(C)and hexadecanol(D)as consideration factors.The appearance and characteristics,centrifugation result,cold-resistant and thermotolreance were taken as quality evaluation indexes.ResultsThe optimal prescription combination was A1B3C3D3.Three batchs of sodium fusidate cream were prepared with A1B3C3D3 prescription.The indexes were all corresponded with the quality standard and examination of Ch.P 2010, and the stability was good.ConclusionThe prescription is reasonable and the result is reliable.
Sodium fusidate;Cream;Orthogonal experiment;Stability
R978.1
A
1003—6350(2014)17—2555—03
10.3969/j.issn.1003-6350.2014.17.0998
2014-02-28)
余邦良。E-mail:yubangliang@126.com
