人白细胞介素-36α蛋白的二级结构及其B细胞抗原表位的预测
2014-05-05陈少英郑坚牛青霞
陈少英,郑坚,牛青霞
(汕头大学医学院炎症与免疫性疾病研究所,广东 汕头 515041)
人白细胞介素-36α蛋白的二级结构及其B细胞抗原表位的预测
陈少英,郑坚,牛青霞
(汕头大学医学院炎症与免疫性疾病研究所,广东 汕头 515041)
目的预测并分析人白细胞介素-36α蛋白的二级结构及其潜在的B细胞抗原表位。方法以人IL-36α蛋白的氨基酸序列为基础,采用生物信息软件和互联网服务器预测人IL-36α蛋白的二级结构及其亲水性、可及性和柔韧性,根据预测结果综合分析IL-36α蛋白可能的B细胞抗原表位。结果IL-36α蛋白潜在的B细胞抗原表位位于N端8~12、33~38、111~116和143~149氨基酸区段。结论预测了IL-36α蛋白的二级结构和B细胞抗原表位,为进一步研究IL-36α的生物学活性部位及利用合成肽制备抗IL-36α的多克隆抗体提供了理论依据。
白细胞介素-36α;生物信息学;二级结构;表位
白细胞介素-1家族(Interleukin-1 family,IL-1F)的细胞因子与急性、慢性炎症有关,在天然免疫应答中发挥重要的作用。IL-1家族由11个成员组成,即IL-1F1~IL-1F11,其中IL-1F5、IL-1F6,IL-1F8、IL-1F9、IL-1F10和IF11是通过分析序列同源性、蛋白质的三维结构、基因位点和受体结合特征发现并鉴定的细胞因子[1-2],2010年上述细胞因子被重新命名为IL-36Ra、IL-36α、IL-36β、IL-36γ、IL-38和IL-33[3]。
IL-36α(曾被命名为IL-1F6)主要表达于皮肤和上皮组织,在免疫和炎症反应中发挥重要的作用。气道上皮细胞表达IL-36α,炎症刺激可增加气道上皮细胞IL-36αmRNA的表达。Ramadas等[4]的研究显示IL-36α刺激CD11c+细胞表达中性粒细胞特异性趋化因子CXCL1、CXCL2和TNFα,增加CD40的表达,增强CD11c+细胞诱导T细胞增殖的能力。IL-36α还可诱导CD4+T分泌IFN-γ、IL-4和IL-17[5]。体内实验显示,支气管灌注重组小鼠IL-36α后,可以引起野生型C57BL/6小鼠和IL-1αβ-/-小鼠肺部中性粒细胞侵润和肺部中性粒细胞特异性趋化因子mRNA表达的增加。最近的研究显示,肿瘤内IL-36α表达减少与肝癌患者的不良预后有关,提示IL-36α有可能成为肝癌患者预后的一个Marker[6]。本文以IL-36α的氨基酸序列为基础,利用生物信息学方法,预测IL-36α蛋白的二级结构和B细胞抗原表位,为抗IL-36α抗体制备及结构与功能研究提供理论依据。
1 材料与方法
1.1 IL-36α的氨基酸序列IL-36α的氨基酸序列来自NCBI提供的蛋白数据库(ACCESSION:NP_ 055255),见图1。

图1 IL-36α的氨基酸序列
1.2 人IL-36α二级结构的预测采用SOPMA计算工具分析IL-36α蛋白的二级结构[7]。
1.3 人IL-36α B细胞抗原表位的预测以7个氨基酸残基为一组,分别按Hopp&Woods亲水性方案[8]、Emini可及性方案[9]和Bhaskaran-Ponnuswamy柔韧性方案[10]进行单参数预测。综合各分析方法,取各参数预测结果的重叠区域,即为可能的B细胞抗原表位。
2 结果
2.1 人IL-36 α二级结构分析结果采用SOPMA服务器预测的IL-36α二级结构见图2。结果显示:IL-36α的二级结构由α-螺旋(15.19%)、β-折叠(35.44%)、β-转角(7.59%)、无规则卷曲(41.77%)组成。IL-36α蛋白的无规卷曲和β-转角主要位于第7~13、26~28、33~41、48~52、56~61、68~71、78~83、97~104、110~116、121~125、130~137、142~150位氨基酸(见图2)。

图2 人IL-36α二级结构预测结果
2.2 人IL-36α B细胞抗原表位的单参数预测结果IL-36α的亲水性、可及性和柔韧性预测结果见图3~图5。应用不同的参数预测的B细胞抗原表位出现的位置有所不同(见表1),但8~12、33~38、111~116和143~149肽段用多种参数分析得到了基本一致的结果,这些肽段可能为人IL-36α的B细胞抗原表位。
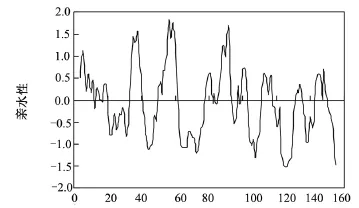
图3 IL-36α的亲水性分析

图4 IL-36α的柔韧性分析
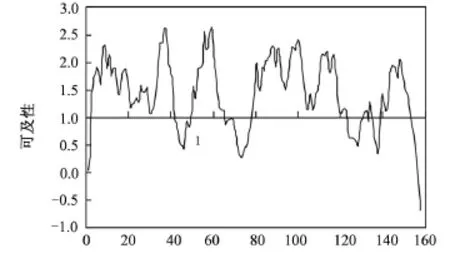
图5 IL-36α的可及性分析

表1 应用不同方法预测人IL-36αB细胞抗原表位的肽段位置
3 讨论
B细胞表位是指抗原中可被B细胞抗原受体(B cell receptor,BCR)或抗体特异性识别并相互结合的线性片段或空间构象型结构。应用生物信息学方法预测蛋白质的B细胞表位,并通过体外合成其肽段进行验证,是目前获得B细胞抗原表位肽段的重要方法。
本研究以人IL-36α的一级结构为基础,采用ProScale、Bcepred服务器上的相应软件和SOPMA软件,通过多参数分析预测人IL-36α的B细胞抗原表位。通过对二级结构、亲水性、柔韧性和可及性的综合分析,结果显示,人IL-36α蛋白可能的B细胞抗原表位位于N端8~12、33~38、111~116和143~149氨基酸区段,这些肽段具有较高的亲水性,在二级结构上位于或富含无规卷曲,符合表位分布的特点,并且与柔韧性参数和可及性参数预测的结果也相符。
由于IL-36α在炎症免疫过程中发挥重要作用,并且与T细胞免疫,特别是CD8+T细胞免疫应答的活化有关,肿瘤内IL-36α表达减少与肝癌患者的不良预后有关,因此,IL-36α有可能成为治疗炎症性疾病和癌症的新靶点。本文结果为人工合成IL-36α的B细胞抗原表位,进而制备抗IL-36α的抗体奠定了基础。
[1]Van de Veerdonk FL,Netta MG.New Insights in the Immunobiology of IL-1 Family Members[J].Front Immunol,2013,8(4):167.
[2]Smith DE,Renshaw BR,Ketchem RR,et al.Four new members expand the interleukin-1 superfamily[J].J Biol Chem,2000,275(2): 1169-1175.
[3]Dinarello C,Arend W,Sims J,et al.IL-1 family nomenclature[J]. Nat Immunol,2010,11(11):973.
[4]Ramadas RA,Ewart SL,Iwakura Y,et al.IL-36α exerts pro-inflammatory effects in the lungs of mice[J].PLoS One,2012,7(9): e45784.
[5]Vigne S,Palmer G,Lamacchia C,et al.IL-36R ligands are potent regulators of dendritic and T cells[J].Blood,2011,118(22): 5813-5823.
[6]Pan QZ,Pan K,Zhao JJ,et al.Decreased expression of interleukin-36α correlates with poor prognosis in hepatocellular carcinoma [J].Cancer Immunol Immunother,2013,62(11):1675-1685.
[7]Geourjon C,Deléage G.SOPMA:significant improvements in protein secondary structure prediction by consensus prediction from multiple alignments[J].ComputAppl Biosci,1995,11(6):681-684.
[8]Hopp TP.Protein surface analysis:methods for identifying antigenic determinants and other interaction sites[J].J Immunol Methods, 1986,88(1):1-18.
[9]Emini EA,Hughes JV,Perlow DS,et al.Induction of hepatitis A virus-neutralizing antibody by a virus-specific synthetic peptide[J].J Virol,1985,55(3):836-839.
[10]Bhaskaran R,Ponnuswamy PK.Positional flexibilities of amino acid residues in globular proteins[J].Int J Pept Protein Res,1988,32 (3):241-255.
Prediction of the secondary structure and B-cell epitopes of human interleukin-36 α.
CHEN Shao-ying,
ZHENG Jian,NIU Qing-xia.
Institute of Inflammation and Immune Diseases,Shantou University Medical College,Shantou 515041,Guangdong,CHINA
ObjectiveTo predict the secondary structure and B-cell epitopes of human interleukin(IL)-36α.MethodsBased on the IL-36α amino acid sequence,the secondary structure,hydrophilicity,flexibility and accessibility indexes of human IL-36α were analyzed with bioinformatics tool and network servers.Combined the results according to these methods,the B-cell epitopes of IL-36α were predicted.ResultsThe predicted B-cell epitopes of human interleukin-36α were probably located in or adjacent to 8~12,33~38,111~116 and 143~149 aa in the N-terminal.ConclusionThe secondary structure and B-cell epitopes predicted provide the basis for estimating the activity sites and developing antibodies against human IL-36α.
Interleukin-36α;Bioinformatics;Secondary structure;Epitope
R392.11
A
1003—6350(2014)08—1097—03
10.3969/j.issn.1003-6350.2014.08.0428
2013-11-05)
国家自然科学基金项目(编号:81072941)
牛青霞。E-mail:chenshaoying222@163.com