酸改性对褐煤半焦脱除烟气中元素态汞性能的影响
2014-04-28刘秀丽张林林张华伟山东科技大学化学与环境工程学院山东青岛266590
王 力,刘秀丽,张林林,李 敏,张华伟 (山东科技大学化学与环境工程学院,山东 青岛 266590)
酸改性对褐煤半焦脱除烟气中元素态汞性能的影响
王 力,刘秀丽*,张林林,李 敏,张华伟 (山东科技大学化学与环境工程学院,山东 青岛 266590)
为减少燃煤烟气中零价汞的排放,利用HCl和HNO3溶液对褐煤半焦改性研制了一种高效、低成本的吸附剂.运用酸碱滴定、Boehm滴定、BET、SEM和FTIR等技术对半焦吸附剂的表面特性进行表征与分析,利用固定床吸附实验装置及烟气测汞仪在线考察了半焦吸附剂对气态Hg0的吸附特性.结果表明,酸改性使半焦灰分含量降低,增加了半焦比表面积和羧基、酚羟基等官能团含量.酸改性处理可提高半焦对元素态单质汞的脱除效率,特别是盐酸溶液改性褐煤半焦可使吸附温度为140℃时的脱汞效率显著提高,这与改性半焦表面羧基、酚羟基和C-Cl官能团的含量及性质有关,半焦表面这些官能团能为Hg0的化学吸附提供活性位.
褐煤半焦;Hg0;酸改性半焦;酸性官能团
汞属于剧毒物质,富集在人体内的汞会对肝、肾以及中枢神经系统造成伤害.Lindqvist等[1]指出人为排放的汞约占大气中汞的 3/4.煤行业已成为最主要的汞污染物排放源[2-3].目前认为,燃煤烟气主要有3种形态的汞:元素态 Hg0、氧化态 Hg2+(主要为 HgCl2)以及颗粒态汞 Hgp[4-5],而 Hg0具有高的挥发性且难溶,在大气中的平均停留时间长达半年至两年,很难除去[6],是最难控制的形态,也是燃煤烟气脱汞的难点.我国褐煤储量丰富,而褐煤燃烧产生的烟气中,汞的形态以元素态为主[7],因此,我国控制治理汞排放的任务相对更加困难.
目前有多种方法可用于燃煤电站汞的脱除,但还没有一种成熟技术能实现广泛的商业应用[8].其中吸附剂法喷入技术是烟气中 Hg0污染物去除的主要方法.国内外燃煤烟气脱汞所用的吸附剂主要包括活性炭吸附剂、飞灰、钙基吸附剂、矿物类吸附剂和金属及金属氧化物等5类[9].活性炭是最常见的吸附剂,由于吸附剂喷射法对Hg0的脱除效率较差,可用硫、氯、溴等元素对活性炭进行改性以增加其吸附活性位.相关实验表明,当溴的掺杂量为 0.33%(质量分数)时,活性炭的吸附能力提高了80倍;经硫、氯化物浸泡后的活性炭对汞的吸附效率最高可达95%~98%[10-11].烟气中适量的HCl和O2是保证活性炭脱汞效率的关键,而 SO2、CO2的存在会使脱汞效率下降[12-13].吸附剂喷射法温度应用范围低,同时可能会影响布袋除尘器(FF)的清灰频率及小型电除尘器(ESP)的稳定运行.并且活性炭在脱汞过程中,需要源源不断地喷入大量新鲜的活性炭颗粒,由此产生了大量被不同类型汞污染的活性炭,解决此问题的一种实用方法是活性炭的再生利用[14].由于活性炭存在低容量、混合性差、低热力学稳定性的问题,使得活性炭注入法操作成本昂贵.美国能源部估计若要削减90%的汞,则每脱除453.6g汞需要25000~70000美元[15].因直接采用活性炭吸附汞的方法成本过高,燃煤电站难以承受,所以人们致力于开发新型、价格低廉吸附剂的研究工作.
半焦作为一种新型吸附材料,以其原料来源丰富、价格低廉、强度高等特点,受到研究者的普遍重视.张华伟[16]和 Tao等[17]分别用 AgNO3溶液和CeCl3⋅3H2O溶液浸渍制备了载银半焦和渗铈活性焦吸附剂进行脱除烟气中 Hg0的研究工作,取得了良好的脱汞效果.但用酸改性半焦进行燃煤烟气中脱汞的试验研究工作,国内外报道较少.本实验详细研究了酸改性半焦的制备及其表面性质的表征,对脱除电厂燃煤烟气中 Hg0具有实际意义.
1 实验部分
1.1 褐煤半焦制备过程
以内蒙古霍林河褐煤为原料,将粒径约 5~10mm样品颗粒置于沙浴中,放入马弗炉,在N2保护下于700℃干馏1h,冷却后,研磨、筛分出80~100目,即得原料半焦样 (NM-SC).
经过前期大量探索性实验,选取使半焦比表面积较大的改性浓度对半焦进行浸渍改性.将约10.0g原料半焦样品浸渍于质量分数为25%硝酸溶液中 80℃水浴 2h,可得到硝酸改性半焦(N-SC);取同样质量的原料半焦浸渍于质量分数为 25%盐酸溶液中在室温下放置 24h,冷却后抽滤、用蒸馏水洗涤至中性,并于60℃烘干,可得到盐酸改性半焦(Cl-SC).
1.2 半焦性质的分析与表征
按照GB/T212-2008《煤的工业分析方法》[18]对褐煤半焦进行工业分析.
采用北京彼奥德电子技术有限公司生产的SSA-4000全自动比表面积及孔径分析仪,在液氮温度77K下进行N2吸附-脱附实验.
采用美国 Nicolet380型傅里叶变换红外光谱(FTIR)测试仪进行样品表面官能团的测定,所记录的波长范围为400~4000cm-1.
采用KYKY2800B型扫描电镜(SEM,中国科学院科仪有限股份公司)对样品的微观形貌进行表征与分析.
1.3 气相中元素态汞的分析测定
采用QM201H燃煤烟气测汞仪对气体中汞的浓度进行在线测量,检测范围为 0~50µg/m3.汞进口浓度30 µg/m3,气体流量1L/min,吸附剂用量0.50g,吸附温度为30℃、140℃.
2 结果与讨论
2.1 原料半焦和酸改性半焦表面物理化学性质
2.1.1 原料半焦工业分析 原料半焦及酸处理半焦的工业分析和元素分析结果见表 1.可以看出,2种酸处理后半焦的灰分含量均会大幅降低,其中HCl溶液处理后半焦灰分降低幅度最大.
2.1.2 比表面积和孔径结构分析 由表2可以看出,原料半焦本身BET较小,HCl溶液处理后半焦的比表面积及总孔容积比原料半焦略有增大,平均孔径增加,表面微孔容积及微孔所占比例降低,这是由于HCl溶液可以与半焦孔隙中的灰分反应生成可溶性氯化物,在HCl溶液处理以及后续的洗涤过程中,半焦中部分原被灰分堵塞的孔道会被打通,从而使表面积和总孔容积增大,但是HCl溶液处理只增加了半焦中孔及大孔的容积,同时造成了部分微孔向中孔和介孔的过渡.HNO3溶液处理可显著提高半焦的比表面积和总孔容积,平均孔径略有降低,而表面微孔所占比例略有升高.HNO3溶液具有一定的脱灰作用,同时又具有一定的氧化性,在处理过程中一方面会由于灰分的脱除生成新孔,另一方面在较为温和的氧化条件下,HNO3溶液会与半焦中的部分有机质以及表面活性较高的碳发生反应,生成丰富的微孔,使得半焦表面积和总孔容积增大.
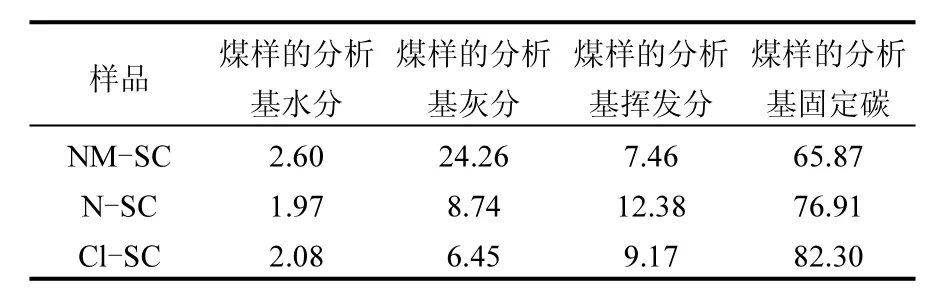
表1 原料半焦及不同酸处理半焦的工业分析(%)Table 1 The proximate analyses of virgin semi-coke and acid modified semi-coke (%)

表2 原料半焦及硝酸处理半焦的比表面积和孔径结构分析Table 2 The BET analyses of virgin semi-coke and acid modified semi-coke
2.1.3 酸碱官能团的分析 用酸碱滴定法[19-20]测定了原料半焦样品和改性半焦样品的表面酸碱性官能团含量,其结果如表3所示.由表3可以看出,硝酸和盐酸改性半焦样品与原料半焦相比,表面碱性官能团含量降低;而表面的酸性官能团含量显著增强,其中Cl-SC>N-SC.硝酸和盐酸改性半焦样品表面总体呈微弱酸性,表面酸性官能团占表面总官能团的90%以上.

表3 原料半焦及酸处理半焦表面酸碱官能团含量(mmol/g)Table 3 Surface acidic and basic groups content on virgin semi-coke and acid modified semi-coke (mmol/g)
Boehm 滴定法[21-22]可用于分析活性炭表面不同含氧官能团的分析,半焦表面含氧官能团酸性由强到弱分别为:羧基>内酯>酚羟基,分别计算出原料半焦及不同酸处理半焦表面的羧基、内酯基和酚羟基官能团的含量,结果见表 4.由表 4可以看出,半焦表面含氧官能团有−COOH, −OH,−C=O.经过硝酸改性后,羧基和酚羟基官能团的含量均有所增多,其中尤以羧基含量的增幅最大,达 380%,这使得半焦表面上总的含氧量比改性前有了大幅度的增加.经而过盐酸改性后,羧基和酚羟基大幅度增加,内酯基减少.

表4 原料半焦及酸处理半焦Boehm分析结果(mmol/g)Table 4 Boehm analysis of virgin semi-coke and acid modified semi-coke (mmol/g)
由图 1可以看出,硝酸处理后半焦在1383.37、1525.85以及1712.38波数处有新的吸收峰出现.在1383.37cm-1的峰归结为硝基的对称收缩振动吸收峰,说明改性过程新生成了含氮官能团;1525.85cm-1是 COO的反对称伸缩振动峰;1712.12cm-1波数处的峰为为羧基、羰基、醛基、酯基或乙酰基的派生物中C=O的伸缩振动峰[23];盐酸处理后的半焦红外谱图与原料半焦比较相似.

图1 原料半焦及酸处理半焦的FTIR分析谱图Fig.1 virgin semi-coke and acid modified semi-coke FTIR analysis spectrum
结合酸碱滴定法、Boehm滴定法和红外光谱分析,可以看出,酸改性处理前后半焦的表面官能团发生了很大变化,硝酸处理后可增加半焦表面多种含氧官能团、含氮官能团,其中以羧基为主;盐酸改性处理后可主要增加羧基和酚羟基等酸性官能团含量.
2.2 半焦对气态Hg0的吸附性能

图2 硝酸/盐酸处理对NM-SC除汞性能的影响Fig.2 Effect of temperature on the adsorption of HNO3/HClsemi-coke
由图2可见,硝酸处理可不同程度提高吸附温度分别为 30℃、140℃半焦的脱汞效率;而盐酸改性可以明显提高吸附温度为140℃时的脱汞效率.
2.3 半焦对于气态Hg0的脱除机理
对于改性后吸附效率的提高,普遍认为半焦除汞能力与其比表面积大小和表面的化学官能团存在一定关系.低温时气态 Hg0在半焦表面以物理吸附作用为主,吸附剂比表面积(BET)越大,微孔越多越有利于吸附,尤其是物理吸附;同样化学吸附中大比表面积亦有利于反应活性位的裸露[24].吸附温度为30℃时,3种半焦的除汞性能顺序为 N-SC>NM-SC>Cl-SC,从比表面积和孔径结构分析数据数据可以看出,由于 N-SC比表面积最大,因此硝酸改性半焦除汞效率最高;盐酸处理使Cl-SC的比表面积和总孔容积略有增大,通过图3可以看出,原料半焦的表面较为平整,分布着形状不规则,大小不均匀的孔道.盐酸处理使Cl-SC表面出现了许多大小不一的新孔,但微孔比例和微孔孔容却有所下降,而气态 Hg0主要物理吸附在半焦的微孔中,因此导致了30℃半焦除汞效率的降低.

图3 原料半焦及不同酸处理改性半焦的表面形貌Fig.3 SEM images of virgin semi-coke and acid modified semi-coke
当吸附温度为140℃时,3种半焦的除汞性能顺序为 Cl-SC>N-SC>NM-SC.高温时气态 Hg0在半焦表面以化学吸附作用为主.盐酸和硝酸处理会改变半焦的表面化学性质,主要表现为羟基、酚羟基等含氧官能团含量增加,他们与气态单质汞发生螯合反应,如图4所示.因此能提高改性半焦脱汞效率.

图4 Hg0与半焦表面官能团螯合反应示意Fig.4 Hg0and semi-coke surface functional group chelation schematic
而盐酸改性半焦的脱汞效率能远高于原料半焦,并且吸附 140min后,除汞效率还可一直保持在 90%以上,这是由于用盐酸溶液改性褐煤半焦时,盐酸溶液中的 Cl-会在半焦表面进行离子交换反应,使部分氯元素负载到半焦表面,形成C-Cl官能团[25],当半焦表面 Cl-浓度较高时,Hg0会与Cl-反应生成HgCl2[26],如式(1)~式(3)所示.
氯原子可能和单质汞发生如下反应:
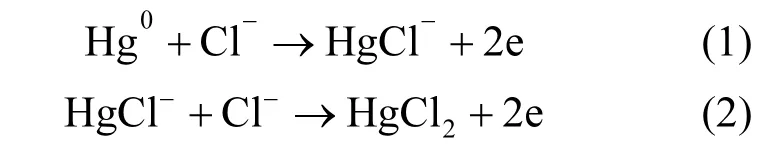
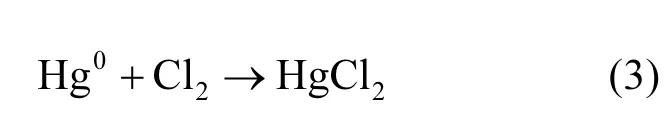
有的学者认为当氯离子足量的时候,还可以进一步反应,生成复杂的四氯化汞的形式[27]:
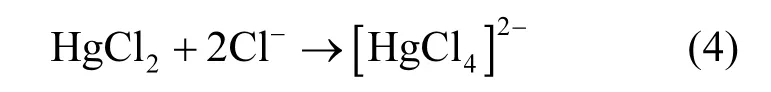
由于它们之间发生了化学反应,因此,在吸附剂的孔内和表面形成了较稳定的含汞化合物[28].
盐酸改性半焦表面的C=O键和离域π电子也可作为电子受体,促使Hg0被氧化为Hg2+,然后与氯元素结合.盐酸处理后半焦表面形成的含氧官能团和含氯基团均可为气态 Hg0的化学吸附提供活性位[29],从而大幅提高了半焦在 140℃时的除汞效率.
3 结论
3.1 硝酸和盐酸改性具有脱灰作用,同时提高了改性半焦比表面积、羧基和酚羟基等官能团的含量,使改性半焦表面酸性增强.
3.2 硝酸改性半焦能提高吸附温度为 30℃和140℃时半焦脱除烟气中汞的效率;而盐酸改性后,可显著提高吸附温度为140℃时的除汞效率. 3.3 吸附温度为 30℃时,比表面积的大小和微孔数量对吸附效率有很大影响;吸附温度为140℃时,官能团的种类对汞的吸附影响因素最大,半焦表面羧基和酚羟基等酸性官能团含量的提高,增加了Hg0的氧化和吸附活性位,从而提高半焦的除汞效率.
3.4 盐酸溶液中的 Cl-会负载到半焦表面,形成C-Cl官能团,半焦表面形成的含氧官能团和含氯基团均可为气态 Hg0的化学吸附提供活性位,Hg0会与Cl-反应生成HgCl2,从而提高半焦表面除汞效率.
[1] Oliver Lindqvist, Henning Rodhe. Atmospheirc mercury-a review [J]. Tellus, Series B: Chemical and physical meteorology, 1985,37B:136-159.
[2] Li P, Feng X B, Qiu G L, et al. Mercury pollution in Asia: A review of the contaminated sites [J]. Journal of Hazardous Materials, 2009,168(2/3):591-601.
[3] Glodek A, Pacyna J M. Mercury emission from coal- fi red power plants in Poland [J]. Atmospheric Environment, 2009,43(35):5668-5673.
[4] 濮洪九.洁净煤技术产业化与我国能源结构优化 [J]. 煤炭学报, 2002,27(1):1-7.
[5] Galbreath K C, Zygarlicke C J. Mercury transformations in coal combustion flue gas [J]. Fule Processing Technology, 2000, 65-66(1):289-310.
[6] 孟素丽,段钮锋,杨立国,等.燃煤烟气中汞脱除技术的研究进展[J]. 锅炉技术, 2008,39(4):77-80.
[7] 赵 毅,张自丽.电厂燃煤过程中汞控制技术研究 [J]. 电力科技与环保, 2010,26(2):31-33.
[8] Robert P. Mercury removal standards are coming, Where’s the technology [J]. Power, 2003,147(4):40-47.
[9] Presto A A, Granite E J. Survey of catalysts for oxidation of mercury in flue gas [J]. Environmental Science and Technology, 2006,40(18):5601-5609.
[10] 孙 巍,晏乃强,贾金平.载溴活性炭去除烟气中的单质汞 [J].中国环境科学, 2006,26(3):257-261.
[11] Radisav D, Douglas P. Vapor phase elemental mercury adsorption by activated carbon impregnate with chloride and chelating agents [J]. Carbon, 2001,39(1):3-14.
[12] 任建莉,周劲松,骆仲泱,等.活性炭吸附烟气中气态汞的试验研究 [J]. 中国电机工程学报, 2004,24(2):171-175.
[13] 高洪亮,周劲松,骆仲泱,等.燃煤烟气中汞在活性炭上的吸附特性 [J]. 煤炭科学技术, 2006,34(5):49-52.
[14] Pavlish J H, Sondreal E A, Mann M D, et al. Status review of mercury control options for coal-fired power plants [J]. Fuel Processing Technology, 2003,82(2):89-165.
[15] Ho T C, Lee Y, Chu H W, et al. Modeling of mercury desorption from activated carbon at elevated temperatures under fluidizedfixed bed operations [J]. Powder Technology, 2005,151(1-3): 54-60.
[16] Zhang Huawei, Liu Shanshan, Chen Jitao, et al. Research on the preparation of silver-loaded semi-coke and its adsorption characteristics to gas-phase Hg0[J]. Advanced Materials Research Vols, 2012,(356-360):1350-1355.
[17] Tao Shasha, Li Caiting, Fan Xiaopeng, et al. Activated coke impregnated with cerium chloride used for elemental mercury removl from simulated flue gas [J]. Chemical Engineering Journal, 2012,210:547-556.
[18] GB/T212-2008 煤的工业分析方法 [S].
[19] Rubio B, Izquierdo M T. Influence of low-rank coal char properties on their SO2removal capacity from flue gas: Ⅰ. Non-activated chares [J]. Carbon, 1997,35(7):1005-1011.
[20] Rubio B, Izquierdo M T. Influence of low-rank coal char properties on their SO2removal capacity from flue gas: Ⅱ. Activated chares [J]. Carbon, 1997,36(3):263-268.
[21] Boehm H P. Some as pects of the surface chemistry of carbon blaeks and other carbons [J]. Carbon, 1994,32(5):759-769.
[22] StrelkoJr V, Malik D J, Streat M. Characterisation of the surface of oxidised carbon adsorbents [J]. Carbon, 2002,40:95-104.
[23] 沈曾名,张文辉,张学军,等.活性碳材料的制备与应用 [M]. 北京:化学工业出版社, 2006.
[24] Zeng H C, Jin F, Guo J 1. Removal of elemental mercury from coal combustion flue gas by choride-impregnated activated carbon1 [J]. Fuel, 2004,83(1):143-146.
[25] Granite E J, Pennline H W, Hargis R A. Novel sorbents for mercury removal from flue gas [J]. Industrial and Engineering Chemistry Research, 2002,39(4):1020-1029.
[26] Zeng Hancai, Jin Feng, Guo Jia. Removal of elemental mercury from coal combustion flue gas by chloride-impregnated activated carbon [J]. Fule, 2004,83(1)143-146.
[27] Carrott P J M, Carrott M M L R, Nabais J M V. Influence of surface ionization on the adsorption of aqueous mereury chlorocomplexes by activated carbons [J]. Carbon, 1998,36(l/2): 11.
[28] 任建莉,周劲松,骆仲泱,等.新型吸附剂脱除烟气中气态汞的试验研究 [J]. 中国电机工程学报, 2007,27(2):48-53.
[29] Li Y H, Lee C W, Gullett B K. Importance of activated carbon’s oxygen surface functional groups on elemental mereury adsorption [J]. Fuel, 2003,82(4):451-457.
Effect of lignite semi-coke by acid solution treatment on its performance for elemental mercury removal in the fluegas.
WANG Li, LIU Xiu-li*, ZHANG Lin-lin, LI Min, ZHANG Hua-wei (College of Chemical and Environmental
Engineering, Shandong University of Science and Technology, Qingdao 266590, China). China Environmental Science, 2014,34(12):3056~3061
The adsorption performance of modified lignite semi-coke with HCl or HNO3solution for gaseous Hg0was investigated to develop more effective and lower price adsorbents for reducing emission of elemental mercury in coal combustion flue. The surface properties of these lignite semi-coke adsorbents were characterized with methods of acid-base titration, Boehm titration, Brunauer-Emmett-Teller (BET) measurement, scanning electron microscope (SEM) and Fourier Transform infrared spectroscopy (FTIR), respectively. The adsorption experiments of semi-coke adsorbents for gas-phase Hg0have been carried out with a laboratory-scale fixed-bed reactor, and elemental mercury analyzer was used to determine the on-line concentrations of gas-phase Hg0. Nitric acid or hydrochloric acid treatment of lignite semi-coke resulted in the decrease in ash content of semi-coke sample, and the values of specific surface area, surface oxygen and phenolic hydroxyl group increasing of modified semi-cokes. Compared to raw lignite semi-coke (NM-SC), the modified lignite semi-coke with HCl or HNO3solution (Cl-SC or N-SC sample) could improve removal performance for gas-phase Hg0. Especially, the removal performance for gas-phase Hg0of Cl-SC semi-coke was obviously improved when adsorption temperature increased to 140℃. These results were related to the surface properties of modified semi-coke and its contents of carboxyl group, phenolic hydroxyl and C-Cl functional groups, which can provide active sites for gaseous Hg0chemical adsorption.
lignite semi-coke;Hg0;semi-coke modified by acid solution;acidic functional group
X513,TQ 536.9
A
1000-6923(2014)12-3056-06
王 力(1966-),男,山东省单县人,教授,博士,主要从事矿物材料的研究.发表论文100余篇.
2014-02-25
国家自然科学基金资助项目(21276146,51406107);山东科技大学研究生创新基金项目(YC140215)
* 责任作者, 硕士, liuxiuli1103@sina.cn
