离子交换树脂对咖啡因溶液提浓性能的研究
2014-04-02杜德清夏丙堃尹进华
杜德清,夏丙堃,尹进华
(1.山东新华制药股份有限公司,山东 淄博 255000;2.青岛科技大学化工学院,山东 青岛 266042)
咖啡因属于黄嘌呤生物碱化合物的一种,分子式C8H10N4O2,存在于茶、咖啡果等植物体中[1],具有较强的中枢兴奋功能,广泛应用于解热镇痛类药品、能量饮料等领域。目前国内普遍采用以氯乙酸为原料的化学法合成咖啡因。现有生产工艺中,母液中咖啡因的质量浓度约为1%,主要通过膜浓缩、氯仿萃取、蒸发、结晶、精制等操作进行回收,然后汽提处理氯仿萃取后的废水,存在工艺复杂、溶剂损耗大、能耗高等弊端[2]。为此,作者利用咖啡因作为生物碱在溶液中易形成离子态的特性,选用不同型号酸性阳离子交换树脂,对低浓度咖啡因溶液的离子交换能力、洗脱速度及提浓性能进行研究,确定了最佳的吸附洗脱条件,拟为工业生产中结晶母液回收咖啡因过程提供参考。
1 实验
1.1 试剂与仪器
盐酸、硫酸(98%)、氢氧化钠、无水乙醇,分析纯,市售;精制咖啡因、非那西汀,山东新华制药股份有限公司;实验用水为蒸馏水。
732、D-151强酸性离子交换树脂、724、D-113弱酸性离子交换树脂,市售;交换洗脱柱Ⅰ(∅1 cm×30 cm)、交换洗脱柱Ⅱ(∅2.8 cm×50 cm),自制。
GC-14C 型气相色谱仪,Shimaden;SHZ-A 型水浴恒温振荡器;METTLER TOLEDO分析天平;CH1015型超级恒温槽。
1.2 色谱条件
FID检测器;毛细管色谱柱(30 m×0.32 mm,0.5 μm),固定相Se-54,柱温230 ℃;进样器、检测器温度260 ℃;进样量0.4 μL;分流比1∶20;内标物:非那西汀。
1.3 树脂的预处理[3-9]
首先将树脂于2 倍体积的饱和食盐水中浸泡18~20 h,用清水洗净,至排出水不带黄色;然后用2%~4%NaOH溶液浸泡2~4 h,用清水冲洗至近中性;最后用5%HCl溶液浸泡4~8 h,用清水漂洗至中性,待用。
1.4 树脂筛选
取已预处理的树脂15 mL,分别装入交换洗脱柱Ⅰ中。将起始浓度为1%的咖啡因溶液以8 BV·h-1的流速上柱进行动态交换,测定交换后溶液的咖啡因浓度,达到1%时为该树脂穿透点。
1.5 洗脱剂筛选
根据1 g咖啡因溶于46 mL水、5.5 mL 80 ℃的水、22 mL体积分数为70%的乙醇溶液的性质,结合咖啡因的弱碱性,分别选用80 ℃水、70%乙醇、质量分数为0.05%和0.5%的硫酸溶液为洗脱剂,对浓度为1%的咖啡因溶液交换饱和后的树脂进行单次洗脱,筛选合适的洗脱剂。
1.6 叠加洗脱实验
目前工业生产过程中,氯仿萃取咖啡因结晶母液后咖啡因浓度约为1%。结合生产经验,通过树脂交换、洗脱后,洗脱液中咖啡因浓度可达到7%,通过结晶可回收咖啡因。采用交换洗脱柱Ⅰ,对交换饱和后的树脂进行洗脱,然后将浓度最高的洗脱液继续用树脂交换、洗脱,获得更高浓度的洗脱液,以此类推、叠加,直至获得咖啡因浓度7%以上的洗脱液。
考虑到交换洗脱柱Ⅰ高径比值较大,可能存在壁流效应,采用交换洗脱柱Ⅱ将处理量放大15倍,验证叠加洗脱效果。
1.7 咖啡因浓度的测定
咖啡因浓度采用气相色谱仪测定。采用内标与标准曲线相结合的方法,获得校准后的校正因子,以减小分析误差。
咖啡因标准溶液:配制0.5%、1.0%、1.5%、2.0%、2.5%、3.0%、3.5%、4.0%、4.5%浓度梯度的咖啡因标准溶液。
内标液:0.5%非那西汀乙醇溶液。
将咖啡因标准溶液与浓度为0.5%的非那西汀溶液配制成标准品溶液。进样标准品溶液,测定峰面积A,以A样(标准品溶液中咖啡因的峰面积)与A内(标准品溶液中内标物的峰面积)的比值为纵坐标、咖啡因浓度(c,%)为横坐标绘制标准曲线,如图1所示。


图1 峰面积比值与咖啡因浓度关系图
2 结果与讨论
2.1 不同树脂的交换容量
交换洗脱柱Ⅰ分别装填724、D-113、732、D-151树脂,将1%咖啡因溶液上柱进行动态交换,结果见图2。
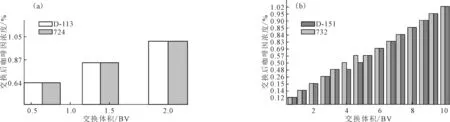
图2 离子交换树脂的交换效果
从图2可以看出,724树脂、D-113树脂的泄漏点很小,大约为2 BV,交换容量较小,不适合提浓咖啡因溶液;732树脂、D-151树脂泄漏点都在10 BV左右,交换容量大,对咖啡因的交换能力更强。因此,选择732树脂、D-151树脂进行后续实验。
2.2 洗脱剂对咖啡因的洗脱效果
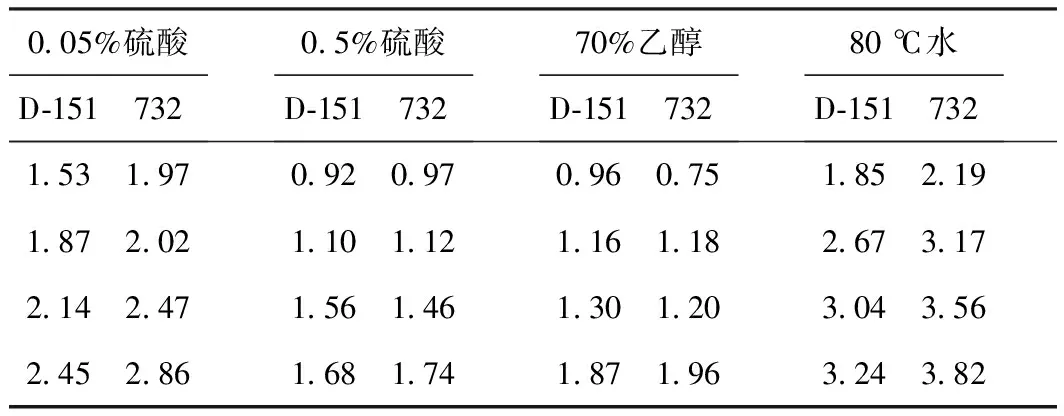
交换洗脱柱Ⅰ分别装填732树脂、D-151树脂,对浓度为1%的咖啡因溶液交换饱和后,选用不同洗脱剂进行洗脱,结果见表1。
由表1可以看出,相比于0.05%硫酸、0.5%硫酸、70%乙醇溶液,80 ℃水更适合作为洗脱剂,而且在使用过程中也不引入其它物质,有利于结晶回收咖啡因;732树脂洗脱时,提浓速度和洗脱液浓度都高于D-151树脂,因此,更适合作为咖啡因溶液的交换洗脱树脂。
表1洗脱剂对咖啡因的洗脱效果/%
Tab.1Theelutionefficiencyforcaffeine/%
005%硫酸D⁃15173205%硫酸D⁃15173270%乙醇D⁃15173280℃水D⁃151732153197092097096075185219187202110112116118267317214247156146130120304356245286168174187196324382
2.3 叠加洗脱效果
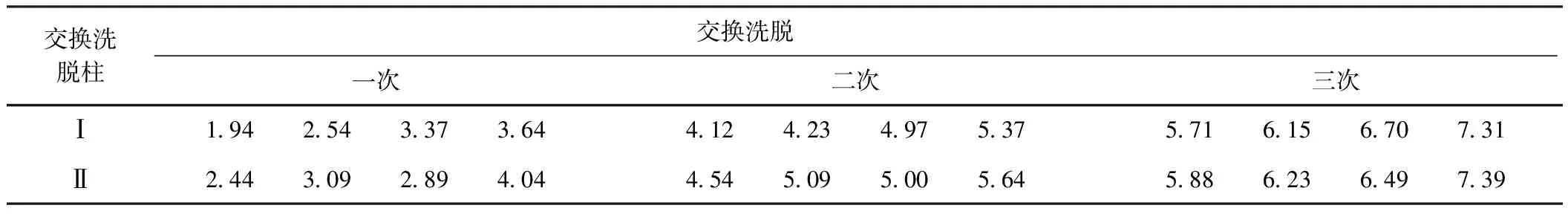
732树脂分别装填于交换洗脱柱Ⅰ、交换洗脱柱Ⅱ,将1%咖啡因溶液进行叠加洗脱实验,结果见表2。
表2叠加洗脱效果/%
Tab.2Theelutionresultsofsuperimposedexperiments/%
交换洗脱柱交换洗脱 一次 二次 三次Ⅰ194 254 337 364 412 423 497 537 571 615 670 731Ⅱ244 309 289 404 454 509 500 564 588 623 649 739
由表2可见,在交换洗脱柱Ⅱ上732树脂对1%咖啡因溶液进行第一次交换、洗脱后,浓度可达4.04%;将浓度为4.04%的洗脱液进行二次交换、洗脱后,浓度可达5.64%;三次交换、洗脱后,浓度可达7.39%,实现了咖啡因溶液提浓的目的。交换洗脱柱Ⅰ与交换洗脱柱Ⅱ的洗脱液浓度增加规律一致,后者效率略高于前者。
3 结论
选用不同型号阳离子交换树脂和洗脱剂,对1%咖啡因溶液交换、洗脱过程进行研究。结果表明:相比于724、D-113、D-151树脂,732树脂交换处理量达10 BV,洗脱速度快,单次洗脱浓度可达3.82%;80 ℃水更适合作为洗脱剂;经过3次叠加交换、洗脱后,1%咖啡因溶液提浓到7.39%,可为工业生产中结晶母液回收咖啡因过程提供参考。
参考文献:
[1]韩佳宾,陈静,王静康,等.咖啡因制备方法研究进展[J].化工时刊,2003,17(3):13-16.
[2]孙培宾,陈江,尹进华,等.XDA-8大孔树脂对高浓度咖啡因的吸附热力学研究[J].化学与生物工程,2011,28(4):62-64.
[3]单鹰飞,刘红霞.氯仿萃取咖啡因工艺的改进[J].黑龙江日化,1997,(4):14-15.
[4]李梦耀,熊玉宝,孙琴.HDX-8树脂吸附咖啡因的研究[J].应用化工,2006,35(12):907-917.
[5]唐课文,周春山,钟世安,等.聚酰胺树脂对茶多酚和咖啡因吸附选择性研究[J].光谱学与光谱分析,2003,23(1):143-145.
[6]GB 5757-86,离子交换树脂含水量测定方法[S].
[7]WANG F,WANG L J,LI J S,et al.Adsorption behavior and mechanism of cadmium on strong-acid cation exchange resin[J].Transact Ions of Nonferrous Metals Society of China,2009,(3):740-744.
[8]GUSLER G M,BROWNE T E,COHEN Y.Sorption of organics from aqueous solution onto polymeric resins[J].Ind Eng Chem Res,1993,32(11):2727-2735.
[9]PAN B C,XIONG Y,LI A M,et al.Adsorption of aromatic acids on an aminated hypercrosslinked macroporous polymer[J].React Funct Polym,2002,53(2):63-72.
