细粒棘球蚴EG95s重组蛋白串联表达免疫原性分析
2014-04-02袁维峰侯绍华郭晓宇马世春朱鸿飞
贾 红,袁维峰,李 杰,侯绍华,郭晓宇,鑫 婷,马世春,朱鸿飞
棘球蚴病(Echinococcosis granulosus)又称包虫病( Hydatidosis),是由细粒棘球蚴绦虫的中绦期幼虫—细粒棘球蚴(Echinococcusgranulosus,Eg)寄生于哺乳动物肝、肺等脏器所引起人类、牛羊的人畜共患寄生虫病。免疫接种是防治该病的方法之一[1-2],近年来, 随着基因工程技术的发展,Eg95 蛋白是一种分子质量为24.5 ku的天然六钩蚴抗原。其编码基因全长为715 bp, 其中462 bp基因可编码分子质量为16. 5 ku的含153个氨基酸的蛋白质[3]。Eg95的作用为使绵羊获得免疫保护[4-6]。本研究力图通过探讨可溶性EG95s重组蛋白的免疫原性,及比较串联后免疫原性差异,为包虫病疫苗研究奠定基础。
1 材料与方法
1.1材料 8w(下同)龄BALB/c购自北京维通利华实验动物技术有限公司。pET-1EG95s、pET-2EG95s和pET-3EG95s重组质粒为本室制备和保存。弗氏完全佐剂和弗氏不完全佐剂购自Sigma公司;OptEIATMSet Mouse IFN-γ试剂盒购自美国BD公司;Tween-20购自索莱宝生物公司;增强型HRP-DAB底物显示试剂盒和可溶性单组分TMB底物溶液购自天根公司;辣根过氧化物酶HRP标记羊抗鼠IgG购自中杉金桥公司;其他试剂为分析纯产品。
1.2重组蛋白的制备与鉴定 将pET-1EG95s、pET-2EG95s、pET-3EG95s重组菌37℃摇振培养过夜,次d按10% 转接40 mL,37℃摇振培养至OD600=2.0时,加入IPTG至终浓度0.025 mmol/L,诱导6 h,表达产物通过AKTA purifier按照His FF crude说明书进行纯化。纯化蛋白分别命名为HIS-1EG95s、HIS-2EG95s、HIS-3EG95s,对纯化后的蛋白进行Western-blot验证。
1.3免疫程序 将32只6-8周龄的BALB/c小鼠,随机分为4组,每组8只。1组作为空白对照,另3组分别免疫HIS-1EG95、HIS-2EG95、HIS-3EG95。将纯化好的蛋白分别用紫外分光光度计定量,免疫剂量为40 μg/次/只。将重组蛋白抗原加弗氏完全佐剂1∶1均匀乳化后,腹部皮下多点注射免疫接种小鼠,首次免疫2 w后,以相同剂量加等量弗氏不完全佐剂腹腔注射进行第2次免疫,间隔4 w后进行第3次免疫,方法同第2次免疫。
1.4样品收集 分别于1免后第1 w、2w、3 w(2免后1 w)、4 w(2免后2 w)对小鼠进行断尾采血, 第6 w(3免后2 w)摘眼球采血。每次采血约50-100 μL,37℃静置1 h,4 ℃过夜,4 ℃、4 000 r/min离心10 min,取上清置于灭菌EP管中,于- 80 ℃保存备用。
1.5免疫小鼠血清特异性抗体检测 参照本实验室建立的羊细粒棘球蚴病抗体间接ELISA检测方法进行[7],具体如下:
以纯化的HIS-1EG95s蛋白包被ELISA板, 100 μL /孔(1 μg),4℃过夜,取出后PBST洗涤3次,每次3 min;再加含10%牛血清的PBST(封闭液),200 μL/孔,于37 ℃封闭2 h,取出洗涤同前;将所有小鼠血清样本进行1∶200倍稀释,加入设定的孔中,100 μL /孔,同一样品作3个重复孔,并作1个空白对照孔,于37℃作用1 h,取出洗涤;接着加100 μL酶标2抗(工作浓度1∶5 000)于37 ℃作用1 h,取出洗涤;继而加入100 μL底物溶液,37 ℃避光反应15 min;最后加入100 μL 2mol/L的H2SO4终止反应。在酶标仪上测定OD450 nm值。
1.6免疫42d后免疫小鼠最终抗体滴度的检测 将3次免疫后2 w所采的小鼠血清样本由1∶200倍开始进行2倍梯度稀释,按以上ELISA方法进行检测,得到小鼠血清最终抗体滴度。
1.7免疫后IFN-γ检测 于1免后第3 d对小鼠采血,离心分离血清,利用BD OptEIATMSet Mouse IFN-γ试剂盒(BD Biosciences, San Diego, CA)检测小鼠血清中IFN-γ的含量。
1.8与血清反应的差异分析 将HIS-1EG95、HIS-2EG95和HIS-3EG95按10和1 μg/mL浓度包被,用足量的羊包虫阳性血清和阴性血清和酶标二抗进行间接ELISA检测,分析HIS-1EG95、HIS-2EG95和HIS-3EG95反应的差异性。

2 结 果
2.1重组蛋白的纯化和检验 将纯化的重组蛋白进行SDS-PAGE电泳,确认其纯化效果(见图1),经Western-blot验证,纯化后的3种重组蛋白均能与绵羊EG95阳性血清反应产生特异性条带(见图2),表明重组蛋白具有反应原性,因此,该种方法纯化的重组蛋白抗原可用于免疫动物,研究其免疫原性。
2.2免疫后小鼠抗体动态水平监测 将免疫后第1、2、3、4、6 w采集到的各组小鼠血清以1∶200倍稀释,进行ELISA检测将采集到的各组小鼠血清以1∶200倍稀释,进行ELISA检测,结果见表1和图3。
结果显示,首次免疫后,3个重组蛋白免疫组抗体水平均迅速上升,免疫后1 w即能检测到特异性抗体,与对照组相比差异显著(P<0.01)。2免和3免后抗体反应OD450nm值与1免相比,差异显著(P<0.05),2免与3免后的抗体反应OD450 nm值相比,无显著差异(P>0.05)。1免后,HIS-1EG95s组抗体水平迅速升高,与其他两组相比P<0.05,而1免后2 w开始,HIS-3EG95s组抗体水平逐渐超过HIS-1EG95s组。而在整个过程中,HIS-2EG95s组抗体水平均低于其他两组,且差异明显(P<0.05)。
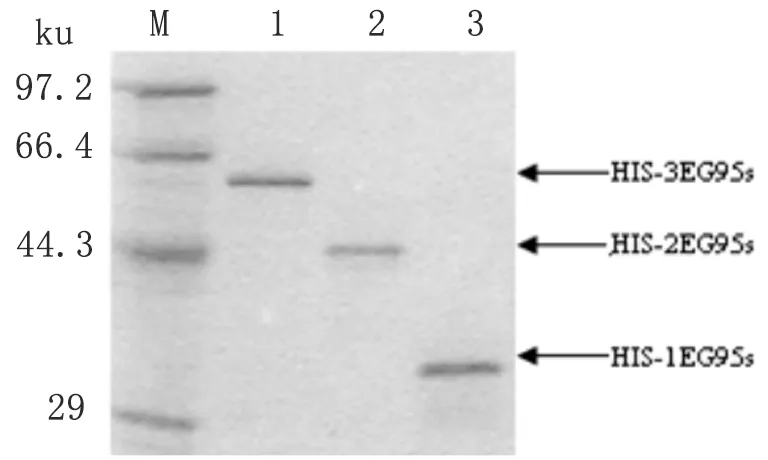
图1蛋白纯化效果鉴定
M: 蛋白低分子量marker; 1: HIS-31EG95s; 2: HIS-2EG95s; 3: HIS-13EG95s.
Fig.1Resultofthepurifiedprotein
M: Low molecular weight protein marker; 1: HIS-1EG95s; 2: HIS-2EG95s; 3: HIS-3EG95s.

图2纯化蛋白的Western-blot鉴定
M: 蛋白低分子量marker; 1: HIS-31EG95s; 2: HIS-2EG95s; 3: HIS-13EG95s.
Fig.2IdentificationofpurifiedproteinbyWestern-blot
M: Low molecular weight protein marker; 1: HIS-1EG95s; 2: HIS-2EG95s; 3: HIS-3EG95s.
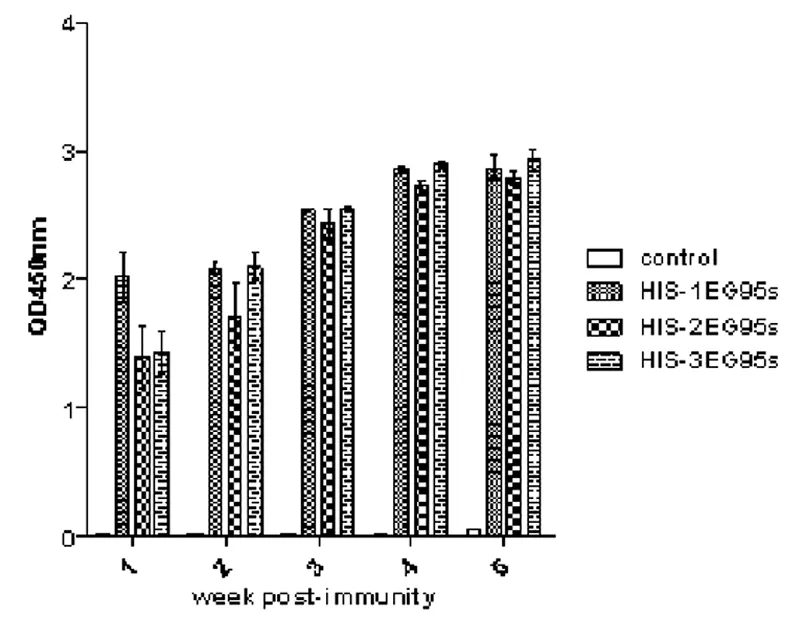
图3 小鼠血清抗体动态水平
2.3免疫42 d后小鼠最终抗体滴度的检测 用ELISA法测定第l次免疫后第6 w(42 d)小鼠的血清抗体滴度,从1∶200开始倍比稀释到1∶1 638 400的OD450nm值,结果见表2及图4。
结果显示,免疫组的抗体水平与对照组的抗体水平在所有滴度上均有明显的统计学差异(P<0.01),说明重组蛋白免疫确实诱导小鼠产生了特异性的抗体。

图4 免疫42 d后小鼠最终抗体滴度
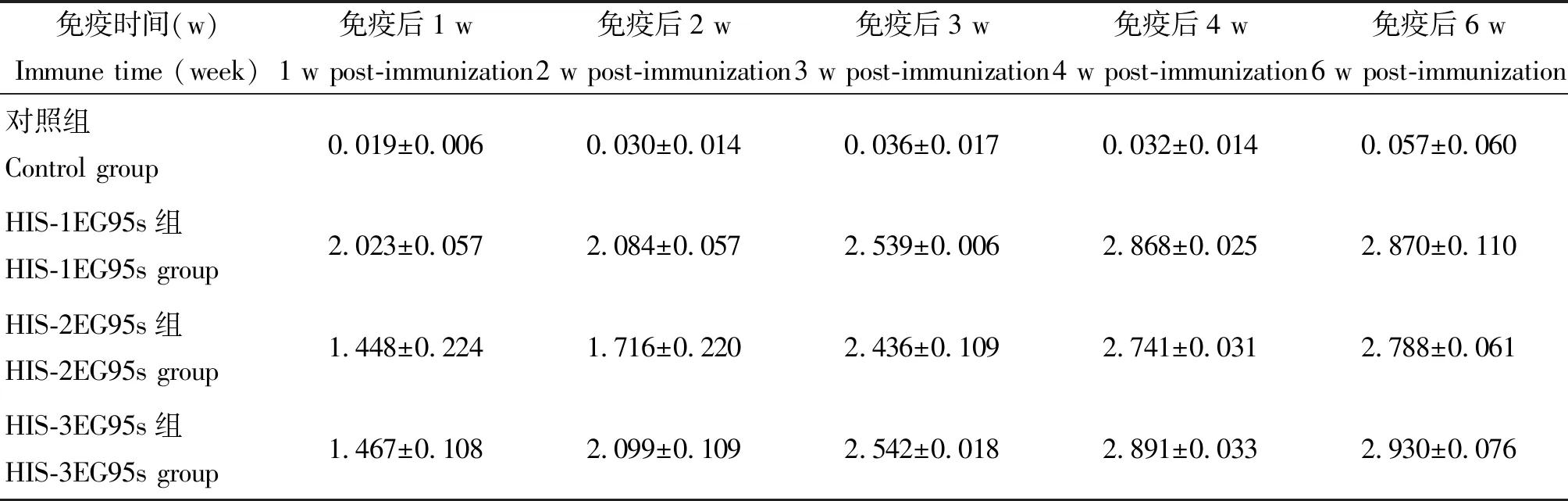
免疫时间(w)Immune time (week)免疫后1 w1 w post-immunization免疫后2 w2 w post-immunization免疫后3 w3 w post-immunization免疫后4 w4 w post-immunization免疫后6 w6 w post-immunization对照组Control group0.019±0.0060.030±0.0140.036±0.0170.032±0.0140.057±0.060HIS-1EG95s组HIS-1EG95s group2.023±0.0572.084±0.0572.539±0.0062.868±0.0252.870±0.110HIS-2EG95s组HIS-2EG95s group1.448±0.2241.716±0.2202.436±0.1092.741±0.0312.788±0.061HIS-3EG95s组HIS-3EG95s group1.467±0.1082.099±0.1092.542±0.0182.891±0.0332.930±0.076
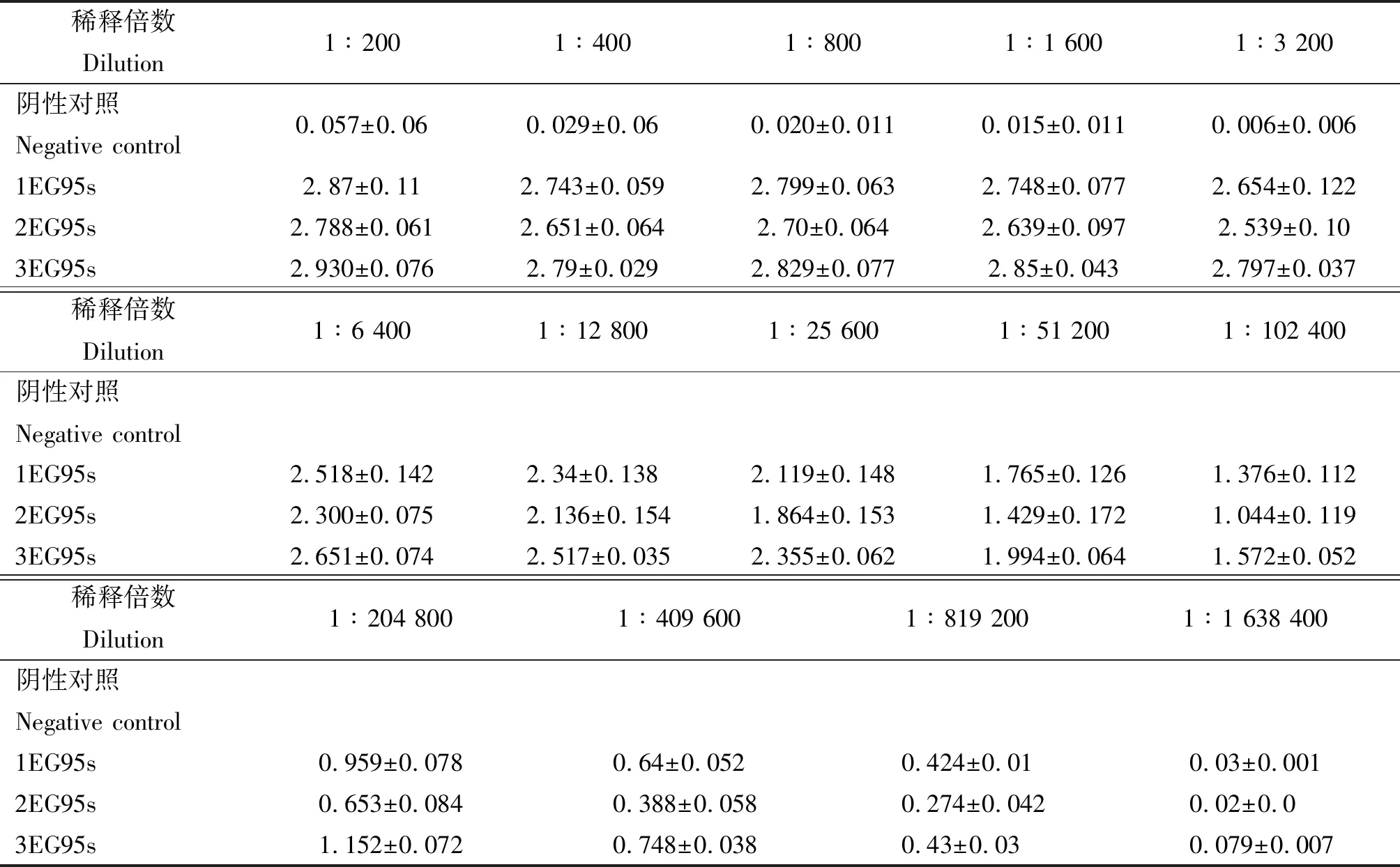
表2 免疫后42 d的抗体滴度
HIS-1EG95s和HIS-2EG95s两组均为1∶819 200,HIS-3EG95s组为1∶1 638 400,提示HIS-3EG95s组与其他两个免疫组有1个倍比稀释的差异。在同一滴度上比较,HIS-2EG95s组低于其他两组,在所有滴度上比较差异均具有统计学意义(P<0.05)。HIS-1EG95s组和HIS-3EG95s组相比,HIS-3EG95s较高,从1∶12 800-1∶819 200的同一滴度上比较差异均具有统计学意义(P<0.05)。提示,HIS-3EG95s刺激小鼠产生特异性抗体的能力比其他两组更持久。
2.4免疫后IFN-γ检测 一免后第3d利用BD OptEIA TM Set Mouse IFN-γ试剂盒(BD Biosciences, San Diego, CA)检测小鼠血清中IFN-γ的含量,结果显示HIS-1EG95s、HIS-2EG95s和HIS-3EG95s免疫后均能诱导小鼠产生较高水平的IFN-γ,但各组之间无显著差异(P>0.05),见图5。
2.5与阳性血清反应的差异分析将HIS-1EG95、HIS-2EG95和HIS-3EG95按10和1 μg/mL浓度包被,用足量的羊包虫阳性血清和阴性血清和酶标二抗进行间接ELISA检测,分析HIS-1EG95、HIS-2EG95和HIS-3EG95反应的差异性,结果显示10和1 μg/mL包被时,HIS-1EG95s的反应性均显著低于HIS-2EG95s和HIS-3EG95s,而HIS-2EG95s和HIS-3EG95s反应性相当,表明HIS-2EG95s和HIS-3EG95s略优于HIS-1EG95s,结果见表3。
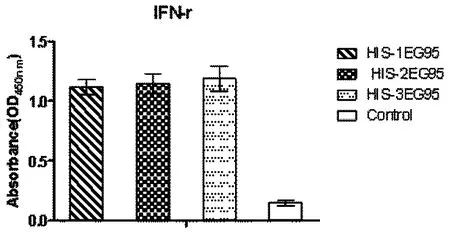
图5 免疫3 d后小鼠血清IFN-γ检测
3 讨论
棘球蚴病在人和动物之间传播,严重危害人畜健康。我国是包虫病危害严重的国家之一[7-8]。我国目前约有近100万人患病,几千万人受到棘球蚴病的威胁[7,11-12]。据临床病例统计和小样本调查结果显示,发病率仍呈持续上升趋势。免疫接种是防控该病的途径之一,寻找高效的疫苗,是羊棘球蚴(包虫)病疫苗研究的一个重要目标[12]。Lightowlers发现Eg95重组蛋白疫苗免疫绵羊,可获得95%~100%的免疫保护作用,其中86%得到完全保护,但因其重组蛋白表达量偏低且为包涵体表达,制约了该疫苗的大规模生产及应用[6]。

表3 与阳性血清反应的差异分析
用HIS-1EG95s作为包被抗原,通过已建立的间接ELISA方法对小鼠血清抗体水平进行检测,各组间的抗体动态变化水平显示,HIS-1EG95s、HIS-2EG95s和HIS-3EG95s重组蛋白均能诱导小鼠的体液免疫应答,产生特异性抗体,因此均具有良好的免疫原性。在一免后1w,HIS-1EG95s组小鼠抗体水平迅速上升,明显高于其他两组,而在第2周时HIS-3EG95s组抗体水平超过HIS-1EG95s组,并在2次免疫及3次免疫后持续略高与HIS-1EG95s组。可能是因为一次免疫是皮下多点注射,抗原蛋白是通过微血管吸收,由于HIS-1EG95s蛋白较小,更易于吸收,因此在第1周的时候抗体水平较高。而免疫两周后,重组蛋白已完全吸收,而后又采用腹腔注射,腹膜面积大,直接吸收,因此抗体水平的升高都没有延缓。 2次免疫之后,抗体水平显著上升,表明加强免疫可有效提高免疫效果。3次免疫之后,抗体水平相比于2免后略有上升,并稳定在一个较高的抗体水平,HIS-2EG95s组略低,其他两组水平差异不大,表明2次免疫足够产生很好的免疫效果。对最终抗体滴度的检测结果表明,HIS-3EG95s组要高于其他两组。在同一抗体滴度水平上比较,HIS-2EG95s始终低于HIS-3EG95s,且差异显著,HIS-1EG95s组也低于HIS-3EG95s组,且在1∶12 800以后差异显著,说明HIS-3EG95s诱导小鼠机体产生特异性抗体的能力和持久性要强于其他两种蛋白,可能产生更好的保护性,表明在进行Eg95重组表达过程中,可通过串联表达,提高基因拷贝数的方法提高表达蛋白的免疫保护效果,从而为制造更为有效的羊棘球蚴(包虫)病疫苗提供了参考依据。
参考文献:
[1]Osborn PJ, Heath DD. Immunization of lambs againstEchinococcusgranulosususing antigens obtained by incubation of oncospheresinvitro[J]. Res Vet Sci, 1982, 33: 132-133.
[2]Heath DD, Holcman B. Vaccination againstEchinococcusin perspective[J]. Acta Trop, 1997, 67(122): 37. DOI: 10.1016/S0001-706X(97)00054-5
[3]Lightowlers MW, Lawrence SB, Gauci CG, et al. Vaccination against hydatidosis using a defined recombinant antigen[J]. Parasite Immunol, 1996, 18(9): 457-462. DOI: 10.1111/j.1365-3024.1996.tb01029
[4]Zhang W, Li J, You H, et al. Short report:Echinococcusgranulosusfrom Xinjiang, PR China: cDNAS encoding the EG95 vaccine antigen are expressed in different life cycle stages and are conserved in the oncosphere[J]. Am J Trop Med Hyg, 2003, 68(1): 40-43.
[5]Lightowlers MW, Jensen O, Fernandez E, et al. Vaccination trials in Australia and Argentina confirm the effectiveness of the EG95 hydatid vaccine in sheep[J]. Int J Parasitol, 1999, 29: 531-534. DOI: 10.1016/S0020-7519(99)00003-X
[6]Carmena D, Cardona GA. Echinococcosis in wild carnivorous species: Epidemiology, genotypic diversity, and implications for veterinary public health[J]. Vet Parasitol, 2014, pii: S0304-4017(14)00158-7. DOI: 10.1016/j.vetpar.2014.03.009
[7]Guo ZX, He DL, Li YQ, et al. Investigation onEchinococcusinfection of wild animals in Qinghai Plateau[J]. Chin J Parasitol Parasit Dis, 1994, S1: 35-37.
[8]Yang YR, Rosenzvit MC, Zhang LH, et al. Molecular study ofEchinococcusin west-central China[J]. Parasitology, 2005, 131, 547-555. DOI: 10.1017/S0031182005007973
[9]Li C. The cloning of sheep complement C3d and the development of recombinant hydatids submit vaccine[M]. Beijing: Chinese Academy of Agricultural Sciences, 2008. (in Chinese)
[10]Jia H, Liu D, Hou SH, et al. Development of an indirect ELISA for detection of sheep antibodies against echinococcosis granulosa[J]. Acta Veterinaria et Zootechnica Sinica, 2011, 42(1): 65-70. (in Chinese)
[11]Lin YG, Lu MK, Hong LX. A review of the current status ofEchinococcusand hydatid disease, with notes on some informative achievements in China[J]. Chin J Zoonoses, 2012, 28(6): 616-627. (in Chinese)
[12]Xu LQ, Jiang ZX, Yu SH, et al. Characteristics and recent trends in endemicity of human parasitic diseases in China[J]. Chin J Parasitol Parasit Dis, 1995, 13: 214-217. (in Chinese)
