青海沙棘果粉抗氧化活性的研究
2014-03-29朱利娜史俊友索有瑞
强 伟,朱利娜,史俊友,索有瑞
(1.中国科学院 西北高原生物研究所,青海 西宁 810001; 2.中国科学院 研究生院,北京 100049)
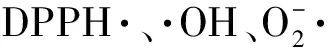
1 材料与方法
1.1 试剂与仪器
1,1-二苯基苦基苯肼自由基(DPPH·,Sigma公司);无水乙醇、硫酸亚铁、水杨酸、盐酸、三羟甲基氨基甲烷(Tris)、邻苯三酚(焦性没食子酸)、亚硝酸钠、柠檬酸、磷酸氢二钠、对氨基苯磺酸、盐酸萘己二胺等均为国产市售分析纯;精密电子天平、电子恒温不锈钢水浴锅、101型电热鼓风干燥箱、Cary300型紫外可见分光光度计(美国Varian公司)。
1.2 沙棘果粉的制备
果粉由本课题组提供,生产流程为:原料采收→果汁验收→果汁灭菌→果汁沉降→果汁过滤→果粉喷雾干燥工艺→产品检验与保存。
1.3 实验过程与方法
1.3.1 沙棘果粉对DPPH·抑制率测定[3]
1,1-二苯基苦基苯肼自由基(DPPH·)是一种很稳定的以氮为中心的自由基,若受试物能将其清除,则提示受试物具有降低羟自由基、烷自由基或过氧化氢自由基的有效浓度和打断脂质过氧化链反应的作用。DPPH·有个单电子,其乙醇水溶液呈紫色,加入受试物后λ 517 nm吸收值下降则表示其对自由基有消除能力[4]。
精确吸取不同质量浓度的沙棘果粉水溶液2 mL,加入4 mL 5×10-5mol/L DPPH·(用无水乙醇溶解)溶液,摇匀后静置30 min,以样品溶液做对照,测517 nm处的吸光光度值A,同时测定样品溶液在517 nm处的A0,空白对照液溶液在517 nm的A1,按下列公式计算其清除率。
式中,A:样品加上DPPH·的吸光度;A0:样品本身的吸光度,以蒸馏水代替显色剂;A1:空白对照液,以蒸馏水代替样品
1.3.2 沙棘果粉对·OH抑制率的测定
Feton反应产生·OH,反应式为:H2O2+Fe2+→·OH+H2O+Fe3+。羟自由基氧化水杨酸得到2,3-二羟基苯甲酸,用其在525 nm处的吸光值表示·OH的多少。吸光值与·OH的量成正比。反应体系中加入具有清除·OH作用的物质即可降低该吸光值[5]。
水杨酸法:取若干支比色管,依次加入9 mmol/L FeSO40.25 mL,9 mmol/L水杨酸-乙醇溶液0.25 mL,不同质量浓度的沙棘果粉溶液5 mL,最后加8.8 mmol/L H2O20.25 mL启动反应,于室温下反应1 h,以蒸馏水做空白对照,525 nm测A,同时测定样品溶液在525 nm处的A0,空白对照液在525 nm的A1,按1.3.1计算方法计算清除率。

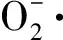
在25mL的比色管中加入3 mL Tris-HCl缓冲液(pH 8.2),1 mL不同质量浓度的沙棘果粉溶液,25℃±0.5℃水浴平衡20 min后,加入0.3 mL 7 mmol/L的邻苯三酚准确反应4 min,加入1 mL 10 mol/L的HCl终止反应,在322 nm处测A。同时测定样品溶液在322 nm处的A0,空白对照液在322 nm的A1,按1.3.1计算方法计算清除率。
当加入沙棘果粉溶液时,溶液中的有效成分与NaNO2作用将NaNO2消耗掉,剩余亚硝酸根在酸性条件下,能使对氨基苯磺酸重氮化,再使其与盐酸萘己二胺偶合生成红色偶联化合物,测定溶液吸光度,计算亚硝酸盐清除率[8]。
将0.5 mol/L的柠檬酸-磷酸缓冲液(pH 3.0)5.0 mL置于25 mL比色管中,加入1 mL质量分数0.01%的NaNO2溶液,再分别加入10 mL不同浓度的沙棘果粉溶液,定容至刻度。37℃反应1 h。取1 mL反应液于50 mL容量瓶中,加入0.4%对氨基苯磺酸溶液2 mL,0.2%的盐酸萘己二胺1 mL,摇匀放置15 min后,用分光光度计在544 nm处测A,同时测定样品溶液在544 nm处的A0,空白对照液在322 nm的A1,按1.3.1计算方法计算清除率。
2 结果与讨论
2.1 对DPPH·自由基的清除作用
不同浓度沙棘果粉溶液加入到5×10-5mol/L DPPH·乙醇溶液,反应30 min后,其清除能力如图1所示。沙棘果粉对DPPH·有很好的清除作用,随着果粉浓度的增大,对DPPH·的清除作用迅速增强。但当果粉用量超过0.4 mg/mL时,对DPPH·的清除作用变化很小,当果粉浓度为0.4 mg/mL时,对DPPH·清除率为96.78%。沙棘果粉清除DPPH·的IC50值为0.22 mg/mL左右。

图1 沙棘果粉对DPPH·的清除率
2.2 对·OH清除作用
羟基自由基(·OH)是最活泼、毒性最大的自由基,它可与活细胞中的任何分子发生反应,引发组织细胞病变,导致各种疾病发生和加速机体衰老,且反应速度非常快。沙棘果粉对·OH的清除效果见图2。由图2可知,随着果粉浓度的增大,清除效果增加,当浓度增大为0.8 mg/mL时,对·OH清除率为56.40%,超过此浓度时,对·OH清除变化很小。沙棘果粉清除·OH的IC50值为0.72 mg/mL 左右。
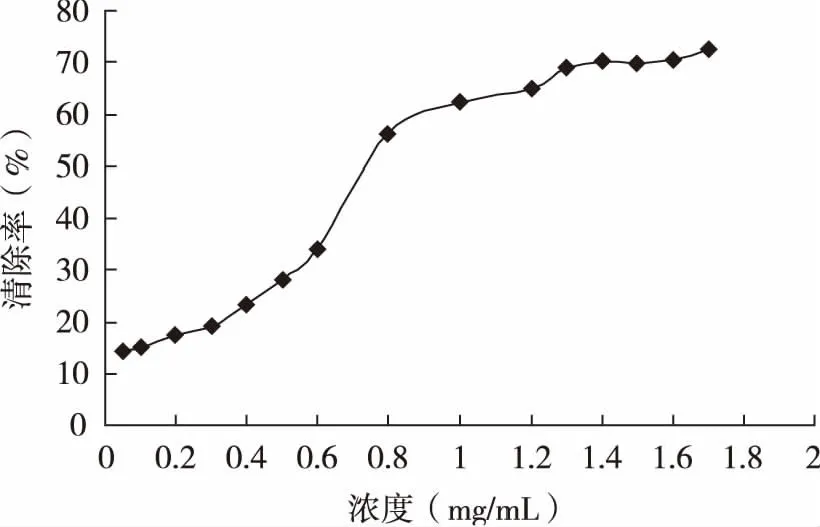
图2 沙棘果粉对·OH的清除率
2.3 对碱性邻苯三酚体系产生的的清除作用
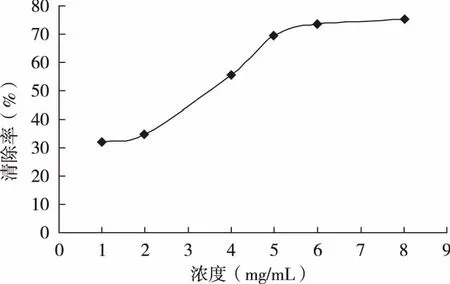
图3 沙棘果粉对O2·的清除率
2.4 对亚硝酸盐清除率的测定
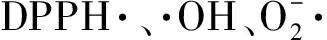
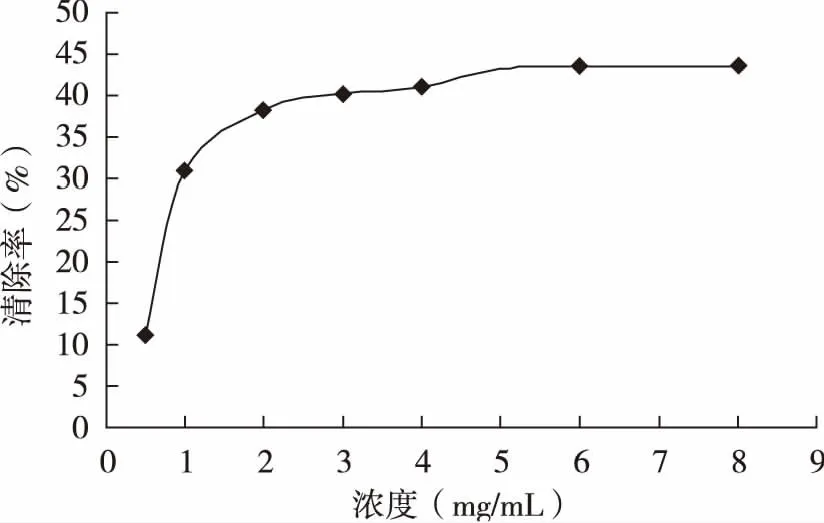
图4 沙棘果粉对亚硝酸盐的清除率
3 结 语
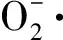
参考文献:
[1] 付媛,李金梅,张霞,等.沙棘的化学成分及其保健功能研究进展[J].内蒙古石油化工,2008,23:13-14.
[2] 鲁长征,山永凯,刘洪智,等.天然维生素之王-沙棘在食品配料中的应用[J].中国食品添加剂,2008:229-235.
[3] 吴雪辉,张喜梅,李廷群,等.板栗花粗提物的抗氧化活性研究[J].现代食品科技,2008,24(1),14-16.
[4] Suzuki M, Mori M.Antioxidant mechanisms of catechins on DPPH radical[J], J Tennen Yuki Kagobutsu Toronkai Koen Yoshishu,2000,40:631-636.
[5] Nicholas S, Quinton J C.Hydroxyl radical scavenging activity of compatible solutes [J].Phytochemistry,1989,28:1057-1060.
[6] 金春英,张小勇,崔胜云.DPPH及邻苯三酚法对牛蒡和小根蒜提取液及其他氧化剂的清除自由基能力的比较研究[J].延边大学学报:自然科学版,2008,34(1):43-46.
[7] 冯翠萍,洪建华,张弋凡.果汁对亚硝酸盐清除作用的研究[J].山西农业大学学报:自然科学版,2009,29(3):261-264.
[8] Conceptión S M, José A L.Free radical scavenging capacity and inhibition of lipid oxidation of wines, grape juices and related polyphenolic constituents[J].Food Res Int,1999,32:407-412.
