Box-Behnken实验设计法优化丹皮酚-羟丙基-β-环糊精包合物的制备工艺
2014-03-26张冕
张冕
(荆楚理工学院化工与药学院,湖北荆门 448000)
丹皮酚(paeonolum,PAE)是毛茛科植物牡丹的根皮和萝摩科植物徐长卿全草的主要活性成分,具有镇静催眠、解热镇痛、抗菌、抗氧化、降血压等多种药理活性,临床上用于治疗风湿痛、胃痛、湿疹、过敏性皮炎等,在牙膏、护肤品等日化方面也有应用。PAE为酚类化合物,具有易挥发、水溶性差、见光易分解的特点[1]。羟丙基-β-环糊精(HP-β-CD)是一种良好的药物载体,较β-环糊精(β-CD)具有水溶性好、毒副作用小、增溶效果显著的优点。近年来,环糊精包合技术在药物增溶方面应用广泛,药物经包合后,通过改善溶解性能进而提高生物利用度[2]。
Box-Behnken实验设计法可以提供3到10个因素,进行低、中、高三水平的的二阶实验设计,评价因素和指标间的非线性关系,与国内常采用的正交设计、均匀设计相比,具有精度高、预测性好、简单、直观的优点,目前已较多地用于药物处方筛选、剂型制备过程、生物过程以及化学合成过程的优化[3-5]。
本实验选取Box-Behnken实验设计法来进行PAE-HP-β-CD包合物制备工艺的优化设计,以提高PAE的溶解度,并采用相溶解度法、红外光谱、薄层色谱对包合物进行表征。
1 仪器与材料
梅特勒-托利多电子天平(上海梅特勒-托利多仪器有限公司);FD-101S集热式磁力搅拌器(巩义市予华仪器有限责任公司);Alpha2-4冷冻干燥机(德国Christ公司);SHZ-82水浴恒温振荡器(金坛市国旺实验仪器厂);Agilent1100高效液相仪(美国Agilent公司);Thermofisher傅立叶红外光谱仪(赛默飞世尔科技中国有限公司);ZF-1型三用紫外线分析仪(上海顾村电光仪器厂)。
PAE(江西吉安华美香料提炼厂,纯度>99%);PAE对照品(中国药品生物制品检定所,批号: 110708-200506);HP-β-CD(进口分装,广州罗盖特中国有限公司赠送);KBr(光谱纯,北京博德恒悦科贸有限公司);甲醇为色谱纯;其余试剂及试药均为分析纯。
2 方法与结果
2.1 包合物的制备[2-6]
按一定质量比准确称取HP-β-CD和PAE,将PAE用适量无水乙醇溶解,将HP-β-CD置于烧杯中,加入适量蒸馏水,30℃水浴加热搅拌(450 r·min-1),使其形成饱和溶液。将PAE醇溶液缓慢滴加到包合材料水溶液中,滴加完毕后继续在同条件反应适当时间。反应完毕,反应液减压旋转蒸发回收乙醇,将剩余的水溶液冷冻干燥24 h,即得PAE-HP-β-CD包合物。
2.2 分析方法的建立
2.2.1 色谱条件
色谱柱:ZORBA×SB-C18柱(5 μm,4.6 mm×250 mm);流动相:甲醇-水=45∶55;流速:1.0 mL ·min-1;进样量:20 μL;紫外检测波长:275 nm;柱温:室温。
2.2.2 标准曲线的制备
精密称定PAE对照品25 mg,加甲醇配制成浓度为1.0 mg·mL-1的储备液。精密移取上述溶液适量,分别稀释至10.0、25.0、50.0、75.0、100.0 μg·mL-1,照“2.2.1”项下条件测定,记录色谱图,以浓度为横坐标、峰面积为纵坐标进行线性回归,得其标准曲线方程为y=14698x+7091(r2=0.999 9),可见PAE在10.0~100.0 μg·mL-1范围内与峰面积线性关系良好。
2.2.3 方法专属性考察
照上述色谱条件,分别注入HP-β-CD溶液、PAE对照品溶液和包合物溶液各20 μL进行测定,结果表明杂质峰与药物峰的分离良好,辅料及试剂不干扰主药的含量测定,PAE的保留时间约为8.0 min。
2.3 包合率的计算
对包合物的评价一般以包合率为主要指标。将所制备的包合物以蒸馏水溶解后定容,照上述分析方法进行含量测定,按下式计算包合物的包合率:

2.4 包合物制备工艺的优化[3-5]
2.4.1 Box-Behnken实验设计
在预试验的基础上,运用Box-Behnken的中心组合试验设计原理,以包合率为响应值,选取对包合物影响较为显著的3个因素进行优化研究,并建立数学模型。实验中的3个因素分别记作X1,X2和X3,每个因素的低、中、高三水平分别记作-1、0、+1,试验的各因素水平见表1;利用Design Expert软件建立的Box-Behnken实验设计及结果如表2所示。第13~17次试验为5次重复的中心点试验,用于考察模型的误差。
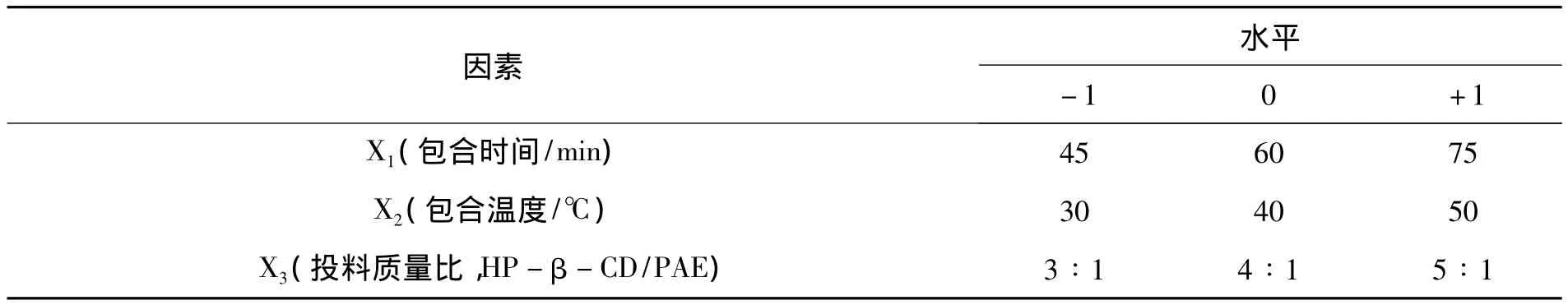
表1 Box-Behnken实验设计的因素和水平
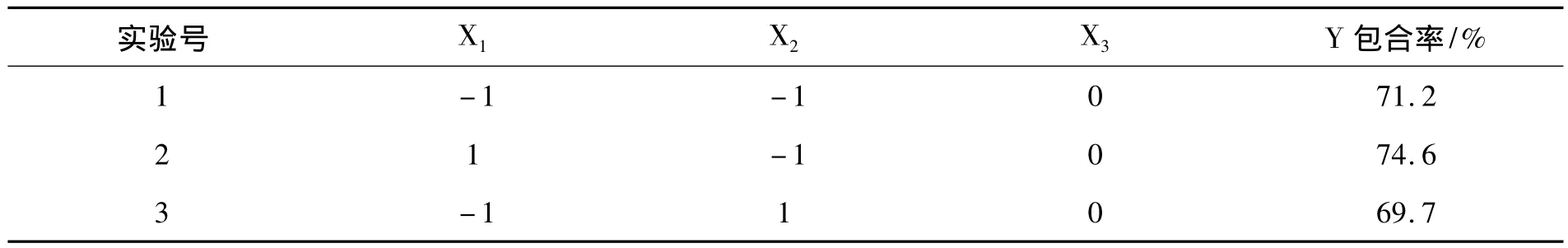
表2 Box-Behnken实验设计及响应值(n=3)
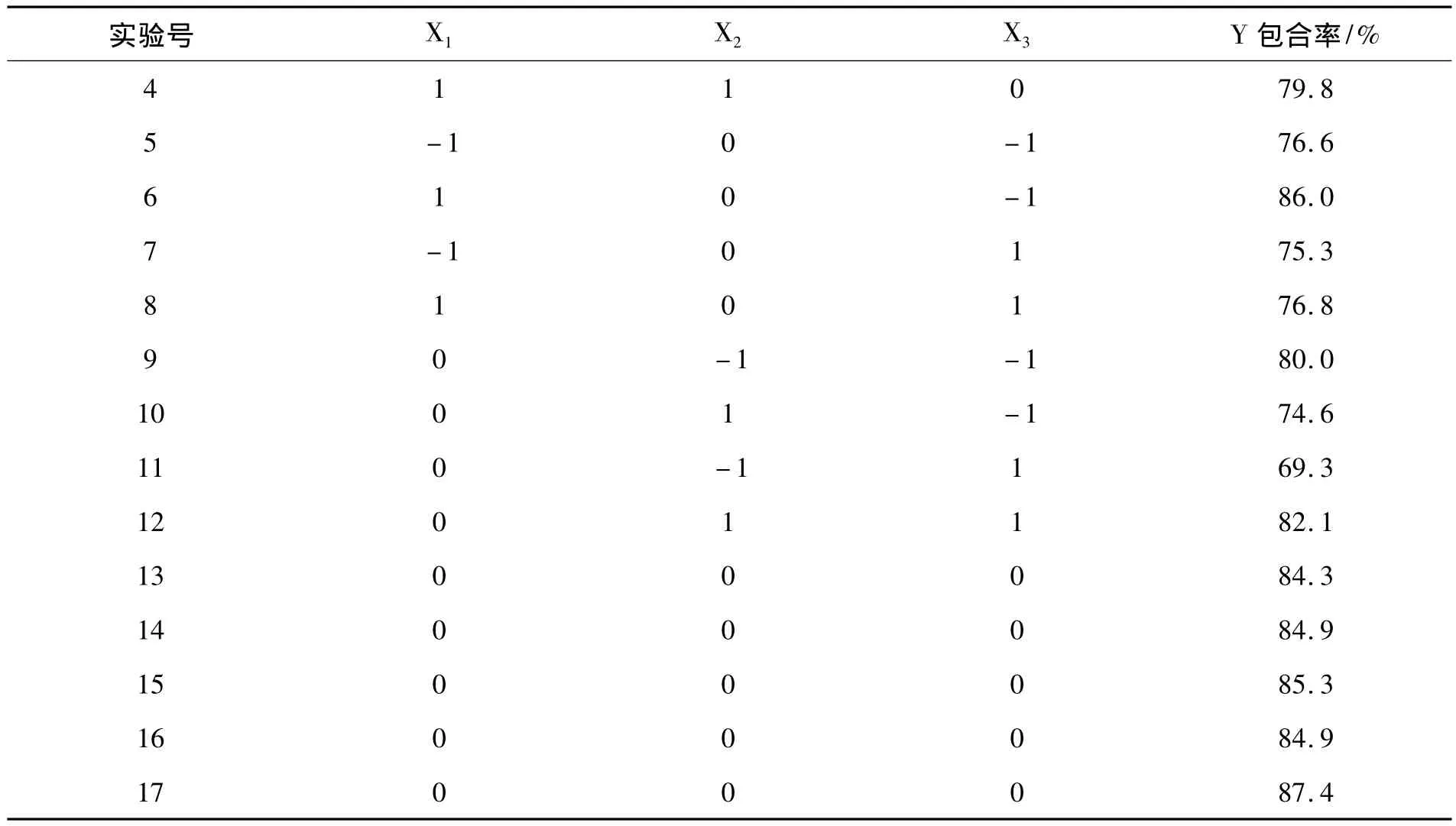
续表2
2.4.2 二次回归模型的建立及显著性检验
分别采用多元线性和多元二项式数学模型回归分析因素X1、X2、X3对响应值Y的影响。多元线性模型回归结果:Y=78.99+3.05X1+1.39X2-1.71X3(R2=0.197 8=0.197 8);多元二项式模型回归结果:Y=85.36+3.05X1+1.39X2-1.71X3+1.68X1X2-1.98X1X3+4.55X2X3-4.68-6.
对该二项式回归模型进行方差分析,见表3。由上述方程可知,对于包合物的包合率,二次多项式的拟合度要好于多元线性模型。该模型方程具有极显著性(P<0.000 1);校正决定系数0.940 4),表明大约有94%的包合率变异分布在所研究的3个相关因素中,其总变异度仅有6%不能该模型来解释;相关系数R为0.986 9(R2=0.973 9),表明包合率的预测值和实测值之间有很好的拟合度;失拟差不显著(P>0.05),表明方程的拟合不足实验不显著,无明显失拟因素存在,对模型是有利的。因此,该模型可用于对丹皮酚包合物的包合率进行分析和预测。
因素X1、X2、X3对包合效果的线性效应显著;因素、对包合效果的曲面效应显著,对包合效果的曲面效应极其显著;X1X3、X2X3对包合效果的交互影响显著,X1X2对包合效果的交互影响不显著。
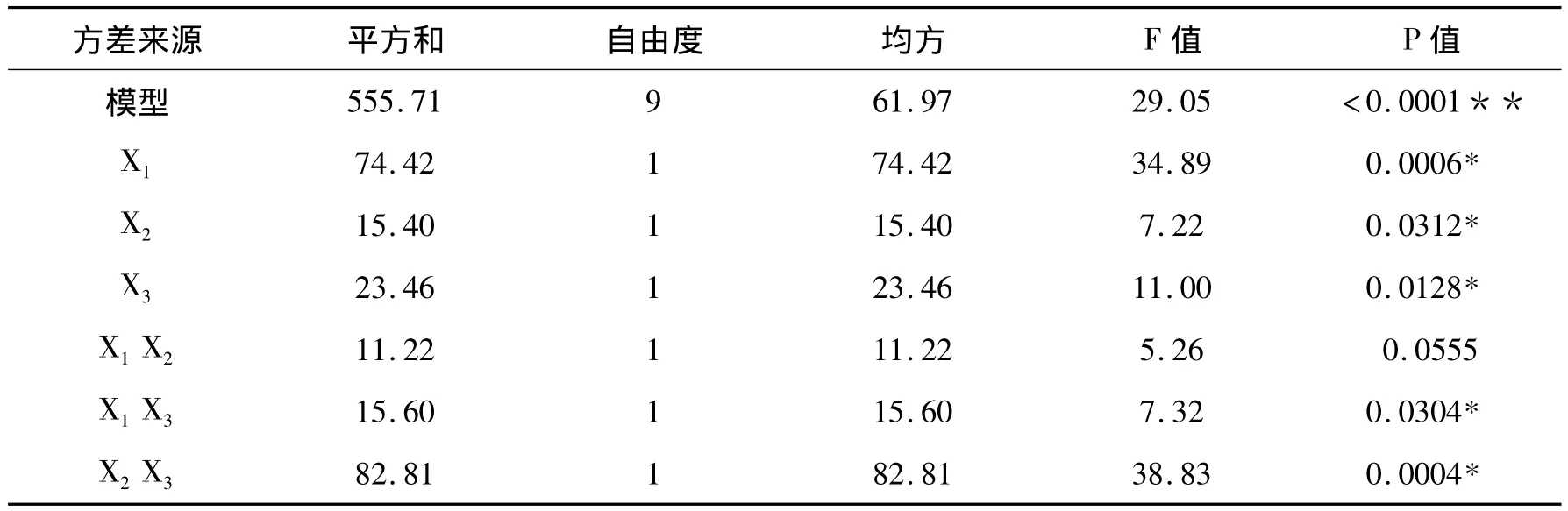
表3 包合率回归模型方差分析
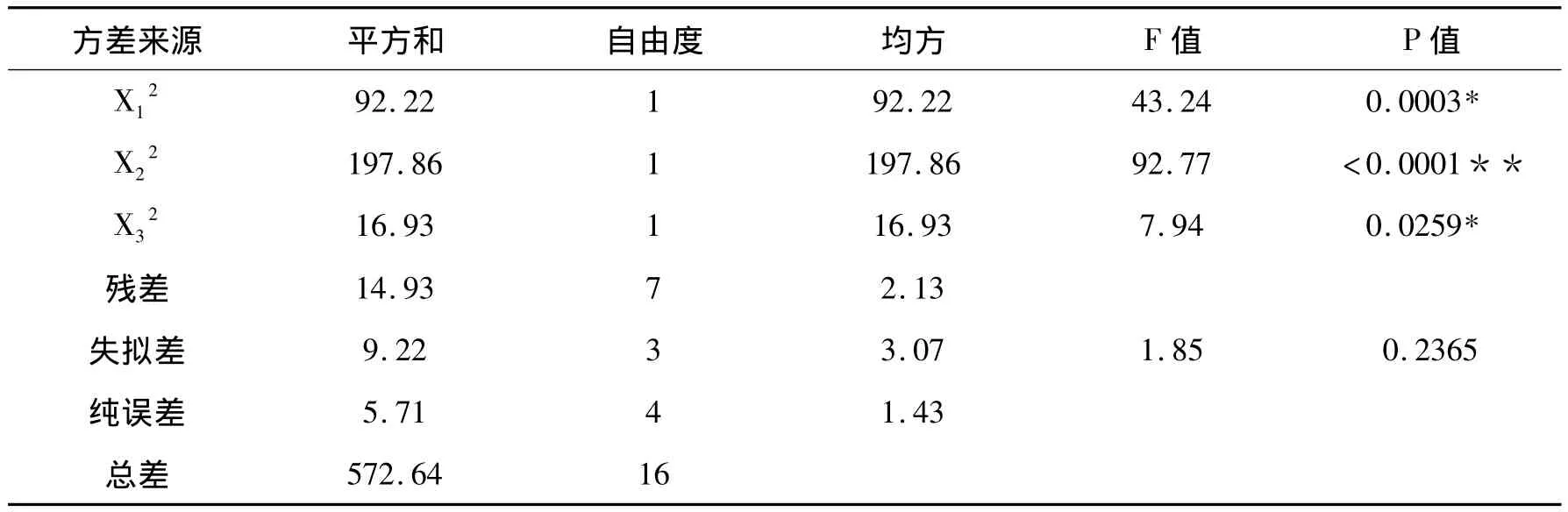
续表3
2.4.3 响应曲面分析与优化条件的确定
根据Design-Expert软件绘制不同影响因素对于响应值的三维曲线图,见图1。图1为分别固定三个影响因素其中之一,考察其他两个因素对响应值影响的曲面图,该图底部平面为等高线图,等高线图的重合区域用来进行各影响因素的优化。
根据Box-Behnken实验设计结果,得到优化条件为:包合时间为67 min,包合温度为39℃,HP-β-CD与PAE的投料比为3.23∶1(质量比)。为检验Box-Behnken实验设计所得结果的可靠性,根据上述优化条件进行实验,制备3批样品分别测定其包合率,理论值为86.7%,实测包合率的平均值为85.3%,相对偏差约0.58%,说明此模型是可靠的。
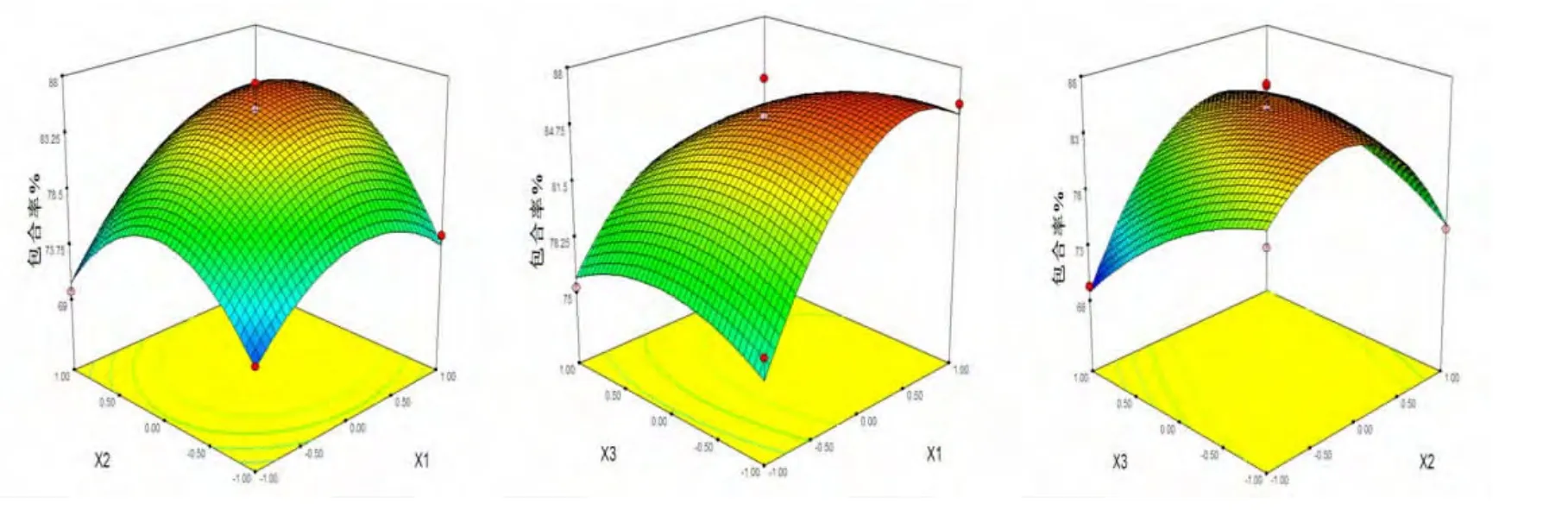
图1 各因素对包合率的响应曲面图
2.5 PAE-HP-β-CD包合物的验证
按最优包合条件制备PAE-HP-β-CD包合物,对其进行验证。
2.5.1 相溶解度
相溶解度法可以确证包合物的形成,也是评价包合物溶解性能的最常用的方法。难溶性药物包合后溶解度增大,通过测定药物在不同浓度的HP-β-CD溶液中的溶解度,绘制溶解度曲线。可从曲线判断包合物是否形成,通过计算平衡常数
判断包合物的稳定性[1,2,6]。
将HP-β-CD加蒸馏水配成浓度分别为0、2.5、5.0、7.5、10.0、12.5、15.0 mmol·L-1的溶液。取上述不同浓度溶液1 mL加入盛有过量PAE的5 mL容量瓶中,25℃条件下于超级恒温水浴振荡器中振荡48 h,使溶液达到平衡后,静置。取上清液滤过,弃去初滤液,取续滤液经稀释适当倍数后进行含量测定。参考Higuchi和Connors的方法,以PAE溶解度为纵坐标,HP-β-CD浓度为横坐标做相溶解度图,进行线性回归后计算稳定常数K。
结果表明,随着HP-β-CD浓度的增加,PAE溶解度呈线性增加,相溶解度曲线为AL型。回归方程为y=0.4696x+2.7982(R2=0.991 6),稳定常数K=315.6 L·mol-1,表明二者结合牢固。

2.5.2 红外光谱分析[6]
取PAE、HP-β-CD、二者的物理混合物(按包合物比例制备)、包合物为样品,以KBr压片,在相同的条件下进行红外光谱扫描,扫描范围为400~4 000 cm-1,如图2。
红外图谱显示,物理混合物图谱表现为PAE图谱和HP-β-CD图谱的叠加,包合物图谱与物理混合物的图谱、PAE的图谱相比较有很大区别,与HP-β-CD的图谱比较类似,其中PAE的特征峰已基本消失,表明PAE已嵌入HP-β-CD的空腔内部形成了包合物。
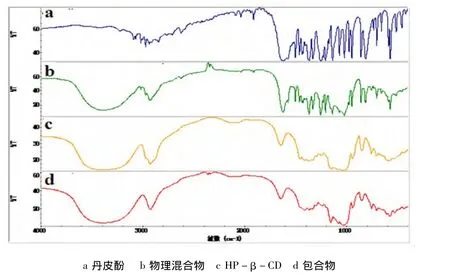
图2 红外光谱图
2.5.3 薄层色谱分析[7-9]
取包合物100 mg适量于具塞试管中,加石油醚10 mL,超声处理10 min,静置,倾出上清液,为石油醚提取液(a)。残渣加入无水乙醇10 mL,超声处理10 min,静置,倾出上清液,此为无水乙醇提取液(b)。再取PAE对照品10 mg,加入无水乙醇溶解10 mL,作为对照品溶液(c)。二者的物理混合物(按包合物比例制备)100 mg加入无水乙醇10 mL,超声处理10 min,静置,倾出上清液,为物理混合物样品(d)。
分别取上述四种溶液10 μL于同一块硅胶G薄板上点样,以甲苯-乙酸乙酯-冰醋酸(12∶4∶0.5)为展开剂,在紫外线分析仪下观察展开结果,见图3。样品a无斑点,样品b、c、d的斑点清晰可见。PAE易溶于石油醚,而其包合物不溶于石油醚,先用石油醚溶解游离的PAE,再用乙醇破坏包合物提取PAE,结果在石油醚中未见PAE的斑点,而乙醇提取液中有PAE的斑点。进一步表明,PAE被HP-β-CD包合形成了新物相,PAE-HP-β-CD包合物已形成。
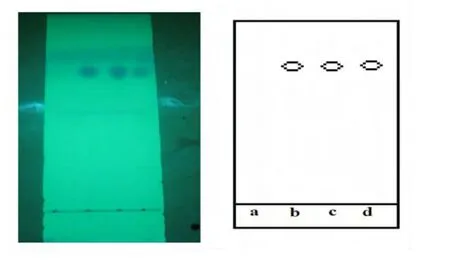
图3 薄层色谱图
3 讨论
1)本实验采用饱和水溶液法制备PAE-HP-β-CD包合物,尝试性采用Box-Behnken实验设计法对制备工艺进行优化,这是一种采用多元二次回归方程来拟合因素与响应值之间函数关系的统计方法,可以评估因素的非线性影响。得到的最佳制备工艺条件为:包合时间67 min,包合温度39℃,HP-β-CD、PAE投料比为3.23∶1(质量比)。该方法合理、可靠、简便,能够较好地预测PAE-HP-β-CD包合物的包合率,可用于制备工艺的优化。
2)对所制得的包合物进行了验证。包合物的溶解度达到了9.75 mmol·L-1,与纯水中PAE的溶解度2.50 mmol·L-1相比提高了约4倍。同时,红外光谱与薄层色谱的实验结果均表明PAE嵌入了HP-β-CD的空腔内部,被HP-β-CD包合形成了新物相,包合物已形成。
3)已有许多文献报道包合物能改善药物的溶解性与稳定性,对于包合物的释放性能及相关影响因素有待进一步考察。
[1]张冕,王德堂,万芳.相溶解度法研究不同环糊精对丹皮酚的增溶作用[J].分子科学学报,2012,28(5):422-426.
[2]周艳,唐亮,周咏梅.芦丁-羟丙基-β-环糊精包合物的制备与验证[J].中国药学杂志,2011,46(16):1 262-1 264.
[3]张冕,王德堂,刘娥.Box-Behnken实验设计法优化胸腺五肽脂质体的处方工艺[J].中国生化药物杂志,2012,33 (6):808-810.
[4]王霏娜,俞菁,赵春霞,等.用响应面法优化β-环糊精包合白术挥发油工艺[J].浙江大学学报:工学版,2008,42 (12):2 160-2 165.
[5]李斌,孟宪军,李元甦,等.响应面法优化超临界CO2萃取北五味子藤茎油工艺[J].食品科学,2010,31(20):132-136.
[6]文震,刘波,郑宗坤,等.玫瑰精油β-环糊精包合物的制备与表征[J].食品科学,2009,30(10):29-32.
[7]岳红坤,常明,张东红,等.薄荷油β-环糊精包合物的制备工艺优化和产品表征[J].井冈山大学学报:自然科学版,2011,32(5):40-45.
[8]任磊,牛小花,韩泳平,等.红景天挥发油/β-环糊精包合物的表征[J].中成药,2007,29(10):1 434-1 436.
[9]余丽丽,杨星星,李春成.白术挥发油/β-环糊精包合物的表征[J].中国药学杂志,2005,40(2):90-93.
