稀H2SO4液滴对PCB初期腐蚀行为的影响
2014-03-26丁康康邹士文董超芳李昊然李晓刚
丁康康,肖 葵,邹士文,董超芳,李昊然,李晓刚
(北京科技大学 腐蚀与防护中心,北京 100083)
印制电路板(PCB)作为电子元器件的支撑体和电子元器件电气连接的提供者,在国民经济生活中占据举足轻重的地位。铜及其合金由于其优异的性能而被大量用作PCB的基材,但PCB-Cu极易发生氧化或腐蚀[1],因而,在实际使用过程中,通常需要对PCB铜箔进行表面处理,包括无电镀镍金(ENIG)、化学浸银(ImAg)和无铅热风整平喷锡(HASL)等。当铜表面涂覆其他涂层时,微孔和其他涂层缺陷的存在,会导致微孔腐蚀的发生。尤其是金属涂层的引入导致PCB成为一个多金属体系,容易诱发电偶腐蚀。随着PCB向进一步微型化和高度集成化方向发展,PCB对环境污染物的浓度要求越发苛刻,极微量的吸附液膜或腐蚀产物都会对电子电路和元器件的性能产生严重的影响,这也使PCB的腐蚀问题突显出来[2]。
PCB的腐蚀行为与环境中污染组分密切关联,受空气温湿度、污染气体(如SO2、H2S等)、灰尘颗粒和霉菌等多种因素影响,国内外在该方面已经做了许多工作。例如,HUANG等[3-4]系统研究含Cl-吸附薄液膜下温湿度和电场对 PCB-Cu电化学腐蚀行为的影响,发现温度提升能够提升腐蚀速率,而电场作用相反;不同湿度下的腐蚀速率由大到小依次为85% RH、95% RH、75% RH、溶液中。KRUMBEIN[5]和BOWCOTT等[6]研究了相对湿度和SO2对PCB-ENIG镀金层空隙处镍金属腐蚀的影响,发现镍腐蚀只有在一定湿度(>70% RH)下才能发生,且腐蚀产物以离散的腐蚀产物丘的形式存在。尘土颗粒[7]和霉菌[8-9]对PCB腐蚀产物的形成和发展也会造成直接影响,灰尘的吸湿作用和霉菌代谢产酸过程均会加速 PCB的腐蚀失效。
在实际使用环境下,由于昼夜温差变化或PCB本身温度场的波动,PCB表面容易发生凝露现象,引发微小液滴下的电化学腐蚀。当电解液以液滴形式存在时,金属腐蚀行为与溶液或薄液膜下存在明显区别,电极阴阳极电流分布不均匀。TAN[10]采用丝束电极研究不同尺寸液滴下碳钢的大气腐蚀行为后发现,当液滴直径达到一定尺寸时(约12 mm),由于液滴中心和液滴边缘之间的距离增大,阳极出现在离液滴中心较远的三相线界面区附近,电流分布为腐蚀环形状。液滴腐蚀过程中,电极表面呈现出的电化学分布不均匀性还会受到液滴浓度和金属表面性质等因素的影响而不断发生变化[11]。对PCB而言,表面处理工艺的不同导致其在液滴作用下的腐蚀失效机制也必然不同。本文作者通过体视学显微镜、扫描电镜(SEM)、X射线能量色谱仪(EDS)、交流阻抗谱(EIS)和扫描Kelvin探针(SKP)等技术研究了PCB-Cu、PCB-ENIG、PCB- ImAg和PCB-HASL 4种试验材料在pH为3.7和2.7的稀H2SO4液滴(经换算,相当于空气中 SO2浓度分别在1×10-6和1×10-4左右)下的腐蚀行为与机理,以模拟在硫污染环境下凝露对PCB的危害,为PCB 实际服役环境下的选材和寿命评估提供数据基础和指导。
1 实验
采用PCB作为实验材料,对基体Cu箔进行不同表面处理,以研究不同表面工艺处理后PCB在试验环境中的腐蚀规律。PCB基板采用FR-4环氧玻璃布层压板,厚度2 mm;铜箔厚度统一为25~30 μm,表面工艺基本参数见表 1。试样有效尺寸为 10 mm×10 mm,实验前试样用丙酮超声清洗10 min后,用去离子水超声清洗10 min,再用无水乙醇擦洗后,自然风干备用。
采用分析纯浓 H2SO4和去离子水配制 pH=3.7和2.7的H2SO4溶液,通过WDYI型微量注射器在PCB试样表面滴加5 μL液滴。随后,将每种材料滴加液滴的 3组平行样和未滴加空白样同时置于 ESPEC SET-Z-022R型湿热箱内,控制温度60 ℃,相对湿度95%,24 h后取出。利用Keyence VHX-2000型体式学显微镜和FEI Quanta 250型环境扫描电镜观察试样表面腐蚀形貌,结合Ametek Apollo-X型EDS能谱分析仪对液滴区域进行元素分布面扫描测试。采用PAR M370扫描电化学工作站对试样进行SKP测试,探针到试样表面距离为(100±2) μm,振动频率80 Hz、振幅30 μm,扫描模式为Step Scan面扫,区域大小4 mm×4 mm,实验室环境控制温度25 ℃,相对湿度60%。
交流阻抗谱的测量仪器为PAR VMP3多通道电化学工作站,采用三电极体系,PCB试样为工作电极,铂片为辅助电极,饱和甘汞电极(SCE)为参比电极。电解液使用pH=2.7的稀H2SO4溶液,在开路电位下进行EIS测试,扫描频率0.01~10 mHz,扰动电位10 mV,采用ZSimpWin V3.20对EIS数据进行拟合,每组测试重复3遍。
2 结果与分析
2.1 液滴下腐蚀形貌
60 ℃时95% RH环境中PCB在不同pH液滴下腐蚀24 h的光学显微照片如图1所示。不同工艺处理的PCB腐蚀形貌存在明显区别:在pH=3.7的液滴下,PCB-Cu仅局部发生轻微的腐蚀;当pH值达到2.7时,则发生全面腐蚀,整个液滴区域覆盖一层黑色腐蚀产物膜。镀Au处理后,随着液滴pH值由3.7降低至2.7,PCB-ENIG腐蚀行为转变为微孔腐蚀,边缘出现颗粒状腐蚀产物,并向液滴中心区域发展;而 PCB-ImAg样液滴中心区域基本不发生腐蚀,仅在边缘腐蚀严重,液滴的 pH=2.7时,边缘腐蚀产物量明显增加但并未扩展到液滴中心;PCB-HASL在稀H2SO4(不同pH值下)基本不腐蚀,或者仅在镀Sn层表面形成一层较薄的腐蚀产物膜。

图1 60 ℃时95% RH环境中PCB在不同pH液滴下腐蚀24 h的光学显微照片Fig. 1 Optical micrographs of PCB under different pH droplets for 24 h under condition of 60 ℃ and 95% RH (void-blank sample without dropping droplet): (a), (b), (c) PCB-Cu; (d), (e), (f) PCB-ENIG; (g), (h), (i) PCB-ImAg; (j), (k), (l) PCB-HASL; (a), (d), (g),(j) Void; (b), (e), (h), (k) pH=3.7; (c), (f), (i), (l) pH=2.7
2.2 腐蚀产物分析
图2所示为pH=2.7稀H2SO4液滴作用下PCB的SEM与EDS元素分布面扫结果。由图2(a)和(c)可以看出,PCB-Cu试样液滴区域O元素含量明显增高,同时还存在微量S元素的富集,表明腐蚀产物主要为Cu的氧化物和硫酸盐。镀Au处理后,PCB-ENIG的腐蚀形貌发生明显改变,试样表面零散地分布着一些颗粒状凸起物,其数量由边缘向液滴中心方向逐渐递减,且凸起处氧元素含量明显升高,表明该处存在基底的腐蚀产物(该条件下Au层不会氧化或腐蚀)。由于实验用PCB-ENIG样品镀Au层厚度只有0.02 μm,不可避免地存在微孔与表面缺陷(镀Au层厚度达到5 μm才能完全消除微孔存在[12]),导致这些区域的中间过渡层(Ni)甚至基底与电解质溶液直接接触,与镀Au层形成电偶而加速腐蚀,腐蚀产物成分主要为Ni或Cu的氧化物/硫酸盐,由于腐蚀产物体积膨胀,其填充微孔并沿孔壁迁移至镀 Au层表面,该腐蚀形式又称为微孔腐蚀[5]。不同于镀Au层,浸Ag层的应用能够显著减少微孔腐蚀的发生,但其腐蚀状况不均匀,液滴边缘堆积了较多腐蚀产物。图2(i)所示为PCB-ImAg液滴边缘区域 Cu元素含量大幅增加,说明该处基底腐蚀产物已迁移至Ag层表面。3种表面工艺中,喷Sn处理的PCB耐蚀性能最佳,从SEM像和EDS面扫图(图2(j)~(l))中可以看出,镀Sn层表面仅存在一层极薄的腐蚀产物膜,液滴处氧元素略有升高,而 Cu基底则完全探测不到。

图2 60 ℃时95% RH环境不同表面工艺处理PCB的EDS元素分布面扫描结果Fig. 2 Elemental distribution map scanning of PCB with different surface treatments under condition of 60 ℃ and 95% RH: (a), (b),(c) PCB-Cu; (d), (e), (f) PCB-ENIG; (g), (h), (i) PCB-ImAg; (j), (k), (l) PCB-HASL; (a), (d), (g), (j) SEM; (b), (e), (h), (k) O; (c) S;(f) Ni; (i), (l) Cu
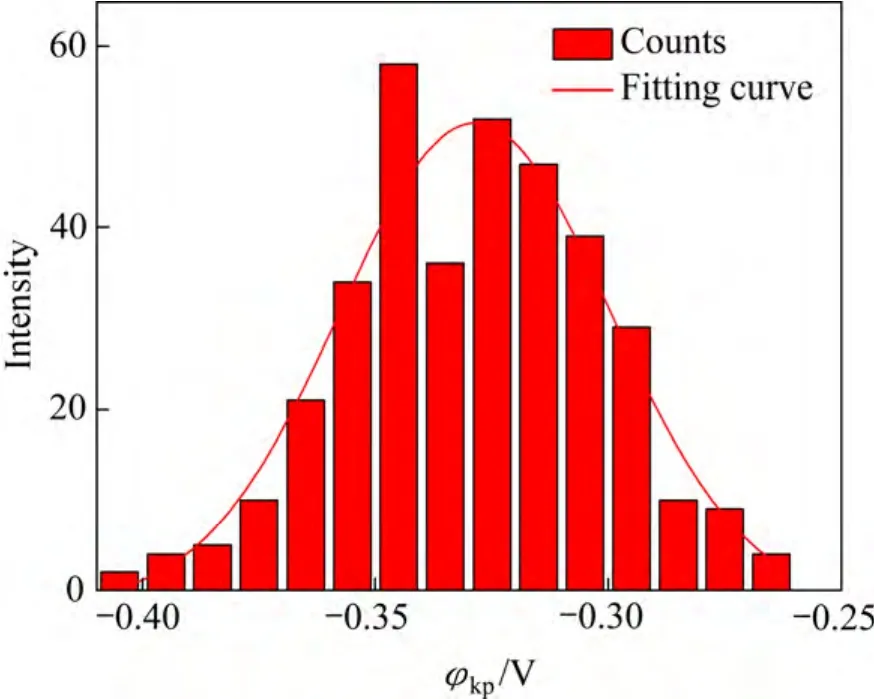
图3 PCB-Cu空白对照试样分布直方图及其高斯拟合示意图Fig. 3 Column diagram and Gauss fitting curves of Kelvin potentials distribution of blank sample
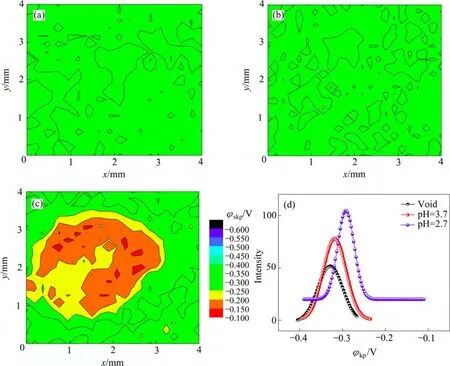
图4 不同试验条件下PCB-Cu表面SKP电位分布与高斯拟合曲线Fig. 4 Surface Kelvin potentials distribution and Gauss fitting curves of PCB-Cu under different test conditions: (a) Void; (b)pH=3.7; (c) pH=2.7; (d) Gauss fitting curves
2.3 扫描Kelvin探针测试分析
为了研究液滴下PCB不同区域腐蚀电位的变化,测定了试验后样品整个液滴区域表面 Kelvin电位φkp。Kelvin探针的原理是通过测量空气中金属表面电子逸出功的方法,测定金属表面的伏打电位差,该电位与金属在大气中的腐蚀电位φcorr存在线性关系:
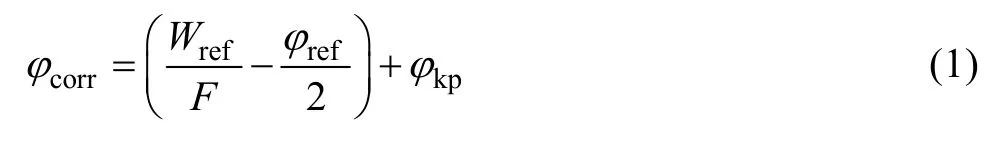
式中:Wref为电极功函数,refφ/2为参比电极(振动探针)的半电池电势,这两项在给定体系下为常数。故kpφ的变化反映了表面腐蚀电位的改变[13-15]。
对不同工艺表面处理PCB液滴区域的表面Kelvin电位分布进行了高斯拟合,拟合方法如图3所示,拟合曲线和相应的参数见表2,拟合公式见式(2)[16]:
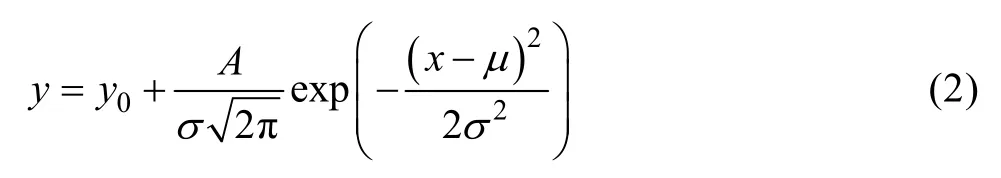
式中:μ是期望值,即电位分布的集中位置;σ是高斯分布的标准差,反映了电位分布的离散程度,该值越大,电位分布越分散。
从图4和表2可以看出, PCB-Cu空白样表面电位分布较均匀,集中于-0.3286 V附近;滴加pH=3.7的H2SO4溶液后,液滴区域局部出现腐蚀产物,腐蚀产物覆盖区域电子逸出困难,电位升高,在电位图中表现为暖色调区域[17],整体期望值上升至-0.3286 V,此外,σ值也有所增加,表面电位分布离散程度加大;pH达到2.7时,腐蚀产物膜增厚,整个液滴区域呈现为颜色较深的暖色调,表面Kelvin电位大幅正移,电位期望达到-0.2920 V,标准差σ出现极大值,表面电位差值最大。

表2 不同试验条件下PCB表面SKP电位分布的高斯拟合结果Table 2 Gauss fitting results of surface Kelvin potentials distribution for PCB under different test conditions

图5 不同试验条件下PCB-ENIG表面SKP电位分布与高斯拟合曲线Fig. 5 Surface Kelvin potentials distribution and Gauss fitting curves of PCB-ENIG under different test conditions: (a) Void; (b)pH=3.7; (c) pH=2.7; (d) Gauss fitting curve
镀Au处理后,空白样的表面电位相对于PCB-Cu分布更为均匀,标准差σ仅为0.02205,电位基本分布于-0.2265 V附近,表明PCB-ENIG表面状态无明显变化,有较好的耐湿热腐蚀的能力;滴加 pH=3.7的液滴后,整个液滴区域电位有所下降,在电位图上呈现颜色较深的冷色调,这是由于液滴中稀H2SO4的活化作用,使得试样表面活性提高,电位负移,这也导致σ值增大,因而表面电位分布差值较大;液滴pH=2.7时,PCB-ENIG则发生严重腐蚀,从电位图(见图 5)可以看到,液滴边缘区域呈高电位的暖色调,表明该处存在较多腐蚀产物,进一步结合图 1(f)形貌可知,微孔腐蚀点数目由边缘向液滴中心方向迅速递减,相应地,电位图也由暖色调逐渐过渡到冷色调,中心区域电位甚至低于空白样电位期望值,产生较大的表面电位差值,σ值达到极大值。
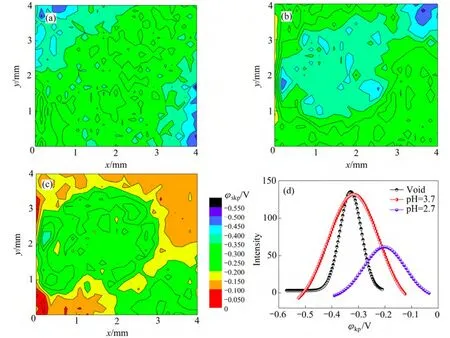
图6 不同试验条件下PCB-ImAg表面SKP电位分布与高斯拟合曲线Fig. 6 Surface Kelvin potentials distribution of Gauss fitting curves and PCB-ImAg under different test conditions: (a) Void;(b) pH=3.7; (c) pH=2.7; (d) Gauss fitting curves

图7 不同试验条件下PCB-HASL表面SKP电位分布与高斯拟合曲线Fig. 7 Surface Kelvin potentials distribution and Gauss fitting curves of PCB-HASL under different test conditions: (a) Void; (b)pH=3.7; (c) pH=2.7; (d) Gauss fitting curves
PCB-ImAg电位分布特征与PCB-ENIG类似,滴加pH=3.7的Na2SO4溶液后,液滴中心区域由于酸的活化作用而呈现低电位的冷色调,此时,σ值出现极大值,表面电位差值最大;pH降低至2.7后,液滴边缘区域的腐蚀程度加剧,暖色调颜色加深,中心区域电位也有所上升,电位期望达到-0.2021 V,而整体上σ值却有所下降,电位差值减小。
PCB-HASL试样滴加pH=3.7液滴后,表面电位仅有轻微的下降,期望值由-0.6678 V降至-0.6869 V。然而,当液滴 pH=2.7时,液滴区域电位急剧下降,电位图上表现为颜色极深的冷色调,电位分布则出现出明显的两个峰,无法进行单次高斯拟合,这表明PCB-HASL表面可能存在两个截然不同的状态,对这两个状态分别进行高斯拟合可以得到图中所示曲线,计算可得整个区域的电位期望值为-0.8078 V,σ值增至0.1478,两个状态的电位差值达到了0.3 V。酸性液滴下PCB-HASL试样表面电位的下降可归因于Sn层表面SnO2保护膜的溶解,导致液滴作用区域表面功函大幅下降。
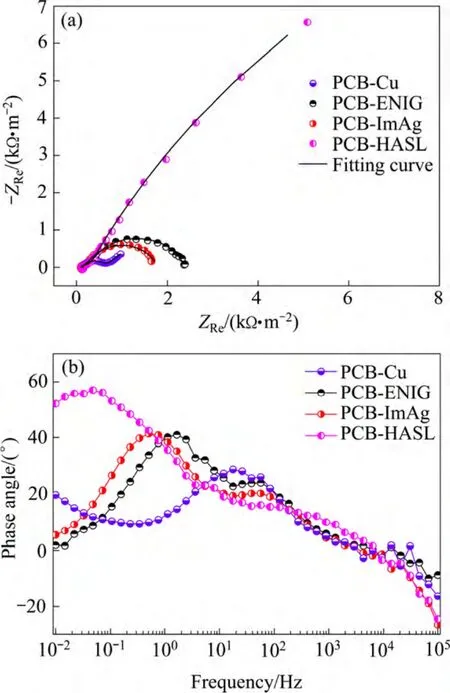
图8 不同表面工艺处理PCB在pH=2.7的H2SO4溶液中的EIS结果Fig. 8 EIS results of PCB with different surface treatments in H2SO4 solution at pH=2.7: (a) Nyquist diagram and fitting curves; (b) Bode diagram
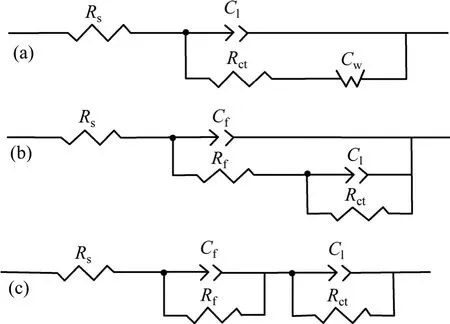
图9 不同表面工艺处理PCB在pH=2.7 H2SO4溶液中EIS谱拟合采用的等效电路Fig. 9 Equivalent circuits of EIS for PCB with different surface treatments in H2SO4 solution at pH=2.7: (a) PCB-Cu;(b) PCB-ENIG, PCB-ImAg; (c) PCB-HASL(Rs: Solution resistance; Cf, Rf: Film capacitor and resistance of surface plating layer/oxides film; Cl: Electric double layer capacitance; Rct: Charge transfer resistance; Cw: Warburg impedance)
2.4 电化学规律
为探究不同表面工艺处理 PCB电化学腐蚀速率或耐蚀性差异,在pH=2.7的稀H2SO4溶液中进行EIS测试,其结果如图 8所示。从图 8(a)中可以看到,PCB-Cu的Nyquist图由一个容抗弧及其末端与x轴成45°的直线构成,直线段的出现表明低频下电极反应过程受反应离子扩散步骤控制,显示腐蚀产物的形成对界面离子扩散过程的阻碍作用[18]。采用图9(a)所示等效电路进行拟合,其结果见表3。其中,Rct在一定程度上反映了电极过程的阻力,常用来表征腐蚀速率,该值越小,腐蚀速率越大。从表3可以看到,未进行任何表面处理的PCB-Cu的电荷转移电阻Rct远小于其他3种带镀层试样的,且其耐蚀性较差。
从图8(b)中Bode图可以看出,带镀层PCB试样均存在两个时间常数,Nyquist图由两个容抗弧组成,高频容抗弧反映了PCB表面镀层/腐蚀产物膜层信息,而低频容抗弧则反映基底界面反应信息。对PCB-ENIG和PCB-ImAg而言,由于镀Au层孔隙的存在,电解液很容易与基底直接接触,因而,采用图9(b)所示等效电路。整体上,PCB-ENIG的Rct要大于PCB-ImAg的(见表3),其耐蚀性能略优于PCB-ImAg的。PCB-HASL电极反应机理则有所不同,结合形貌与EDS能谱分析结果(见图2)可知,Sn层能有效地隔离Cu基底与电解液的接触,故EIS反映的主要是Sn层表面信息。在干燥大气存储过程中,Sn表面倾向于生成一层 SnO2氧化膜,其结构相对致密,因而,图9(c)中等效电路被采用(Rf和Cf分别代表表面氧化膜层电电阻和电容)。结合表3拟合结果,PCB-HASL试样的Rct值远大于其他3种材料,即pH=2.7时稀H2SO4溶液中 PCB-HASL存在较大反应阻力,这也解释了PCB-HASL腐蚀轻微的原因。

表3 不同表面工艺处理PCB在pH=2.7的H2SO4溶液中EIS谱拟合结果Table 3 EIS fitting results of PCB with different surface treatments in H2SO4 solution at pH=2.7
2.5 液滴下腐蚀机理
Cu是一种对大气中SO2/S等污染介质较为敏感的材料[2],在暴露初期,Cu表面会迅速形成一层相对致密的 Cu2O薄膜,对基底具有一定的保护作用[19-20];但当长期遭受 SO2作用时,Cu2O膜的外表面会受到侵蚀而逐渐转变为Cu4SO4(OH)6等腐蚀产物(见式(3)~(4))[21-22]。其腐蚀形式接近全面腐蚀,因而整个液滴(pH=2.7)区域覆盖一层较厚的腐蚀产物膜,严重损害PCB-Cu的电气连接性能和可焊性。
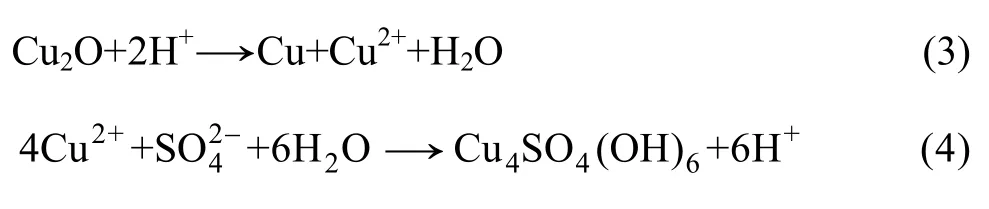
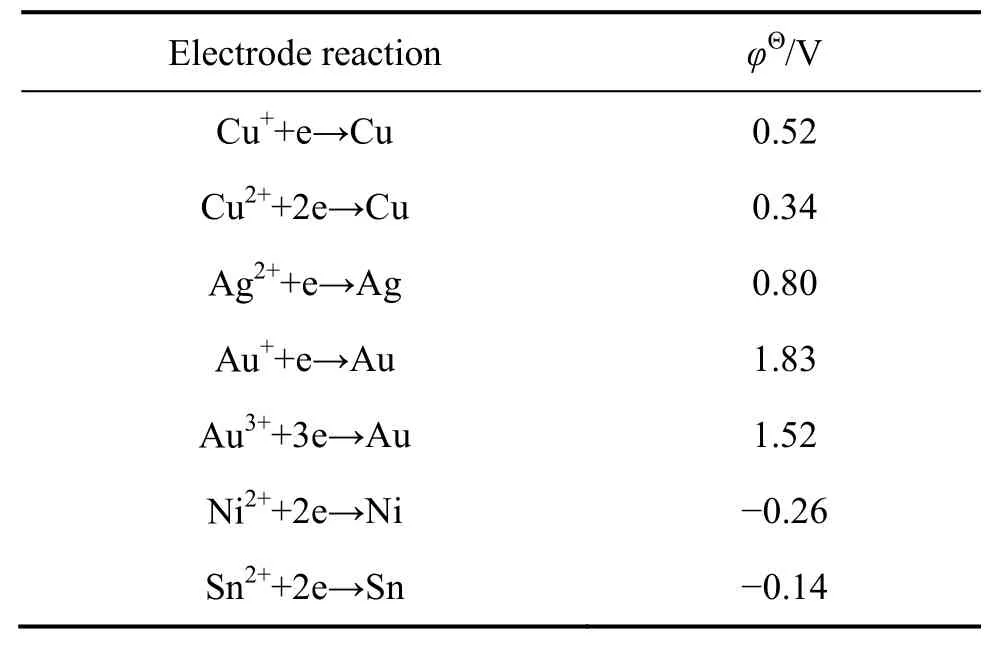
表3 典型金属的标准电极电位[23]Table 3 Standard electrode potentials for common metals[23]
对PCB-ENIG和PCB-ImAg而言,Au和Ag对SO2/S腐蚀敏感性较低[2],腐蚀反应主要发生在涂层缺陷或微孔处的Cu/Ni基底。当电解液以液滴形式存在时,其气/液/固三相界面区将发生强烈的氧还原阴极反应[24],金属离子向该处迁移聚集,并在附近沉积析出圆环状腐蚀产物。腐蚀产物的堆积导致试样表面电位有所升高,而液滴覆盖区域则由于酸的活化作用电位下降,结果在液滴中心和边缘区域形成了较大电位差。随时间推移,液滴逐渐蒸发并在试样表面形成一层薄液膜,金属离子水化、迁移过程较为困难,抑制阳极区反应进程。故PCB-ImAg的腐蚀主要发生在靠近液滴边缘的腐蚀产物环附近,难以向液滴中心区域发展,在Ag/Cu电偶和腐蚀产物吸湿效应作用下基底腐蚀程度进一步加剧,腐蚀产物通过镀层缺陷或裂缝迁移至试样表面[25]。PCB-ENIG的情况则不同,其液滴边缘腐蚀程度相对较轻,主要以微孔腐蚀的形式,从表4可以看出,Au/Ni/Cu电偶腐蚀倾向远大于Ag/Cu电偶对,其离子传输过程主要集中在镀Au层微孔内部;另一方面,从 SKP电位图中不难看出,PCB-ENIG表面电位差值要大于 PCB-ImAg,腐蚀区域更容易向液滴中心方向发展。
Sn作为保护镀层,暴露于干燥空气中几分钟,表面即可生成一层2~3 nm 厚的保护性氧化膜[26],因此,PCB-HASL在干燥大气下可长期保持光亮。然而,在空气污染(SO2)及水膜凝结的条件下,则会发生以酸性液滴为活化中心的腐蚀破坏,Sn表面原有的保护性氧化膜遭到破坏,底部新鲜的 Sn原子将进一步与电解质发生电化学溶解反应(式(5)~(7))[27-28]。从SKP电位图(图 3(d))中可以看到,PCB-HASL液滴作用区域由于酸的活化溶解作用,电位明显降低,有着较高的腐蚀倾向,但从动力学角度,EIS结果反映Sn层的腐蚀速率远低于其他3种PCB材料,结果PCB-HASL腐蚀最为轻微,表面的电位差保持相对稳定状态。

3 结论
1) 未进行表面处理的PCB-Cu在液滴作用下发生严重的全面腐蚀;镀 Au处理后,腐蚀形式主要为微孔腐蚀,腐蚀微孔由边缘区域向液滴中心蔓延;而PCB-ImAg腐蚀区域局限于液滴边缘区域;PCB-HASL腐蚀最为轻微。
2) 酸能够活化PCB-ENIG和PCB-ImAg表面,造成液滴区域电位下降,在试样表面形成较大电位差而促进腐蚀;对PCB-HASL而言,酸能够溶解Sn表面致密氧化层而致使液滴作用区域表面电位大幅下降,具有较高电偶腐蚀倾向,EIS结果反映Sn层腐蚀速率极低。
3) 4种PCB材料中,PCB-HASL耐蚀性最好,PCB-ENIG和PCB-ImAg在液滴作用下基底金属均发生了不同程度的腐蚀,但整体上,PCB-ENIG的耐蚀和防护性能略优,PCB-Cu腐蚀最为严重。因而,在容易产生凝露现象的含硫污染大气环境下,推荐使用PCB-HASL,其次为PCB-ENIG。
[1] FITZGERALD K P, NAIRN J, SKENNERTON G, ATRENS A.Atmospheric corrosion of copper and the colour, structure and composition of natural patinas on copper[J]. Corrosion Science,2006, 48(9): 2480-2509.
[2] LEYGRAF C, GRAEDEL T. Atmospheric corrosion[M]. New York: John Wiley & Sons, 2000: 142-151.
[3] HUANG H, GUO X, ZHANG G, DONG Z. The effects of temperature and electric field on atmospheric corrosion behavior of PCB-Cu under absorbed thin electrolyte layer[J]. Corrosion Science, 2011, 53(5): 1700-1707.
[4] HUANG H, DONG Z, CHEN Z, GUO X. The effects of Cl-ion concentration and relative humidity on atmospheric corrosion behavior of PCB-Cu under adsorbed thin electrolyte layer[J].Corrosion Science, 2011, 53(4): 1230-1236.
[5] KRUMBEIN S J. Corrosion through porous gold plate[J]. IEEE Transactions on Parts, Materials and Packaging, 1969, 5(2):89-98.
[6] BOWCOTT H J, CLEAVER A J. Corrosion of electrical components by their atmospheric environment[J]. Proceedings of the IEE-Part B: Electronic and Communication Engineering,1962, 109(22S): 559-566.
[7] SLADE P G. Electrical contacts: Principles and applications[M].2nd Ed. Boca Raton: CRC Press, 2013: 185-218.
[8] 邹士文, 李晓刚, 董超芳, 李慧艳, 肖 葵. 霉菌对裸铜和镀金处理的印制电路板腐蚀行为的影响[J]. 金属学报, 2012,48(6): 687-695.ZOU Shi-wen, LI Xiao-gang, DONG Chao-fang, LI Hui-yan,XIAO Kui. Effect of mold on corrosion behavior of printed circuit board-copper and ENIG finished[J]. Acta Metallurgica Sinica, 2012, 48(6): 687-695.
[9] 邹士文, 肖 葵, 董超芳, 李慧艳, 李晓刚. 霉菌环境下喷锡处理印制电路板的腐蚀行为[J]. 中国有色金属学报, 2013,23(3): 809-815.ZOU Shi-wen, XIAO Kui, DONG Chao-fang, LI Hui-yan, LI Xiao-gang. Corrosion behavior of hot air solder level finished printed circuit board in mold environment[J]. The Chinese Journal of Nonferrous Metals Society, 2013, 23(3): 809-815.
[10] TAN Y J. Wire beam electrode: A new tool for studying localized corrosion and other heterogeneous electrochemical processes[J].Corrosion Science, 1998, 41(2): 229-247.
[11] 刘园园. 液滴下金属表面电化学性质研究[D]. 青岛: 中国海洋大学, 2012: 4-9.LIU Yuan-yuan. Study of the electrochemical characteristics of metal under an electrolytic drop[D]. Qingdao: Ocean University of China, 2012: 4-9.
[12] NOTTER I M, GABE D R. Porosity of electrodeposited coatings:Its cause, nature, effect and management[J]. Corrosion Reviews,1992, 10(3/4): 217-280.
[13] STRATMANN M. The investigation of the corrosion properties of metals covered with adsorbed electrolyte layers—A new experimental technique[J]. Corrosion Science, 1987, 7(8):869-872.
[14] STRATMANN M, STRECKEL H. On the atmospheric corrosion of metals which are covered with thin electrolyte layers-I.Verification of the experimental technique[J]. Corrosion Science, 1990, 30 (6): 681-696.
[15] STRATMANN M, STRECKEL H. On the atmospheric corrosion of metals which are covered with thin electrolyte layers-II.Experimental results[J]. Corrosion Science, 1990, 30(6):697-714.
[16] 孙 敏, 肖 葵, 董超芳, 李晓刚, 钟 平. 带腐蚀产物超高强度钢的电化学行为[J]. 金属学报, 2011, 47(4): 442-448.SUN Min, XIAO Kui, DONG Chao-fang, LI Xiao-gang,ZHONG Ping. Electrochemical behaviors of ultra high strength steels with corrosion products[J]. Acta Metallurgica Sinica, 2011,47(4): 442-448.
[17] ROHWERDER M, TURCU F. High-resolution Kelvin probe microscopy in corrosion science: scanning Kelvin probe force microscopy (SKPFM) versus classical scanning Kelvin probe(SKP)[J]. Electrochimica Acta, 2007, 53(2): 290-299.
[18] LIU Q, DONG C, XIAO K, LI X. The influence of HSO3-activity on electrochemical characteristics of copper[J].Advanced Materials Research, 2011, 146/147: 654-660.
[19] HERNÁNDEZ R P B, PÁSZTI Z, de MELO H G, AOKI I V.Chemical characterization and anticorrosion properties of corrosion products formed on pure copper in synthetic rainwater of Rio de Janeiro and São Paulo[J]. Corrosion Science, 2010,52(3): 826-837.
[20] 崔中雨, 肖 葵, 董超芳, 丁 源, 王 涛, 李晓刚. 西沙严酷海洋大气环境下紫铜和黄铜的腐蚀行为[J]. 中国有色金属学报, 2013, 23(3): 742-749.CUI Zhong-yu, XIAO Kui, DONG Chao-fang, DING Yuan,WANG Tao, LI Xiao-gang. Corrosion behavior of copper and brass in serious Xisha marine atmosphere[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(3): 742-749.
[21] 严川伟, 何毓番, 林海潮, 曹楚南. 铜在含 SO2大气中的腐蚀初期规律和机理[J]. 中国有色金属学报, 2000, 10(5): 645-648.YAN Chuan-wei, HE Yu-fan, LIN Hai-chao, CAO Chu-nan.Atmospheric corrosion of copper at initial stage in air containing sulfur dioxide[J]. The Chinese Journal of Nonferrous Metals Society, 2000, 10(5): 645-648.
[22] 吴红艳, 周琼宇, 钟庆东, 盛敏奇, 王 毅, 林 海. 阵列电极研究F-对铜在5% Na2SO4溶液中腐蚀电化学行为的影响[J].中国有色金属学报, 2011, 21(7): 1614-1622.WU Hong-yan, ZHOU Qiong-yu, ZHONG Qing-dong, SHENG Min-qi, WANG Yi, LIN Hai. Effect of F-on corrosion electrochemical behavior of copper in 5% Na2SO4solution by using electrode array[J]. The Chinese Journal of Nonferrous Metals Society, 2011, 21(7): 1614-1622.
[23] SPEIGHT J G. Lange’s handbook of chemistry[M]. New York:McGraw-Hill, 2005: 951-966.
[24] JIANG J, WANG J, LU Y, HU J. Effect of length of gas/liquid/solid three-phase boundary zone on cathodic and corrosion behavior of metals[J]. Electrochimica Acta, 2009,54(5): 1426-1435.
[25] 万 晔, 王秀梅, 张 扬, 刘思宇, 孙 红. 银在氢氧化钠溶液中的电化学行为[J]. 中国有色金属学报, 2014, 24(2):535-541.WAN Ye, WANG Xiu-mei, ZHANG Yang, LIU Si-yu, SUN Hong. Electrochemical behavior of silver in NaOH solution[J].The Chinese Journal of Nonferrous Metals Society, 2014, 24(2):535-541.
[26] JOUEN S, HANNOYER B, PIANA O. Non-destructive surface analysis applied to atmospheric corrosion of tin[J]. Surface and Interface Analysis, 2002, 34(1): 192-196.
[27] 颜 忠, 冼爱平. 工业纯Sn和Sn-3Ag-0.5Cu合金在沈阳大气环境下自然暴露的初期腐蚀行为[J]. 中国有色金属学报,2012, 22(5): 1398-1406.YAN Zhong, XIAN Ai-ping. Initial corrosion behavior of Sn and Sn-3Ag-0.5Cu alloy exposed in atmospheric environment of Shenyang[J]. The Chinese Journal of Nonferrous Metals Society,2012, 22(5): 1398-1406.
[28] SASAKI T, KANAGAWA R, OHTSUKA T, MIURA K.Corrosion products of tin in humid air containing sulfur dioxide and nitrogen dioxide at room temperature[J]. Corrosion Science,2003, 45(4): 847-854.
