总汞环境样品的前处理技术及分析方法研究进展
2014-03-24路新燕
于 莉, 陈 纯,李 贝, 路新燕, 刘 丹, 高 勇
河南省环境监测中心,河南 郑州 450004
汞及其化合物都是毒性物质。环境中任何形态的汞均可在一定条件下转化为剧毒且危害不可逆的甲基汞,被人体吸收后穿越血脑屏障,造成脑损伤甚至死亡[1]。无机汞中毒是可逆的,因而危害较轻,但即便如此,在人体中也可到达肾脏,重者可出现急性肾功能衰竭[2]。汞具有很强的迁移性、持久性和高度的生物富集性,是除了温室气体外惟一具有跨国污染属性的重金属,已被联合国环境规划署列为全球性优先控制污染物[3]。在联合国环境规划署的组织下,2010年6月7日全球汞控制公约政府间谈判委员会的第一次会议在斯德哥尔摩正式召开。具有法律约束力的全球性汞问题文书预计在2015年将正式达成签署,全球范围内的“清汞运动”也将随之开始。
随着汞对生态环境影响的日益加剧,在全球范围内对汞污染控制愈发严格;各行业对汞的限值标准也越来越低。2003年联合食品添加剂专家委员会(JECFA)建议对汞允许摄入量 由1972年的每周每公斤体重5 g降至每周每公斤体重1.6 g[4]。2003年2月13日2002/ 95/ EC欧盟公布电子电气产品环保指令ROHS标准规定,从2006年7月1日起,新投放欧盟市场的电子电气设备中不得含有铅、汞、镉、铬(Ⅵ)、多溴联苯(PBB) 和多溴二苯醚( PBDE) 6种有害物质。从2011年3月15日起,欧盟将全面禁止金属汞、汞矿石、汞化合物和汞齐出口,要求把再生汞作为废物管理和处置,不得用于氯碱生产等工业用途;而我国2006年新颁布的《生活饮用水卫生标准》中限定饮用水中总汞含量必须小于1 μg/L;2011年我国新出台的《火电厂污染排放标准》中增加了汞的排放标准,控制质量浓度为0.03 mg/m3。因此,梳理、建立完善的环境总汞的检测体系具有重要的现实意义。
该文对环境样品中汞的前处理和分析方法进行了较为系统的论述,展望了环境样品中总汞检测的发展趋势,为研究者进行总汞新分析方法的开发和标准化提供了借鉴。
1 总汞环境样品的前处理技术
1.1水样中总汞的前处理技术
水体中存在大量Cl-、OH-、SO42-、腐殖酸、悬浮颗粒物和各种微生物,它们能以物理或化学吸附的形式与不同价态的汞结合,形成Hg0、Hg2+、Hg(OH)n、HgCln、HgO、HgS、CH3Hg+、CH3Hg(OH)、CH3HgCl、CH3Hg(SR)及(CH3Hg)2S等各种形态构成环境中复杂的汞形态体系[5-6]。目前,对水体中总汞的检测常用的方法有冷原子吸收法、冷原子荧光法、原子荧光法、双硫腙分光光度法,电感耦合等离子体-发射光谱法(ICP-AES)也有所应用,上述方法由于研究不够深入或存在各种限制因素而并未标准化,因而应用较少。然而在测定水样总汞时,不论是何种测定方法,均需将样品中各形态汞转变为Hg2+。一般采用高锰酸钾+过硫酸钾或溴酸钾+溴化钾来消解水样[7],也有仅采用HNO3、HNO3-HF-HClO4或HNO3-H2O2等酸氧化体系的报道[8-9],在消解工具的使用方面,可采用常规消解仪器(电炉、电热板等),也有采用高压消解或红外消解[10-11]。近年来,微波溶样技术发展迅速, 与传统的加热方式热对流相比, 微波加热是利用分子极化或离子导电效应直接对物质进行加热, 热效率高, 升温速度均匀快速,应用于样品的处理高速有效, 消化试剂用量小, 污染少, 故微波消解用于重金属的测定受到广泛重视[12-14]。
由于汞在天然水体中的含量为微量或痕量,甚至低于分析方法的检出限,若直接检测汞含量是不准确的,当存在干扰物质或试剂纯度不够时更是如此。因而对于痕量汞的测定,有时需要用吸附性物质去除试剂中的汞,消解过以后还需经过预富集和分离,才能提高汞浓度并将待测痕量组分与干扰组分分开,从而降低检出限,提高分析结果的精密度和准确度并扩大测定技术的应用范围。因此,选用合适的分离富集方法很重要。目前, 在该研究领域中比较成熟的方法主要有如下几种:
1)改性天然高分子吸附剂,如巯基棉、巯基葡聚糖、羧甲基壳聚糖等。其中巯基棉对不同浓度汞和其他金属离子均有较快的吸附速度,选用10 mL/min的速度富集汞时,吸附率可达99.2%[15],因而在痕量汞的富集分离方面应用广泛。众多研究表明,采用高分子吸附剂吸附待测液中的汞和杂质,再通过调节酸度洗脱,可以提高方法的检出限并消除很多杂质的干扰[15-16]。
2)改性树脂。如孙俊梅等[17]用奎宁负载树脂(QCR) 分离氢化物发生ICP-AES法测定汞, 在最佳实验条件下, QCR对汞的吸附容量为19.7 mg/g。
3)液膜法。如王献科等报道了用HEHEHP-TOA-SPAN80-甲苯乳状液膜体,考察了Hg2+的迁移富集行为, 在适宜条件下, Hg2+的迁移率达99.6%以上。在此条件下、许多共存金属离子(如Cu2+、Mn2+、Fe3+、Cd2+、Pb2+、Zn2+、Al3+等)都不迁移,达到了Hg2+与杂质分离的效果,应用于测定水和工业废水中微量汞, 结果令人满意[18]。
总体来讲,汞的消解前处理技术已经较为纯熟,微波消解作为更加环保有效的消解手段正逐渐成为发展趋势。而汞的富集前处理技术虽然方法多,但过程大多较为烦琐,应在简便和环保方面加大研究力度, 并可望进一步对汞元素的不同形态进行分析。
1.2土壤中总汞的前处理技术
土壤中汞按化学形态主要分为金属汞、无机化合态汞和有机化合态汞,一般情况下以无机化合态汞为主要存在形式。其在各种土壤中的含量差异很大。受人类活动影响小的土壤中汞的含量为微量,全球土壤汞的背景值为0.01~0.05 mg/kg,我国土壤汞的背景含量平均为0.04 mg/kg[19-20],而受矿山或人类活动影响的土壤汞含量会剧增,如西安郊区6个污灌区土壤汞含量均处于0.52~0.90 mg/kg[21],贵州万山汞矿区土壤中汞含量为1.3~360 mg/kg[22]。
土壤重金属的消解体系有碱熔法和酸溶法,碱熔法常用的体系有Na2O2-NaOH、Na2O2-Na2CO3、KHSO4-K2S2O7等,一般认为碱熔法试剂用量较大,杂质带来很高的空白,因而在汞的分析中较少使用碱熔法作为前处理手段。
而酸溶法(即湿法)消解与碱熔法相比,具有耗时短、试剂用量少等优点,是土壤汞消解的常用方法。目前常用的酸溶法体系主要有H2SO4-HNO3-V2O5、H2SO4-HNO3-KMnO4、H2SO4- KMnO4、HNO3-HClO4-HF、H2SO4-HNO3-HClO4、HNO3、王水等。不同的消解体系操作程序繁简各异,适用于不同的土壤样品,对测定结果的影响也很大。单独使用HNO3消解土样,一般只能溶出样品中1/5~1/3的总汞; H2SO4-HNO3-V2O5、H2SO4-HNO3-KMnO4、H2SO4-HNO3-HClO4等方法消解过程较为烦琐,但消解彻底,对HgS和氯化甲基汞分解效果好,特别对有机质含量多的样品采用V2O5分解更为彻底[23];王水消解氧化能力强,分解迅速,但温度高,有一定的危险性[24]。
在消解工具的使用方面,常用的有电热消解、水浴消解、微波消解等方式。资料表明,消解效率从高到低顺序一般为微波消解>水浴消解>电热消解。其中,水浴消解是土壤元素汞常用的消解方法,有研究表明,王水+水浴消解方法消解程度完全、测定结果稳定[1];微波消解是以被分解的土样和酸的混合液为发热体,从内部进行加热而使试样分解,具有分解彻底、节省时间和药品用量等优点,近年来被广泛使用[25-28]。
1.3大气中总汞的前处理技术
汞在大气中以2种形态存在:气态总汞和颗粒态汞,一般来讲,前者约占95%左右,气态总汞在ng/m3级别,而颗粒态汞小于100 pg/m3[29]。目前对大气总汞的检测方法主要有冷原子吸收光谱法、冷原子荧光光谱法、分光光度法、中子活化法等。其中冷原子吸收光谱法和冷原子荧光光谱法应用较为广泛,中子活化法由于灵敏度低,应用受到限制。普通的分光光度法检测限较低,不太适用于大气中痕量汞的测定,因而相关报道也较少。
与水体和土壤不同,大气中总汞的测定一般不涉及消解前处理,但均需用一定吸附装置富集,再通过某种方法转化为汞单质蒸气,以便仪器测定。目前主要的富集手段:
1)湿法吸收。用含强氧化剂的吸收液[如H2O2、(NH4)2S2O8、KMnO4-H2SO4、K2Cr2O7-HNO3、HI-I2、KI-I2、K2Cr2O7-H2SO4等]吸收大气中的汞,同时将所有形态的汞氧化为Hg2+,然后利用SnCl2还原为汞单质蒸气测定。该方法多用于污染源监测,日本JIS K0222—1997方法即采用此类技术收集废气中的汞。
2)固体吸附剂(如MnO2或KMnO4、用碘或其他卤素处理过的活性炭等)。利用固体吸附剂直接汞蒸气吸附后,再进行直接热裂解或热解析分析。该方法在新型烟气汞采样设备中有较多应用,EPA的30B方法就是基于此种技术的采样。
3)巯基棉富集。在微酸性介质中,用巯基棉富集空气中的各形态汞,再用盐酸-氯化钠解吸,经氯化亚锡还原后用仪器测定。受到巯基棉制备和吸附效率差异的影响,近年来此方法应用已经较少。
4)汞齐富集。一般用金或银等贵金属富集管吸附空气中的微量汞,形成汞齐,然后加热至500 ℃以上,将汞蒸气释放出来进入冷原子吸收或冷原子荧光检测器中测定。这一方法消除了化学分析中的试剂空白问题, 灵敏度好、空白低, 金管和银管等可以重复使用, 非常方便。该方法目前在汞的仪器分析中被广泛使用。
近年来,研究者对汞的富集方法提出了不少新的改进措施,取得了很好的检测结果。如李金兰等[30]在已有仪器基础上进行改装, 建立了二次金汞齐冷原子荧光光谱法(CVAFS)测定大气中痕量气态元素汞(GEM) 和颗粒态总汞(TPM) 的方法,该方法的检出限为2 pg/L, 二次金汞齐的转移效率为99%, 在0~2 ng 范围内绘制标准曲线,线性相关系数为0.999 5,检测精密度为1.89%。汤庆合等[31]采用镀金石英砂来富集大气中的气态总汞,结果表明, 不同采样时间下的单级吸附管的吸附效率均在90%以上, 采样40 min时的相对标准偏差为5%左右,方法具有吸收效果好、多次采样的精密度高、操作简便、可以再生重复使用等优点。
2 总汞的分析方法
2.1分光光度法
分光光度法具有仪器设备简单、操作较简便、分析成本低等优点,在汞的检测中应用十分广泛。除了作为国家标准的双硫腙分光光度法外,若丹宁偶氮类、三氮烯类、催化动力学、Hg-X-阳离子染料体系也被用于汞的监测。不同的光度法分析技术见表1。
光度分析法测定总汞的仪器投入较少,简便易行;在一些部门的例行分析及科研院所的科学研究中仍被采用;与汞的仪器分析法相比,光度法具有操作步骤较烦琐、方法检出限较高、抗干扰能力不足等缺点,在实验室监测领域近年来已经逐步被冷原子吸收、原子荧光等方法替代。近年来,新型显色剂的开发及高灵敏度紫外-可见光度检测器、光敏传感电极等仪器联用新技术的发展,使光度分析法在汞的在线监测等领域有了快速发展。

表1 总汞的光度分析方法
2.2冷原子吸收光谱法
冷原子吸收光谱法是《水和废水监测分析方法》中测定汞的方法之一。该方法具有较高的灵敏度、较低的检出限和测定下限,且操作简便,是当今痕量汞测定最普遍使用的方法。该方法最低检出浓度为0.1~0.5 μg/L[32]。结合其他的富集方法,可测定ng/L级别的汞。KBH4和NaBH还原剂的引入较传统的SnCl2还原法操作简便,且还原速度快。冷原子吸收光谱法的主要干扰因素:
1)试剂中的微量汞。天然水中含汞量一般是极微量的,试剂中含一定量的汞必然会对测定产生严重干扰。有研究已经证明,消解水样时的硫酸和高锰酸钾均含有微量的汞,可能会使测定结果偏高[56]。
2)吸附作用。张朝明等[56-58]研究表明,进气口使用的硅胶管对汞的吸附作用很强,受热时,在温度适应时即释放, 加上气路的记忆效应等因素, 造成测量结果偏高。
2.3冷原子荧光法
原子荧光法用于汞的测定主要有2种模式:原子荧光光谱法(热汞法)和冷原子荧光光谱法(冷汞法)。相比于热汞法,冷汞法的检出限更低、灵敏度更高,干扰因素也更少[32],目前冷汞法已被列为汞测定的标准方法之一。冷原子荧光光谱法灵敏度比原子吸收法高,而且具有线性动态范围宽、原子化器和测量系统记忆效应小等优点,在《水和废水监测分析方法》中检出限为1.5 ng/L,测定上限为1 μg/L。冷原子荧光光谱法的主要干扰因素:①荧光猝灭。当载气纯度不足时,载气中氧气、一氧化碳、二氧化碳等气体含量相对升高,激发态的汞原子易与这些气体粒子发生碰撞而造成荧光猝灭,最终使测定结果偏低。②水汽干扰。如仪器长时间不用,内部荧光池会潮湿,操作时氯化亚锡和强碱性介质样品液反应时,产生的中和热导致生成大量水汽,对光源产生散射作用,这对荧光信号的测定产生很大干扰。
2.4阳极溶出伏安法
阳极溶出伏安法将汞的富集和测定结合起来,并具有较高的灵敏度和选择性。应用中,通常采用玻碳电极作为阳极,并用特殊物质对之进行修饰以实现Hg2+的高效富集。同时需要加入底液以提高灵敏度。谢红旗等[59]用聚苯基荧光酮修饰玻碳电极,以0.1 mol/L氨水-NH4Cl 缓冲溶液为底液,对汞富集还原后进行阳极化线性扫描,在0 V左右得到灵敏的汞的溶出峰。峰电流与Hg2+在9.8×10-8~8.0×10-7mol/L范围内线性相关,检出限达2.0×10-8mol/L。易洪潮等[60]用钠型蒙脱石修饰玻碳电极,以pH=4.0的磷酸盐缓冲液为底液建立了一种同时测定痕量镉、汞离子的方法。其中测定汞的线性范围为4×10-8~7.5×10-6mol/L,检出限为8×10-9mol/L。阳极溶出伏安法的缺点在于容易产生记忆效应, 洗脱不良;同时,其适用性取决于测定样品基体的复杂性,较多的干扰因素限制了这种方法的广泛应用。
2.5电感耦合等离子体质谱法
电感耦合等离子体光源(ICP)和质谱仪(MS)联用技术(ICP-MS)始于1980年。方法有高灵敏度、干扰少、分析速度快和检出限超低等优点,现阶段是ICP-MS法和现行国标方法反复对比验证的试验阶段[61],对ICP-MS测汞的研究也正在不断深入。
谢云欣等[62]对ICP-MS检测水中的汞进行研究,得出方法的检出限、定量限和精密度分别达到0.002 74 ng/mL、0.009 1 ng/mL和6.18%(n=12),并指出了汞的ICP-MS分析过程中容易被忽视的问题:不同的盛装容器将对分析结果会产生显著影响,应该采用玻璃容器盛装待测试样;标准系列必须现用现配;测试过程中浓度超过0.10 ng/mL会产生较强记忆效应,需要在线内标溶液含200 ng/mL的Au进行消除,为消除前一个样品的记忆效应清洗时间不能少于3 min。王琳等[63]用微波梯度升温消解技术处理样品,ICP-MS法测定鲤鱼和河蚌中Hg和As,建立的方法简便、快速、准确, 标准曲线的线性关系均大于0.999 0, 样品加标回收率为97.9%~ 104%。王英锋等[64]建立了用微波消解技术-ICP-MS法同时测定丙烯腈-丁二烯-苯乙烯共聚物(ABS) 塑料中的铅、镉、汞、铬、砷五种元素的方法,得到汞的检出限为3.6ng/g,回收率为91.45%~110.8%,相对标准偏差为8.7%,方法检出限低、精确度好、准确度高、简单快速、无需基体匹配。陈国友等[65]用ICP-MS、AFS、GF-AAS分别测定食品中的As、Cd、Hg、Pb,发现用ICP-MS测定得出的Hg值略高于AFS法,3种方法测定结果不存在显著性差异。
2.6生化检测方法
随着材料科学、生物传感技术的发展,近些年来,人们逐渐致力于研制简单便捷的“绿色”的检测汞离子的方法。2004年Ono小组首次报道了汞离子能与DNA序列中T-T碱基对发生特异性结合形成稳定的T-Hg2+-T结构,由此拉开了利用汞的核酸适配体进行汞离子的生化检测的新篇章。
2.6.1酶检测方法
重金属离子可以和一些酶活性位点上的巯基基团特异性结合, 从而对酶的活性产生抑制,通过测定这些酶被抑制的程度, 来对汞化合物进行总量甚至形态分析。这些酶主要有脲酶、辣根过氧化物酶、蔗糖酶、L-乳酸脱氢酶、葡萄糖氧化酶等。
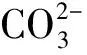
2.6.2基于核酸适配体探针的汞检测方法
核酸适配体探针是近些年来新发展起来的一种元素分析方法,利用在荧光生物传感器、比色生物传感器等方面,均取得了很好的研究成果。
2.6.2.1荧光生物传感器技术
荧光生物传感器利用荧光基因标记核酸适配体,或将荧光基因和猝灭基因分别标于核酸适体或直接利用荧光嵌入剂嵌入核酸适配体,通过目标物质引入体系后荧光信号的改变来实现对待测物质的定量分析[69]。由于具有高选择性、高灵敏度和易于应用等特点,目前已经发展了用荧光生物传感器检测多种元素的方法[70]。
Ono等[71]在2004年发现了Hg2+可与寡核苷酸(ODN)中的T-T碱基对发生特异性结合并具有强的热稳定性,而其他金属离子(如Cu2+、Pd2+)均不显示此种性质。由此设计了“Turn-Off”状态的汞离子荧光传感器:分别将荧光基团和猝灭基团标记到ODN的3’和5’端,形成D-ODN-F探针。该DNA探针与Hg2+结合后形成发卡结构,产生荧光猝灭。通过检测DNA探针与Hg2+结合前后荧光强度的变化实现对Hg2+的特异性检测。该方法具有较高的特异性,可排除实际样品体系中大多数离子的干扰,检测限达4×10-8mol/L。
2.6.2.2比色生物传感器技术
比色生物传感器主要利用了纳米金颗粒的独特性质。纳米金不仅拥有一般纳米材料的特点,还具有独特的生物兼容性,同时对光的吸收强、反射弱、具有优异的光学性能。研究表明,纳米金溶液的颜色与纳米金颗粒的间距以及纳米金聚集体的大小有关。纳米金颗粒的间距若明显超过其平均直径,纳米金颗粒呈分散状态,溶液为红色;若该间距小于平均直径,则纳米金颗粒易团聚,呈现聚集状态,表现为紫色或蓝色。1996年,Mirkin等[72]在纳米金探针溶液中加入一段两端均与纳米金探针中的寡核苷酸互补的靶核酸后,使13 nm的纳米金的表面等离子体共振吸收峰从520 nm红移到574 nm,这种现象使纳米金探针用于生物检测成为可能。随后,Lee等[73]在47 ℃下通过修饰在纳米金颗粒表面上的DNA与Hg2+的特异性作用将纳米金颗粒聚集在一起形成聚集态,在聚集过程中发生由红色向蓝紫色转变,由此发展出一种用生物比色法检测Hg2+的方法。该方法对Au-S键的形成和表面DNA自组装密度都有较高要求;整个方法过程耗时较长、成本高、操作复杂。因此,对非标记核酸探针检测Hg2+的研究逐渐增多。Wu等[74]发现孔雀绿(MG)能与Hg2+核酸适配体及Hg2+形成Hg2+(aptamer)-MG-Hg2+复合体,导致共振光散射强度在611 nm处增加,由此建立了一种非标记核酸探针检测Hg2+的方法,方法灵敏度高,检测限达1.7 nmol/L。
2.7在线监测技术
随着经济的发展,环境重金属(特别是汞)的污染事故越来越频发。因此,发展快速有效的在线监测技术,建立全面的监控预警体系十分必要。
2.7.1水质在线监测
由于水中汞的控制浓度较低,传统的在线设备无法满足要求,因此目前水质汞的在线监测产品还相对较少[75-77]。考虑到仪器的自动化设计难度及运维成本,原子吸收光谱法、原子发射光谱法、电感耦合等离子体质谱法等方法较少应用于汞在线监测领域。目前,国内外用于此领域的技术主要是光度法和电化学分析法。
光度法应用于水质汞在线分析时,选择合适的显色剂及消除其他金属组分干扰是关键,其次是获得稳定可靠的单色光以及光强检测系统。同时,为了提高测量的准确性和稳定性,可靠稳定的进样装置也是非常关键的技术;考虑到在线仪器运营维护费用,小体积进样也是重要的参考指标之一。目前,水质汞在线设备多采用若丹宁偶氮类物质(如苯基重氮氨基偶氮苯)作为显色剂,依靠紫外-可见光度计来对水中的汞进行比色分析。由于此类显色剂的稳定性多数欠佳,多数显色反应需控制在碱性条件下,对复杂基体的抗干扰能力不足,因此应用受限。
相比于光度法,电化学溶出分析的技术更适合于汞的在线监测,其优势:检测模块较简单,易于实现自动化;在合适的工作电极、合适的分析环境条件下,可以对水中μg/L级浓度的汞进行准确定量;能够同时分析水中的多种重金属离子,分析过程本身不会产生危害性大的副产物。但是电化学分析方法易受到干扰,因此往往需要预处理;另外,方法的稳定性对工作电极的要求极高;如果电极使用了液态汞或者镀汞膜,分析过程会引入汞,对环境和分析操作维护人员存在较大的危害。这些因素都限制了电化学溶出分析技术在水质自动监测中的普遍推广。
2.7.2烟气在线监测
与水质汞的在线监测相比,汞污染源实时在线监测技术近年取得了较大的进展和实际应用。该技术主要是基于冷蒸气原子吸收光谱、冷蒸气原子荧光光谱、塞曼调制原子吸收光谱、紫外差分吸收光谱和新兴的化学微传感器等先进技术发展起来的,优点是能获得在线的实时的分析结果[78]。
我国当前主要在燃煤电厂进行汞在线烟气排放监测。汞烟气排放连续监测系统(CEMS)由烟气取样与输送系统、汞形态转化系统、汞分析系统、校准系统及数据的采集处理传输系统5个部分组成。在通常情况下,汞CEMS是用装有颗粒物过滤装置的采样探头可连续从烟道内抽取烟气,用伴热管线将其通入Hg收集转换装置中,将Hg2+还原为Hg0再输送到分析仪,测定排放源排放的总气态(即元素汞Hg2+与Hg0之和),分析数据又直接被传输到数据记录、储存系统[79]。
汞在线监测系统的采样探头内部件加热可达250 ℃,探头内有过滤装置,可有效去除烟气颗粒物对测试结果的影响;同时,配置有稀释探头或惯性分离探头,具有动态加标口,可进行动态加标测试[79]。
汞转换装置通过高温裂解或者化学转换的方法将化合物汞转化为元素汞Hg0;传输系统则在配有反吹气管、校准气管、气水分离装置、加热系统等;有效防止汞吸附和管道腐蚀。校准单元则配置汞标气或自带的汞蒸气发生校准装置[79]。
中国环境科学研究院曾开展燃煤电厂大气汞污染排放特征的研究,脱硫装置出口后的混合烟道上安装美国Thermo-Fisher公司生产的烟气汞连续监测系统。该系统采用的原理是冷原子吸收荧光法。经过1年多的连续监测,并经河北省环境监测中心站监测检验,测定数据准确可靠[80]。
3 展望
随着社会的进步,科学研究对环境中汞检测的灵敏度、检出限和便捷性提出了越来越高的要求。原有的分光光度法、原子荧光、原子吸收等方法目前虽然能满足大多数的汞分析要求,但在检出限和快速测定等方面已逐渐显示出与新分析方法的差距。通过对汞分析方法的调研,总结了未来汞监测的几个研究方向:
1)ICP-MS方法具有高灵敏、超低检出限、测定速度快、可实现多种元素同时分析等优点,在汞的测定方面的应用也日趋广泛,有望成为汞检测的标准方法。国产ICP-MS及配套汞采样设备的开发将大大推动此类技术在汞环境监测中的应用。
2)汞的在线监测技术在我国起步较晚,发展较慢,目前针对Hg的在线监测技术还正处于发展和成熟阶段;加强重金属在线监测仪器的技术研发、建立起重金属在线监测仪的技术标准和质量控制措施是亟待解决的问题。
3)基于核酸适配体的汞的传感器检测方法,具有选择性好、干扰少、测定灵敏快捷,具有非常广阔的发展前景。
参考文献:
[1]Counter S A, Buchanan L H. Mercury exposure in children: A review[J]. Toxicology and Applied Pharmacology, 2004, 198(2): 209-230.
[2]Rothschild R F N, Duffy L K. Mercury concentrations in muscle, brain and bone of Western Alaskan waterfowl[J]. Science of the Total Environment, 2005, 349(1): 277-283.
[3]胡月红. 国内外汞污染分布状况研究综述[J]. 环境保护科学, 2008, 34(1): 38-41.
[4]WHO Food Additivers Series:59Safety evaluation of certain food additives and contaminants[S].
[5]陈宏. 三峡库区消落带土壤汞库及其风险评价[D]. 重庆:西南大学, 2009.
[6]冯新斌, 仇广乐, 付学吾,等. 环境汞污染[J]. 化学进展, 2009, 21(2/3):436-457.
[7]李咏梅, 李人宇, 张龙,等. Hg2+-碘化物-吖啶橙-聚乙烯醇缔合体系褪色光度法测定痕量汞[J]. 冶金分析, 2010, 30(5): 61-64.
[8]李琼芳, 莫海洪, 陈爽爽,等. 催化分光光度法测定痕量汞[J]. 佛山科学技术学院学报: 自然科学版, 2006, 24(2): 64-66.
[9]李耕. 石墨炉原子吸收光谱法测定水样消解研究[J]. 福建分析测试, 2006, 15(1): 12-14.
[10]何应深, 吴毓. 高压消解罐消解-原子荧光光谱分析法测定稻谷中的总汞[J]. 粮食科技与经济, 2011, 36(5): 47-48.
[11]王北洪, 马智宏, 付伟利. 密封高压消解罐消解-原子吸收光谱法测定土壤重金属[J]. 农业工程学报, 2008, 24(增刊2): 255-259.
[12]范华均, 李攻科, 栾伟,等. 微波溶样-石墨炉原子吸收光谱法测定石蒜中的镉铬铅[J]. 光谱学与光谱分析, 2005, 25(9): 1 503-1 506.
[13]肖振林, 刘玉静, 王敏. 微波消解-等离子体发射光谱法测定野生山葡萄中的金属元素[J]. 食品科学, 2011, 32(10): 153-155.
[14]雷蓓, 张敏. 微波消解-火焰原子吸收光谱法测定某推进剂中Pb, Cu和Ca 元素含量[J]. 含能材料, 2006, 14(2): 99-101.
[15]宋吉英, 侯明. 羧甲基壳聚糖吸附痕量汞研究[J]. 分析试验室, 2006, 25(5): 69-73.
[16]宋吉英, 李军德, 王东强,等. 交联羧甲基壳聚糖吸附痕量汞研究[J]. 离子交换与吸附, 2008, 24(2): 175-182.
[17]孙俊梅, 刘怀志. 奎宁负载树脂分离氢化物发生ICP-AES测定汞的研究[J]. 分析科学学报, 1998, 14(4): 288-291.
[18]王献科, 李玉萍. 用 HEHEHP-TOA 为协同流动载体的乳状液膜分离富集汞 (Ⅱ) 的研究[J]. 新疆有色金属, 2000(4): 35-38.
[19]洪春来, 贾彦博, 杨肖娥,等. 农业土壤中汞的生物地球化学行为及其生态效应[J]. 土壤通报, 2007, 38(3): 590-596.
[20]杨燕娜, 温小乐.土壤汞污染及其治理措施的研究综述[J]. 能源与环境, 2006(3): 9-11.
[21]栾文楼, 温小亚, 崔邢涛,等. 石家庄污灌区表层土壤中重金属环境地球化学研究[J]. 中国地质, 2009, 26(2): 465-473.
[22]Qiu G, Feng, Wang S et al. Mercury contaminations from historic mining to water, soil and vegetation in Lanmuchang, Guizhou, southwestern China[J]. Science of the Total Environment, 2006, 368(1): 56-68.
[23]魏复盛. 土壤元素的近代分析方法[M]. 北京:中国环境科学出版社, 1992.
[24]李忠根, 冯新斌, 何天容,等. 王水水浴消解-冷原子荧光法测定土壤和沉积物中的总汞[J]. 矿物岩石地球化学通报, 2005, 24(2): 141-143.
[25]冷庚, 杨嘉伟, 谢晴,等. 微波消解-氢化物发生原子荧光光度法测定土壤中的汞[J]. 环境工程学报, 2011, 5(8): 1 893-1 896.
[26]李波, 崔杰华, 刘东波,等. 微波消解-氢化物发生原子荧光法同时测定土壤中的砷汞[J]. 分析试验室, 2008, 27(7): 106-108.
[27]许建华, 田锋, 杜青,等. 微波消解-原子荧光法测定土壤中汞, 砷, 硒[J]. 环境监测管理与技术, 2007, 19(4): 34-35.
[28]马伟. 两种土壤消解方法测定汞元素的验证[J]. 青海环境, 2012, 21(4): 188-190.
[29]李仲根, 冯新斌, 郑伟,等. 大气中不同形态汞的采集和分析方法[J]. 中国环境监测, 2007, 23(2): 19-25.
[30]李金兰, 罗津晶, 张龙东,等. 二次金汞齐冷原子荧光光谱法测定大气痕量汞[J]. 厦门大学学报: 自然科学版, 2011, 50(3): 574-578.
[31]汤庆合, 王文华, 黄丽华. 镀金石英砂吸附-AMA254 测汞仪测定大气中痕量汞的研究[J]. 中国环境监测, 2007, 23(2): 8-11.
[32]魏复盛. 水和废水监测分析方法[M]. 北京:中国环境科学出版社, 2002: 361.
[33]李松, 黎国兰. 双硫腙分光光度法测定空气中汞的改进[J]. 光谱实验室, 2005, 22(6): 1 280-1 283.
[34]蔡慧华, 彭速标. 痕量汞的测定方法进展[J]. 理化检验:化学分册, 2008, 44(4): 385-390.
[35]李满秀, 吕艳华. 石蜡相分光光度法测定汞的研究[J]. 冶金分析, 2006, 26(5): 87-88.
[36]张海明, 李成海, 唐雅娟. 胶束增溶二苯硫腙吸光光度法测定水溶液中汞[J]. 理化检验: 化学分册, 2008, 44(2): 191-192.
[37]赵会峰, 张加玲. 浊点萃取分光光度法测定水样中的痕量汞[J]. 中国卫生检验杂志, 2009(2): 302-304.
[38]吴献花, 台希, 李海涛,等. 4-羟基萘-1-亚甲基若丹宁固相萃取光度法测定环境样品中的汞[J]. 环境研究与监测, 2005, 17(3): 8-10.
[39]吴玉萍, 王东丹, 徐照丽,等. 对磺酸基苯亚甲基硫代若丹宁固相萃取光度法测定烟草添加剂中的汞[J]. 分析科学学报, 2005, 21(1): 60-62.
[40]王琳, 王炯, 尹家元. 固相萃取光度法测定环境水样中汞的研究[J]. 冶金分析, 2005, 25(6): 39-41.
[41]阮琼, 胡秋芬, 杨光宇,等. 新试剂 SBDR 固相萃取光度法测定烟草中汞[J]. 理化检验: 化学分册, 2006, 42(1): 12-15.
[42]崔永春, 翟平, 胡永,等. 用对磺酸苯亚甲基硫代若丹宁固相萃取法测定食品和水中的微量汞[J]. 稀有金属, 2006, 30(2): 168-171.
[43]陈文宾, 陈璧珠, 林艳,等. 巯基葡聚糖凝胶分离富集对硝基苯基重氮氨基偶氮苯分光光度法测定微量汞 (Ⅱ)[J]. 冶金分析, 2009, 29(12): 61-65.
[44]王贵方, 何其戈, 张光. 新显色剂 2, 4, 4’-三基苯基重氮氨基偶氮苯的合成及其与汞的显色反应[J]. 分析试验室, 2006, 25(9): 18-21.
[45]王海青, 岳志劲, 刘永文,等. 新显色剂 2-羟基-3-磺酸基-5-硝基苯基重氮氨基偶氮苯与汞的显色反应研究[J]. 光谱实验室, 2005, 22(5): 966-968.
[46]王君玲, 孟双明, 樊月琴,等. 新显色剂 2-磺酸基苯基-1, 4-二重氮氨基偶氮苯与 Hg (Ⅱ) 的显色反应及其应用[J]. 分析试验室, 2008, 27(1): 77-79.
[47]王文革, 赵书林, 李舒婷. 1-偶氮苯-3-(6-甲氧基-2-苯并噻唑)-三氮烯的合成及用于汞的光度测定[J]. 理化检验: 化学分册, 2006, 42(2): 100-102.
[48]徐国想, 马卫兴, 陈文宾,等. 巯基葡聚糖凝胶分离富集5-(对羧基苯偶氮)-8-羟基喹哪啶分光光度法测定微量汞(Ⅱ)[J]. 冶金分析, 2009, 29(11): 29-33.
[49]许琳, 胡志勇, 刘永文,等. 4-甲氧基-2-磺酸基苯基重氮氨基偶氮苯的合成及其与汞 (Ⅱ) 的显色反应[J]. 光谱实验室, 2008, 25(3): 319-322.
[50]许琳, 孟双明, 王君玲,等. 4, 6-二甲氧基-2-嘧啶重氮氨基偶氮苯的合成及其与汞 (Ⅱ) 的显色反应[J]. 分析试验室, 2007, 25(12): 23-25.
[51]张春牛, 郑云法. 1-偶氮苯-3-(3-硝基-5-氯-2-吡啶)-三氮烯的合成及其与汞的显色反应[J]. 理化检验: 化学分册, 2008, 44(2): 146-148.
[52]姚绍龙. 阻抑甲基橙褪色动力学光度法测定痕量汞[J]. 分析化学, 2001(8):79-81.
[53]张穗娟, 李琼芳, 莫海洪. K4[Fe(CN)6]-K3[Fe(CN)6]体系催化分光光度法测定痕量汞[J]. 分析试验室, 2007, 26(3): 81-83.
[54]刘梅, 樊静, 孙玉平. 汞 (Ⅱ)-硫氰酸盐-罗丹明 6G 多元络合物混合胶束增敏分光光度法测定环境水中痕量汞[J]. 冶金分析, 2009, 29(2): 28-31.
[55]谢跃勤, 盛良全, 杨俊,等. 高灵敏度固相光度法测定微量汞 (Ⅱ) 的研究[J]. 理化检验: 化学分册, 2005, 40(11): 664-666.
[56]周利萍, 赵秀兰, 王正银,等. 冷原子吸收法测水体汞的影响因素[J]. 微量元素与健康研究, 2005, 21(6): 45-47.
[57]张朝明,朱方保. 汞观测中干扰因素的研究[J]. 地震, 1994, 2(1): 79-86.
[58]王振升. 水汞观测中值得注意的几个问题[J]. 地震, 1996, 16(3): 311-316.
[59]谢红旗, 周春山, 刘梦琴,等. 聚苯基荧光酮修饰玻碳电极吸附溶出伏安法测定痕量汞[J]. 理化检验: 化学分册, 2007, 43(2): 141-143.
[60]易洪潮,吴康兵,胡胜水,等. 离子交换伏安法同时测定水体中的镉、汞[J].分析科学学报,2001,17(4):275-278.
[61]毛红, 刘丽萍, 张妮娜,等. 应用 ICP-MS 与 AAS 测定食品中铅、镉、铜方法研究及比较[J]. 中国卫生检验杂志, 2008, 17(11): 1 954-1 955.
[62]谢云欣, 李东雷, 左宇昕. ICP-MS检测饮用水中汞的方法研究[J]. 生命科学仪器, 2009, (12): 19-21.
[63]王琳, 黄晶, 董铮. 微波消解-ICP-MS 法测定鲤鱼和河蚌中汞和砷[J]. 四川环境, 2010, 29(4): 47-49.
[64]王英锋, 施燕支, 张华,等. 微波消解-电感耦合等离子体质谱法测定丙烯腈-丁二烯-苯乙烯共聚物塑料中的铅、镉、汞、铬、砷[J]. 光谱学与光谱分析, 2008, 28(1): 191-194.
[65]陈国友, 杜英秋, 马永华. 应用ICP-MS, AFS, GF-AAS 测定食品中 As、Cd、Hg、Pb 方法的对比研究[J]. 分析化学, 2009, 37(A01): 73-73.
[66]Ögren L, Johansson G. Determination of traces of mercury (II) by inhibition of an enzyme reactor electrode loaded with immobilized urease[J]. Analytica Chimica Acta, 1978, 96(1): 1-11.
[67]Shi R, Stein K, Schwedt G. Determination of mercury (II) traces in drinking water by inhibition of an urease reactor in a flow injection analysis (FIA) system[J]. Fresenius′ journal of analytical chemistry, 1997, 357(6): 752-755.
[68]Bertocchi P, Ciranni E, Compagnone D, et al. Flow injection analysis of mercury (II) in pharmaceuticals based on enzyme inhibition and biosensor detection[J]. Journal of pharmaceutical and biomedical analysis, 1999, 20(1/2): 263-269.
[69]Gunnlaugsson T, Leonard J P, Murray N S. Highly selective colorimetric naked-eye Cu (II) detection using an azobenzene chemosensor[J]. Organic letters, 2004, 6(10): 1 557-1 560.
[70]Tan J, Yan X P. 2, 1, 3-Benzoxadiazole-based selective chromogenic chemosensor for rapid naked-eye detection of Hg2+and Cu2+[J]. Talanta, 2008, 76(1): 9-14.
[71]Ono A, Togashi H. Highly Selective Oligonucleotide-Based Sensor for Mercury (II) in Aqueous Solutions[J]. Angewandte Chemie International Edition, 2004, 43(33): 4 300-4 302.
[72]Mirkin C A, Letsinger R L, Mucic R C, et al. A DNA-based method for rationally assembling nanoparticles into macroscopic materials[J]. 1996,382:607-609.
[73]Lee J S, Han M S, Mirkin C A. Colorimetric Detection of Mercuric Ion (Hg2+) in Aqueous Media using DNA-Functionalized Gold Nanoparticles[J]. Angewandte Chemie, 2007, 119(22): 4 171-4 174.
[74]Wu Y, Zhan S, Xu L, et al. A simple and label-free sensor for mercury (II) detection in aqueous solution by malachite green based on a resonance scattering spectral assay[J]. Chemical Communications, 2011,47:6 027-6 029.
[75]张思相, 王静. 水中重金属在线监测技术探讨[J]. 中国环保产业, 2010(8): 41-43.
[76]孙海林, 李巨峰, 朱媛媛. 我国水质在线监测系统的发展与展望[J]. 中国环保产业, 2009(3): 12-16.
[77]马颢珺, 左航, 白明. 水中重金属在线监测技术发展概述[J]. 环境科学与管理, 2011, 36(8): 130-132.
[78]陈纪灵,王志轩. 燃煤电厂烟气中汞的排放与控制研究进展[J].电力环境保护,2007,23(6):45-47.
[79]武成利,曹晏,董众兵,等. 燃煤电厂烟气汞的监测方法评价[J].环境与健康,2010,27(3):270-271.
[80]杨凯. 固定污染源烟气汞监测技术与设备[M]. 北京:中国电力出版社, 2012.
