甲基肼-水二元体系汽液平衡数据的测定及回归
2014-03-23韩冰高凌云齐鸣斋
韩冰 高凌云 齐鸣斋
华东理工大学化工学院 (上海 200237)
技术进步
甲基肼-水二元体系汽液平衡数据的测定及回归
韩冰 高凌云 齐鸣斋
华东理工大学化工学院 (上海 200237)
采用改进的Ellis汽液平衡釜在常压下测定甲基肼(MMH)-水二元体系的汽液平衡数据。用Herington半经验法对其进行了热力学一致性检验。借助化工流程模拟软件Aspen Plus中的物性数据回归(Data Regression)功能,关联得到实验数据的Wilson和NRTL活度系数方程参数。用两种方程计算得到的汽相组成与实验数据进行比较,平均偏差分别为0.0185、0.0252。结果表明两种模型都可用于化工工程设计。
甲基肼 汽液平衡 活度系数模型
甲基肼(MMH)是航空、航天中所使用的重要推进剂,同时其水溶液也是医药化工、生物化工和农药等领域重要的中间体,日益成为一种很有前景的化工产品[1]。汽液平衡数据是精馏过程开发和设备设计的重要基础数据,也是优化工艺条件,降低能耗和节约成本的重要依据。本实验对甲基肼-水二元体系常压下的汽液平衡数据进行测定,并借助化工流程模拟软件Aspen Plus中的物性数据回归(Data Regression)功能,采用Wilson和NRTL活度系数模型对实验数据进行回归关联,为甲基肼-水二元体系精馏分离的工业设计提供基础数据。
1 汽液平衡数据的测定
1.1 实验试剂及仪器
主要试剂:工业合成甲基肼水溶液;去离子水,华东理工大学化工学院;硫酸,分析纯,含量95.0%~98.0%,上海凌峰化学试剂有限公司。
主要仪器:改进的Ellis汽液平衡釜,华东理工大学;手持式折光仪,广州市普析通仪器有限公司;分度为0.1℃的水银温度计;正反双液封罐。实验装置如图1所示。

图1 汽液平衡实验装置
1.2 实验方法
本实验冷凝器后接正反双液封罐,可在开停釜阶段隔绝釜内甲基肼与外界空气直接接触。从加料口加入配置好的甲基肼-水二元溶液。接通加热电源,调节加热电压为150~200 V,缓慢升温加热至釜液沸腾,此时左侧液封瓶内液位下降,右侧液封瓶内液位上升。分别接通上、下保温电源,其电压调节在20~25 V。调节加热量,使冷凝液控制在每分钟60滴左右。调节上下保温电压,最终使平衡温度趋于稳定,汽相温度控制在比平衡温度高0.5~1℃左右,以防止汽相在上升过程中冷凝回流;当平衡温度稳定约30min后,即可认为其达到平衡状态[2]。记下平衡温度,停止加热,此时左侧液封瓶中液位上升,右侧液封瓶中液位下降。用注射器分别吸取液相和汽相冷凝液样品,甲基肼-水溶液中甲基肼质量分数在70%以下的采用折光仪分析汽液两相组成[3],质量分数在70%以上的汽液两相组成采用酸碱滴定的方法进行分析[4]。
1.3 实验测定数据
在常压下,测定的甲基肼(1)-水(2)二元物系的汽液平衡数据见表1,甲基肼(1)-水(2)二元汽液平衡相图见图1。
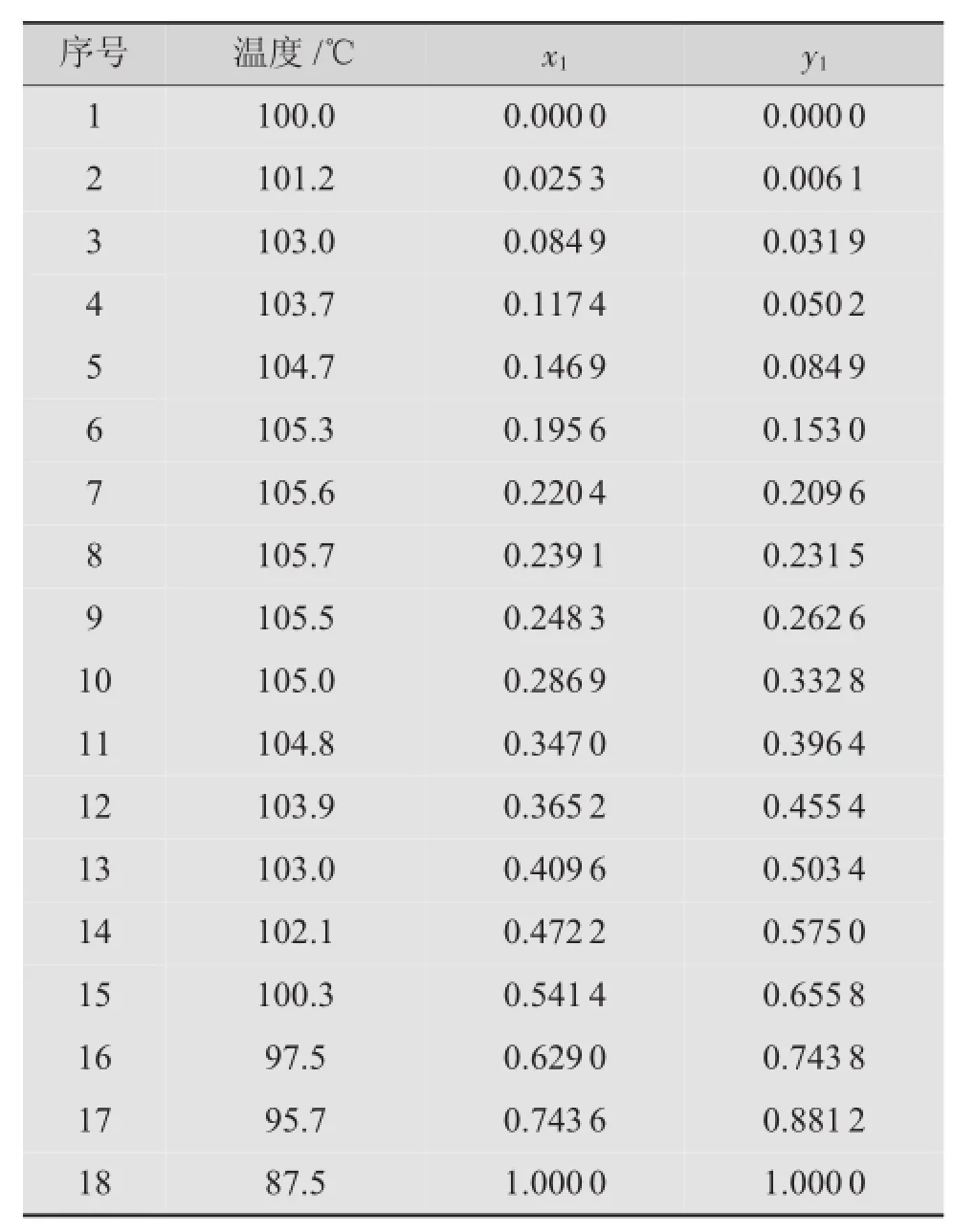
表1 常压下甲基肼(1)-水(2)二元物系的汽液平衡数据

图1 常压下甲基肼-水二元物系的汽液平衡相图
1.4 汽液平衡数据热力学一致性检验
表1数据为等压汽液相平衡数据,因此采用Herington推荐的半经验方法对其进行热力学一致性检验[5]。甲基肼-水物系的ln(γ2/γ1)~x1关系见表2,其中γ1、γ2分别为甲基肼、水的液相活度系数。

表2 甲基肼-水物系ln穴γ2/γ1)~χ1关系
为了方便计算积分值(即面积),将ln(γ2/γ1)拟合为x1的三次多项式,即:

进而计算出D值和J值,其中[6]:
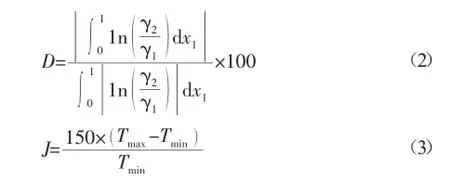
其中Tmax,Tmin分别为体系的最高、最低沸点。
由式(2)、(3)计算得到D=25.80,J=31.20,因为(D-J)=-5.4<10,根据Herington规则,本实验汽液相平衡数据符合热力学一致性检验。
2 活度系数法关联汽液平衡数据
2.1 汽液平衡基本方程
在常压下,甲基肼-水二元体系的汽相可视为理想气体,液相采用活度系数法计算液相逸度,相平衡公式为:

其中yi、xi分别为组分i的汽液相组成,γi为液相活度系数,p为总压,psi为饱和蒸汽压,可由Antoine方程计算,其公式为:

式中ps单位为kPa,T单位为K。
甲基肼和水的Antoine常数[7-8]见表3。
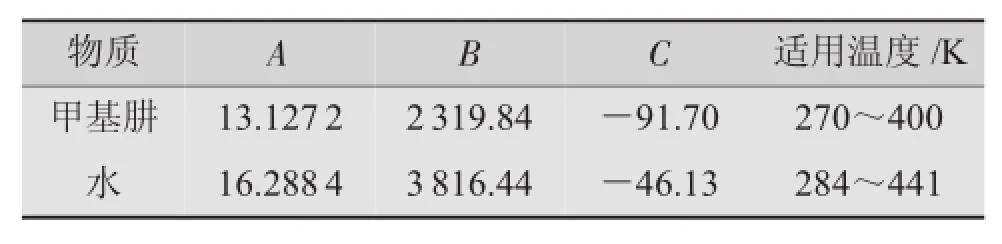
表3 甲基肼和水的Antoine常数值
2.2 Wilson液相活度系数方程与参数回归
Wilson液相活度系数方程基于溶液局部组成概念,其二元体系的Wilson活度系数方程为[9]:

式中:Λ12,Λ21为Wilson液相活度系数方程参数;a,b为回归参数;λ12-λ11,λ21-λ22为二元交互作用能量参数。
实验数据经Aspen Plus软件回归,可得回归参数a,b,见表4。

表4 Wilson模型回归参数
2.3 NRTL液相活度系数方程与参数回归
NRTL方程全称为非随机双液相活度系数方程。它也采用局部组成概念,避免了Wilson方程无法应用于液液相平衡的缺陷。该方程应用十分广泛,能够成功预计多种极性物系的相平衡,二元体系的NRTL活度系数方程为[9]:

α12=α21=0.3为模型参数;c、d为回归参数;τ12,τ21为二元交互作用能量参数。实验数据经Aspen Plus软件回归,可得回归参数c、d,见表5。

表5 NRTL模型回归参数
2.4 Wilson和NRTL模型方程关联误差对比
根据汽液平衡方程,自编matlab程序计算出汽相组成yi,并与实验数据进行比较,见表6。

表6 Wilson和NRTL模型方程关联误差对比
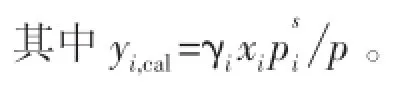
对于甲基肼-水二元体系,由表5数据可计算Wilson和NRTL模型方程关联结果对甲基肼组分的偏差,见表7。
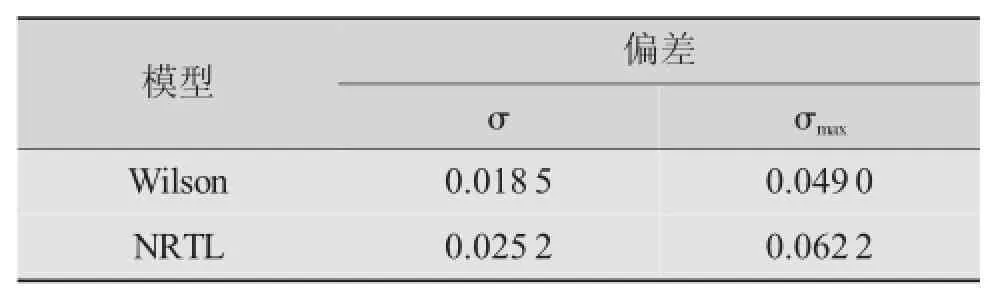
表7 Wilson和NRTL模型方程关联结果偏差

由表7可知,Wilson和NRTL模型拟合结果均能满足该体系的汽液相平衡计算。
3 结论
(1)用改进型Ellis汽液平衡釜在常压下测定甲基肼-水二元体系的汽液平衡数据,经Herington推荐的半经验方法检验,该组汽液相平衡数据满足热力学一致性。
(2)通过对Wilson和NRTL模型方程关联结果偏差进行分析,Wilson和NRTL模型拟合结果均能满足该体系的汽液相平衡计算,为相关工程计算提供了可靠的汽液相平衡数据。
[1]曹广宏.一甲基肼的性质、合成和应用[J].湖北化工, 1993(4):22-25.
[2]乐清华.化学工程与工艺专业实验[M].北京:化学工业出版社,2008.
[3]米镇涛,李德庆,邱立勤.液体推进剂一甲肼与水二元物系汽液相平衡的研究[J].推进技术,1998,19(2): 72-75.
[4]王丽,李春燕,周岩.甲基肼溶液含量的测定方法[J].沈阳化工,1999,28(2):50-52.
[5]冯新,宣爱国,周彩荣.化工热力学[M].北京:化学工业出版社,2009.
[6]季伟,齐鸣斋.减压下N,N-二甲基乙酰胺-水二元汽液平衡数据的测定与关联[J].徐州工程学院学报(自然科学版),2013,28(3):37-41.
[7]M Ferriol,A Laachach,M TCohen-Adad,etal.Vapor-liquid equilibria in the binary systemswater-methylhydrazine and water-1,1-dimethylhydrazine.Thermodynamicmodeling in relation to the structure of the liquid phase[J].Fluid Phase Equilibria,1992,71(3):287-299.
[8]《化学工程手册》编辑委员会.化学工程手册(第1篇)——化工基础数据[M].北京:化学工业出版社,1980.
[9]HenriRenon,JM Prausnitz.Local compositions in thermodynamic excess functions for liquid mixtures[J].AIChE Journal,1968,14(1):135-144.
Measurement and Regression of Vapor-liquid Equilibrium Data for Methylhydrazine-water Binary System
Han Bing Gao Lingyun QiMingzhai
The vapor-liquid equilibrium(VLE)data ofmethylhydrazine-water binary system were determined at normal pressure with an improved Ellis VLE caldron.The thermodynamic consistency testwas conducted for the data by Herington semi-empirical method.By virtue of the data regression function of Aspen Plus,a software for chemical process simulation,the VLE datawere correlated and the binary interaction parameters ofWilson and NRTL activity coefficient equations were obtained.The vapor compositions calculated with the two equations were compared with corresponding experimental data,and the average deviations were 0.018 5 and 0.025 2 respectively.The result indicated that the Wilson model and NRTLmodel could be used for relevant chemical engineering design.
Methylhydrazine;Vapor-liquid equilibrium;Activity coefficientmodel
TQ 226.5+2
2013年11月
韩冰 男 1989年生 硕士研究生 主要从事化工分离与模拟
