壳聚糖水热交联炭材料研究
2014-03-18张文龙马儒超周志伟韩琪胜
张文龙 马儒超 周志伟 韩琪胜
(东华理工大学,江西 南昌 330013)
1 壳聚糖
壳聚糖(Chitosan, CTS)又称为聚葡萄糖胺(1-4)-2-氨基-B-D葡萄糖,是一种天然高分子化合物,由甲壳素经脱乙酰处理制备而成。壳聚糖是目前为止唯一发现的天然碱性多糖,具有线性共聚高分子的材料结构,其链上氨基、羟基能交联形成具有类似网状结构的笼形分子对金属离子起稳定的配位作用[1]。壳聚糖因氨基易质子化而溶于酸性溶液,一般实际应用中需经过改性和交联来改变材料的溶解性,制备出耐酸碱的材料[2]。
通过交联的方法可以使壳聚糖具有许多优点,如可以制备具有不同结构形状的吸附材料(凝胶,微球,膜,纤维等)并能改变其机械强度,可以在酸性,碱性或有机溶剂中使用,具有耐高温性。交联壳聚糖在吸附过程中还有以下优势:(1)吸附速度更快,由于交联壳聚糖有较好的溶胀性能,吸附网络扩张后利于金属离在材料内部的扩散。(2)交联壳聚糖易于改性接枝,可通过在表面接枝不同的官能团提升吸附性能。(3)交联壳聚糖的吸附行为受溶液pH值的影响较小,适用于低放废液苛刻的酸性环境。但是,随着壳聚糖交联度的增加,吸附容量会相应减少,在高交联度的情况下其溶胀性能大幅下降并阻碍整个吸附过程,交联剂的使用在整个工艺中尤为重要。
Pang[3]采用壳聚糖包覆凹凸棒石复合材料研究其对溶液中铀酰离子的去除效果,实验表明吸附行为符合准二级动力学模型,吸附容量有所提升,壳聚糖对吸附过程有促进效果。
Wang[4]以戊二醛为交联剂制得丝氨酸改性的壳聚糖树脂并研究其吸附性能,实验结果表明材料具有90%左右的去除率和55.9 mg/g的吸附容量,重复利用4次以上仍不影响其吸附性能。
Liu[5]分别用乙二醇二缩水甘油醚、环氧氯丙烷和戊二醛为交联剂制备交联壳聚糖并研究其对溶液中铀酰离子吸附机理,详细比较了三者的吸附容量,建立相关吸附模型。结果表明不同交联剂的选用会对吸附容量产生较大影响,吸附行为均为自发的吸热反应。
Liu[6]采用离子印记技术制备了聚乙烯醇/壳聚糖水凝胶材料并研究了其对铀酰离子的吸附效果和选择性,实验结果表明最佳吸附pH值在5.0-6.0之间,吸附饱和容量能达到156 mg/g,证实离子印迹法能提高材料对铀酰离子的吸附选择性,相对选择系数较原材料有较大提高。
Atia[7]研究了改性壳聚糖树脂对铀的吸附行为后对吸附机理进行了深入研究,结论认为氨基在吸附行为中起重要作用,提出吸附模型如图1所示。
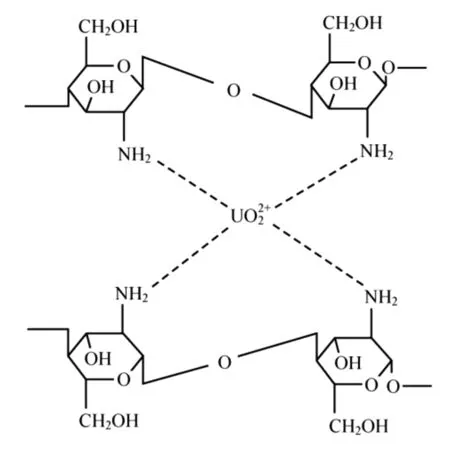
图1 壳聚糖螯合铀酰离子示意图Fig.1 Chitosan chelating uranyl ion diagram
2 水热法
水热(Hydrothermal)一词起源于地质学。水热法通过模拟自然界的成矿环境进行水热合成反应,多用于水热炭化和水热晶化过程[8]。
与其他材料制备方法相比,水热制备技术具有如下特点:(1)水热法在密闭容器中进行,反应氛围可控,能形成特定的氧化还原条件。(2)水热法使用相对较低的反应温度,反应条件温和操作简便。(3)水热体系中发生的化学反应具有更快的反应速率。在水热条件下,体系存在温度梯度,溶液具有较低的黏度和较大的密度变化,溶液快速对流,溶质传输更为有效,化学反应能快速进行。(4)水热法可通过脱水与聚合作用通过生物质得到炭化材料[9]。
水热法制备生物质炭最初的目的是为了模拟自然界形成煤炭的过程,后来人们发现水热法制备炭材料有着种种的优势,如水热炭化法的条件在水溶液的环境下进行,省去预干燥过程;水热反应中生物质脱水会释放出1/3的燃烧能具有高能效的特点;水热过程中水介质的气氛有利于炭化材料表面形成含氧官能团,炭化后的产物一般都含有较多表面官能团;水热炭化法要求的设备简单,操作又简便而且具有较高的产率等。
Cui[10]采用淀粉为原料[Fe(NH4)2(SO4)2]为活化剂,溶剂pH为4水热温度为200oC的条件下反应12小时,制得的炭球比表面积为113.8 m2/g 。研究表明水热过程促进淀粉水解为葡萄糖,葡萄糖的炭链断裂并脱水缩合最终形成炭微球。表征结果显示水热炭球含丰富的官能团。
Guiotoku[11]用松木屑以及 α纤维素作为原材料料,采用微波炭化法与水热炭化法联用制备出生物质炭。生物质材料在微波炭化以及柠檬酸作为催化的条件下,在温度为200oC以及弱酸性水作为介质参与了炭化反应。微波在反应时起到了辅助催化和加热的作用。
Liu[12]采用水热法制备生物质炭为原料制备了羧基化水热炭,研究了材料对溶液中铀酰离子的吸附行为,实验证明羧基化水热炭有良好的吸附效果,吸附容量能达到205 mg/g,成本低廉处理工艺简单。
Geng[13]采用水热法制备炭微球并用酰氨肟进行接枝提高其对铀酰离子的选择性能,表征结果证实接枝成功,制备出的接枝水热炭微球对溶液中铀酰离子的选择性提升,在溶液最佳pH下吸附能力提高至214 mg/g 。葡萄糖水热过程如图2所示。

图2 葡萄糖水热过程Fig.2 Hydrothermal carbonization for glocose
Chen[14]以葡萄糖为原料采用低温水热法制备了炭微球并对其进行氧化,表征结果证实氧化后水热炭微球的官能团量有较大提升。文中详细比较了以淀粉、蔗糖和葡萄糖为原料制备炭微球的羧基含量,得出含羧基量葡萄糖水热炭微球>蔗糖水热炭微球>淀粉水热炭微球。实验采用SEM表征葡萄糖水热炭微球的微观结构如图3所示。

图3 葡萄糖水热炭微球SEM图Fig.3 Hydrothermal carbonization for glocose
3 壳聚糖水热炭简介
壳聚糖拥有可降解性、能产生絮凝作用和无毒无污染等特性,被广泛应用于医学,水处理和食品领域。Yang以壳聚糖为原料采用水热交联的方式一步法制备出自带氨基的炭纳米材料,提出壳聚糖水热炭纳米粒子的制备流程如图4。表征证实水热后炭材料中仍含有氨基且无细胞毒性。
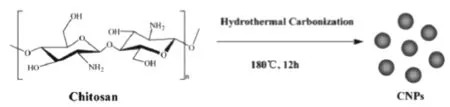
图4 壳聚糖水热炭纳米材料制备流程Fig.4 A schematic illustration of the prepration procedure of CNPs by hydrothermal carbonization of chitosan
Nie制备了壳聚糖水热炭材料并将其实际应用于含铀废水的处理,吸附实验表明材料有高吸附容量,较好的耐酸性,研究水热时间和水热温度对材料酸溶性和吸附容量的影响,结果证实时间越长温度越高材料耐酸性就越强,但吸附容量则与之成反比。壳聚糖水热炭水热时间与温度对耐酸性的影响如图5所示。提出壳聚糖水热交联主要为类似糖类物质的羟基间脱水缩合,如图6所示。

图5 不同水热时间和水热温度对壳聚糖的酸溶率影响Fig.5 The acid soluble rate of chitosan of different hydrothermal time and temperature

图6 壳聚糖水热缩合示意图Fig.6 Chitosan hydrothermal carbon connection diagram
壳聚糖水热炭的静态实验表明整个吸附过程为单分子层的化学吸附,吸附行为是自发吸热的,提升铀酰离子初始浓度有助于提高吸附容量。壳聚糖通过水热法交联后比化学交联法的吸附容量更大,效果更好。
[1]蒋挺大.壳聚糖金属配合物的催化作用研究进展[J].化学通报,1996(1):22-27.
[2]蒋挺大,甘友新,张春萍.交联壳聚糖对氨基酸的吸附性能[J].1994.
[3]Pang C, Liu Y, Cao X, et al. Adsorptive removal of uranium from aqueous solution using chitosan-coated attapulgite[J]. Journal of radioanalytical and nuclear chemistry,2010,286(1):185-193.
[4]王彩霞,刘云海,黄德娟,等.丝氨酸改性壳聚糖的合成及其对铀的吸附研究[J].化学研究与应用, 2009,21(10):1361-1364.
[5]Liu Y, Liu Y, Cao X, et al. Biosorption studies of uranium (VI) on cross-linked chitosan: isotherm, kinetic and thermodynamic aspects[J].Journal of Radioanalytical and Nuclear Chemistry,2011,290(2):231-239.
[6]Liu Y, Cao X, Hua R, et al. Selective adsorption of uranyl ion on ion-imprinted chitosan/PVA cross-linked hydrogel[J].Hydrometallurgy,2010,104(2):150-155.
[7]Atia A A. Studies on the interaction of mercury (II) and uranyl (II) with modified chitosan resins[J].Hydrometallurgy,2005,80(1):13-22.
[8]高英,石韬,汪君,等.生物质水热技术研究现状及发展[J].可再生能源,2011,29(4):77-83.
[9]伍超文,吴诗勇,彭文才,等.不同气氛下的纤维素水热液化过程[J].华东理工大学学报:自然科学版, 2011,37(4):430-434.
[10]CUI Xian-jin,ANTONIETII M,YU Shu—hang.Structural e~cts of iron oxide nanoparticles and iron ions on the hydrothermal carbonization of starch and rice carbohydrates[J].Small,2006,2(6):756—759.
[11]GUIOTOKU M,RAMBO C R,HANSEL F A,et a1.Microwave—assisted hydrothermal carbonization of lignocelhlosic materials[J].Materials Letters,2009,63(30):2707—2709.
[12]Liu Y H, Wang Y Q, Zhang Z B, et al. Removal of uranium from aqueous solution by a low cost and high-efficient adsorbent[J].Applied Surface Science,2013.
[13]Geng J, Ma L, Wang H, et al. Amidoxime-Grafted Hydrothermal Carbon Microspheres for Highly Selective Separation of Uranium[J].Journal of Nanoscience and Nanotechnology,2012,12(9):7354-7363.
[14]Chen Z, Ma L, Li S, et al. Simple approach to carboxyl-rich materials through low-temperature heat treatment of hydrothermal carbon in air[J].Applied Surface Science, 2011,257(20):8686-8691.
