橙酮类化合物合成研究进展
2014-03-10陈启绪
陈启绪
(浙江工业大学药学院,浙江 杭州 310014)
橙酮化合物(Aurones,2),可看作为取代的苯并呋喃酮衍生物,是黄酮的同分异构体,同时也是一类稀有类黄酮化合物[1]。橙酮类化合物具有广泛的生物活性,医学方面如抗肿瘤、抗氧化、抗微生物、抗肥胖等活性[2];在农用方面有拒食、除草等活性[3]。橙酮类化合物多存在于植物中,且含量不高,所以在对橙酮类化合物进行研究时,亟待需要一些化学方法对其进行合成。
1 合成路线
橙酮的合成有生物合成和化学合成两种方式,生物合成方法需要相应的生物酶[4],且底物受到很大的限制[5],因此主要是通过化学合成方法来进行合成,下面介绍一些化学合成方法。
1.1 通过2’-羟基查尔酮氧化环合
2’-羟基查尔酮衍生物可以直接在Hg(OAc)2[6]、硝酸铊(III)(TNN)[7]的催化体系下氧化环合成相应的橙酮(Scheme 1)。该方法的优点:原料易于制备、催化体系简单、操作简便;缺点:催化剂用量太大(≥1 equiv)、底物有一定结构限制,如硝酸铊(III) 催化体系中2’-羟基查尔酮衍生物中羟基的对位需要有甲氧基取代。

Scheme 1
Khan 等[8]在2001 年报道了以2’-乙酰氧查尔酮(3)为原料分两步高产率合成橙酮类化合物。首先,2’-乙酰氧查尔酮(3)在正四丁基三溴化胺(TBATB)和碳酸钙的条件下,发生溴代反应生成溴代的查尔酮(4)。然后,溴代产物在强碱氢氧化钾的催化下,发生环合生成橙酮类化合物(Scheme 2)。该方法的产率较高,总产率在60%~72%,溶剂较常见,但步骤较多,较繁琐。
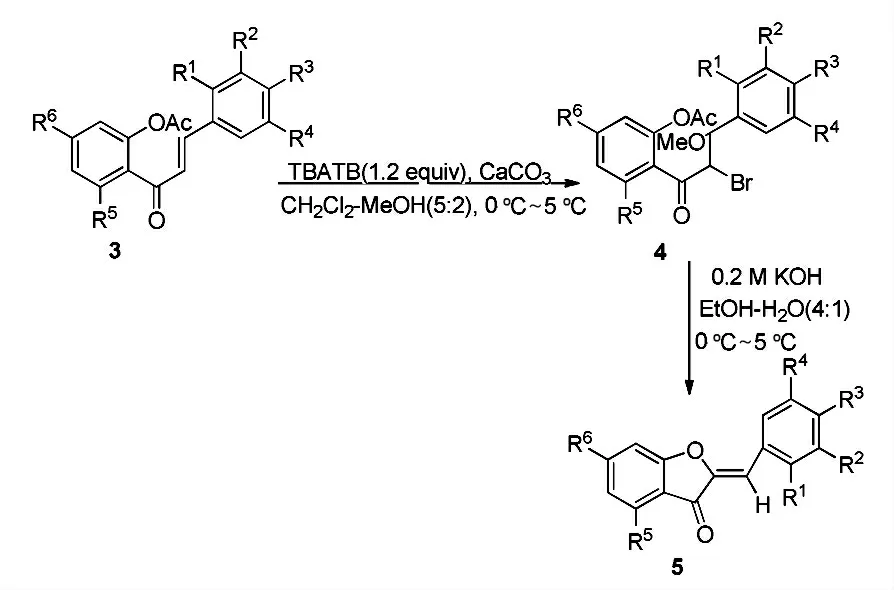
Scheme 2
1.2 经由3(2H)-苯并呋喃酮为关键中间体
Zhou 等[9]在2010 年报道了1,4-二甲氧基苯(7)在无水氯化铝催化下,与氯乙酰氯发生Friedel-Crafts 反应生成化合物8;化合物8 在碱性条件下发生环合反应,生成3(2H)-苯并呋喃酮类化合物(9)。然后,与苯甲醛类化合物在酸催化下进行羟醛缩合生成橙酮类化合物(10)(Scheme 3)。
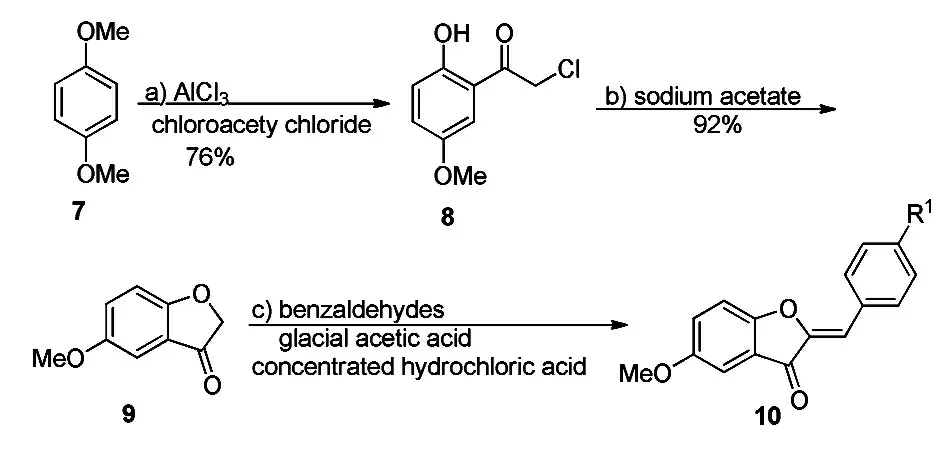
Scheme 3
Qing 等[10]在2003 年报道了1,3-苯二酚(11)在ZnCl2催化下,与氯乙腈发生反应,接着通入HCl 气体进行水解反应生成化合物12;化合物12 在碱性条件下发生环合反应,生成3(2H)-苯并呋喃酮类化合物(13)。然后,与苯甲醛类化合物在碱的催化下进行羟醛缩合生成橙酮类化合物(14)(Scheme 4)。

Scheme 4
Varma 等[11]在1992 年报道了3(2H)-苯并呋喃酮与苯甲醛在温和的氧化铝催化下进行羟醛缩合生成橙酮类化合物(Scheme 5)。

Scheme 5
经由3(2H)-苯并呋喃酮为中间体合成橙酮类化合物,3(2H)-苯并呋喃酮类化合物与取代的苯甲醛在酸、碱或氧化铝催化条件下进行羟醛缩合生成橙酮类化合物。在实际合成中,大部分都是通过该方法合成的,但该方法中3(2H)-苯并呋喃酮的合成实验条件比较苛刻,同时一些底物的反应产率较低。
1.3 通过过渡金属催化合成
Li 等[12]在2009 年报道了一种高效的末端炔16(4 equiv)与水杨醛(15)(1 equiv)的炔基化环合反应,以Cy3P-银复合物为催化剂在水溶液中生成的为(Z)-2,3-二氢苯并呋喃-3-醇衍生物(17);而以Cy3PAgCl 复合物为催化剂,生成的为(E)-2,3-二氢苯并呋喃-3-醇衍生物(18),产物的立体构型Z/E 主要由银复合物中的阴离子所调控的,生成的产物不必纯化,可直接用MnO2进行氧化生成相应的橙酮(Scheme 6)。用该方法可以分别获得(Z)-橙酮和(E)-橙酮,有立体选择性。

Scheme 6
Jong 等[13]在1990 年报道了水杨醛与苯乙炔化合物在试剂正丁基锂的条件下,发生炔化反应,接着进行氧化,生成中间体22,然后该中间体在硝酸银的甲醇溶液下生成相应环合产物,其中橙酮为主产物和极少量的黄酮(Scheme 7)。

Scheme 7
通过以2-(1-羟基-3-苯基-2-炔基)苯酚类化合物为关键中间体进行合成,取代的水杨醛和苯乙炔类化合物在低温条件下,发生炔化反应生成中间体2-(1-羟基-3-苯基-2-炔基) 苯酚类化合物(Scheme 8)。Pale 等[14]在2008 年报道了2-(1-羟基-3-苯基-2-炔基) 苯酚类化合物可在Au-Cl 催化下环合,然后环合产物在二氧化锰的氧化下,氧化成目标产物橙酮(Scheme 8)。Yao 等[15]在2010 年报道了2-(1-羟基-3-苯基-2-炔基) 苯酚类化合物可在碳黑负载银纳米材料催化下环合,然后环合产物进行氧化,可得到目标产物橙酮(Scheme 9)。

Scheme 8

Scheme 9
通过过渡金属催化方法制备目标产物,过渡金属催化体系的多样性,极大地扩大了底物的适用性,丰富了橙酮的合成方法;有些催化体系有特定的选择性,能够合成单一立体构型的橙酮。但有些反应产物中有副产物黄酮的生成;有的原料制备条件较苛刻;也有的原料易得、产率较高且无副产物产生,但用到了昂贵的Au 或Ag 复合物做催化剂。
2 小结
综上所述,橙酮类化合物具有多种多样的生物活性,无论是在医学研究还是农用方面,具有很高的潜在应用价值。目前橙酮类化合物的生物活性受到国内外许多学者的关注,因而开发一种有效的合成方法,对其活性成分进行深入研究,具有重要的意义。
[1]张培成.黄酮化学[M].北京:化学工业出版社,2008,1:1-77.
[2]Haudecoeur R,Boumendjel A.Recent advances in the medicinal chemistry of aurones[J].Curr.Med.Chem.,2012,19:2861-2875.
[3]Morimoto M,Fukumoto H,Nozoe T,et al.Synthesis and insect antifeedant activity of aurones against spodoptera litura larvae[J].J.Agric.Food Chem.,2007,55:700-705.
[4]Li X C,Cai L,Wu C D.Antimicrobial compounds from Ceanothus americanus against oral pathogens [J].Phyto chemistry,1997,46(1):97-102.
[5]Nakayama T,Yonekura-Sakakibara K,Sato T,et al.Aureusidin synthase:a polyphenol oxidase homolog responsible for flower coloration[J].Science,2000,290(5494):1163-1166.
[6]Patel A K,Patel N H,Patel M A,et al.Synthesis of some 3-(4-aryl-benzofuro [3,2-b]pyridin-2-yl)coumarins and their antimicrobial screening[J].J.Heterocyclic Chem.,2012,49:504-510.
[7]Thakkar K,Cushman M.A novel oxidative cyclization of 2'-hydroxychalcones to 4,5-dialkoxyaurones by thallium(III) nitrate[J].J.Org.Chem.,1995,60:6499-6510.
[8]Bose G,Mondal E,Khan A T,et al.An environmentally benign synthesis of aurones and flavones from 2'-acetoxychalcones using n-tetrabutylammonium tribromide [J].Te trahedron Lett.,2001,42:8907-8909.
[9]Cheng H,Zheng L,Liu Y,et al.Design,synthesis and discovery of 5-hydroxyaurone derivatives as growth inhibitors against HUVEC and some cancer cell lines[J].Eur.J.Med.Chem.,2010,45:5950-5957.
[10]Zheng X,Cao J G,Meng W D,et.al.Synthesis and anticancer effect of B-ring trifluoromethylated flavonoids[J].Bioorg.Med.Chem.Lett.,2003,13:3423-3427.
[11]Varma R S,Varma M.Alumina-mediated condensation.A simple synthesis of aurones[J].Tetrahedron Lett.,1992,33:5937-5940.
[12]Yu M,Skouta R,Zhou L,et.al.Water-triggered,counteranion-controlled,and silver-phosphines complex-catalyzed stereoselective cascade alkynylation/cyclization of terminal alkynes with salicylaldehydes[J].J.Org.Chem.,2009,74:3378-3383.
[13]Jong T T,Leu S J J.Intramolecular cyclization catalyzed by silver(I) ion;a convenient synthesis of aurones[J].J.Chem.Soc.Perkin Trans.1.,1990,423-424.
[14]Harkat H,Blanc A,Weibel J M,et al.Versatile and expeditious synthesis of aurones via AuI-catalyzed cyclization[J].J.Org.Chem.,2008,73:1620-1623.
[15]Yu M,Lin M D,Han C Y,et al.Ligand-promoted reaction on silver nanoparticles:phosphine -promoted,silver nanoparticle-catalyzed cyclization of 2-(1-hydroxy-3-arylprop-2-ynyl)phenols[J].Tetrahedron Lett.,2010,51:6722-6725.
