吲哚美辛预防ERCP术后胰腺炎的Meta分析
2014-03-08于久飞
黄 坤,于久飞
(民航总医院消化内科,北京100123)
内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatograph,ERCP)近年来已被广泛应用于肝胆胰疾病的诊断与治疗,但同时也带来一系列并发症,包括胆道感染、出血、穿孔、高淀粉酶血症和急性胰腺炎等[1],而其中ERCP术后胰腺炎(post-ERCP pancreatitis,PEP)是最常见也是最为凶险的并发症,其发生率可达2%~15%[1-3]。PEP的发生不仅加重患者的身心痛苦,还大大增加了患者的住院时间与住院费用,同时也是困扰广大临床医生已久的难题。PEP的发病机制目前尚未明确,研究发现可能与感染、十二指肠乳头的痉挛、机械性及化学性损伤等因素导致的胰酶激活,及其继发的一系列炎性反应有关。为了减少PEP的发病率,国内外学者们进行了大量的研究,研究显示胰酶抑制剂、生长抑素类制剂、肝素、皮质类固醇及抗菌药物等多种药物对于预防PEP有一定的疗效[4],但是上述药物存在诸如费用高、不良反应较大等问题而影响其应用的推广。近年来,吲哚美辛在PEP预防中的作用逐渐引起了人们关注,吲哚美辛不仅应用方便,价格也低廉,易于推广,但应用吲哚美辛预防PEP的疗效尚无定论。本研究旨在通过荟萃分析的方法对吲哚美辛预防PEP作用进行系统评价。
1 资料与方法
1.1 文献检索 计算机检索Cochrane图书馆(1970年1月至2013年6月)、Pubmed(1966年1月至2013年6月)、EMBASE(1966年1月至2013年6月)和中国生物医学文献资料库(1978年1月至2013年6月)中收录的文献。英文检索关键词:post-ERCP pancreatitis、indomethacin;中文检索关键词:ERCP术后胰腺炎、吲哚美辛。纳入标准:(1)公开发表的文献;(2)采用盲法、前瞻性、随机对照研究,干预组仅预防性使用吲哚美辛,并设接受安慰剂或空白对照组;(3)试验有明确的纳入、排除标准;(4)有明确的PEP诊断标准。排除标准:(1)非盲法、前瞻性、随机对照研究;(2)非预防性使用吲哚美辛;(3)无明确的纳入或排除标准;(4)综述、专门的不良反应报道及药理学、药代动力学等非临床试验研究。
1.2 方法
1.2.1 文献质量评价 文献的筛选由2名研究者独立完成,首先阅读文献的题目,选取符合标准的题目继续阅读文献摘要以及全文。最后两位研究者进行交叉评价,如遇意见不统一等情况,则请第三者进行评判。并采用Jadad量表[5](0~2分为低质量,3~5分为高质量)评价纳入论文的质量。
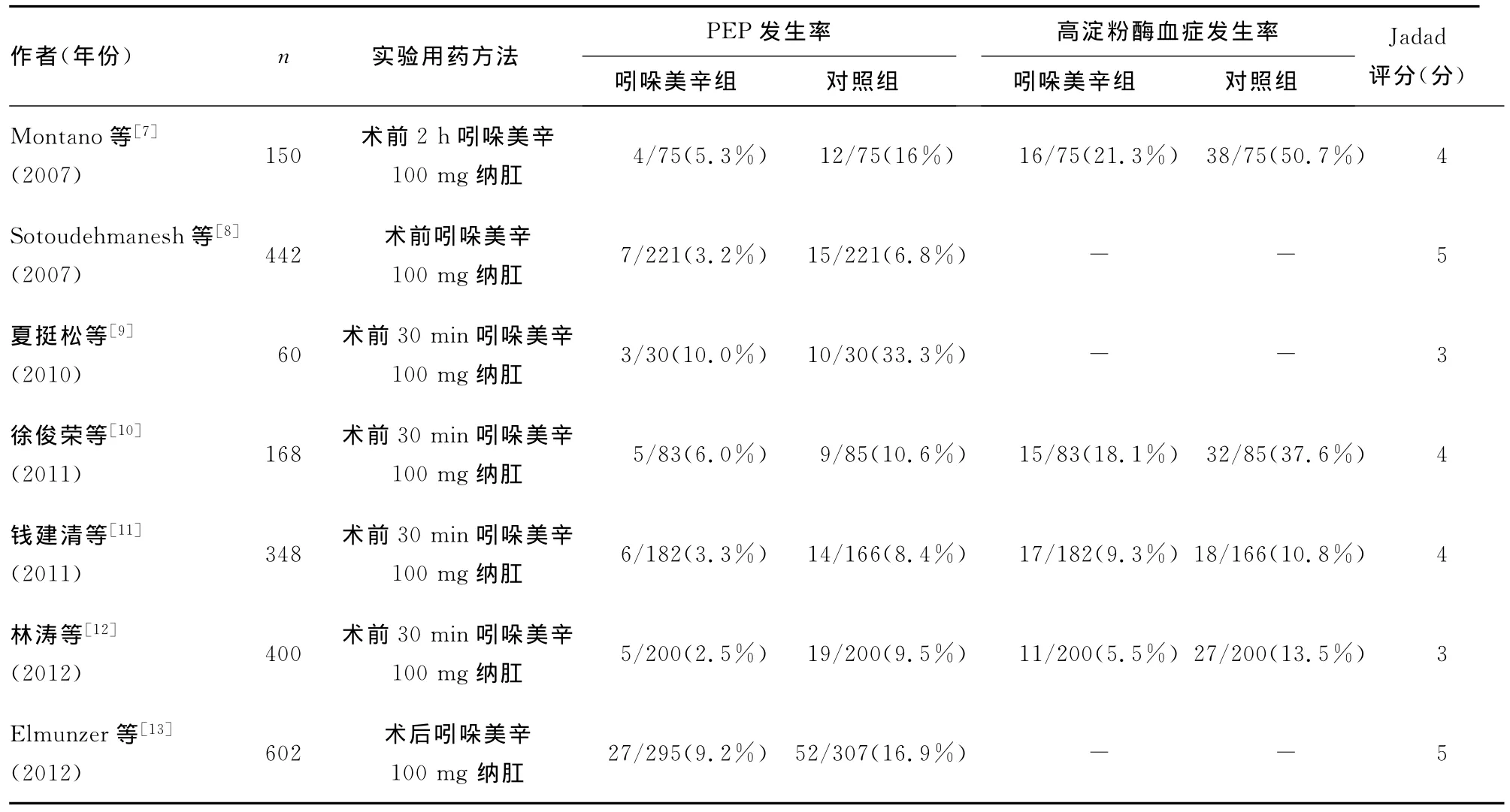
表1 吲哚美辛预防PEP相关文献质量评价

图1 吲哚美辛组与对照组PEP发生率的比较
1.2.2 观察指标 观察指标包括吲哚美辛组与安慰剂/对照组的PEP发生率,轻、中、重度PEP发生率和ERCP术后高淀粉酶血症发生率,同时包括对不良反应、并发症及死亡病例的报道。PEP的定义采用1991年Cotton等[6]建议的诊断标准:ERCP术后当患者有持续24h以上的腹痛,同时伴有血淀粉酶超过正常上限3倍以上可诊断PEP。严重程度分级:轻度,临床胰腺炎,术后患者住院时间持续3d以内;中度,住院时间为4~10d;重度,住院时间持续10d以上。ERCP术后高淀粉酶血症定义为ERCP术后24h血清淀粉酶超过正常范围上限时,并无其他PEP的症状(腹痛等),定义为ERCP术后高淀粉酶血症。
1.3 统计学处理 采用Cochrane图书馆提供的RevMan 5.2软件进行统计学分析,结果采用二分类变量计算相对风险系数(RR)值及95%可信区间(CI)表示。评价文献的统计学异质性采用χ2检验,如文献异质性差异无统计学意义(P>0.05),采用固定效应模型;如果文献异质性差异有统计学意义(P<0.05),则进行敏感性分析找出异质性原因,并采用随机效应模型。
2 结 果
2.1 资料数量和质量评价 根据主题词共检得英文文献17篇,中文文献4篇。通过剔除重复文献及非临床试验研究、或研究目的不相符的文献,最后共有7篇文献[7-13]入选,3篇英文文献及4篇中文文献,文献特征及质量评价,见表1。各文献纳入患者的年龄、性别等的差异在该文献内差异均无统计学意义(P>0.05)。
2.2 PEP发生率比较 入选总例数2 170例,其中吲哚美辛组1 086例,57例发生PEP,对照组1 084例,131例发生PEP,两组PEP发生率分别为5.2%和12.1%。纳入的7篇文献行异质性检验,差异无统计学意义(P>0.05),故采用固定效应模型。Meta分析两组患者PEP发生率差异有统计学意义(P<0.05),合并RR=0.45,95%CI:0.33~0.60,见图1。
2.3 PEP的严重程度分析 7项研究中有6项[7-10,12-13]研究对PEP的严重程度进行了描述,其中4项研究[8-9,12-13]中发生了中、重度的胰腺炎。总例数1 822例,吲哚美辛组904例,13例发生中、重度PEP,对照组918例,38例发生中、重度PEP,两组中、重度PEP发生率分别为1.4%和4.1%,见表2。行异质性检验,结果差异无统计学意义(P>0.05),采用固定效应模型,Meta分析两组患者中、重度PEP发生率差异有统计学意义(P<0.05),合并RR=0.43,95%CI:0.23~0.78,见图2。
2.4 ERCP术后高淀粉酶血症的发生率比较 纳入的7项研究中有4项研究[7,10-12]描述了ERCP术后高淀粉酶血症发生情况(表1),入选总例数1 066例,其中吲哚美辛组540例,59例发生高淀粉酶血症,对照组526例,115例发生高淀粉酶血症,两组ERCP术后高淀粉酶血症的发生率分别为10.9%和21.9%。纳入的4篇文献行异质性检验,差异无统计学意义(P>0.05),故亦采用固定效应模型。Meta分析两组患者ERCP术后高淀粉酶血症发生率差异有统计学意义(P<0.05),位于无效线左侧,合并RR=0.51,95%CI:0.37~0.70,见图3。
2.5 不同用药时间的亚组分析 7项研究中4项[9-12]于ERCP术前30min应用吲哚美辛100mg纳肛,总例数976例,吲哚美辛组495例,19例发生PEP,对照组481例,52例发生PEP,行异质性检验,差异无统计学意义(P>0.05),Meta分析两组患者PEP发生率差异有统计学意义(P<0.05),合并RR=0.36,95%CI:0.22~0.61,如图4。

表2 吲哚美辛组与对照组中/重度PEP发生率
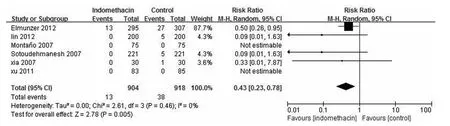
图2 吲哚美辛组与对照组发生中/重PEP的比较

图3 吲哚美辛组与对照组ERCP术后高淀粉酶血症发生率的比较

图4 吲哚美辛组与对照组PEP发生率的比较
2.6 不良反应及并发症发生率分析 7篇文献中有4篇[7-8,11,13]对研究的不良反应及并发症情况进行了描述,3篇[7-8,11]报道无不良反应及并发症的发生。Elmunzer等[13]报道了11例消化道出血病例,其中吲哚美辛组4例,对照组7例,两组间差异无统计学意义(P>0.05)。另外还有2例急性肾衰竭病例的报道,均发生于对照组。纳入的所有研究中无死亡病例报道。
3 讨 论
ERCP术后高胰淀粉酶血症、PEP是ERCP术后常见并发症,预防上述并发症除了要求内镜操作医师的技术熟练之外,预防性应用药物治疗也显得越来越重要。吲哚美辛作为非甾体类解热镇痛抗感染药,其机制是通过对环氧酶的抑制而减少前列腺素的合成,制止炎症组织痛觉神经冲动的形成,抑制炎性反应,包括抑制白细胞的趋化性及溶酶体酶的释放等。近年研究发现,围术期应用吲哚美辛可能会预防PEP的发生[14-15]。由于吲哚美辛具有价格低廉、应用简便等诸多优势,如果其预防PEP疗效确定,那么它作为PEP的预防药物,将会使患者、医生以及社会均受益。
本研究共纳入7项随机对照研究,包括2 170例患者,均采用固定效应模型行Meta分析,分析结果提示吲哚美辛组的PEP发生率(RR=0.45,P<0.05)及高胰淀粉酶血症的发生率(RR=0.51,P<0.05)显著低于安慰剂/空白对照组。并且预防应用吲哚美辛后其所发生PEP的严重程度(RR=0.43,P<0.05)也较安慰剂/对照组明显为轻,从而可以得出吲哚美辛能有效的预防PEP的发生之结论。另外,本研究未发现应用吲哚美辛预防PEP可引发严重不良反应或并发症,表明应用吲哚美辛预防PEP安全性较好。
对于吲哚美辛应用时间的的选择,ERCP术前30min应用吲哚美辛纳肛被证实相较安慰剂/空白对照组可有效降低PEP发生率(RR=0.36,P<0.05)。Montano等[7]于 ERCP术前2h、应用吲哚美辛,Sotoudehmanesh等[8]于ERCP术前立即应用吲哚美辛及Elmunzer等[13]于ERCP术后立即应用吲哚美辛,3组研究也均提示应用吲哚美辛后PEP发生率明显降低,但是单从用药时间方面考虑尚缺乏更多试验数据支持。从吲哚美辛的药代动力学角度分析,口服药物1.0~4.0h即可达到血药浓度峰值,通过直肠给药吸收则更迅速,血浆蛋白结合率为99%,其半衰期约为4.5h[16],因此提示我们于ERCP术前应用药物可能更有利于术中即达到有效血药浓度,从而更有效的预防PEP。
综上所述,吲哚美辛具有使用方便、价格低廉、不良反应少等优点,围术期应用吲哚美辛可有效的预防PEP的发生,且安全可靠。本研究的结论建立在多个临床随机对照试验的基础上,行Meta分析“倒漏斗图”显示不对称,考虑可能存在发表偏倚。同时荟萃分析并非试验性研究,质量控制标本并不能保证完全一致,还需要更严谨的大样本多中心随机对照试验的进一步验证。
[1] 李兆申,许国铭,孙振兴,等.诊断性与治疗性ERCP早期并发症与处理[J].中华消化内镜杂志,2002,19(2):77-80.
[2] Freeman ML,Guda NM.Prevention of post-ERCP pancreatitis:a comprehensive review[J].Gastrointest Endosc,2004,59(7):845-864.
[3] Cheng CL,Sherman S,Watkins JL,et al.Risk factors for post ERCP pancreatitis:aprospective multicenter study[J].Am J Gastroenterol,2006,101(1):139-147.
[4] Feurer ME,Adler DG.Post-ERCP pancreatitis:review of current preventive strategies[J].Curr Opin Gastroenterol,2012,28(3):280-286.
[5] Jadad AR,Carroll D,Glynn CJ,et al.Morphine responsiveness of chronic pain:double-blind randomised crossover study with patient-controlled analgesia[J].Lancet,1992,339(8806):1367-1371.
[6] Cotton PB,Lehman G,Vennes J,et al.Endoscopic sphincterotomy complications and their management:an attempt at consensus[J].Gastrointest Endosc,1991,37(3):383-393.
[7] Montano Loza A,Rodríguez Lomeli X,Garcia Correa JE,et al.Effect of the administration of rectal indomethacin on amylase serum levels after endoscopic retrograde cholangiopancreatography,and its impact on the development of secondary pancreatitis episodes[J].Rev Esp Enferm Dig,2007,99(6):330-336.
[8] Sotoudehmanesh R,Khatibian M,Kolahdoozan S,et al.Indomethacin may reduce the incidence and severity of acute pancreatitis after ERCP[J].Am J Gastroenterol,2007,102(5):978-983.
[9] 夏挺松,刘鹏飞.直肠非甾体类抗炎药对ERCP术后胰腺炎的预防作用[J].中华消化内镜杂志,2010,27(6):301-302.
[10] 徐俊荣,楚有良,韩坤,等.吲哚美辛在预防ERCP术后胰腺炎中作用的研究[J].胃肠病学和肝病学杂志,2011,20(9):858-860.
[11] 钱健清,戴建军,王卫军,等.吲哚美辛对内镜下逆行性胰胆管造影术后胰腺炎的预防[J].中华胰腺病杂志,2011,11(5):326-328.
[12] 林涛,周毅,王钧,等.吲哚美辛预防经内镜逆行胰胆管造影术后胰腺炎和高淀粉酶血症的临床研究[J].中华消化内镜杂志,2012,29(4):185-187.
[13] Elmunzer BJ,Scheiman JM,Lehman GA,et al.A randomized trial of rectal indomethacin to prevent post-ERCP pancreatitis[J].N Engl J Med,2012,366(15):1414-1422.
[14] Gross V,Leser HG,Heinisch A,et al.Inflammatory mediators and cytokines-new aspects of the pathophysiology and assessment of severity of acute pancreatitis[J].Hepatogastroenterology,1993,40(6):522-530.
[15] Makela A,Kuusi T,Schroder T.Inhibition of serum phospholipase-A2in acute pancreatitis by pharmacological agents in vitro[J].Scand J Clin Lab Invest,1997,57(5):401-407.
[16] 卫生部合理用药专家委员会.中国医师药师临床用药指南[M].重庆:重庆出版社,2009:1359-1361.
