外周T细胞淋巴瘤治疗药
——Beleodaq
2014-03-08商艳丽冯巧巧
商艳丽,冯巧巧
(1.山东省阳信县人民医院,山东阳信251800;2.山东省食品药品监督管理局审评认证中心,山东济南250013)
·药物信息·
外周T细胞淋巴瘤治疗药
——Beleodaq
商艳丽1,冯巧巧2
(1.山东省阳信县人民医院,山东阳信251800;2.山东省食品药品监督管理局审评认证中心,山东济南250013)
2014年7月3 日,美国FDA批准Beleodaq(belinostat)用于外周T细胞淋巴瘤(PTCL)患者的治疗,这次的批准是在FDA加速批准程序下完成。外周T细胞淋巴瘤是一种罕见并发展迅速的非霍奇金淋巴瘤,Beleodaq通过阻止有助于T细胞(一种免疫细胞)发生癌变的酶起作用。这款药物适用于治疗后(复发性)疾病或对以前治疗无效(难治性)的患者。
商品名:Beleodaq
通用名:Belinostat
化学名:(2E)-N-hydroxy-3-[3-(phenylsulfamoyl)phenyl]prop-2-enamide
分子式:C15H14N2O4S
结构式:

1 作用机制
Belinostat是一种组蛋白去乙酰化酶(HDAC)抑制剂。HDACs催化组蛋白和一些非-组蛋白的赖氨酸残基去除乙酰基。在体外,belinostat使乙酰化组蛋白和其他蛋白积蓄,诱导细胞周期停滞和(或)一些转化细胞凋亡。与正常细胞比较,belinostat显示优先向肿瘤细胞产生细胞毒性。Belinostat在纳摩尔浓度(<250 nM)下抑制组蛋白去乙酰化酶的酶活性。
2 药效动力学
临床心电图(ECG)和belinostat血浆浓度数据分析显示,Belinostat对心脏复极化作用无有意义的影响。没有一个试验显示Belinostat对心率、PR持续时间或QRS持续时间有任何临床上的相关变化,作为自主状态、房室传导或去极化的措施;没有扭转性室速病例。
3 药代动力学
Belinostat剂量范围为150~1 200 mg·m-2的Ⅰ/Ⅱ期临床研究合并数据分析了belinostat的药代动力学特征。总体平均血浆清除率和消除半衰期分别为1 240 mL·min-1和1.1 h。总体清除率接近平均肝脏血流量(1 500 mL· min-1),这表明了高肝脏提取率(清除率具有血流依赖性)。
分布:belinostat的血浆平均分布容积接近身体总水量,表明belinostat有受限的机体组织分布。体外血浆研究表明,在一项平衡透析分析中,92.9%~95.8%的belinostat与蛋白结合,在500~25 000 ng·mL-1范围内不依赖于血浆浓度。
代谢:Belinostat主要被肝脏UGT1A1代谢。强有力的UGT1A1抑制剂可增加belinostat暴露量。Belinostat同样经历肝脏代谢,被CYP2A6、CYP2C9和CYP3A4酶代谢形成belinostat酰胺化物和belinostat酸化物。
排泄:Belinostat主要通过新陈代谢被消除,低于剂量2%的未变化药物在尿中被回收。给药后24 h内,所有的主要代谢产物(甲基belinostat、belinostat酰胺化物、belinostat酸化物、belinostat葡萄糖醛酸苷和3-ASBA)经尿排泄。代谢物3-ASBA和belinostat葡萄糖醛酸苷代表了经尿排泄belinostat剂量的最高部分(分别为4.61%和30.5%)。
4 临床研究
在62个中心进行的一项标签公开、单组、非-随机化国际试验中,129例有复发或难治周边T细胞淋巴瘤(PTCL)的患者在21 d疗程中的第1~5天每天1次静脉输注、历时30 min给予Beleodaq 1 000 mg·m-2。有120例通过中央审查评价疗效而在组织学上被确证的PTCL患者。患者每三周重复周期治疗直至疾病恶化或出现不可接受的毒性。
主要疗效终点是应答率(完全有效和部分有效),通过一个独立审评委员会(IRC)利用国际标准研讨会(IWC)(Cheson 2007)进行评价。关键性次要疗效终点为应答持续时间。在前12个月每6周、然后每12周对应答进行评价,直至从研究治疗开始2年。应答持续时间的测量是从记录应答的第一天到疾病恶化或死亡。疾病应答和恶化由IRC利用IWC进行评价。
表1总结了研究人群的基线人口统计学和疾病特征,其疗效是可评价的。
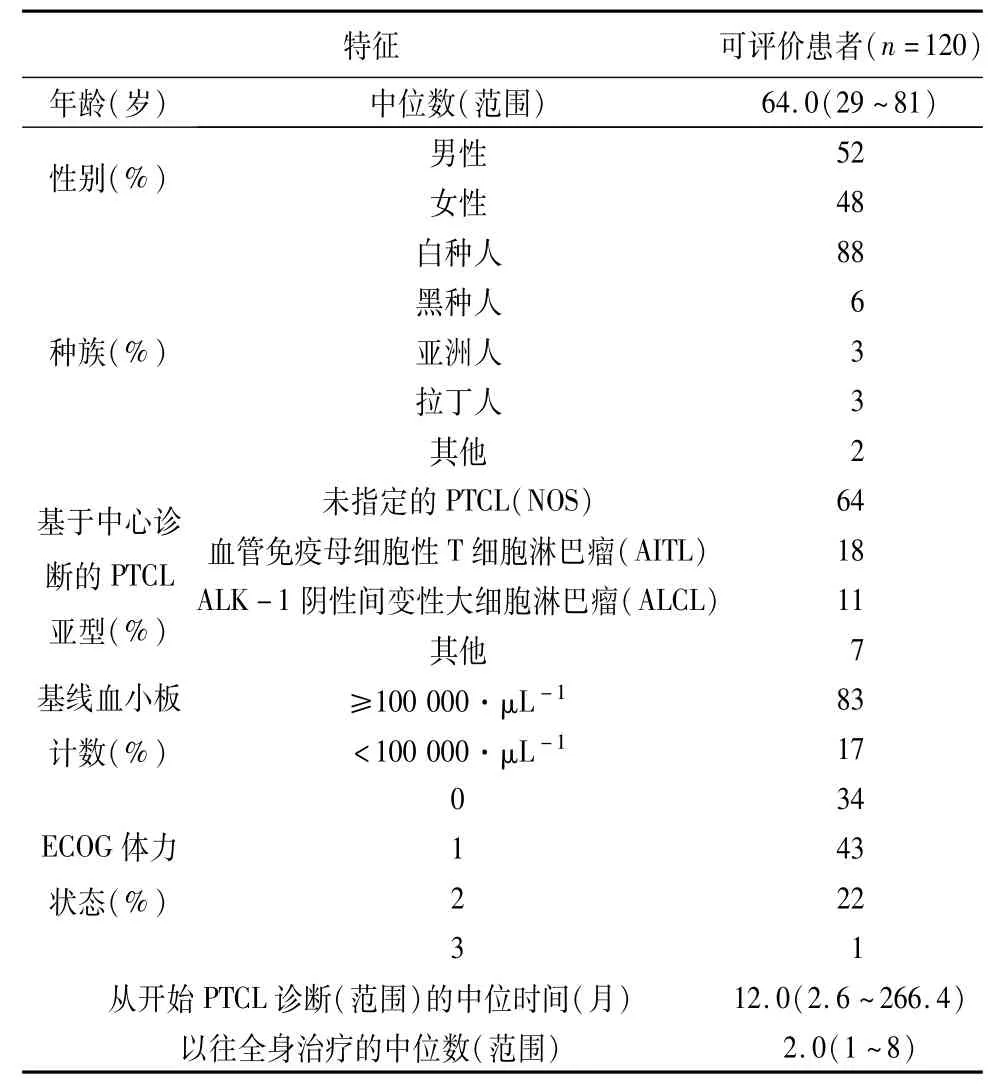
表1 PTCL患者基线特征
在所有用Beleodaq治疗的可评价患者(n=120)中,每个中心利用IWC评价的总体应答率为25.8%(n=31)(见表2),两个纳入的最大亚型的应答率分别为PTCL与NOS 23.4%,AITL 45.5%。

表2 复发或难治愈PTCL患者利用IWC的每个中心评价的应答分析
基于应答第一天到疾病恶化或死亡的中位应答时间为8.4个月(95%CI:4.5~29.4)。对于应答者,应答的中位时间为5.6周(范围4.3~50.4周)。利用Beleodaq治疗后,9例患者(7.5%)能够进行干细胞移植。
5 规格与剂量
注射剂:500 mg,冻干粉为重建的一次性使用小瓶。
剂量:Beleodaq的推荐剂量是在21 d疗程的第1~5天每天1次1 000 mg·m-2通过静脉历时30 min输注给药。
6 适应证
Beleodaq适用于有复发或难治周边T细胞淋巴瘤(PTCL)患者的治疗。
7 不良反应
Beleodaq最常见不良反应是恶心、疲劳、发热、贫血和呕吐。
R979.1
A
2095-5375(2014)09-0557-002
商艳丽,女,研究方向:医院药学,E-mail:shangshang112233@126.com
