沸石特性对负载纳米TiO2光催化去除水中土霉素的影响
2014-03-05黄文婷孙永军郑怀礼
赵 纯,周 宇,黄文婷,孙永军,王 亮,郑怀礼
(1.重庆大学a.三峡库区生态环境教育部重点实验室;b.低碳绿色建筑国际联合研究中心,重庆400045;2.重庆市规划设计研究院,重庆401147)
土霉素(oxtetracycline,OTC)是四环素类抗生素的一种,作为抗菌剂和生长因子被广泛应用于药物治疗和畜牧养殖业,每年有大量含有土霉素的生产废水排入水体[1-4]。毒理学研究证明,土霉素不但对环境中的微生物、两栖动物、鱼类具备慢性毒性,还能增强细菌的抗药性[5-8]。此外,由于土霉素的强极性和抗生素特性,常规的水处理工艺对其难以有效去除[9-10]。
研究发现,四环素类抗生素在模拟太阳光的照射下可被光解[11-12],在此过程中会生成危害性更强的中间产物,它的主体四环结构难以被破坏[5,9,13]。当前,光催化氧化技术作为一种绿色环保、低能耗的水处理技术,具有广阔应用前景。纳米TiO2在一定波段的光波照射下产生的羟基自由基几乎能够无选择性地氧化一切难降解有机物,但是其难以和水分离且易团聚失活的缺点制约了其在水处理中的应用。沸石分子筛是一种微孔材料,具有物相和成分单一、杂质少、结构内孔道和孔穴大小均一、比表面积大、交换性能、吸附性能及催化性能较稳定等优点[1,14]。其多孔结构可以有效地支撑纳米TiO2在其表面的负载,使用沸石作为纳米TiO2的承载材料,对土霉素进行光催化处理,可实现光催化剂的重复使用并能克服纳米TiO2的团聚失活问题[5]。笔者通过固体扩散法将纳米TiO2分别负载在亲水和疏水型沸石及5A和13X沸石分子筛上制成复合光催化剂,研究沸石的亲疏水性及其孔径大小对其负载纳米TiO2光催化去除和降解水中土霉素的影响。
1 材料与方法
1.1 实验仪器、试剂和材料
液相色谱仪(HPLC-1100,美国 Agilent Series);磁力搅拌器(79-2型,江苏金坛市荣华仪器制造有限公司);Rigaku D/max 2550型 X 射 线 衍 射仪;FEI Company Quanta 200FEG 型 电 场 放 射 扫 描 电 镜(FESEM);TOC分析仪(V-CPN,日本SHIMADZU);电热恒温鼓风干燥箱(DGG-9620A型,上海森信实验仪器有限公司);数字程控马弗炉(Paragon HT-22-D,美国 Thermcraft);吸附速率测定反应器(自制,直径110mm,高45mm,有效容积350mL);紫外杀菌灯管(单灯功率16W,主波长254nm,美国Light Sources公司)。NaOH、HCl、草酸、无水乙醇和其他试剂都为分析纯,购自上海国药集团化学试剂有限公司。
土霉素(色谱纯,上海艾德生物科技有限公司);纳米 TiO2(P25,比 表 面 积 50m2/g,平 均 粒 径30nm,德国Degussa公司);疏水沸石(直径3μm,上海卓悦化工有限公司);亲水沸石(40~50目,化学纯,上海国药集团化学试剂有限公司);5A分子筛(直径3μm,上海分子筛有限公司);13X分子筛(直径3μm,上海分子筛有限公司)。
1.2 负载型复合光催化剂的制备
先把不同配比的纳米TiO2和沸石放入研钵里,然后倒入酒精对其充分研磨使两者混合均匀,一直研磨到酒精挥发完毕,接着在110℃下烘箱中干燥,干燥后的样品置于450℃的马弗炉中煅烧6h即制得不同纳米TiO2负载比例的复合光催化剂[15]。
1.3 实验装置
将反应器置于磁力搅拌器上,把2根同型号的紫外杀菌灯管平行放置于反应器上方110mm处,然后用遮光罩将整个反应器罩住,以防其他光源的干扰,同时于反应器中插入一根通气管,将其另一端连接到微型空气泵上。实验装置如图1所示。

图1 实验装置
1.4 实验方法
1.4.1 光催化氧化实验 用实验室制的超纯水将土霉素标准样品配成50mg/L的储备液,试验分批依次进行,室温条件下,取200mL的土霉素水溶液置于反应器,然后在磁力搅拌下,用氢氧化钠和盐酸溶液调节pH至设定值,接着加入一定量的复合光催化剂,启动紫外灯管和曝气空气泵,分别于不同的反应时间取样,离心分离后放入冰箱避光4℃冷藏,待分析。
1.4.2 复合光催化材料的表征
1)表面负载成分的确定
复合光催化表面负载成分的确定由X射线衍射(XRD)法来完成。X射线衍射(XRD)法得到的是与固体表面粒子或结晶中原子的排列和结构有关的信息。用此方法可以测定催化剂材料表面的结构和成分。采用Rigaku D/max 2550型X射线衍射仪测定复合材料的表面结构,测试条件为:辐射源为CuKα,衍射角2θ为3°~60°,扫描速度0.01°,温度25℃,电压40kV。
2)表面形貌分析
采用FEI Company Quanta 200FEG型电场放射扫描电镜(FESEM)(表面镀Au)进行表征,观察吸附材料的表面形貌。
1.5 分析方法
使用高效液相色谱对样品中的土霉素浓度进行检测。检测前所有样品需通过0.45μm滤膜进行预处理。HPLC检测条件如下:色谱柱采用C18反向柱 (250mm×4.6mm);流动相A为0.01mol/L的草酸溶液,流动相B为体积比2:1的乙腈和甲醇混合液;柱温308K;流动相流速0.8mL/min;检测波长355nm;进样量20μL。
2 结果与讨论
2.1 纳米TiO2在沸石上的负载
通过X射线衍射(XRD)法和放射扫描电镜(FESEM)法,从负载前后的对比可知,使用固体扩散法可以将纳米TiO2(平均粒径30nm)成功地负载在微米级(直径3μm)沸石(5A和13X)上,且负载后并不会改变5A和13X沸石分子筛的结构[11]。
2.2 沸石的亲疏水性对负载TiO2光催化去除土霉素的影响
2.2.1 亲疏水性的沸石负载不同配比TiO2对土霉素的去除效果 通过实验研究了亲水性沸石(Z1)和疏水性沸石(Z2)负载不同配比纳米TiO2对土霉素的去除效果[5,9]。结果表明,对于疏水沸石而言,40%的纳米TiO2和60%的疏水沸石质量分数构成的复合光催化剂(40%TZ1)对土霉素具有最佳的降解效果。这是由于纳米TiO2改善了疏水沸石对土霉素的吸附性能,并使复合光催化剂的光催化活性得到很大提升。当TiO2的负载比例进一步提高时,复合光催化剂对土霉素的吸附效果呈现下降趋势,此时其光催化性能也同样降低,这可能是由于沸石表面的活性吸附位已经达到饱和,多余的纳米TiO2在沸石的外表面相互屏蔽,进而影响了土霉素的吸附和降解效果。对于亲水沸石而言,10%的纳米TiO2和90%的亲水沸石组成的复合光催化剂(10%TZ2)在波长为254nm的紫外线照射下对土霉素的去除可取得最理想的效果,这是由于纳米TiO2优化了沸石的吸附性能和复合光催化剂的光催化氧化性能。
2.2.2 亲疏水性沸石负载前后对土霉素的去除对比 取土霉素溶液的初始浓度为50mg/L,通气搅拌的条件下,比较5种处理工艺:UV、UV/Z1、UV/Z2、UV/40%TZ1和UV/10%TZ2对土霉素的去除效果。结果如图2所示,在40%TZ1和10%TZ2复合光催化剂500mg/L及与之对应的Z1和Z2沸石等沸石质量投加的情况下,UV/10%TZ2对水中的土霉素具有最佳的去除效果,UV/40%TZ1工艺次之,UV/Z2再次之,UV远逊前3种工艺,UV/Z1最差。该结果表明,沸石负载纳米TiO2,可以同时发挥TiO2的光催化活性和沸石对土霉素的吸附作用,协同去除水中的土霉素,因此在UV照射下,使用亲水沸石负载纳米TiO2比疏水沸石载纳米TiO2对土霉素具有更好去除效果。如图2所示复合光催化剂投加量500mg/L,Z1投加量300mg/L,Z2投加量450mg/L,pH=7。

图2 亲疏水沸石负载纳米TiO2前后对土霉素的去除对比
2.2.3 不同处理工艺对TOC和土霉素的去除比较 研究发现,土霉素类四环素物质的结构极其稳定,其四环结构很难被破坏,所以其TOC去除率较低[9,13,16],因此,有 必 要 对 几 种 工 艺 对 土 霉 素 溶 液TOC的去除情况进行考察。由图3可知,在反应120min后,UV/10%TZ2工艺具备最佳的土霉素和TOC去除率,此时的复合光催化剂综合了TiO2和沸石的优点。图3所示土霉素初始浓度为50mg/L,复合光催化剂投加量500mg/L,Z1投加量300mg/L,Z2投加量450mg/L,pH=7,反应时间120min。

图3 不同处理工艺对土霉素和TOC的去除率
2.3 沸石孔径对负载TiO2去除土霉素的影响
2.3.1 土霉素分子尺寸的计算 使用化学软件ChemSketch 11.0对土霉素的分子结构进行3D绘图和计算,得到土霉素分子的近似尺寸,见图4。由图4可知,土霉素分子的长度约在1.395nm,宽度约在0.711 5nm。因此,5A沸石分子筛孔径约为0.5nm,土霉素分子不可能进入其内孔结构中;13X沸石分子筛孔径约为1nm,土霉素分子有可能进入其内孔结构。

图4 土霉素的分子尺寸
2.3.2 土霉素在5A和13X上的吸附和解吸
1)不同pH下的吸附等温线
由于土霉素属于一种离子化有机物,其形态受到pH的较大影响,通过前期的研究表明,在沸石投加量0.02g、298K温度下,5A和13X两种沸石在不同pH条件下对土霉素的吸附等温线可用Langmuir吸附模型进行拟合,在pH=11.0时,由于电荷排斥力的作用,2种沸石对水溶液中的土霉素几乎没有吸附;在pH=7.0时2种沸石对水中土霉素的吸附达 最大值,分别为654mg/g(5A)和1 497mg/ (13X)[11,12]。这 是 由 于 13X 具 有 比 5A更大的孔径,根据计算得出的土霉素分子尺寸,其宽度为7.11,能够进入内孔道为10的13X分子筛内部进行吸附和离子交换反应,却不能进入内孔道为5的5A分子筛进行吸附和离子交换。
2)吸附和脱附
土霉素原始浓度为50mg/L、沸石投加量为0.1g、溶液pH=7.0、293K室温、避光和搅拌条件下,5A和13X两种沸石对土霉素的吸附随时间的变化如图5所示。由图可知,13X与5A对土霉素的吸附分别在70min和90min达到平衡后均能去除溶液中90%左右的土霉素,且13X具有比5A沸石分子筛更快的土霉素吸附去除速率。在吸附进行210min后,调节溶液pH至12以上,搅拌30min后,5A和13X可分别得到91%和95%的土霉素脱附率[11]。
2.3.3 5A和13X负载纳米TiO2对土霉素的降解
1)最佳纳米TiO2负载量的确定
通过实验研究了不同孔径的小孔亲水沸石5A和13X负载不同配比(1%、5%、10%、15%)纳米TiO2对土霉素的去除效果。结果表明,15%TiO2/5A和10%TiO2/13X构成的复合光催化剂在254 nm紫外线照射下对溶液中的土霉素具有最佳的去除和降解效果[11]。

图5 土霉素在5A和13X上的吸附和脱附[11]
2)5A和13X负载TiO2前后对土霉素的去除对比
土霉素初始浓度50mg/L,在通气搅拌的条件下,比较了 UV/13X、UV/5A、UV/10%T13X 和UV/15%T5A5种处理工艺对土霉素的去除和降解效果,结果如图6所示。图中所示复合光催化剂投加量500mg/L,13X 投加量400mg/L,5A 投加量350mg/L,pH=7。在10%T13X和15%T5A复合光催化剂500mg/L及与之对应的13X和5A沸石等沸石质量投加的情况下,在光反应阶段(0~210min),对土霉素的去除依靠复合光催化剂的吸附和降解,在暗反应阶段(210~240min)通过调节pH=12进行解吸附,得到土霉素的纯降解率。结果表明:UV/10%T13X对水中的土霉素具有最快的去除效果,UV/15%T5A对水中的土霉素具有最好的去除和降解效果。因此,在UV照射下,UV/15%T5A对水中的土霉素具有最佳的降解效果。15%TiO2/5A对土霉素的去除主要依靠TiO2的光催化降解,10%TiO2/13X主要依靠13X对土霉素的快速吸附。由于羟基自由基的作用距离有限,吸附在13X内部的土霉素无法有效降解。

图6 不同孔径沸石负载最佳配比纳米TiO2前后对土霉素的降解对比
3)对TOC和OTC的去除效果比较
土霉素初始浓度50mg/L,在通气搅拌的条件下,比较 UV、10%TiO2/5A 和 15%TiO2/13X3种处理工艺10h后对土霉素的降解效果,结果如图7所示。图中所示土霉素初始浓度为50mg/L,复合光催化剂投加量500mg/L,13X投加量400mg/L,5A投加量350mg/L,pH=7,反应时间600min。由图7可知,虽然单独使用UV也可以缓慢降解土霉素,但当土霉素完全降解后,TOC仅仅去除了5.37%。而15%TiO2/5A和10%TiO2/13X两种复合光催化剂对水中土霉素的去除率可分别达到30.57%和16%,并且,由于土霉素的四环结构非常牢固,被降解的土霉素转化为了中间产物,所以,随着反应的进行,对土霉素的矿化变得越来越难。
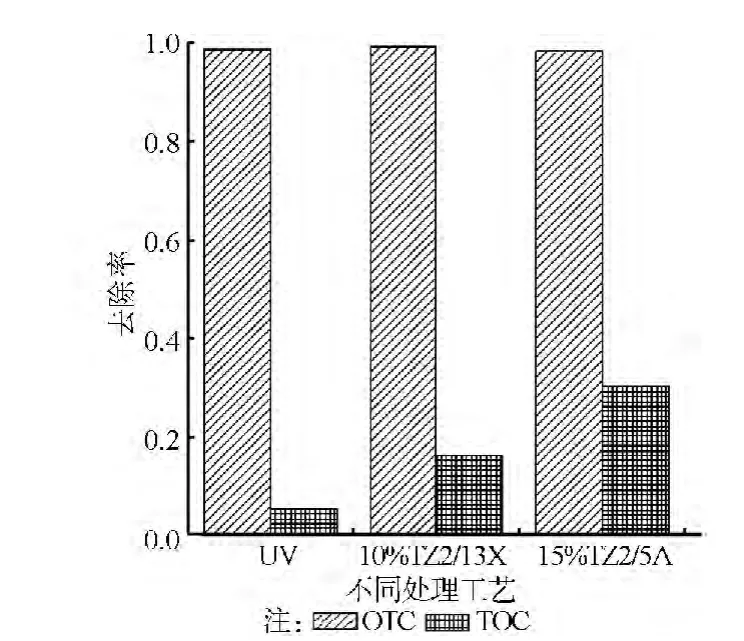
图7 不同处理工艺对土霉素降解和矿化
2.3.4 机理分析 由于13X沸石分子筛对土霉素具备更好的吸附性能,所以10%TiO2/13X具备比15%TiO2/5A更快的土霉素去除能力。同时,吸附在13X内孔的土霉素并不能被有效降解,这可能是因为纳米TiO2只能被负载于沸石分子筛的外表面,且TiO2在光照下产生的羟基自由基存在时间只有10-9s[17],因此只有靠近5A 和13X 外表面的土霉素才能被光催化降解。其机理如图8所示。

图8 10%TiO2/13X和15%TiO2/5A光催化降解土霉素原理示意图
3 结 论
1)UV/10%TZ2 比 UV、UV/Z1、UV/Z2 和UV/40%TZ1对水中的土霉素具有更佳的去除效果,亲水沸石更宜作为载体负责纳米TiO2光催化去除水中的土霉素。
2)UV/15%T5A 比 UV、UV/13X、UV/5A、UV/10%T13X对水中的土霉素具有更佳的去除效果,因此在UV照射下,小孔径沸石更宜作为载体负责纳米TiO2光催化去除水中的土霉素。
3)5A和13X沸石负载的两种复合光催化剂对土霉素都具备较好的去除、降解性能。其中,由于13X具备更大的孔径,对土霉素及其降解中间产物具备比5A沸石分子筛更好的吸附性能,因此13X更易将中间产物固定在复合光催化剂内外表面。
4)15%TiO2/5A对土霉素的去除主要依靠TiO2的光催化降解,10t%TiO2/13X主要依靠13X对土霉素的快速吸附。由于羟基自由基的作用距离有限,吸附在13X内部的土霉素无法有效降解。
[1]黎园,赵纯,邓慧萍.2种孔径沸石分子筛对水中土霉素的去除研究[J].环境科学,2010(4):990-995.Li Y,Zhao C,Deng H P.Oxytetracycline removal in aqueous by two kinds of zeolites with different bore diameter[J].Environmental Science,2010(4):990-995.
[2]Li K,Yediler A,Yang M,et al.Ozonation of oxytetracycline and toxicological assessment of its oxidation by-products [J].Chemosphere,2008,72(3):473-478.
[3]Jacobsen P,Berglind L.Persistence of oxytetracycline in sediments from fish farms[J].Aquaculture,1988,70(4):365-370.
[4]Madden J C, Enoch S J, Hewitt M,et al.Pharmaceuticals in the environment:good practice in predicting acute ecotoxicological effects[J].Toxicology Letters,2009,185(2):85-101.
[5]赵纯,邓慧萍.疏水沸石负载纳米TiO2光催化去除水中土霉素[J].同济大学学报:自然科学版,2009(10):1360-1365.Zhao C,Deng H P.Removal of oxytetracycline in water by UV/hydrophobic zeolite loaded with TiO2[J].Journal of Tongji University:Natural Science,2009(10):1360-1365.
[6]张浩,罗义,周启星.四环素类抗生素生态毒性研究进展[J].农业环境科学学报,2008(2):407-413.Zhang H,Luo Y,Zhou Q X.Research advancement of eco-toxicity of tetracycline antibiotics [J].Journal of Agro-environment Science,2008(2):407-413.
[7]Wei R,Ge F,Huang S,et al.Occurrence of veterinary antibiotics in animal wastewater and surface water around farms in Jiangsu Province, China [J].Chemosphere,2011,82(10):1408-1414.
[8]冯新,韩文瑜,雷连成.细菌对四环素类抗生素的耐药机制研究进展[J].中国兽药杂志,2004(2):38-42.Feng X,Han W Y,Lei L C.Advanced research in the bacterial resistance mechanisms of tetracycline [J].Chinese Journal of Veterinary Drug,2004(2):38-42.
[9]赵纯,邓慧萍,商冉.改进紫外消毒工艺去除水中土霉素[J].土木建筑与环境工程,2009(2):152-156.Zhao C, Deng H P, Shang R.Removal of oxytetracycline in water by improved UV disinfection process [J].Journal of Civil, Architectural &Environmental Engineering,2009(2):152-156.
[10]Mompelat S,Le Bot B,Thomas O.Occurrence and fate of pharmaceutical products and by-products,from resource to drinking water [J].Environment International,2009,35(5):803-814.
[11]Zhao C,Deng H,Li Y,et al.Photodegradation of oxytetracycline in aqueous by 5Aand 13Xloaded with TiO2under UV irradiation [J].Journal of Hazardous Materials,2010,176(1/2/3):884-892.
[12]Zhao C,Pelaez M,Duan X D,et al.Role of pH on photolytic and photocatalytic degradation of antibiotic oxytetracycline in aqueous solution under visible/solar light:kinetics and mechanism studies [J].Applied Catalysis B-Environmental,2013,134/135:83-92.
[13]Jiao S,Zheng S,Yin D,et al.Aqueous oxytetracycline degradation and the toxicity change of degradation compounds in photoirradiation process [J].Journal of Environmental Sciences-China,2008,20(7):806-813.
[14]庞文琴,于吉红,徐如人,等.分子筛与多孔材料化学[M].北京:科技出版社,2004:356-409.
[15]Durgakumari V,Subrahmanyam M,Subba Rao K V.An easy and efficient use of TiO2supported HZSM-5 and TiO2+ HZSM-5zeolite combinate in the photodegradation of aqueous phenol and p-chlorophenol[J].Applied Catalysis A-General,2002,234(1/2):155-165.
[16]Dalmázio I, Almeida M O, Augusti R,et al.Monitoring the degradation of tetracycline by ozone in aqueous medium via atmospheric pressure ionization mass spectrometry[J].Journal of the American Society for Mass Spectrometry,2007,18(4):679-687.
