两种仪器检测自身免疫性甲减患者*血清促甲状腺激素结果的比较评价
2014-02-05胡锡林杨湘越王开宇兰小鹏
胡锡林 杨湘越 王开宇 兰小鹏
两种仪器检测自身免疫性甲减患者*血清促甲状腺激素结果的比较评价
胡锡林①杨湘越②*王开宇②兰小鹏②
目的:探讨两种免疫分析系统检测自身免疫性甲状腺功能减退(甲减)患者血清促甲状腺激素(TSH)结果的一致性。方法:采用宝太BIOT-YG-I与罗氏E601免疫分析系统,检测80例自身免疫性甲减患者和40例正常人血清的TSH水平,通过Kappa检验分析两种系统检测结果的一致程度,并利用线性回归分析两种系统定量检测TSH的相对偏差。结果:两种系统检测TSH结果的符合率及一致性较高;两系统间TSH定量测定结果直线相关性良好(r≥0.975),在相应医学参考水平浓度测定结果的相对偏差均可被临床接受。结论:两种免疫分析系统检测TSH的结果一致性较高。
荧光免疫分析系统;促甲状腺激素;一致性
胡锡林,男,(1965- ),本科学历,副主任技师。南京军区鼓浪屿疗养院检验科主任,研究方向:临床检验、免疫学。
[First-author’s address]Department of laboratory Medicine, Gulangyu Sanatorium of Nanjing Military Command, Xiamen361002, China.
甲状腺功能减退(甲减),是由于甲状腺激素的合成、分泌或生物效应不足而引起的一种综合征,其特征是机体代谢率降低,严重者可形成黏液性水肿。临床上引起甲减的原因很多,其中自身抗甲状腺球蛋白抗体(TgAb)和抗甲状腺过氧化物酶抗体(TPOAb)阳性的桥本甲状腺炎是亚临床甲减的最常见病因,其次为甲状腺肿,甲状腺腺瘤较少见[1-2]。此外,促甲状腺素受体抗体(TRAb)根据其功能不同分为两类,其中甲状腺阻断性抗体(TBAb)可通过阻断血清促甲状腺激素(thyrotropin,thyroid stimulating hormone,TSH)与受体的结合及TSH功能而引起甲减[3]。据报道,我国农村地区男性甲减患病率为2.8%,女性为3.2%[4]。美国的一项研究显示男性患病率为5.7%,女性为13%,且每年有2%~5%的亚临床甲减患者进展为临床甲减[2,5-6]。因此,在甲减的诊疗过程中,血清TSH水平是十分重要的检测指标。
目前,TSH定量测定的传统方法为放射免疫测定法和(或)免疫放射分析法,但均存在试剂有效期短、操作繁琐、环境污染和放射危害等问题,而且检测浓度范围偏窄。近年来,国外相继开发出化学发光免疫测定法、时间分辨免疫荧光法及电化学发光法等非放射标记免疫测定技术的试剂盒,其优点为灵敏度和操作自动化程度高、稳定性好,无放射性辐射危害及环境污染,但其试剂和仪器价格昂贵,试剂封闭不通用,容易形成垄断市场,给患者带来很大的经济负担。因此,迫切需要开发出国产开放式试剂和仪器,配置低廉、通用的POCT诊断试剂,以满足国内各级医疗机构临床诊断的需求,而荧光免疫层析试剂正符合国内市场需求。为验证该系统的可行性,按照美国临床和实验室标准协会(CLSI)系列文件,利用患者样本进行方法对比及偏差评估(批准指南第2版(EP9-A2)文件),对罗氏E601全自动电化学发光系统和厦门宝太公司免疫荧光分析仪I及其配套试剂盒,分别进行血清TSH的检测并对结果加以比较分析[7]。
1 资料与方法
1.1 一般资料
选取2013年1-12月在南京军区福州总医院确诊的80例自身免疫性甲减患者纳入本研究,其中男性41例,女性39例;年龄18~55岁。80例患者中原发性甲减51例,继发性甲减26例,急性甲状腺炎3例;所有患者标本要求为未溶血、无严重脂浊、无黄疸及标本量足够的血清,均用罗氏检测系统检测TSH,检测结果均符合甲减的诊断标准。
1.2 仪器试剂与检测方法
罗氏公司E601型全自动电化学发光分析仪及配套试剂;厦门宝太公司BIOT-YG-I型免疫荧光分析仪及配套试剂。
每份样本均用两种方法按照说明书要求进行检测,并进行统计学分析。每日选取8份临床阳性甲减患者样本,分别用两种方法按顺序(1→8)进行样本测定,再按相反顺序(8→1)重复测定,连续测定5 d,共40例样本,样本的浓度均匀分布在线性范围内。
1.3 TSH检测判定标准
宝太公司免疫荧光分析仪(宝太)和罗氏E601全自动电化学发光系统I及其配套试剂盒(罗氏)的TSH检测判定标准(见表1)。

表1 两种检测系统TSH检测判定标准
1.4 两种系统定量检测TSH结果的偏倚评估
记录测定结果(Xij和Yij),计算每个样本测定结果的均值(Xi和Yi)、样本重复测定值间差值的绝对值(Dxi和Dyi)及两种方法测定结果均值间的差值(Yi-Xi)。以Yi对Xi作散点图计算线性回归方程:Y=bX+a。以(Yi-Xi)对Xi作偏差图。按EP9-A2文件进行方法间离群值检查:计算样本重复测定值间差值(Dxi和Dyi)的平均数。计算两种方法测定结果均值间差值(Yi-Xi)的平均数。判断:超出上述平均数4倍时,检验结果视为无效。根据临床使用要求,依据各个项目给定的医学决定水平浓度X及允许偏倚(T<20%)计算两系统之间的系统误差即预期偏倚和相对偏倚[9-10]。
1.5 统计学方法
采用SPSS 19.0软件进行数据的统计与分析,TSH检测对比结果的一致性使用Kappa检验[8]。检测结果一致性的程度分为6个区段:极强,Kappa系数0.81~1.0;高度,Kappa系数0.61~0.8;中度,Kappa系数0.41~0.6;弱,Kappa系数0.21~0.4;微弱,0~0.2;极差,Kappa系数<0。
2 结果
2.1 两种检测系统的样本检测结果
采用厦门宝太公司免疫荧光分析仪(宝太)和罗氏E601全自动电化学发光系统I及其配套试剂盒(罗氏),同时对80例甲减及正常人血清样本TSH进行检测,其结果显示两种检测系统具有极强的一致性(见表2)。

表2 两种检测系统检测80例TSH的结果比较(例)
2.2 两种检测系统的样本检测符合率
厦门宝太公司免疫荧光分析仪和罗氏E601全自动电化学发光系统两种检测系统的样本检测阳性符合率、阴性符合率及总符合率分别为97.50%、97.50%及97.50%,95%置信区间下限均>90%(见表3)。

表3 两种检测系统一致率的比较(%)
2.3 两种检测系统间TSH的直线相关与回归分析
两种检测系统间TSH的直线相关性与回归分析结果如图1所示。
图中显示,两种检测系统间TSH的直线相关性良好,据有统计学意义(r2=0.9815,P<0.001),见表4。

图1 宝太与罗氏系统测试结果散点图

表4 两种检测系统测试TSH直线相关与回归分析
2.4 两种检测系统间的相对偏差
选择TSH值为5 mIU/L及60 mIU/L作为医学参考水平,在医学参考水平[11-13]处使用公式1计算两种检测系统间的相对偏差即偏倚:
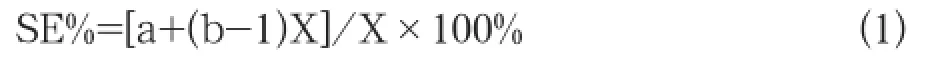
式中b为直线回归方程的斜率,a为截距,X为医学参考水平。
依据各个项目给定的医学决定水平浓度X及允许偏倚(T<20%)计算两系统之间的系统误差即预期偏倚和相对偏倚[9-10](如图2所示)。
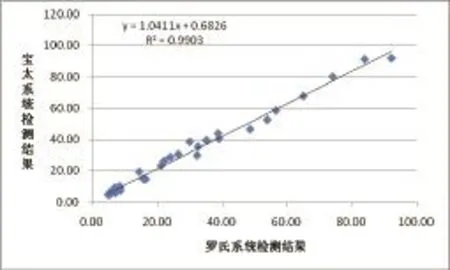
图2 宝太与罗氏系统偏倚分析散点图
通常,相对偏差(即偏倚)>20%被认为将影响临床上对疾病的诊断。两系统间的预期偏倚和相对偏倚结果具有高度一致性(r2=0.9903,P<0.001),见表5。
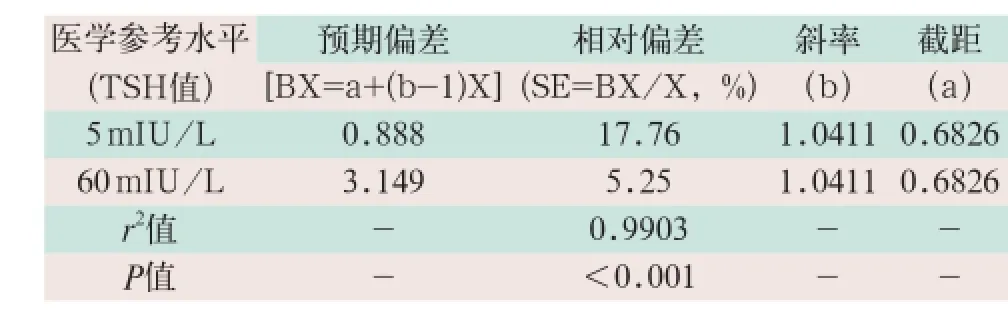
表5 两种检测系统间的偏倚
3 讨论
目前,实验室检测在疾病诊断和治疗等方面的作用越来越受到临床的重视,随着标本数量的不断增加,越来越多的临床实验室采用两套或多套检测系统来检测同一项目。在甲减的诊疗过程中,血清TSH水平是十分重要的指标,但其在临床不同检测系统间存在较大的差异,其原因在于各厂家仪器检测原理不同,采用的试剂来源不同等[14]。因此,使用不同免疫分析系统进行对比,以了解检测结果的可比性和偏倚评估非常重要[15]。本研究显示,宝太公司免疫荧光分析仪BIOT-YG-I及配套试剂与罗氏E601型电化学发光仪及配套试剂相比,两种系统在TSH水平的检测上具有极强的一致性,阳性、阴性符合率及总符合率分别为97.50%、97.50%及95%置信区间下限均>90%。分析两种系统的TSH检测值发现,在TSH浓度水平≥5 mIU/L时,相对偏差均在允许偏差之内,可以被接受,但偏差较大,分析原因可能是两种系统所采用分析方法不同及试剂、校准品和质控品的来源不同,并且罗氏E601系统与宝太系统参考值范围不一致,但就临床诊断需求而言,此偏倚对甲减的辅助诊断影响甚微。
4 结论
本研究按照CLSI的 EP9-A2文件要求,对TSH在两种全自动化学发光分析系统(罗氏E601和宝太BIOTYG-I)的检验结果进行对比分析和偏倚评估。结果表明,由于使用了配套试剂、校准品和质控品,TSH在两种分析系统之间的检验结果显示良好的相关性,线性回归方程良好,绝对相关系数r2均>0.975。本研究结果显示,以上两种系统对TSH水平的检测具有高度一致性。
[1]董松,卢桂芝,高燕明,等.亚临床甲状腺功能异常临床细胞病理学分析[J].中国实用内科学杂志,2009,29(3):231-233.
[2]Surks MI,Oritz E,Daniels GH,et al.Subclinical thyroid disease scentific review and guidelines for diagnosis and management[J]. JAMA,2004,291(2):228-238.
[3]梁华举,马玉琴,许耀玲,等.甲状腺自身抗体在碘-131治疗甲亢后致早发甲减的临床意义[J].2008, 17(2):161-162.
[4]单忠艳,滕卫平,李玉姝,等.碘致甲状腺功能减退症的流行病对比研究[J].中华内分泌代谢杂志,2001, 17(2):71-74.
[5]Michae IW,Tunbridge G,Vabderpump MPJ. Population screen for autoimmune thyroid disease[J].Endocrinnol Metab North Am,2000, 29:239-254.
[6]滕卫平.开展亚临床甲状腺功能减退症的临床研究[J].中华内分泌代谢杂志,2004,20(2):93-95.
[7]National Committee for Clinical Laboratory Standants,NCCLS Document EP9-A2.Method Comparison and Bias Estimation Using Patient Samples;Approved Guideline[M].Second Edition. Wayne NCCLS,2002.
[8]夏邦世,吴金华.Kappa一致性检验在检验医学研究中的应用[J].中华检验医学杂志,2006,29(1):83-84.
[9]郭健,谢洁红,赵海舰.方法学比较实验的设计及对两种白蛋白测定法的比较[J].中华检验医学杂志,2000,23(6):343-345.
[10]柳渊洁,陈进凡,黄仕君.ALT、AST、GGT、AKP、CHE在两生化分析系统间的偏倚评估[J].卫生职业教育,2005,23(11):114-115.
[11]曾鸿毅.新生儿脐带血甲状腺激素检测的意义[J].放射免疫学杂志,2008,21 (2):191-192.
[12]胡蓉.化学发光法检测甲状腺激素的临床应用[J].中国医药导刊,2012,14(5):877-878.
[13]凌文龙.甲状腺疾病的临床诊断与治疗[J].齐齐哈尔医学院学报,2012,33(21):2913-2914.
[14]欧阳彬.电化学发光免疫分析检测血清促甲状腺激素在甲状腺功能减退中的应用[J].中国民康医学,2010,22(9):1116-1118.
[15]王刚.比对验证国内外两台血细胞分析仪检测结果的一致性[J].检验医学与临床,2012,9(16):2066-2068.
Comparison of serum TSH in patients with autoimmune hypothyroidism detected by BIOT- YG-I and Roche E601
/HU Xi-lin, YANG Xiang-yue, WANG Kai-yu, et al// China Medical Equipment,2014,11(12):7-10.
Objective:To compare the results of TSH serum samples in patients with autoimmune hypothyroidism detected by two different immune analyze systems BIOT-YG-I and Roche E601.Methods:TSH in serum samples from 80 patients with autoimmune hypothyroidism and 40 normal controls were quantified by BIOT-YG-I and Roche E601 systems. Kappa statistic was used to analyze the agreement between the results from two immune analyze systems. The relatively deviation at medical reference level of the quantitative results of TSH were further studied using linear regressive analysis.Results:The quantitative results from two immune analyze systems presents good accordance rate and the agreement as well as a significant linear correlation (r≥0.975). TSH quantitative results from two systems are both clinically acceptable at medical reference level.Conclusion:The consistency of two immune analyze systems is high for detecting TSH serum.
Fluorescence immune analyze system; Thyroid stimulating hormone; Consistency
1672-8270(2014)12-007-04
R581.9
A
10.3969/J.ISSN.1672-8270.2014.12.003

2014-07-11
福建省科技计划重点项目(2013Y0075)“多种自身抗体快速联合检测试剂盒—(复合斑点胶体金法)的研发”
①南京军区鼓浪屿疗养院检验科 福建 厦门 361002
②南京军区福州总医院检验科 福建 福州 350025
*通讯作者:yangxy3737@163.com
