油脂微波加热模型中3-氯-1,2-丙二 醇脂肪酸酯的形成
2014-01-21周勇强朱建鹏聂少平
周勇强,李 昌,朱建鹏,聂少平
油脂微波加热模型中3-氯-1,2-丙二 醇脂肪酸酯的形成
周勇强,李 昌,朱建鹏,聂少平*
(南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047)
通过建立油脂微波加热模型,研究不同的油脂微波加热后3-氯-1,2-丙二醇(3-chloropropane-1,2-diol,3-MCPD)脂肪酸酯含量的变化情况以及NaCl溶液、pH值、时间、不连续微波和金属离子等因素对3-MCPD脂肪酸酯形成的影响。结果表明:1)熟榨植物油微波加热后3-MCPD脂肪酸酯含量增加均超过9 mg/kg,远超过其他植物油。2)3-MCPD脂肪酸酯含量随NaCl的质量浓度增加而增加,随NaCl溶液体积分数的增加呈先增加后减少趋势。3)酸性环境促进3-MCPD脂肪酸酯形成。4)微波加热10 min内,3-MCPD脂肪酸酯含量与时间呈正相关。5)微波总时间一定的情况下,不连续微波产生的3-MCPD脂肪酸酯明显少于连续微波。6)金属离子作为催化剂参与活性中间物的形成,能明显地促进3-MCPD脂肪酸酯的形成。上述结果可为食品微波加工处理过程中危害物3-MCPD脂肪酸酯的控制研究提供数据支持。
微波;3-氯-1,2-丙二醇脂肪酸酯;NaCl;pH值;时间;不连续微波;金属离子
3-氯-1,2-丙二醇(3-chloropropane-1,2-diol,3-MCPD)作为一种有害性物质,广泛地存在于各种热加工食品中,谷物类食品如吐司、面包皮、饼干[1-2]、咖啡[3]、烤奶酪[4]以及烟熏食品[5],婴幼儿食品也有检出[6]。另外,3-MCPD大多以脂肪酸酯的形式存在,而非自由态。这种化合物主要形成于食品的加工过程中[7],尤其是热加工过程,如油脂的精炼、氢化、脱臭等加工工艺。3-MCPD脂肪酸酯的危害正越来越受到广泛重视,这是由于它被活体摄入后,在体内被脂肪酶水解成游离的3-MCPD而具有致癌性、神经毒性、遗传毒性、生殖毒性以及免疫毒性等危害[8]。
Rahn等[9]对3-MCPD脂肪酸酯形成的机理进行了综述,提出4 种形成机理,这4 种形成机理均发生Cl-的SN2亲核攻击,其中有两种机理均发生了Cl-的直接亲核取代,分别取代了甘油碳原子上连接取代酯基基团和质子羟基化基团[10];另外两种为Cl-与发生亲核反应分别形成酰基氧鎓离子和环氧环等两种活性中间物[11-12]。为研究3-MCPD脂肪酸酯形成的机理以及影响因素建立了食品加工模型,探究加热温度、NaCl、水和大豆油的含量对3-MCPD脂肪酸酯形成的影响,结果表明3-MCPD脂肪酸酯的形成与加热的温度、NaCl、水和大豆油的含量有着密切的关系[13-15]。
微波加热由于其高效、节能以及杀菌效果。如今已广泛地应用在日常烹饪中,因此有必要通过建立油脂的微波加热模型,研究微波加热对油脂中3-MCPD脂肪酸酯形成的影响以期探讨其危害。本实验建立油脂微波加热模型,研究不同油脂种类、NaCl溶液、pH值、时间、不连续微波以及金属离子等因素对3-MCPD脂肪酸酯形成的影响,并对日常烹饪提出指导性的意见以减少饮食中3-MCPD脂肪酸酯的含量。
1 材料与方法
1.1 材料与试剂
自榨植物油(包括生榨和熟榨);玉米油、大豆油等9 种市售食用油购自南昌某市场。
硝酸盐、NaCl(分析纯) 天津大茂化学试剂厂;甲醇钠、苯硼酸(分析纯) 阿拉丁试剂(上海)有限公司;3-MCPD标准品(纯度98.4%) 德国Sigma-Aldrich公司;氘代同位素d5-3-MCPD标准品(纯度98.3%) 加拿大C/D/N ISOTopes公司。
1.2 仪器与设备
WD700A型微波炉 格兰仕集团有限公司;MD200-1氮气吹扫仪 杭州奥盛仪器有限公司;安捷伦7890A/7000气相色谱-质谱联用仪(配置HP-5色谱柱(0.25 mm×30 m,0.25 μm)) 美国 Agilent公司。
1.3 方法
1.3.1 建立微波加热模型
将10 mL油脂与1 mL NaCl溶液混合,涡旋均匀,然后放置在微波炉中加热一定时间,通过控制油脂的种类、NaCl溶液质量浓度、混合液的pH值、微波加热时间,使用不连续微波方式以及向混合液中添加金属元素等形式以模拟不同程度的微波烹饪。
1.3.2 不同的油脂
分别量取10 mL不同种类的油脂,加入1 mL 21.6 g/100 mL NaCl溶液,涡旋混匀,微波4 min,待油样冷却至室温后,贮藏备用。
1.3.3 NaCl溶液
1)NaCl溶液质量浓度:量取10 mL生榨菜籽油与1 mL不同质量浓度(0、7.2、14.4、21.6、28.8、36 g/100 mL)的NaCl溶液涡旋混匀,微波加热4 min,待油样冷却至室温后,贮藏备用。
2)NaCl溶液体积比:保持生榨菜籽油与NaCl溶液总量10 mL不变,将生榨菜籽油和21.6 g/100 mL NaCl溶液按体积比(5∶0、4∶1、3∶2、2∶3、1∶4)配比,涡旋混匀,微波4 min,待油样冷却至室温后,贮藏备用。
1.3.4 pH值
以21.6 g/100 mL NaCl溶液作为溶剂,分别配制不同pH值(4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0)的缓冲溶液。再分别取1 mL不同pH值的缓冲溶液与10 mL生榨菜籽油混合均匀,微波加热4 min,待油样冷却至室温后,贮藏备用。
1.3.5 微波时间
量取10 mL生榨菜籽油与1 mL 21.6 g/100 mL NaCl溶液涡旋混匀,然后分别微波2、3、4、6、8、10 min,待油样冷却至室温后,贮藏备用。
1.3.6 不连续微波
量取10 mL生榨菜籽油与1 mL 21.6 g/100 mL NaCl溶液涡旋混匀,然后分别微波1 次6 min,2 次3 min,3 次2 min,6 次1 min,待油样冷却至室温后,贮藏备用。
1.3.7 金属元素
以21.6 g/100 mL NaCl溶液作为溶剂,配制0.1 mol/L金属离子(Zn2+、Al3+、Ca2+、Cu2+、Fe2+、Fe3+、Mg2+)的硝酸盐溶液,取1 mL与10 mL生榨菜籽油涡旋混匀,微波4 min,待油样冷却至室温后,贮藏备用。
1.4 样品中3-MCPD脂肪酸酯检测
根据文献[17]的方法对各种微波加热模型体系中产生的3-MCPD脂肪酸酯进行分析检测,并记录其含量。
1.5 3-MCPD脂肪酸酯的计算
[16],按式(1)计算样品峰面积比值;按式(2)计算样品中3-MCPD的总含量;按式(3)计算样品中3-MCPD脂肪酸酯的含量。
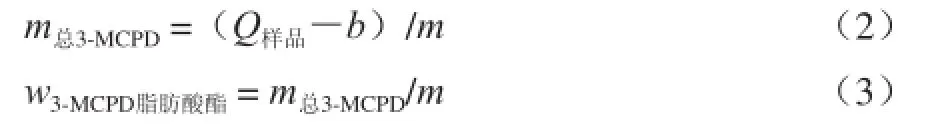
式中:Q表示为峰面积的比值;m3-MCPD表示为衍生化产物中3-MCPD的含量/μg;a表示为回归线的斜率;b表示为回归线的截距。式中:Q样品表示为样品峰面积的比值;m总3-MCPD表示为样品中3-MCPD的总量/μg;w3-MCPD脂肪酸酯为3-MCPD脂肪酸酯的含量/(μg/g);m表示为测试样品的质量/g。
由于油脂中3-MCPD 脂肪酸酯有SN1-3-MCPD 单酯、SN2-3-MCPD 单酯和3-MCPD二酯3 种化合物,且种类较多,目前无法通过内标法直接检测,而是通过酯交换将油脂中存在的各种3-MCPD 酯转化为游离态3-MCPD,测定3-MCPD的含量,以3-MCPD 的含量来表示3-MCPD酯的总量。
2 结果与分析
2.1 不同的油脂微波后3-MCPD脂肪酸酯含量的变化
本实验选择常用的几种食用油作为研究对象,研究微波处理前后食用油中3-MCPD脂肪酸酯含量的变化情况,结果如表1所示。同时对生榨、熟榨和市售植物原油中3-MCPD脂肪酸酯含量及微波后3-MCPD脂肪酸酯的增量做了相应的对比分析。
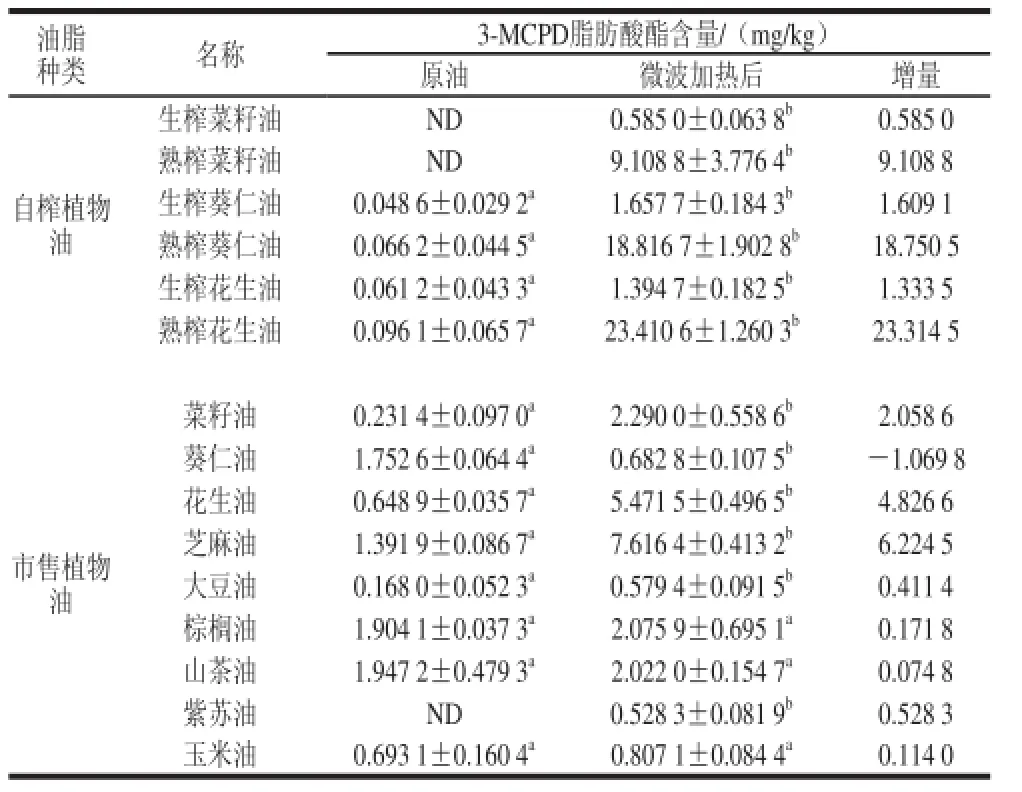
表1 不同的食用油中3-MCPD脂肪酸酯的含量Table 1 Contents of 3-MCPD in different edible oils
由表1可知,对比3 种类型的菜籽、葵仁和花生原油中3-MCPD脂肪酸酯的含量时发现:1)市售植物油中的3-MCPD脂肪酸酯含量远大于生榨和熟榨植物油,产生这种差异性的原因可能是市售植物油在脱酸、脱臭、脱脂等精炼过程中形成了较多的3-MCPD脂肪酸酯。2)熟榨植物油中3-MCPD脂肪酸酯略高于生榨植物油,这可能是熟榨植物油的原料炒制过程促进了3-MCPD脂肪酸酯的产生,但由于原料的炒制对植物油的3-MCPD脂肪酸酯含量属于间接性的影响,故差异性较小。
通过分析微波加热前后油脂中3-MCPD脂肪酸酯含量发现:大部分食用油在微波加热后3-MCPD脂肪酸酯含量与原油中的含量呈显著性差异(P<0.05)(市售棕榈油、山茶油、玉米油除外)。因此,微波加热可以促进油脂中3-MCPD脂肪酸酯的形成。
由图1可知:1)经微波处理后,植物油中的3-MCPD脂肪酸酯含量出现增加(市售葵仁油除外),这表明微波加热会促进3-MCPD脂肪酸酯的产生。2)熟榨植物油中3-MCPD脂肪酸酯含量增加显著,远大于生榨植物油和市售植物油。3 种熟榨植物油的增加量均超过9 mg/kg,熟榨葵仁油和熟榨花生油的增量分别达到18.750 5 mg/kg和23.314 5 mg/kg。

图1 微波处理后植物油中3-MCPD脂肪酸含量变化Fig.1 Change in 3-MCPD content in edible oil samples after microwave heating
与生榨植物油不同的是,熟榨植物油是由原料经炒制后压榨而得,但是熟榨植物原油中的3-MCPD脂肪酸酯含量仅仅略大于生榨植物原油。因此,造成熟榨植物油和生榨植物油微波后3-MCPD脂肪酸酯含量的巨大差异原因可能是炒制加工过程使原料的油脂成分发生了变化,产生更多的3-MCPD脂肪酯前体物(而非3-MCPD脂肪酸酯本身),这些前体物在微波加热处理后能迅速形成3-MCPD脂肪酸酯。
另外,由表1数据分析可知:1)自榨原油中3-MCPD脂肪酸酯含量均小于0.096 1 mg/kg,市售原油中的3-MCPD脂肪酸酯范围在0.168 0~1.947 2 mg/kg,远大于自榨原油的含量,这与市售植物油的加工方式及加工过程有着密切的关系。2)在传统中药理念看来食用和药用价值很高的山茶原油中的3-MCPD脂肪酸酯的含量较高,高于一般的市售用油。3)市售植物油在经微波加热后3-MCPD脂肪酸酯含量基本增加(市售葵仁油除外),其中芝麻油、菜籽油、花生油的增加最为明显,增量均超过2 mg/kg,其他市售植物油则为小范围地增加。
2.2 油脂微波加热模型
2.2.1 NaCl溶液对3-MCPD脂肪酸酯形成的影响
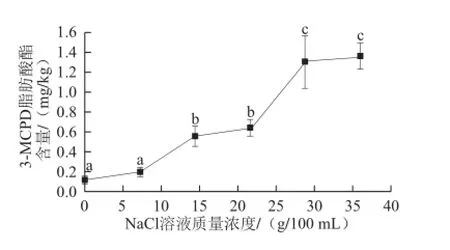
图2 NaCl溶液质量浓度对3-MCPD脂肪酸酯形成的影响Fig.2 Formation of 3-MCPD in the model system containing NaCl at various concentrations
在日常的烹饪中,NaCl和水是不可或缺的因素,参与3-MCPD脂肪酸酯反应的Cl-一般是由NaCl溶液离子化而得,因此3-MCPD脂肪酸酯的形成和NaCl溶液质量浓度有着密切的联系。如图2所示,添加不同量的NaCl溶液后,油脂中3-MCPD脂肪酸酯含量呈现差异性,且随着NaCl溶液质量浓度的增加而增加,并在36 g/100 mL(饱和溶液)时达到最大值1.369 0 mg/kg。因此在微波烹饪过程中,可以通过降低NaCl溶液质量浓度来减少3-MCPD脂肪酸酯的产生。

图3 NaCl溶液体积分数对3-MCPD脂肪酸酯形成的影响Fig.3 Formation of 3-MCPD in the model system containing NaCl solution at various ratios
除了NaCl溶液质量浓度之外,NaCl溶液的体积分数同样也会影响3-MCPD脂肪酸酯的形成,如图3所示,不同NaCl溶液体积分数的样品中3-MCPD脂肪酸酯含量呈现一定的差异性。当NaCl溶液占混合溶液的0%~20%时,3-MCPD脂肪酸酯的含量随着NaCl溶液的体积分数增加而增加。继续增加NaCl溶液体积分数时,3-MCPD脂肪酸酯含量随着体积分数增加而减少,当超过60%后,3-MCPD脂肪酸酯含量与0%时的含量无显著性差异(P>0.05),在80%时达到最小值0.175 8 mg/kg,甚至低于0%的0.230 4 mg/kg。
在微波加热中,当NaCl溶液体积分数在0%~20%范围内,Cl-的增加会有利于3-MCPD脂肪酸酯的形成,并在20%时Cl-达到相对饱和状态。若继续增加Cl-,促进作用不再明显增加。然而,因为NaCl溶液的增加对油脂产生了稀释作用,造成了形成反应的空间阻碍,3-MCPD脂肪酸酯含量随之减少。所以,在微波烹饪过程中,降低油脂的含量(NaCl溶液体积分数大于20%)可抑制3-MCPD脂肪酸酯的形成。
2.2.2 pH值对3-MCPD脂肪酸酯形成的影响
由图4可知,当pH<5.5时,不同pH值样品中3-MCPD脂肪酸酯含量呈显著性差异(P<0.05),且随着pH值的增加而降低,在pH 4.0达到最大值12.710 1 mg/kg。当pH>5.5时,各pH值样品中3-MCPD脂肪酸酯含量无显著性差异(P>0.05)。因此,酸性pH值环境对3-MCPD脂肪酸酯的形成具有促进作用,碱性环境对3-MCPD脂肪酸酯形成的影响不明显。这表明3-MCPD脂肪酸酯的形成反应中很可能有氢离子的参与,存在酸水解反应。可以通过控制pH值来抑制微波烹饪过程中3-MCPD脂肪酸酯的形成。
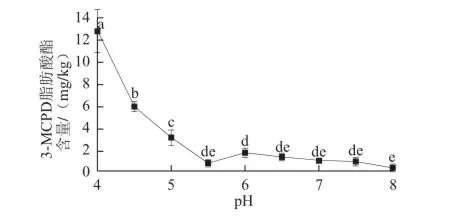
图4 pH值对3-MCPD脂肪酸酯形成的影响Fig.4 Formation of 3-MCPD in the model system with microwave heating at different pH
2.2.3 微波时间对3-MCPD脂肪酸酯形成的影响
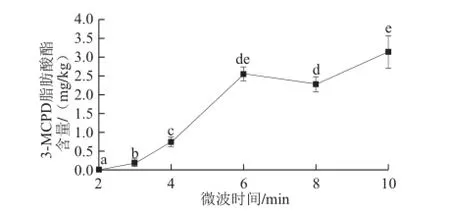
图5 微波时间对3-MCPD脂肪酸酯形成的影响Fig.5 Formation of 3-MCPD in the model system with microwave heating for different periods of time
鉴于日常微波烹饪一般在10 min以内,因此本实验选取了10 min内的6 个时间点作研究,得出微波时间与3-MCPD脂肪酸酯形成之间的关系。由图5可知,不同时间的微波加热后,油脂中3-MCPD脂肪酸酯含量呈显著性差异(P<0.05),且随微波时间的增加而增加,10 min达到最大值3.141 5 mg/kg,2 min时3-MCPD脂肪酸酯含量未检出。结果表明,2 min时间内的微波加热对3-MCPD脂肪酸酯的形成影响较小。因此,减少微波的时间能降低烹饪中3-MCPD脂肪酸酯的产生。
2.2.4 不连续微波对3-MCPD脂肪酸酯形成的影响

图6 不连续微波加热对3-MCPD脂肪酸酯形成的影响Fig.6 Formation of 3-MCPD in the model system with intermittent microwave heating
微波最常用于熟食和方便食品的二次加热,因此有必要对油脂的微波多次不连续加热进行考察,以探究微波的不连续加热对油脂中3-MCPD脂肪酸酯形成的影响。由图6可知,不同加热方式的样品中3-MCPD脂肪酸酯含量呈显著性差异(P<0.05),连续微波6 min后,油脂中的3-MCPD脂肪酸酯含量最高为2.553 1 mg/kg,在总微波时间不变的情况下,多次不连续微波后油脂中的3-MCPD脂肪酸酯含量均远小于连续微波6 min,其中6 次微波1 min的油脂中3-MCPD脂肪酸酯含量未检出。因此,在微波时间相同的情况下,不连续微波加热产生的3-MCPD脂肪酸酯更少。
2.2.5 金属元素对3-MCPD脂肪酸酯形成的影响

图7 金属离子对3-MCPD脂肪酸酯形成的影响Fig.7 Formation of 3-MCPD in the model system containing different metal ions
Cindric等[17]研究表明,不同的油脂中微量元素的含量不尽相同,实验研究了7 种常见的金属离子对3-MCPD脂肪酸酯形成的影响。由图7可知,添加金属离子的样品组的3-MCPD脂肪酸酯含量与空白组呈显著性差异(P<0.05),且含量远远大于空白组的0.579 4 mg/kg。其中添加Ca2+的样品中3-MCPD脂肪酸酯含量最低为33.504 2 mg/kg,远远大于空白组,这表明金属离子能大大地促进3-MCPD脂肪酸酯的形成,这是因为金属离子在3-MCPD脂肪酸酯的形成反应中作为催化剂参与反应,促进了如酰基氧鎓离子和环氧环等活性中间物的形成。Zn2+、Al3+、Fe2+3 组的3-MCPD脂肪酸酯含量无显著性差异(P>0.05),即三者对3-MCPD脂肪酸酯形成的促进作用相当。其中,Fe3+的促进效果最为明显,Fe3+组的3-MCPD脂肪酸酯含量最高为990.609 0 mg/kg,同为铁元素的Fe2+组含量仅有111.615 1 mg/kg,与Fe3+组相差近7 倍,因此Fe3+在3-MCPD脂肪酸酯形成反应中的催化剂效应远强于Fe2+。鉴于金属离子的显著促进作用,微波烹饪时应尽可能地避免金属离子的存在。
3 结 论
本实验通过建立油脂的微波加热模型,研究微波加热对油脂中3-MCPD脂肪酸酯形成的影响。结果表明:3-MCPD脂肪酸酯的形成与NaCl、pH值、时间、不连续微波以及金属离子等因素均有着密切的联系,其中金属离子作为催化剂能明显地促进3-MCPD脂肪酸酯的形成。因此,在不影响正常微波烹饪前提下,应该合理地控制食盐的用量,减少加热时间,尽量避免酸性物质以及金属离子的参与,以减少3-MCPD脂肪酸酯的产生。
参考文献:
[1] BREITLING-UTZMANN C M, KOBLER H, HERBOLZHEIMER D, et al. 3-MCPD: occurrence in bread crust and various food groups as well as formation in toast[J]. Deut Lebensm-Rundsch, 2003, 99(7): 280-285.
[2] HAMLET C G, SADD P A, GRAY D A, et al. Chloropropanols and their esters in baked cereal products[J]. Czech Journal of Food Sciences, 2004, 22: 259-262.
[3] HAMLET C G, SADD P A, CREWS C, et al. 3-Monochloropropane-1,2-diol (3-MCPD) in food ingredients from UK food producers and ingredient suppliers[J]. Food Additives Contaminants, 2002, 19(1): 15-21. [4] DOLEZAL M, CHALOUPSKA M, DIVINOVA V, et al. Occurrence of 3-chloropropane-1,2-diol and its esters in coffee[J]. European Food Research and Technology, 2005, 221(3/4): 221-225.
[5] KUNTZER J, WEISSHAAR R. 3-MCPD-the smoking process- A potent source for 3-chloropropane,1,2-diol (3-MCPD) in meat products[J]. Deutsche Lebensmittel-Rundschau, 2006, 102(9): 397-400.
[6] WEISSHAAR R. Fatty acid esters of 3-MCPD: overview of occurrence and exposure estimates[J]. European Journal of Lipid Science and Technology, 2011, 113(3): 304-308.
[7] HAMLETY C G, SADD P A, CREWS C. Occurrence of 3-chloropropane-1,2-diol (3-MCPD) and related compounds in foods: a review[J]. Food Additives and Contaminants, 2002, 19(7): 619-631.
[8] SCHLATTER J, BAARS A, DINOVI M, et al. Safety evaluation of certain food additives and contaminants, prepared by the fifty-seventh meeting of the joint FAO/WHO Expert Committee on food additives series[M]. Geneva: FAO/WHO Expert Committee on Food Additives (JECFA), 2002.
[9] RAHN A K K, YAYLAYAN V A. What do we know about the molecular mechanism of 3-MCPD ester formation[J]. European Journal of Lipid Science and Technology, 2011, 113: 323-329.
[10] COLLIER P D, CROMIE D D O, DAVIES A P. Mechanism of formation of chloropropanols present in protein hydrolysates[J]. Journal of the American Oil Chemists Society, 1991, 68: 785-790.
[11] VELISEK J, DOLEZAL M, CREWS C, et al. Optical isomers of chloropropanediols: mechanisms of their formation and decomposition in protein hydrolysates[J]. Czech Journal of Food Sciences, 2002, 20(5): 161-170.
[12] SONNET P E. A short highly regio-and stereoselective synthesis of triacylglycerols[J]. Chemistry and Physics of Lipids, 1991, 58(1/2): 35-39.
[13] SVEJKOVSKA B, DOLEZAL M, VELISEK J. Formation and decomposition of 3-chloropropane-1,2-diol esters in models simulating processed foods[J]. Czech Journal of Food Sciences, 2006, 24(4): 172-179.
[14] VELISEK J, CALTA P, CREWS C, et al. 3-Chloropropane-1,2-diol in models simulating processed foods: precursors and agents causing its decomposition[J]. Czech Journal of Food Sciences, 2003, 21(5): 153-161.
[15] CALTA P, VELISEK J, DOLEZAL M, et al. Formation of 3-chloropropane-1,2-diol in systems simulating processed foods[J]. European Food Research and Technology, 2004, 218: 501-506.
[16] 周勇强, 李昌, 聂少平, 等. 气相色谱-质谱联用法测定食用油中3-MCPD脂肪酸酯[J]. 中国粮油学报, 2014, 29(3): 110-113.
[17] CINDRIC I J, ZEINER M, STEFFAN I. Trace elemental characterization of edible oils by ICP-AES and GFAAS[J]. Microchemical Journal, 2007, 85(1): 136-139.
Formation of 3-Chloropropane-1,2-diol in Microwave Heating Model of Edible Oil
ZHOU Yong-qiang, LI Chang, ZHU Jian-peng, NIE Shao-ping*
(State Key Laboratory of Food Science and Technology, Nanchang University, Nanchang 330047, China)
A series of experiments have been conducted to establish a model system through microwave heating to explore the formation of 3-chloropropane-1,2-diol (3-MCPD) in edible oil as a function of oil type, NaCl, pH, heating time, intermittent microwave heating and metal ions. The results showed that 1) microwave heating resulted in formation of over 9 mg/kg 3-MCPD in hot-pressed oils, whereas much less 3-MCPD was formed in cold-pressed oils and commercial oils; 2) the amount of 3-MCPD esters increased with increasing concentration of sodium chloride solution, and increased firstly and then decreased with increasing proportion of sodium chloride solution added, reaching maximum value at 20%; 3) acidic condition could promote the formation of 3-MCPD; 4) the amount of 3-MCPD increased with increasing time up to 10 minutes; 5) compared to continuous microwave heating for an equal time, intermittent microwave heating could inhibit the production of 3-MCPD; and 6) metal ions could significantly promote the formation of 3-MCPD esters because metal ions could act as catalysts to promote the formation of intermediates during the formation of 3-MCPD. Therefore, this study can be regarded as a data support for limiting the formation of 3-MCPD esters during microwave heating of foods.
microwave; 3-chloropropane-1,2-diol (3-MCPD) esters; NaCl; pH; time; intermittent microwave; metal ions
TS227
A
1002-6630(2014)17-0036-05
10.7506/spkx1002-6630-201417008
2014-03-19
“十二五”国家科技支撑计划项目(2014BAD04B03);国家重点基础研究发展计划(973计划)项目(2012CB720805)
周勇强(1990—),男,硕士,研究方向为食品安全。E-mail:ncuskzhouyongqiang@163.com
*通信作者:聂少平(1978—),男,教授,博士,研究方向为食品化学与分析、食品营养与安全。E-mail:spnie@ncu.edu.cn
