典型酚类化合物清除亚硝酸钠及对二乙基亚硝胺生成的影响
2014-01-18董彦佐李学理何秀丽
董彦佐,李学理,何秀丽,何 强*
(四川大学轻纺与食品学院,四川 成都 610065)
典型酚类化合物清除亚硝酸钠及对二乙基亚硝胺生成的影响
董彦佐,李学理,何秀丽,何 强*
(四川大学轻纺与食品学院,四川 成都 610065)
在不同酚与亚硝酸钠物质量比、温度和pH值条件下,研究5 种典型酚类化合物(苯酚、邻苯二酚、间苯二酚、对苯二酚和连苯三酚)对亚硝酸钠的清除和对二乙基亚硝胺(diethylnitrosamine,NDEA)生成的影响。结果表明:5 种酚类化合物对亚硝酸钠都具有一定的清除作用,并随酚含量增加作用增强,其清除能力从强到弱依次为间苯二酚、邻苯二酚、连苯三酚、对苯二酚、苯酚,酸性环境和升高温度有利于清除作用。连苯三酚、对苯二酚和邻苯二酚在较低的浓度下就可显著抑制NDEA生成;苯酚不但不具有抑制作用,反而促进了NDEA生成;间苯二酚在低浓度时表现为促进作用,但在高浓度时可显著抑制NDEA生成。升高温度和弱酸性环境有利于酚类化合物对NDEA的抑制作用。
亚硝酸钠;二乙基亚硝胺;酚类化合物;清除;抑制
作为护色剂和防腐剂,亚硝酸盐在食品加工中应用广泛,但其安全性也深受人们关注[1]。此外,在微生物作用或酸性条件下,亚硝酸盐可与食物分解产生的胺作用,生成具有强致癌性的亚硝胺[2]。正因为此,如何清除亚硝酸盐以及如何阻断亚硝胺合成就显得特别重要。某些食源性多酚对亚硝酸盐表现出了一定的清除作用,如茶多酚[3-4]、苹果多酚[5]、石榴皮多酚[6]、荔枝皮色素[7]、紫薯花色苷[8]等。由于这些食源性多酚通常成分复杂,难以从构效关系上讨论对亚硝酸钠的清除特性,也不能揭示其影响亚硝胺形成的机理。 基于此,本实验以几种典型简单酚(苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚)为对象,研究它们对亚硝酸钠的清除和对二乙基亚硝胺(diethylnitrosamine,NDEA)形成的阻断作用,探讨了反应物的物质量比、温度和pH值条件对清除和阻断作用的影响,本研究结果可为揭示其作用机理提供参考。
1 材料与方法
1.1 材料与试剂
苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚、亚硝酸钠、盐酸萘乙二胺、乙二胺、柠檬酸、柠檬酸钠为分析纯,二乙基亚硝胺为色谱纯,均购自成都科龙化工试剂厂。
以30%醋酸配制对氨基苯磺酸溶液(0.5%)和盐酸萘乙二胺溶液(0.1%),以蒸馏水配制亚硝酸钠储备液(100 mmol/L)和使用液,上述溶液避光保存。
1.2 仪器与设备
UV-1800 PC紫外-可见分光光度计 上海美谱达仪器有限公司;Agilent 1100液相色谱系统 美国Agilent公司;HWS-26电热恒温水浴锅 上海齐欣科学仪器有限公司。
1.3 方法
1.3.1 亚硝酸钠和NDEA分析
基于盐酸萘乙二胺法[9]获得在550 nm波长处亚硝酸钠标准曲线方程:Y = 0.196 8X+0.015 5(R² = 0.999 4),X为亚硝酸钠浓度/(mmol/L),Y为吸光度,线性范围0~0.1 mmol/L。取1 mL样品溶液,加入1.5 mL对氨基苯磺酸溶液,摇匀静置5 min后,加入1.5 mL盐酸萘乙二胺溶液,在550 nm波长处测定吸光度Ai,以0.05 mmol/L亚硝酸钠溶液替代样品溶液,同样方法测得空白组吸光度A0,按下式计算酚对亚硝酸钠的清除率。

基于高效液相色谱法[10]分析NDEA。Agilent 1 1 0 0液相色谱系统,A r c h r o m B o n d-A Q C18(150 mm × 4.6 mm,5 μm)反相色谱柱,进样量30 μL,柱温30 ℃,流动相为甲醇-水(35∶65,V/V),流速1 mL/min,检测波长 230 nm。测定样品中NDEA浓度(c),加入相同体积的蒸馏水代替酚溶液作为空白对照,测定空白组中NDEA浓度(c0),以NDEA相对生成量c/c0表征酚对NDEA生成的影响。若c/c0>1,表示所添加酚促进了NDEA 的生成,若c/c0≤1则表明抑制了NDEA 生成。
1.3.2 不同条件下酚对亚硝酸钠的清除特性影响
1.3.2.1 酚与钠的物质量比对亚硝酸钠的清除特性影响
在20 mL刻度试管中分别加入1 mL 0.05 mmol/L亚硝酸钠溶液,再分别加入0.1、0.2、0.5、1、2、5、10 mL 0.05 mmol/L各酚溶液(苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚),用pH 3的柠檬酸-柠檬酸钠溶液定容至20 mL,在37 ℃恒温水浴中反应4 h,在550 nm波长处测定吸光度,计算其清除率。实验中加入相同体积的蒸馏水代替酚溶液,作为空白组。
1.3.2.2 温度对亚硝酸钠的清除特性影响
在20 mL刻度试管中分别加入1 mL 0.05 mmol/L亚硝酸钠溶液,再分别加入1 mL 0.05 mmol/L苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚溶液,用pH 3的柠檬酸-柠檬酸钠溶液定容至20 mL,分别在4、25、37、60、100 ℃恒温水浴中反应4 h,在550 nm波长处测定吸光度,计算其清除率。实验中加入相同体积的蒸馏水代替酚溶液,作为空白组。
1.3.2.3 pH值对亚硝酸钠的清除特性影响
参照1.3.2.2节将反应物混合,分别用pH 2、3、4、5、6的柠檬酸-柠檬酸钠溶液定容至20 mL,在37 ℃恒温水浴中反应4 h,在550 nm波长处测定吸光度,计算其清除率。实验中加入相同体积的蒸馏水代替酚溶液,作为空白组。
1.3.3 不同条件下酚对NDEA生成的影响
由于NDEA形成缓慢,实验中采用了较高浓度的反应物和酚浓度,以模拟NDEA的生成过程,研究酚类化合物对反应的影响。
1.3.3.1 酚与钠的物质量比对NDEA生成的影响
在10 mL刻度试管中分别加入1 mL 100 mmol/L亚硝酸钠溶液和4 mL 100 mmol/L乙二胺溶液,再分别加入0.2、0.4、0.6、0.8、1.0、1.2 mL 100 mmol/L各酚溶液(苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚),用pH 3的柠檬酸-柠檬酸钠溶液定容至10 mL,在37 ℃恒温水浴中反应24 h后,加入0.05 g对氨基苯磺酸终止亚硝化反应,测定反应液中NDEA浓度(c)和空白组中NDEA浓度(c0),并计算NDEA相对生成量(c/c0)。
1.3.3.2 温度对NDEA生成的影响
在10 mL刻度试管中分别加入1 mL 100 mmol/L亚硝酸钠溶液和4 mL 100 mmol/L乙二胺溶液,再分别加入邻苯二酚、对苯二酚、连苯三酚溶液(均为0.4 mL)和间苯二酚溶液(1 mL),用pH 3的柠檬酸-柠檬酸钠溶液定容至10 mL,在4、37、60、80 ℃恒温水浴反应24 h后,加入0.05 g对氨基苯磺酸终止亚硝化反应,测定反应液中NDEA浓度(c)和空白组中NDEA浓度(c0),并计算NDEA相对生成量(c/c0)。
1.3.3.3 pH值对NDEA生成的影响
参照1.3.3.2节将反应物混合,用pH 2、3、4、5、6的柠檬酸-柠檬酸钠溶液定容至10 mL,在37℃恒温水浴反应24 h后,加入0.05 g对氨基苯磺酸终止亚硝化反应,测定反应液中NDEA浓度(c)和空白组中NDEA浓度(c0),并计算NDEA相对生成量(c/c0)。
1.4 数据处理
2 结果与分析
2.1 不同条件下酚对亚硝酸钠清除特性的影响结果
2.1.1 酚与钠的物质的量比对亚硝酸钠清除特性的影响
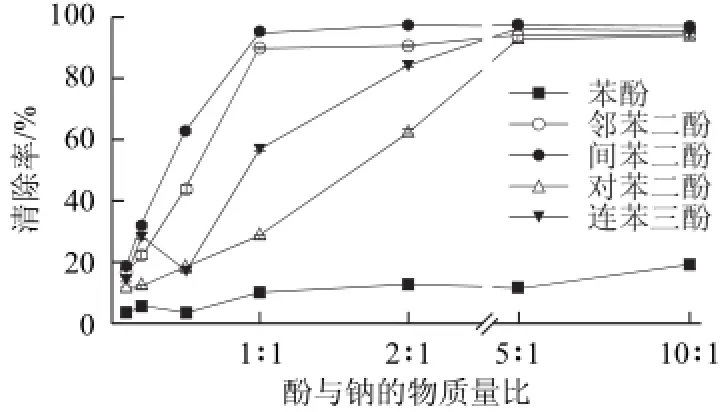
图1 不同酚与钠的物质的量比条件下酚对亚硝酸钠的清除特性Fig.1 Scavenging effects of penols at different ratios of sodium nitrite to phenols
由图1可知,在37 ℃、pH 3、反应4 h的条件下,苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚对亚硝酸钠都表现出了一定的清除作用,随着酚与钠的物质量比增加,清除率逐渐升高。邻苯二酚和间苯二酚表现了较强的清除作用,在酚与钠的物质量比为1∶1时,4 h内对亚硝酸钠的清除率分别达(89.63±0.5)%和(95.2±0.8)%。连苯三酚虽然有较多数量的酚羟基,但其清除能力弱于前两者,这可能与连苯三酚极易被空气氧化而稳定性较差有关。对苯二酚对亚硝酸钠的清除能力相对较低,在物质量比5∶1时达到较高水平(92.9±0.5)%,而苯酚体现了最弱的清除能力。有研究表明酚羟基具有一定的抗氧化活性,可与亚硝酸盐发生反应,从而达到清除效果[11]。酚类化合物的抗氧化性与其分子结构密切相关,因酚羟基位置和数量的不同[12],与亚硝酸盐表现出不同的反应特性,通常较多的酚羟基具有更强的反应能力。苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚对亚硝酸钠表现了不同的清除能力,这应源于不同位置和数量酚羟基的综合作用结果。
2.1.2 温度对亚硝酸钠清除特性的影响

图2 不同温度条件下酚对亚硝酸钠的清除率Fig.2 Sodium nitrite-scavenging rates of phenols at different temperatures
为了反映在生物体和食品贮藏、加工环境下酚类化合物对亚硝酸盐的清除特性,实验中以4 ℃和25 ℃分别模拟冷藏和室温,以60 ℃和100 ℃模拟热加工和高温条件,而以37 ℃反映人体温度。由图2可知,在酚与钠的物质量比1∶1、pH 3、反应4 h的条件下,随着温度升高,各酚类化合物对亚硝酸钠的清除能力逐渐增强,不同酚清除能力强弱顺序与前述结果相同。低温条件下(4 ℃),间苯二酚与其他酚相比,可实现相对较高的亚硝酸钠清除率,在酚与钠物质量比1∶1条件下其清除率达(63.4±0.7)%。37 ℃条件下,间苯二酚和邻苯二酚接近其清除能力的最大值,进一步提高温度没有本质改变。升高温度可显著提高连苯三酚对亚硝酸钠的清除率到(92.5±0.6)%,而对苯二酚和苯酚即使在高温条件下对亚硝酸钠的清除也维持在较低的水平。
2.1.3 pH值对亚硝酸钠清除特性的影响
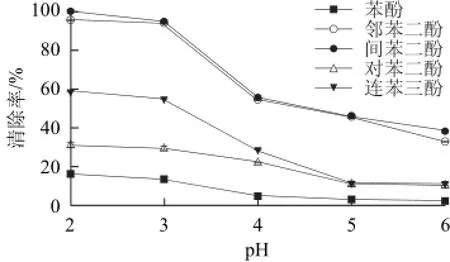
图3 不同pH值条件下酚对亚硝酸钠的清除率Fig.3 Sodium nitrite-scavenging rates of phenols at different pH values
酚在酸性条件下表现了较强的亚硝酸钠清除能力,由图3可知,在酚与钠的物质量比1∶1、37℃、反应4 h的条件下,随pH值降低清除率逐渐增大,在pH 3时达到相对稳定,这一结果与文献[13-14]研究结果一致。酚羟基在酸性介质中结构稳定,具有更强的抗氧化性,而亚硝酸钠在低pH值条件下可与H+结合生成亚硝酸,易被酚类化合物还原为NO,或与酚类化合物发生取代反应,从而使得亚硝酸根含量降低[15-17]。由于酚羟基位置和数量不同以及各化合物的稳定性差异,苯酚、邻苯二酚、间苯二酚、对苯二酚、连苯三酚具有不同的亚硝酸钠清除特性。总体而言,邻苯二酚和间苯二酚具有较强和相似的清除能力,其他3 种酚的清除能力顺序为连苯三酚>对苯二酚>苯酚。
2.2 不同条件下酚对NDEA生成的影响
2.2.1 酚与钠的物质量比对NDEA生成的影响
通过在酸性条件下亚硝酸钠与乙二胺作用(亚硝化),模拟二乙基亚硝胺(NDEA)的生成过程,研究了酚对亚硝胺类化合物形成的影响,结果见图4。

图4 不同酚与钠的物质的量比条件下酚对NDEA生成的影响Fig.4 Effects of phenols on the synthesis of NDEA at different ratios of phenols to sodium nitrite
由图4可知,在连苯三酚、对苯二酚和邻苯二酚存在的条件下,NDEA相对生成量c/c0<1,表明这3 种酚对NDEA的形成具有较强的抑制作用,随着酚与钠物质量比增大,其抑制作用增强,直至完全抑制NDEA的形成(c/c0=0)。这可能由于连苯三酚、对苯二酚和邻苯二酚可与乙二胺竞争性地与亚硝酸钠作用,生成较稳定的醌,阻断了亚硝酸钠与乙二胺的作用,从而抑制了NDEA的生成[12]。间苯二酚在较高的酚与钠物质量比≥0.8∶1条件下,对NDEA的形成具有一定的抑制作用(NDEA相对生成量c/c0<1),但在较低酚/钠物质量比条件下,对NDEA的形成却体现了较强的促进作用(NDEA相对生成量c/c0>1)。这可能是因为间苯二酚不能被氧化成醌,它与亚硝酸钠发生亲电取代反应,可生成亚硝基苯酚,而该类物质可极大地催化亚硝酸钠与乙二胺作用生成NDEA[15]。在高的酚/钠物质量比条件下,间苯二酚可通过极强的亚硝酸钠清除作用(如前所述)抑制NDEA生成,在物质量比1.2∶1时,其抑制程度达100%(c/c0=0)。苯酚对NDEA的形成具有较强的促进作用,在酚与钠物质量比0.6∶1时达到最大,这一方面是由于苯酚较弱的亚硝酸盐清除能力所致,另一方面与间苯二酚类似,其与亚硝酸钠的作用产物可能催化了亚硝酸钠与乙二胺之间的亚硝化反应[18]。在酚与钠物质量比0.4∶1时,邻苯二酚、对苯二酚、连苯三酚可很好地抑制亚硝酸钠与乙二胺之间的亚硝化反应,而间苯二酚在高浓度时(酚与钠物质量比1∶1)也具有良好的抑制作用。
2.2.2 温度对NDEA生成的影响

图5 不同温度条件下酚对NDEA生成的影响Fig.5 Effects of phenols on the synthesis of NDEA at different temperatures
有研究[19]表明,温度每升高10 ℃,亚硝胺的合成速率可增加一倍。由图5可知,随着温度升高,NDEA相对生成量(c/c0)逐渐降低,在80 ℃时各测试酚c/c0值都低于0.2,表明极大程度地抑制了亚硝酸钠与乙二胺之间的亚硝化反应(酚对NDEA生成抑制率>80%)。基于此,可以推断在高温条件下,邻苯二酚、对苯二酚、连苯三酚和间苯二酚对NDEA生成的抑制应主要源于它们对亚硝酸钠的清除作用。
2.2.3 pH值对NDEA生成的影响
由图6可知,pH值对邻苯二酚、对苯二酚和连苯三酚抑制NDEA生成能力的影响不大。虽然前述研究结果表明pH 3.0有利于酚清除亚硝酸钠,但在该环境条件下,各酚可能因较大程度地促进了亚硝酸钠与乙二胺之间的亚硝化反应,从而导致了较高的NDEA相对生成量(c/c0),这与文献[20]研究结果一致。随着pH值增大,各测定酚的c/c0逐渐减小,在pH 6.0时几乎完全抑制了NDEA的生成。由于在pH 6.0条件下,酚对亚硝酸钠的清除作用较弱,所以各酚对亚硝酸钠与乙二胺之间亚硝化反应的完全抑制,是该条件下酚抑制NDEA生成的主要原因。

图6 不同pH值条件下酚对NDEA生成的影响Fig.6 Effect of phenols on the synthesis of NDEA at different pH values
3 讨 论
如何清除亚硝酸盐以及阻断亚硝胺的生成是当前食品安全领域的研究热点,而食源性多酚可通过氧化还原反应和取代反应,消除环境中的亚硝酸盐。此外酚类化合物还可通过多种途径抑制亚硝酸盐与胺类化合物之间的亚硝化反应,从而降低亚硝胺类化合物风险。由于结构(酚羟基数量和位置)和自身稳定性不同,各酚类化合物具有不同的亚硝酸盐清除能力,对NDEA的生成也产生了不同的影响。本实验有助于从构效关系上,揭示酚类化合物清除亚硝酸盐和抑制亚硝胺生成的机理,同时也有助于食品生产中合理地选择和使用不同酚类化合物,以降低亚硝酸盐和亚硝胺的潜在健康风险。
[1] 皇甫超申, 许靖华, 秦明周, 等. 亚硝酸盐与癌的关系[J]. 河南大学学报: 自然科学版, 2009, 39(1): 35-41.
[2] 李玲, 夏天兰, 徐幸莲, 等. 肉制品和胃酸条件下亚硝胺合成阻断作用的研究进展[J]. 食品科学, 2013, 34(5): 284-288.
[3] 吴彬彰, 赵阳, 王剑清, 等. 茶多酚对外源性亚硝酸盐清除作用的研究[J]. 癌变·畸变·突变, 2010, 22(6): 473-476.
[4] PANZELLA L, MANINI P, NAPOLITANO A, et al. The acidpromoted reaction of the green tea polyphenol epigallocatechin gallate with nitrite ions[J]. Chemical Research in Toxicology, 2005, 18(4): 722-729.
[5] 李桂星, 胡晓丹, 孙红男, 等. 模拟胃液条件下苹果多酚对亚硝酸盐的清除作用[J]. 食品科学, 2011, 32(11): 1-4.
[6] 刘钢, 贾冬英, 赵甲元, 等. 石榴皮多酚提取物对亚硝酸盐的体外清除作用研究[J]. 中国调味品, 2011, 36(7): 41-44.
[7] 宋茹, 韦荣, 胡金申, 等. 荔枝皮色素体外清除亚硝酸盐作用研究[J].食品科学, 2010, 31(5): 104-107.
[8] 王莹. 模拟胃酸条件下紫甘薯花色苷清除亚硝酸盐的效果[J]. 食品科学, 2009, 30(5): 109-111.
[9] 周文斌. 泡菜中亚硝酸盐测定方法研究[J]. 食品科学, 2006, 27(2): 241-243.
[10] 姜慧萍. 黄酮类化合物体外抑制N-亚硝基二乙胺生成的研究[D]. 杭州: 浙江工商大学, 2009.
[11] 孙艳辉, 董英. 壳聚糖对亚硝酸盐清除作用的研究[J]. 食品科学, 2005, 26(12): 71-73.
[12] 汪锋, 杜美霞, 郑群雄. 不同结构黄酮类化合物对阻断亚硝胺合成能力关系的研究[J]. 江苏预防医学, 2010, 21(5): 14-16.
[13] 陈秋丽, 蔡秀成, 郭英. 葡多酚, 大豆异黄酮和大豆皂苷对亚硝酸盐的清除作用[J]. 中国卫生检验杂志, 2009, 18(12): 2577-2578.
[14] 张瑞宇, 王词钦. 香辛蔬菜苦藠粗提液对亚硝酸盐的清除作用[J].食品科学, 2010, 31(17): 86-91.
[15] 吴永宁, 王淮洲. 食物中酚类对亚硝胺体内外合成的影响[J]. 国外医学: 卫生学分册, 1985, 1(5): 282-285.
[16] BALZER J, RASSAF T, KELM M. Reductase activity of polyphenols: a commentary on “red wine-dependent reduction of nitrite to nitric oxide in the stomach”[J]. Free Radical Biology and Medicine, 2007, 43(9): 1226-1228.
[17] ROCHA B S, GAGO B, BARBOSA R M, et al. Dietary polyphenols generate nitric oxide from nitrite in the stomach and induce smooth muscle relaxation[J]. Toxicology, 2009, 265(1): 41-48.
[18] WALKER E A, PIGNATELLI B, FRIESEN M. The role of phenols in catalysis of nitrosamine formation[J]. Journal of the Science of Food and Agriculture, 1982, 33(1): 81-88.
[19] FOREMAN J K, GOODHEAD K. The formation and analysis of N-nitrosamines[J]. Journal of the Science of Food and Agriculture, 1975, 26(11): 1771-1783.
[20] 杨华, 孟培培, 王昌禄, 等. 模拟肉制品加工条件下影响N-亚硝胺的形成因素[J]. 食品工业科技, 2013, 34(16): 95-99.
Scavenging of Sodium Nitrite and Inhibition of Diethylnitrosamine Formation by Typical Phenols
DONG Yan-zuo, LI Xue-li, HE Xiu-li, HE Qiang*
(College of Light Industry, Textile and Food Engineering, Sichuan University, Chengdu 610065, China)
The scavenging effects of fi ve typical phenols on sodium nitrite under varying conditions of phenol-to-nitrite molar ratio, temperatur e and pH were investigated as well as the inhibitory effects on the synthesis of diethylnitrosamine (NDEA). Results showed that the fi ve phenols were all capable of scavenging sodium nitrite in a concentration-dependent manner, and their scavenging capabilities followed the decreasing order: 1,3-benzenediol > o-benzenediol > pyrogallol >p-benzenediol > phenol. A higher temperature and an acid condition promoted the scavenging of sodium nitrite by phenols. Pyrogallol, p-benzenediol and o-benzenediol could apparently restrain the generation of NDEA at low concentration. Phenol promoted rather than inhibited the generation of NDEA. 1,3-Benzenediol benefi ted NDEA formation at low concentration, but an inhibitory effect was observed at high concentration. The blocking of nitrosamine synthesis by phenols was favored under the conditions of high temperature and weak acid.
sodium nitrite; diethylnitrosamine; phenolic compounds; scavenging; inhibition
TS201.6
A
1002-6630(2014)13-0132-05
10.7506/spkx1002-6630-201413025
2014-06-15
董彦佐(1991—),男,硕士研究生,研究方向为食品安全。E-mail:sunshinezuo@163.com
*通信作者:何强(1971—),男,教授,博士,研究方向为农产品加工及质量安全。E-mail:heq361@163.com
