Ce改性Ti基PbO2电极的制备及电催化氧化4—氯酚的研究
2014-01-15段小月范晓宇宋玉新车海龙
段小月,范晓宇,宋玉新,车海龙,张 俊
(吉林师范大学 环境科学与工程学院,吉林 四平 136000)
4—氯酚(4—CP)是工业中广泛应用的有机化合物,很容易流失到水环境中,但该化合物是典型的难生物降解有机物,一旦通过食物链进入人体内具有致畸、致癌、致突变性[1,2].由于4—CP的毒性会对活性污泥产生抑制作用,因此该类废水不适合采用生物法进行处理.于是科研人员采用各种高级氧化方法降解有机废水[3—5],其中电催化氧化技术具有氧化能力强、有机物降解速度快、操作简单、无二次污染等优点[6],可有效降解4—CP废水.PbO2电极是电催化氧化过程的常用电极,该电极具有电催化活性高、耐腐蚀性强、价格较低等优点[7].因此,前人对Ti基PbO2电极(Ti/PbO2)电极进行了大量研究,有研究表明对PbO2膜层进行合理改性,能提高电极的电催化活性或稳定性[8,9].本文采用Ce对Ti基PbO2电极(Ti/PbO2—Ce)进行改性,以提高Ti/PbO2电极的电催化氧化活性.对改性前后电极的形貌、晶相结构、电化学性能及催化氧化能力进行比较研究,并考察了电催化氧化4—CP废水的可生化性变化.
1 实验部分
1.1 电极的制备
Ti板预处理:将3 cm×5 cm的Ti板用砂纸打磨去除氧化层;用去离子水洗净后置于丙酮、去离子水中各超声10 min;再将钛板置于85 ℃的15%(质量分数)的草酸溶液中刻蚀2 h.
Ti/PbO2电极:先采用热沉积法制备SnO2—Sb2O3底层;然后,采用电沉积法在碱性镀液中电沉积α—PbO2中间层;最后,在酸性镀液中电沉积β—PbO2表面活性层.具体实验细节参考文献[10].
Ti/PbO2—Ce电极:与Ti/PbO2电极的制备方法相同,只是在β—PbO2表面活性层的电沉积液中加入4 mmol/L Ce(NO3)3·6H2O.
1.2 电催化氧化实验
用Ti/PbO2和Ti/PbO2—Ce电极做阳极,不锈钢板做阴极,温度30℃.取200 mL初始质量浓度为50 mg/L的4—CP溶液,用0.05 mol/L的Na2SO4做电解质,在30 mA/cm2的电流密度下电解.
1.3 分析方法
采用4—氨基安替比林直接光度法测定4—CP的浓度;采用SEM测试电极的表面形貌;利用PGSTAT302型电化学工作站进行循环伏安测试,测试中Ti/PbO2和Ti/PbO2—Ce电极为工作电极,饱和甘汞电极(SCE)为参比电极,铂片为辅助电极,扫速为50 mV/s;采用重铬酸钾标准氧化法测定溶液的COD值;采用稀释接种法测定溶液的BOD5;采用Elab型TOC测定仪测定溶液的TOC值.
2 结果与讨论
2.1 电极的形貌与晶体结构
将改性前后的PbO2电极进行SEM和XRD测试,考察改性前后电极表面形貌和晶体结构的变化.
图1是Ti/PbO2和Ti/PbO2—Ce电极的SEM照片.比较可知,Ti/PbO2—Ce电极比Ti/PbO2电极表面更致密,晶体颗粒尺寸更小,仅为Ti/PbO2电极的1/2左右.众所周知,电极的晶粒越小越有利于电极活性表面积的提,可见Ce掺杂可以有效改善电极的表面结构,我们推测具有最小晶体颗粒的Ti/PbO2—Ce电极具有比Ti/PbO2电极更高的催化活性.

图1 不同电极的SEM照片
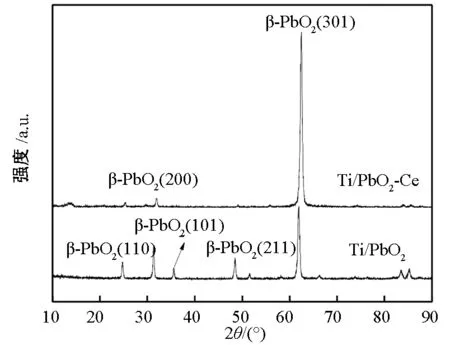
图2 Ti/PbO2和Ti/PbO2—Ce电极的XRD谱图
图2为Ti/PbO2和Ti/PbO2—Ce电极的XRD谱图.将谱图中的衍射峰与标准卡片(卡片号:760564)进行对比分析,所有衍射峰均为β—PbO2晶相的衍射峰,其中在2θ=62.452°处的衍射峰最强,为β—PbO2晶相的(301)晶面.根据Debye—Sherrer公式,利用主峰(301)晶面的半峰宽计算Ti/PbO2和Ti/PbO2—Ce电极的晶粒尺寸分别为48.25 nm和41.78 nm,可见Ti/PbO2—Ce电极的晶粒尺寸远小于Ti/PbO2电极,Ce的掺杂能明显减小β—PbO2的晶粒尺寸,该结果与SEM结果是一致的.这可能是因为电沉积液中Ce离子的引入为PbO2晶粒形成过程提供了新的形核中心,形核数量的增加抑制了PbO2晶粒的生长速度[11].由图还可知,Ti/PbO2—Ce电极的谱图中并无Ce的氧化物衍射峰出现,这是因为PbO2膜层中引入的Ce量较少,没有达到XRD的最低检测限.
2.2 循环伏安
采用循环伏安技术研究了4—CP在 Ti/PbO2电极上的氧化情况,结果如图3a所示.由图可知,在空白Na2SO4溶液中,循环伏安曲线没有任何氧化峰出现.当在电解液中加入4—CP以后,循环伏安曲线都出现一个不可逆的氧化峰,该氧化峰应为4—CP在Ti/PbO2电极表面的氧化峰.图3b为Ti/PbO2和Ti/PbO2—Ce电极在含有200 mg/L 4—CP的0.5 mol/L Na2SO4溶液中的循环伏安曲线.由图可知,4—CP均可在两电极上发生直接氧化反应,但比较两曲线上氧化峰的峰电流和电位,发现Ti/PbO2—Ce电极具有更高的氧化峰电流和相对低的氧化峰电位,说明Ti/PbO2—Ce电极具有较Ti/PbO2电极更强的直接氧化4—CP的能力.
2.3 电催化氧化降解4—CP
图4a为Ti/PbO2和Ti/PbO2—Ce电极电催化氧化降解4—CP过程中4—CP去除率随电解时间的变化曲线.由图可知,电解2 h后,Ti/PbO2—Ce电极能将4—CP完全去除;而Ti/PbO2电极上4—CP的去除率仅为89.8%.电催化氧化有机物过程中,有机物很可能被降解为小分子有机物,而不是直接矿化为二氧化碳和水.为了考察4—CP在电催化氧化过程中的矿化情况,对Ti/PbO2和Ti/PbO2—Ce电极电催化氧化降解4—CP过程中TOC去除率进行了测试,结果如图4b所示.由图可知,两电极上的TOC去除率均随电解时间的延长逐渐增加.3 h电解后,Ti/PbO2—Ce电极的TOC去除率较高,达到77.0%;而Ti/PbO2电极略低,为60.4%.可见,Ce改性能有效提高PbO2电极电催化氧化有机污染物的能力.

图3(a)Ti/PbO2电极在有和无200mg/L4—CP的0.5mol/LNa2SO4溶液中的循环伏安曲线;(b)Ti/PbO2和Ti/PbO2—Ce电极在含有200mg/L4—CP的0.5mol/LNa2SO4溶液中的循环伏安曲线

图4 不同电极4—CP (a)和TOC (b)去除率随电解时间变化曲线
2.4 4—CP降解液可生化性变化分析
电催化氧化技术虽然能有效去除溶液中的有机物,但耗能较高,因此我们考虑将电催化氧化技术与生物法相结合,先采用电催化氧化技术提高溶液的可生化性,再利用生物法继续处理.两者相结合既能有效降解有机废水,又能降低水处理费用.为了考察电催化氧化降解4—CP过程中,溶液的可生化性变化,测试了电解过程中溶液COD和BOD5值的变化情况.图5a和b分别为降解过程中溶液的COD去除率和BOD5/COD变化曲线.由图可知,降解前4—CP溶液的BOD5/COD值仅为0.03,远远小于0.3,可生化性较差.随着电解的持续进行,COD去除率和BOD5/COD值均逐渐升高,说明溶液的可生化性随降解时间的延长而升高.电解90 min后,COD去除率和BOD5/COD值分别为40.59%和0.34,溶液已经具有可生物降解性;当电解120 min后,BOD5/COD达到0.48,溶液的可生化性达到最高,然而此时溶液COD去除率仅为52.61%;之后随着电解的继续进行,COD去除率仍继续升高,但BOD5/COD值却减小.可见,电催化氧化降解4—CP 120 min时,4—CP废水的COD去除率还较低,仅去除一半左右,但溶液的可生化性明显提高,说明如果采用生物法继续处理电催化氧化120 min后的4—CP废水是完全可行的.
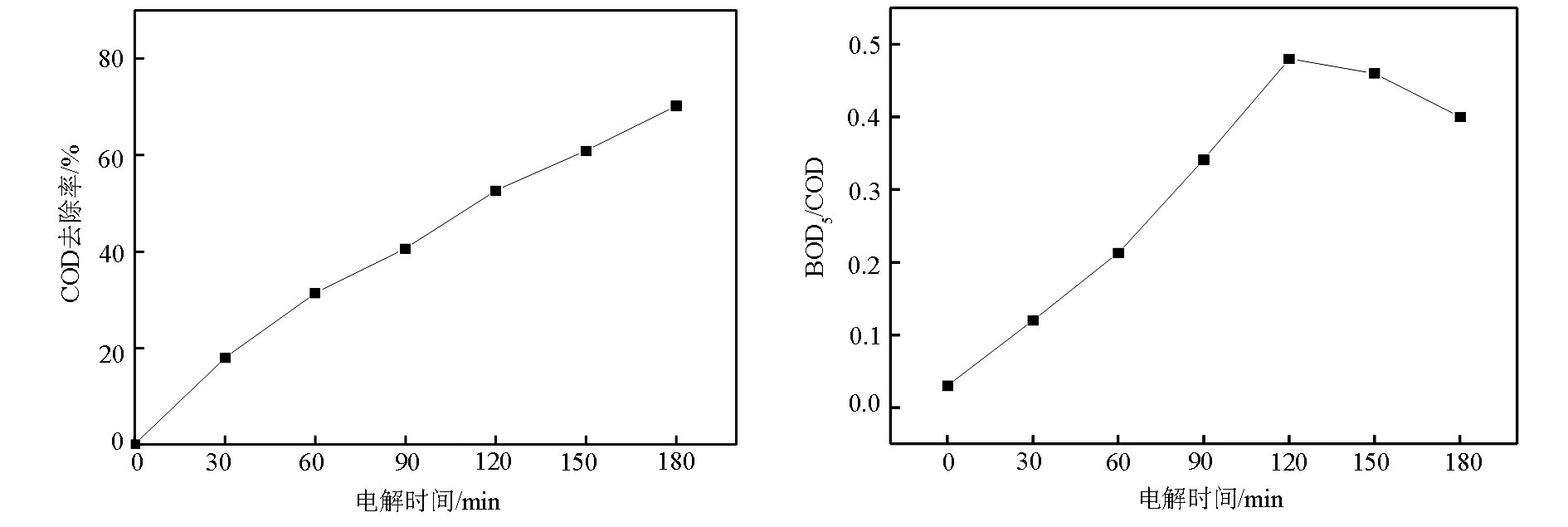
图5 COD去除率和BOD5/COD值随电解时间的变化
3 结论
(1) Ti/PbO2—Ce电极比Ti/PbO2电极表面更致密,晶体颗粒尺寸更小.(2) 在循环伏安测试中,4—CP可以在Ti/PbO2和Ti/PbO2—Ce电极上发生直接氧化反应,且在Ti/PbO2—Ce电极上的氧化峰电流更大,氧化峰电位更低.(3) Ce改性能有效提高PbO2电极电催化氧化有机污染物的能力.(4) Ti/PbO2—Ce电极电催化氧化降解4—CP 2 h后,溶液的BOD5/COD值由0.03升高到0.48,有效地提高了4—CP废水的可生化性.
[1]Wang H,Bian Z Y,Sun D Z.Degradation mechanism of 4-chlorophenol with electrogenerated hydrogen peroxide on Pd/C gas-diffusion electrode [J].Water Science and Technology,2011,63(3):484~490.
[2]Gaya U I,Abdullah A H,Zainal Z,et al.Photocatalytic treatment of 4-chlorophenol in aqueous ZnO suspensions:intermediates,influence of dosage and inorganic anions [J].Journal of Hazardous Materials 2009,168(1):57~63.
[3]任百祥,王丽梅.超声降解糠醛废水的研究[J].吉林师范大学学报(自然科学版),2008,29(3):108~109.
[4]刘 伟,常立民.超声波电解氧化苯酚的研究[J].吉林师范大学学报(自然科学版),2009,30(3):129~131.
[5]李秀艳,王健.ZnO光催化降解甲基橙动力学研究[J].吉林师范大学学报(自然科学版),2011,32(3):13~16.
[6]Nadakatti S,Tendulkar M,Kadam M.Use of mesoporous conductive carbon black to enhance performance of activated carbon electrodes in capacitive deionization technology [J].Desalination,2011,268(1-3):182~188.
[7]Zhan Y,Nie C,Li H,et al.Kinetics and isotherm studies on electrosorption of NaCl by activated carbon fiber,carbon nanotube and carbon nanotube-carbon nanofiber composite film [J].Phys Status Solidi C,2012,9(1):55~58.
[8]Yang W,Yang W,Lin X.Research on PEG modified Bi-doping lead dioxide electrode and mechanism [J].Appl.Surf.Sci.2012,258(15):5716~5722.
[9]Wang Y,Shen Z,Li Y,et al.Electrochemical properties of the erbium-chitosan-fluorine-modified PbO2electrode for the degradation of 2,4-dichlorophenol in aqueous solution [J].Chemosphere 2010,79(10):987~996.
[10]Duan X,Ma F,Yuan Z,et al.Electrochemical degradation of phenol in aqueous solution using PbO2anode[J].Journal of the Taiwan Institute of Chemical Engineers,2013,44(1):95~102.
[11]Casellato U,Cattarin S,Musiani M.Preparation of porous PbO2electrodes by electrochemical deposition of composites[J].Electrochimica Acta,2003,48(27):3991~3998.
