一次方程式听写引起的思考
2014-01-12林秋成
林秋成
(南京市秣陵中学江苏南京211111)
一次方程式听写引起的思考
林秋成
(南京市秣陵中学江苏南京211111)
作者在一次方程式听写过程中发现了学生方程式典型错误,讨论了产生错误的原因,从四个方面探讨了优化化学方程式教学策略,强调在进行化学方程式教学的过程中要让学生树立建构意识,帮助学生系统地提升化学用语的表达能力。
化学方程式;典型错误;教学策略
化学方程式既是中学化学中重要的化学用语,又是化学计算应用的基础。可能许多老师认为化学方程式的教学非常简单,就是老师讲讲,学生听听,平时加强记忆,加强抄写,基本上就能搞定!事实真是如此吗,一次方程式的听写改变了我的看法。
一次方程式听写中的典型错误及原因分析
笔者进行方程式听写是在学过铝与氢氧化钠溶液反应后进行的,听写情况统计如下:

典型错误1.Al+2NaOH=Na+Al(OH)3
典型错误2.Al+3NaOH=3Na+Al(OH)3
典型错误3.Al+NaOH=NaAlO2+3H2↑
典型错误4.Al+NaOH+H2O=AlNaO3+CO2↑
典型错误5.4Al+6NaOH+H2O=2Al2(OH)3+3Na2O
典型错误6.2Al+3Na2OH+H2O=Al2(OH)3+6Na
典型错误7.Al+NaOH=Na+Al(OH)3
典型错误8.2Al+2NaOH+2H2O=2NaAlO3+3H2↑
典型错误9.Al+NaOH+H2O=NaAlOH+H2↑
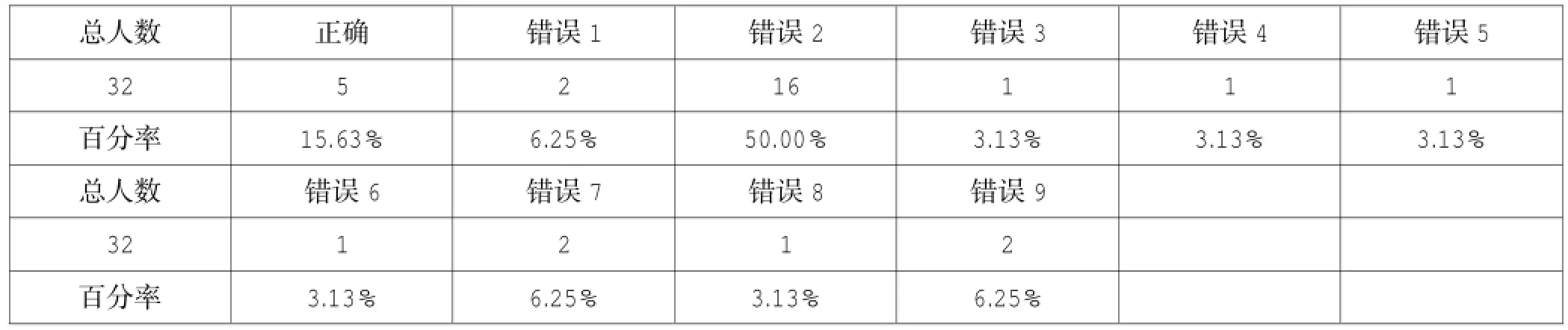
表1 方程式听写统计表
通过表1反映出的方程式听写统计情况分析我们发现,就这一个方程式,学生出现的错误就五花八门,错误的主要原因归纳起来有以下几个方面①化学式书写错误,如典型错误4中的AlNaO3,典型错误5、6中的Al2(OH)3,典型错误9中的NaAlOH②生成物瞎猜想,没有基本的化学思维,如典型错误4中出现的CO2,典型错误1、2、、6、7生成物中出现的Na,典型错误5中出现的Na2O,稍有化学常识的同学都不会出现这些错误,可是我们的同学却反复出现,说明一方面我们同学化学基础很差,另一方面也说明同学们虽然是高中生,可是对方程式出现的化学式及化学意义只有机械记忆,没有理解,这是制约同学们化学学习的很重要因素。③部分同学在不知道反应如何书写的时候,会机械地套用初中学过的置换反应,典型错误1、2、7都是这种思想的体现,而且所占比例特别高,典型错误2所占比例达到50%。④绝大多数同学书写方程式时没有守恒的思想,不会从氧化还原反应思想进行方程式反应物和错误的分析,当然更不会配平,缺反应物时不会根据质量守恒来进行补齐。
二、优化化学方程式教学策略探讨
在教学实践中,化学方程式既是化学教学的难点,也是学生化学成绩的分化点,许多学生刚进入高一,就感觉化学繁琐难学,特别是遇到较难方程式,很多学生都记不住,还称化学为“第二外语”。从某种意义上来说,化学方程式的教学已经严重影响了学生学习化学的积极性。那么,在化学教学过程中我们有哪些较好的优化化学方程式教学效率的策略呢?笔者想通过这次方程式听写情况谈谈提高优化化学方程式教学效率的一些策略和方法。
1.遵循原则,规范书写
在学生了解化学方程式意义的基础上,强调书写学方程式要遵循的两个原则:①要以客观事实为基础。不能随意臆造事实上不存在的物质和化学反应,不能任意编造物质的化学式。要正确书写物质的化学式,一是要熟练记忆元素符号,二是书写化合物的化学式时,要熟练记忆常见元素和原子团的化合价,三是书写化合物的化学式要符合各元素正负化合价的代数和为零的原则,四是掌握书写化学式的一般方法。例如典型错误4中的AlNaO3,典型错误5、6中的Al2(OH)3,典型错误9中的NaAlOH,我们只要按照各元素正负化合价的代数和为零的原则进行检验,很容易发现上面几例化学式均是错误的。②遵循质量守恒定律及电子转移守恒。这是书写化学方程式的核心问题,要让学生明确认识到:化学方程式中各个化学式前的化学量数绝不是任意拼凑的,它必须准确反映各物质发生化反应前后的定量关系。典型错误4中出现的CO2,我们只要有质量守恒的意识,就会发觉它是错的,因为反应前没有C元素。
2.加强三重表征训练,建立方程式有机联系
化学是一门研究物质的组成、结构、性质和变化规律的科学,由于化学学科的特点,要求学生从不同的角度去认识物质:物质的性质体现在宏观上,而宏观性质是学生最容易通过直觉感受到,从而完成一系列的直观感知,形成对物质的宏观表征的认识。宏观表征的难度不大且有记忆再现性,例如铝在和氢氧化钠溶液反应过程中,通过化学实验,录像解说,图片浏览,让学生从多角度感受铝片的不断溶解,试管中气泡的产生,反应留下溶液在滴加盐酸的过程中经过一段时间会产生沉淀,再继续滴加盐酸沉淀又会消失,这些宏观表征如果能在学生头脑里生根,有利于我们对方程式的意义建构,合理的书写方程式中要出现的反应物和生成物。例如通过上述宏观表征中有气泡产生,而产生的气泡性质检验燃烧前需要检验纯度,可以燃烧,这些宏观性质的存在,让我们猜测生成物有H2,那么典型错误1、2、4、5、6、7不会出现,而通过留下溶液与盐酸的作用,还可以让我们猜测到,生成物中应该有一种我们以前不熟悉的物质,自然地转入到让学生对NaAlO2有一个全新的感知。物质的组成结构等微观理论比较抽象,只有让学生在宏观上充分感知,然后通过让学生理解、想象,从而认识物质的本质;化学符号则是化学学科独特的表达方式,运用化学符号来代表事物,把化学符号作为思维运演的工具和媒介而进行的思维活动方式就是化学符号思维,毫无疑问,化学方程式的教学是化学符号思维的集大成者,非常抽象。我们只有在化学方程式教学中进行“宏观—微观—符号”三重表征以及建立三者间的联系,才能建立化学学科特有的思维方式,对学生学习化学知识会有极大的促进作用。所以教师必须重视学生在化学学习过程中的宏观表征、微观表征及其符号表征的形成及融合的问题。
3.加强过程分析,理解反应原理
有些同学在铝与碱液反应过程中书写方程式的过程中,不知道反应物要加水,有些资料上通过把反应分解为两步,通过加和反应的方式很容易得到总反应。
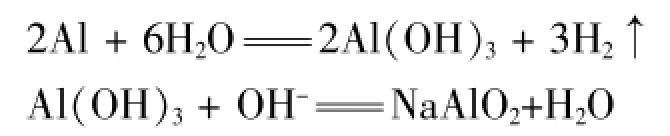
两式相加,消去Al(OH)3得2Al+2 OH-+2H2O =2AlO2-+3H2↑
通过反应的分解与加和,可以让同学理解反应原理,形成对反应的意义建构,有利于反应方程式的记忆。
4.形成核心化学思想,理性分析反应
在高一化学教学过程中,现在由于课时比较紧,因此可能很多学校在进行方程式教学时只有简单的死记硬背,没有方法的总结升华,没有核心化学思想的指引,导致很多同学在学习化学方程式时把有意义的建构学习变成了枯燥无味的死记硬背,短时间看老师是省事省时,从长远看对学生学习化学的兴趣却是致命打击。因此,从长远看,为了把学生留到化学课堂,我们宁愿进度慢一些,我们也要把一些核心化学思想告诉学生,例如氧化还原反应的原理,氧化还原方程式的配平,这样有助于学生在学习化学的过程中不仅知其然,而且能知其所以然。例如典型错误5中4Al+6NaOH+H2O=2Al2(OH)3+3Na2O,学生如果有氧化还原反应基本思想,就会发觉这个反应只有元素化合价升高,而没有元素化合价降低,很明显是个错误的方程式。如果学生具有一些基本的核心化学思想,他就会理性分析反应,不会出现一些明显的低级错误。
三、思考
化学方程式的教学看似简单,但是通过在学生方程式听写过程中的超高错误率,我们这一点正是教材原实验方案中所欠缺的。
我们知道,空白试验是指在不加试样的情况下,按照试样的分析步骤和条件而进行分析的试验,所得结果称为“空白值”。从试样分析的结果中扣除空白值,就可以得到更接近于真实含量的分析结果。笔者查阅系列相关科研论文[4-5]后发现,氢氧化钠标准溶液在标定时一般都需进行空白试验。实际上,空白试验的操作也并不繁琐,从学生的认知水平考虑是完全可以接受和理解的,而对学生认识和感受定量试验准确性、完整性来说这样的改变也是很有必要的。
因此,笔者认为教材的方案中可补充空白试验的相应内容:取1个250 mL锥形瓶,加入新煮沸而又迅速冷却的蒸馏水50 mL和2滴酚酞指示剂,然后用待标定的NaOH标准溶液滴定至溶液呈现浅红色且在半分钟内不褪色,记录所消耗的NaOH标准溶液的体积(即空白值)。
以上是笔者对配制并标定氢氧化钠溶液拓展课题中两处细节内容的一些粗浅认识,不妥、不宜之处敬请广大编者、同行斧正!
[1]王祖浩,王程杰.普通高中化学课程标准实验教科书《实验化学》(选修)[M].南京:江苏教育出版社.2010.5
[2]马世昌.化学物质辞典[M].陕西科学技术出版社,2002:10
[3]华中师范大学,东北师范大学,陕西师范大学编.分析化学[M].北京:高等教育出版社,2000.3
[4]魏丹琦.氢氧化钠溶液标定的不确定度评定[J].海峡预防医学杂志,2006,(1):45-47
[5]邓乐平.氢氧化钠标准溶液浓度不确定度的评定[J].化学分析计量,2004,(3):1-5
1008-0546(2014)01-0079-02
G633.8
B
10.3969/j.issn.1008-0546.2014.01.032
