离子液体萃取精馏分离乙酸甲酯-甲醇共沸物
2013-12-23崔现宝彭艳枚薛乐星包振宇
田 征,崔现宝,彭艳枚,薛乐星,包振宇
(天津大学 化工学院 化学工程联合国家重点实验室,天津 300072)
乙酸甲酯是一种重要的有机原料,主要用于合成醋酸、醋酐、丙烯酸甲酯、醋酸乙烯酯和乙酰胺等,广泛用于纺织、香料、医药等行业[1]。乙酸甲酯又是一种优良溶剂,它能和醇、醚、烃类互溶[2]。目前国内乙酸甲酯主要以传统酯化法生产[3-7],该法成本较高。
在维尼纶行业中,生产聚乙烯醇产生的醇解液中含有大量的乙酸甲酯和甲醇,目前主要的处理手段是将其水解为乙酸和甲醇循环使用[8-9]。有效地将该醇解废液分离以回收其中的乙酸甲酯,对乙酸甲酯工业和聚乙烯醇工业都有非常重要的意义。由于乙酸甲酯和甲醇形成共沸物,普通精馏难以对其进行分离。在化工行业中,分离共沸物系常采用萃取精馏[10-12]。水是一种分离乙酸甲酯-甲醇共沸物系的有效萃取剂[13],但由于水和乙酸甲酯会形成共沸物,在萃取精馏塔塔顶得到含水的乙酸甲酯,因此,该方法得到的乙酸甲酯纯度较低,且以水为萃取剂时溶剂量较大,造成后续分离能耗大。加盐萃取精馏可减少水的用量[9],但加盐萃取精馏过程存在盐水蒸发浓缩、盐的回收与结晶及盐水腐蚀设备等问题[14-15]。
离子液体萃取精馏是近些年提出的一种新型分离方法。Seiler等[16]研究了乙醇-水物系和四氢呋喃-水物系的离子液体萃取精馏分离过程,与传统萃取精馏相比,离子液体萃取剂可采用闪蒸分离,不需萃取剂回收塔,因此节省设备投资,节约能耗。汽液平衡数据是离子液体萃取精馏的基础。Orchillés等[17]测定了以1-乙基-3-甲基咪唑三氟甲磺酸盐([EMIM][Triflate])为萃取剂时乙酸甲酯-甲醇物系的汽液平衡数据。Cai等[18]测定了以1-乙基-3-甲基咪唑醋酸盐([EMIM][Ac])为萃取剂时乙酸甲酯-甲醇物系的汽液平衡数据,并发现[EMIM][Ac]对乙酸甲酯-甲醇物系的分离具有较高的选择性。
本工作以[EMIM][Ac]为萃取剂,利用流程模拟软件ChemCAD对萃取精馏分离乙酸甲酯-甲醇共沸物系的过程进行模拟计算,研究了各项操作参数和结构参数对萃取精馏过程的影响,获得优化的操作参数。
1 汽液平衡
图1是采用ChemCAD软件计算的乙酸甲酯-甲醇的T-x-y相图。由图1可看出,在101.3 kPa下,乙酸甲酯-甲醇的共沸组成为:乙酸甲酯的摩尔分数为0.66,甲醇的摩尔分数为0.34,共沸温度为326.75 K。
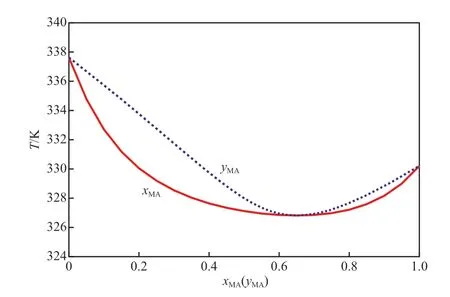
图1 101.3 kPa下乙酸甲酯-甲醇的T-x-y相图Fig.1 T-x-y phase diagram of methyl acetate-methanol system at 101.3 kPa.
在模拟过程中,采用ChemCAD软件中的SCDS Column模块,活度系数模型采用NRTL方程:

其中,乙酸甲酯-甲醇-[EMIM][Ac]三组分物系的二元交互作用参数见表1[18]。

表1 NRTL模型的二元交互作用参数Table 1 Binary interaction parameters of the NRTL model
采用N RT L 模型计算的乙酸甲酯-甲醇-[EMIM][Ac]物系的汽液平衡相图见图2。图2表明,[EMIM][Ac]能打破乙酸甲酯-甲醇的共沸点,是分离乙酸甲酯-甲醇共沸物系的有效萃取剂。
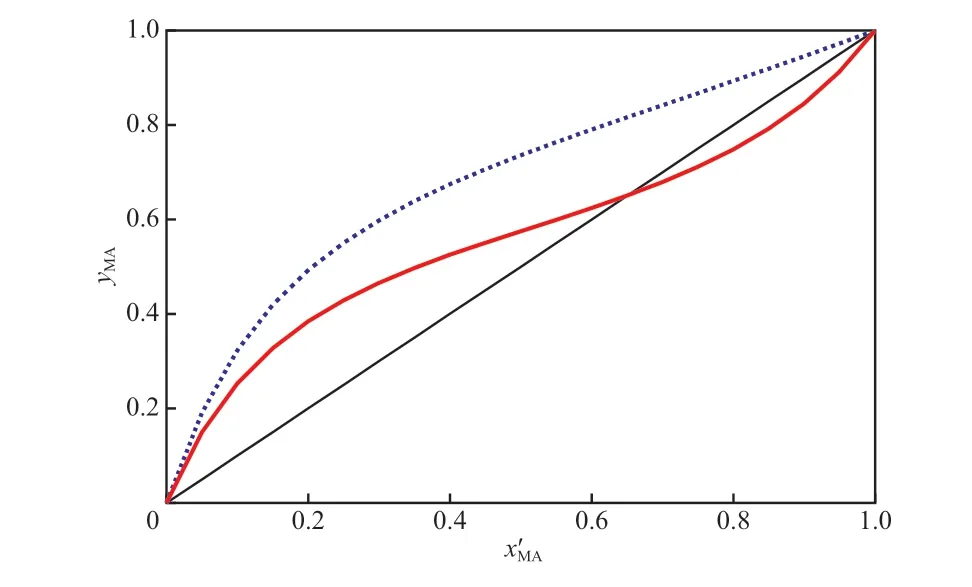
图2 101.3 kPa下乙酸甲酯-甲醇物系的汽液平衡相图Fig.2 Vapor-liquid equilibrium of the methyl acetate-methanol system at 101.3 kPa.
2 流程模拟
由图2可看出,[EMIM][Ac]可增大乙酸甲酯对甲醇的相对挥发度。Cai等[18]指出,在乙酸甲酯-甲醇-[EMIM][Ac]物系中,当[EMIM][Ac]摩尔分数大于0.087时,可打破乙酸甲酯和甲醇的共沸。因此,可采用[EMIM][Ac]为萃取剂利用萃取精馏来分离乙酸甲酯和甲醇的共沸物,分离流程见图3。

图3 采用离子液体为萃取剂的萃取精馏模拟流程Fig.3 Technological process of the extractive distillation with an ionic liquid(IL) as the solvent.
在离子液体萃取精馏流程中,主要包括萃取精馏塔和闪蒸罐。萃取精馏塔总理论板数为27(从上往下计数,不包含冷凝器,再沸器为最后一块理论板)。在萃取精馏塔的塔顶采出乙酸甲酯,塔底采出甲醇和离子液体的混合物,该流股进入闪蒸罐进行绝热闪蒸,由其底部采出高纯度离子液体,并通过泵和换热器循环返回萃取精馏塔。
为将离子液体萃取精馏与传统萃取精馏过程进行对比,对以离子液体为萃取剂的萃取精馏过程进行了模拟,模拟条件和计算结果见表2。

表2 模拟条件及计算结果Table 2 Conditions and results of the simulation
秦海洋等[13]曾采用1,3-丙二醇为萃取剂进行乙酸甲酯-甲醇物系的分离。在同样的原料进料条件下,若达到与离子液体萃取精馏相同的分离效果(xMA≥0.996,xME≥0.993),以1,3-丙二醇为萃取剂时,通过ChemCAD软件的灵敏度分析,萃取精馏塔所需的理论板数为29,塔底流股需通过溶剂回收塔进行萃取剂的回收,溶剂回收塔所需理论板数为6,所需总热负荷为8.566 GJ/h。而从表2可看出,以离子液体为萃取剂时,萃取精馏塔所需的理论板数为27,塔底流股只需通过闪蒸就可回收萃取剂,所需总热负荷为4.732 GJ/h。因此,与传统萃取精馏相比,离子液体萃取精馏能节省能耗和设备投资。
3 离子液体萃取精馏的影响因素
3.1 原料进料位置的影响
原料进料位置影响萃取精馏塔的萃取段和提馏段的塔板数,从而对乙酸甲酯-甲醇的分离有一定影响。图4为进料位置对塔顶乙酸甲酯纯度和再沸器热负荷的影响。从图4可看出,随原料进料位置由塔顶向下移动,乙酸甲酯纯度先提高后下降,当原料进料位置为第18块理论板时,乙酸甲酯纯度达到最大值;同时,当塔顶乙酸甲酯摩尔分数大于0.96时,改变进料位置对再沸器热负荷影响很小。因此,在离子液体萃取精馏分离乙酸甲酯-甲醇时,最佳原料进料位置为第18块理论板。
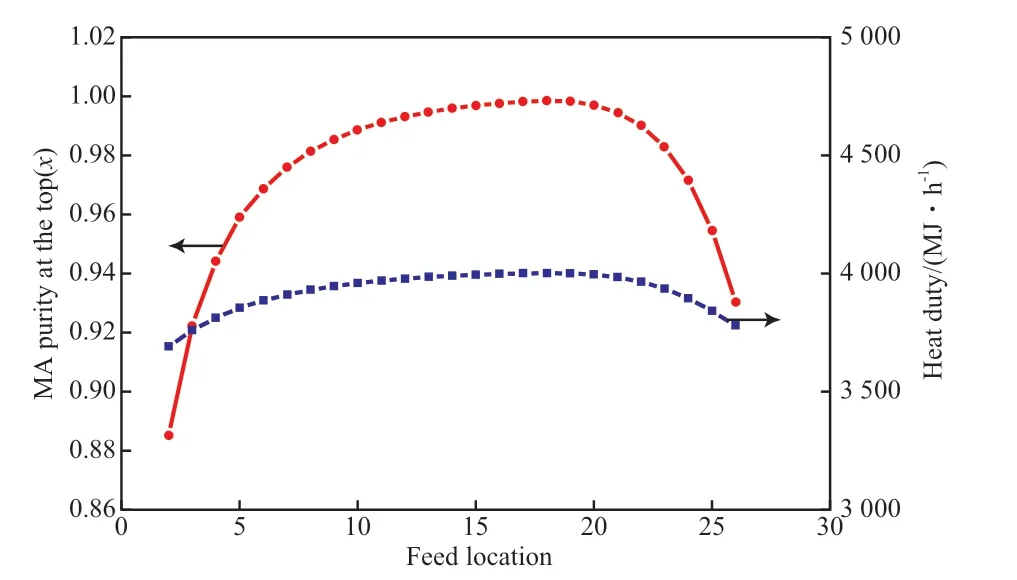
图4 进料位置对乙酸甲酯纯度和热负荷的影响Fig.4 Effects of feed location on the MA purity and heat duty.
3.2 理论板数的影响
理论板数是表征精馏塔分离效率的一个重要参数,理论板数不足,不能达到分离要求;理论板数过多,会造成设备投资过大。图5为理论板数对塔顶乙酸甲酯纯度和再沸器热负荷的影响。从图5可看出,随理论板数的增加,乙酸甲酯纯度先增加后趋于恒定;当理论板数小于25时,再沸器热负荷随理论板数的增加而增加,且乙酸甲酯纯度偏低;当理论板数大于25时,再沸器热负荷趋于恒定。综合考虑乙酸甲酯纯度和再沸器热负荷,确定较佳的理论板数为27。
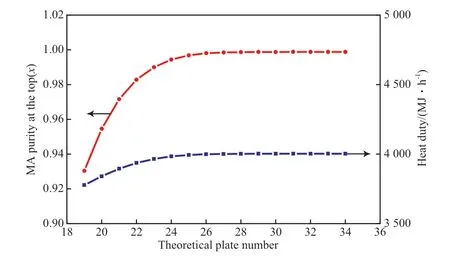
图5 理论板数对乙酸甲酯纯度和热负荷的影响Fig.5 Effects of the theoretical plate number on the MA purity and heat duty.
3.3 离子液体进料位置的影响
图6为离子液体进料位置对乙酸甲酯纯度和再沸器热负荷的影响。由图6可看出,当离子液体从塔顶第1块理论板进料时,乙酸甲酯纯度最高;随离子液体进料位置由塔顶向下移动,乙酸甲酯的纯度不断降低,再沸器热负荷变化较小。因此,选取适宜的离子液体进料位置为第一块理论板。

图6 离子液体进料位置对乙酸甲酯纯度和热负荷的影响Fig.6 Effects of IL feeding location on the MA purity and heat duty.
由于离子液体在常压下饱和蒸气压极低,很容易与乙酸甲酯分离,因此常规萃取精馏用于分离萃取剂和塔顶产品的精馏段在离子液体萃取精馏中可取消。离子液体萃取精馏和传统萃取精馏的对比见图7。由图7可看出,常规萃取精馏塔包括精馏段、萃取段和提馏段;而离子液体萃取精馏塔只有萃取段和提馏段。
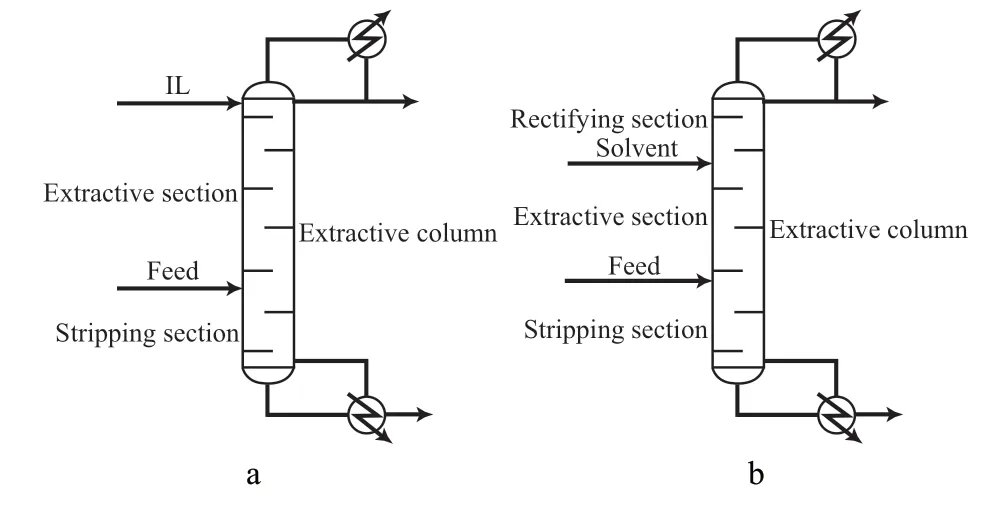
图7 离子液体萃取精馏(a)和传统萃取精馏的对比(b)Fig.7 Comparison of the extractive distillation with IL as the solvent(a) with conventional extractive distillation(b).
3.4 回流比的影响
回流比对精馏过程至关重要,它不仅影响塔顶和塔釜流股的组成,还影响整个系统的能耗。图8为回流比对乙酸甲酯纯度和再沸器热负荷的影响。由图8可看出,随回流比的增加,乙酸甲酯纯度提高;当回流比增加到一定程度后,乙酸甲酯纯度开始下降。因此回流比存在最优值。在萃取精馏过程中,回流比增加会产生两方面的作用:1)促进汽液两相传质,使塔顶产品纯度提高;2)当回流比增加时,塔板上离子液体的浓度下降,乙酸甲酯和甲醇的相对挥发度减小。当回流比较小时,第一方面的作用较大,因此塔顶产品纯度随回流比的增加而提高;当回流比大于一定数值后,第二方面的作用较大,因此塔顶产品纯度随回流比的增加而降低。而再沸器热负荷与回流比呈线性关系,随回流比的增加,再沸器热负荷增加。综合考虑产品纯度和能耗,适宜的回流比为0.3。

图8 回流比对乙酸甲酯纯度和热负荷的影响Fig.8 Effects of reflux ratio on the MA purity and heat duty.
3.5 溶剂比的影响
溶剂比是萃取剂进料摩尔流量与原料进料摩尔流量的比值,是萃取精馏的一个重要参数。图9为溶剂比对塔顶乙酸甲酯纯度和再沸器热负荷的影响。由图9可看出,随溶剂比的增加,乙酸甲酯的纯度增加;但当溶剂比大于0.26时,乙酸甲酯纯度变化很小。在其他条件相同的情况下,随溶剂比的增加,再沸器热负荷不断增加。综合考虑能耗和离子液体用量,最佳溶剂比为0.26。
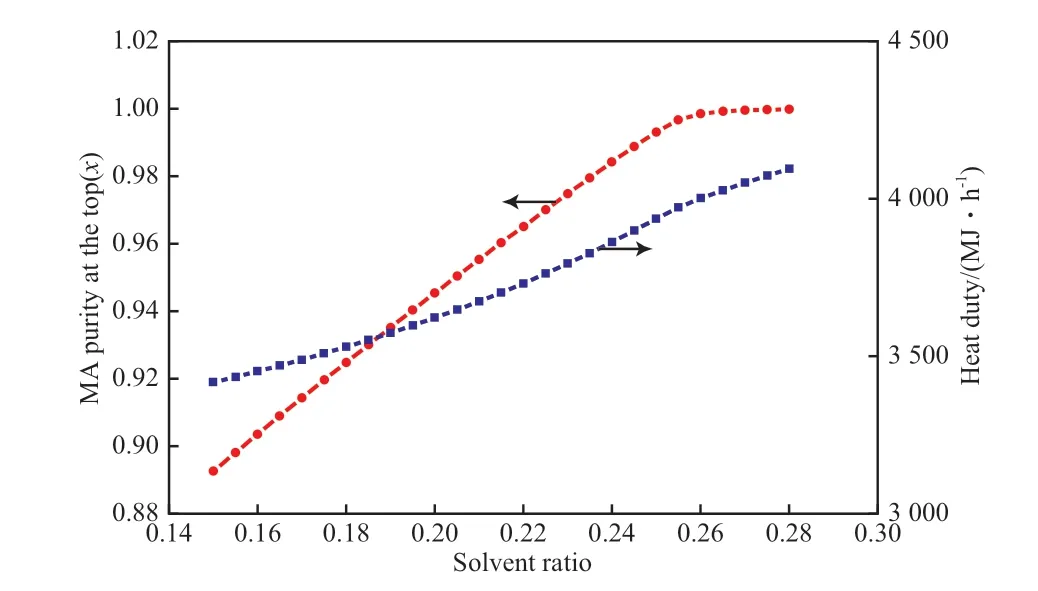
图9 溶剂比对乙酸甲酯纯度和热负荷的影响Fig.9 Effects of solvent ratio on the MA purity and heat duty.
4 结论
1)采用Chem CAD 流程模拟软件,对以[EMIM][Ac]为萃取剂萃取精馏分离乙酸甲酯-甲醇共沸物的流程进行了模拟。模拟结果表明,以离子液体[EMIM][Ac]为萃取剂能得到纯度达到0.996 6的乙酸甲酯。
2)利用模拟计算结果,研究了理论板数、原料进料位置、离子液体进料位置、回流比和溶剂比对离子液体萃取精馏的影响。研究结果表明,乙酸甲酯的纯度随理论板数的增加先增大后趋于恒定,随离子液体进料位置由塔顶向下移动而减小,原料进料位置、回流比和溶剂比存在最优值。
3)通过模拟计算获得的优化操作参数为:萃取精馏塔的理论板数为27,原料进料位置为第18块理论板,离子液体进料位置为第1块理论板,回流比为0.3,溶剂比为0.26。
符 号 说 明
Bij二元交互作用参数
T 温度,K
xk组分k在液相中的摩尔分数
xj组分j在液相中的摩尔分数
xMA乙酸甲酯在液相中的摩尔分数
x′MA去除[EMIM][Ac]时液相中乙酸甲酯的摩尔分数
yMA乙酸甲酯在汽相中的摩尔分数
αij非随机参数
γi组分i的活度系数
[1] 吴文炳,陈梁,张世玲. 乙酸甲酯的合成与应用新进展[J].江苏化工,2004,32(5):11 - 14.
[2] 艾臻,张靖,施云海. 醋酸甲酯和甲醇混合物的加盐萃取精馏分离过程的研究[C]//《化学世界》编辑部. 上海市化学化工学会2011年度学术年会论文集. 上海:《化学世界》编辑部,2011:3 - 5.
[3] 吴文炳,陈樑,张世玲. 醋酸甲酯合成研究新进展[J]. 天然气化工:C1化学与化工,2004,29(4):62 - 65.
[4] 吴文炳,陈樑,张世玲,等. 反应萃取精馏合成醋酸甲酯的研究[J]. 天然气化工:C1化学与化工,2004,29(6):5 -9.
[5] 曲宇霞,蔡旺锋,许春建,等. 浆料催化精馏制备醋酸甲酯[J]. 化学工业与工程,2006,23(1):1 - 5.
[6] 田敉,王孝科. 采用质子酸离子液体反应萃取精馏制备醋酸甲酯[J]. 石油化工,2009,38(6):603 - 607.
[7] 李柏春,张克强,杨振生,等. 反应精馏法制备高纯度醋酸甲酯[J]. 石油化工,2007,36(1):40 - 43.
[8] 赵之山,王良恩,赵素英. 用离子交换树脂催化水解醋酸甲酯的反应动力学研究[J]. 化学工程,1996,24(5):28 -32.
[9] 赵林秀,王小燕,崔建兰,等. 加盐萃取精馏分离醋酸甲酯-甲醇二元恒沸物[J]. 石油化工,2005,34(2):144 - 147.
[10] Berg L,Bozeman M T. Separation of Methyl Acetate from Methanol by Extractive Distillation:US,4597834[P]. 1986-07-01.
[11] Berg L,Bozeman M T. Separation of Methanol from Methyl Acetate by Extractive Distillation:US,4549938[P]. 1985-10-29.
[12] 张志刚,李债倩,李文秀,等. 萃取精馏分离乙酸甲酯-甲醇溶剂[J]. 化学工程,2011,39(5):36 - 38.
[13] 秦海洋,黄雪莉,李永霞. 萃取精馏过程中萃取剂选择及萃取条件研究[J]. 化学工业与工程,2009,26(4):342 -346.
[14] 田晶,顾正桂,詹其伟. 醋酸甲酯-甲醇-水的分离方法比较及展望[J]. 化学世界,2011,52(4):248 - 250.
[15] 刘奇琳. 浅析萃取精馏技术的研究[J]. 佳木斯教育学院学报,2010(6):124 - 126.
[16] Seiler M,Jork C,Kavarnou A,et al. Separation of Azeotropic Mixtures Using Hyperbranched Polymers or Ionic Liquids[J]. AIChE J,2004,50(10):2439 - 2454.
[17] Orchillés A,Miguel P,Vercher E,et al. Isobaric Vapor-Liquid Equilibria for Methyl Acetate + Methanol + 1-Ethyl-3-Methylimidazolium Trifluoromethanesulfonate at 100 kPa[J].J Chem Eng Data,2007,52(3):915 - 920.
[18] Cai Jialin,Cui Xianbao,Zhang Ying,et al. Vapor-Liquid Equilibrium and Liquid-Liquid Equilibrium of Methyl Acetate +Methanol + 1-Ethyl-3-Methylimidazolium Acetate[J]. J Chem Eng Data,2010,56(2):282 - 287.
