放疗联合唑来膦酸治疗骨转移癌止痛疗效分析
2013-12-04陈宝玉张鸣竹房振羽
陈宝玉 张鸣竹 房振羽
骨是晚期恶性肿瘤常见的转移部位,多引起顽固性疼痛和功能障碍,严重影响患者的生活质量,放射治疗是较好的治疗方法之一,但多数患者为多发骨转移且病灶受部位影响而使放疗受限制,提示临床工作者应探索放射治疗联合其他方法治疗骨转移癌。现将本科室2008年5月-2011年5月收治的62例骨转移癌单纯放疗及放疗联合唑来膦酸治疗报告如下。
1 资料与方法
1.1 一般资料 将2008年5月-2011年5月本科室收治的62例骨转移癌放射治疗患者,随机分为放疗联合唑来膦酸组31例和单纯放疗组31例。放疗联合唑来膦酸组:男20例,女11例;年龄38~81岁,中位年龄59岁;疼痛:重度15例,中度11例,轻度5例。单纯放疗组:男22例,女9例;年龄39~81岁,中位年龄58岁;疼痛:重度16例,中度10例,轻度5例。全组病例预计生存时间大于3个月,无心肺功能严重不全。原发病灶均病理学诊断,骨转移病灶均经X线片、CT、ECT、MRI、PET-CT中两种以上影像检查明确诊断,34例单发,28例多发。
1.2 治疗方法 放射治疗采用西门子PRIMUS M型直线加速器6MVX射线或15MVX射线或电子线。根据患者病情及全身状况不同而给予放疗分次剂量不等。对行走严重困难给予大分割,每次Dt 3 Gy,每周5次,总量30 Gy;其余给予常规分割,每次Dt 2 Gy,每周5次,总量40~50 Gy。放疗联合唑来膦酸组,第1天唑来膦酸4 mg静滴,每4周重复,共用4~6个周期。第2天开始行放射治疗。
1.3 观察指标及判断标准
1.3.1 疼痛评价标准 VRS法分为四级。0级:无疼痛;Ⅰ级:疼痛可忍受,能正常生活,睡眠不受干扰;Ⅱ级:疼痛明显,不能忍受,要求服用镇痛药,睡眠受干扰;Ⅲ级:疼痛剧烈,不能忍受,需要服用镇痛药,睡眠严重受干扰,可伴有植物神经功能紊乱表现或被动体位[1]。
1.3.2 止痛疗效评价标准 完全缓解(CR):治疗后完全无痛;部分缓解(PR):疼痛较治疗前明显减轻,睡眠基本不受影响,能正常生活;轻度缓解(MR):疼痛较前减轻,但仍明显,睡眠受干扰;无效(NR):与治疗前相比无减轻。总有效率为CR+PR+MR。
1.3.3 活动能力分级 0级:活动自如;Ⅰ级:活动受限;Ⅱ级:活动明显受限;Ⅲ级:完全不能活动。
1.3.4 活动能力的改善评价标准 显效:活动能力提高2级以上;有效:提高1级者;无效:未提高或降低者。
1.4 统计学处理 采用SPSS 10.0统计软件,计数资料行字2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组止痛效果比较 放疗前疼痛分布:单纯放疗组Ⅰ级5例;Ⅱ级例15;Ⅲ级11例。放疗联合唑来膦酸组Ⅰ级4例;Ⅱ级16例;Ⅲ级11例。放疗后疼痛分布:单纯放疗组0级13例,Ⅰ级6例,Ⅱ级7例,Ⅲ级5例。放疗联合唑来膦酸组0级18例,Ⅰ级7例,Ⅱ级5例,Ⅲ级1例。单纯放疗组缓解22例,总有效率71%;放疗联合唑来膦酸组缓解29例,总有效率93.5%,两组总有效率比较,差异有统计学意义(字2=5.42,P<0.05)。见表1。
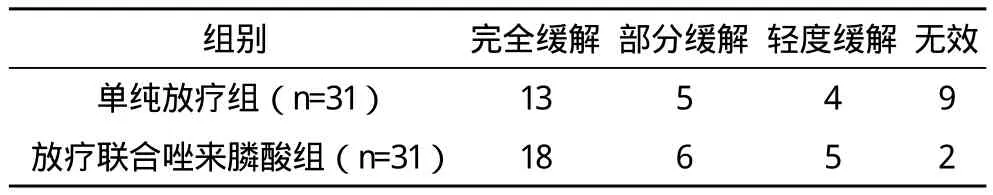
表1 治疗后两组止痛效果比较 例
2.2 两组活动能力改善情况比较 治疗后两组活动能力均有改善。放疗前活动能力情况:单纯放疗组Ⅰ级14例;Ⅱ级15例;Ⅲ级2例。放疗联合唑来膦酸组Ⅰ级10例;Ⅱ级20例;Ⅲ级1例。放疗后活动能力情况:单纯放疗组0级17例,Ⅰ级8例,Ⅱ级5例,Ⅲ级1例。放疗联合唑来膦酸组0级23例,Ⅰ级5例,Ⅱ级3例,Ⅲ级0例。单纯放疗组显效11例,有效8例,无效12例,总有效率61.3%;放疗联合唑来膦酸组显效15例有效11例,无效5例,总有效率83.9%,两组比较,差异有统计学意义(字2=3.97,P<0.05)。见表2。

表2 治疗后两组活动能力改善情况 例
2.3 不良反应 主要不良反应为白细胞下降及恶心及呕吐,主要为照射野包及部分消化器官,联合组有患者出现发热及肌肉酸痛。
3 讨论
骨是中晚期恶性肿瘤常见远处转移器官,仅次于肺、肝。骨转移可导致剧烈疼痛、功能活动障、病理性骨折、高钙血症、脊髓压迫,可以加快病情的发展,是患者生活质量下降和死亡的主要原因之一。
骨转移癌最常见于乳腺癌、肺癌、前列腺癌、甲状腺癌及多发性骨髓瘤的骨破坏,转移癌发生部位以椎骨、骨盆骨及肋骨最为多见,约占80%左右,其次为股骨、颅骨、和肱骨。骨转移癌的预后依原发病的不同而异。骨转移癌治疗方法有手术、化学治疗、放射治疗、内分泌治疗、双膦酸盐、止痛药等。
放射治疗可有效地缓解大多数骨转移引起骨疼痛和神经痛。放射治疗骨转移癌止痛作用又快又好,骨转移癌放疗后80%~90%的患者可以获得较持久的止痛效果,同时也有延长生存期的作用[2]。放射治疗缓解疼痛的机制尚不完全清楚,化学性疼痛介质释放减少和受到抑制可能是放疗作用的主要机制,在数天内疼痛开始缓解应主要归因于各种化学疼痛介质的减少,而长期持续缓解效应则应归因于肿瘤负荷减少和重新钙化[3]。但多数患者为多发骨转移且病灶受部位影响而使局部放疗受限制,而要加用全身治疗。
唑来膦酸是一种特异性地作用于骨的二磷酸化合物,它能抑制因破骨活性增加而导致的骨吸收。主要作用机制是通过抑制破骨细胞的活化和活化破骨细胞的增生来抑制骨吸收,减少骨基质生长因子的释放或抑制癌细胞粘附于骨基质;抑制破骨细胞的对骨小梁的溶解和破坏,从而阻滞肿瘤引起的溶骨性病变、减少骨吸收、减轻疼痛及降低由骨转移所致的高钙血症及其他并发症的发生率;通过抑制甲醛戊酸途径,阻滞细胞周期来诱导破骨细胞和单核细胞前体细胞的凋亡,从而达到抑制骨吸收的目的;具有直接的体内、外抗肿瘤作用[4-5]。故放射治疗联合唑来膦酸两者可以在时间和空间起协同作用,共同发挥控制疼痛,在缓解骨痛的同时,对骨转移癌有明显的治疗作用,可保护和修复被破坏骨质的功能,明显延缓病变的进展;可以降低骨转移癌患者发生骨相关事件的风险,改善生活质量,为骨转移癌患者带来临床益处[6-7]。
本报道骨转移癌单纯放疗止痛总有效率71%,比大多数文献报道低,主要原因为本研究病例有部分患者为多发骨转移,且有些病灶放疗受限制。放疗联合唑来膦酸止痛总有效率93.5%,与单纯放疗组比较,差异有统计学意义(字2=5.42,P<0.05)。治疗后两组活动能力均有改善。单纯放疗组总有效率61.3%,放疗联合唑来膦酸组总有效率83.9%,两组比较,差异有统计学意义(字2=3.97,P<0.05)。骨转移癌放射治疗的目的在于缓解患者疼痛,保持功能。特别是负重骨的功能,改善生活质量[8]。故放疗联合唑来膦酸能提高放疗效果,特别对多发骨转移癌有些病灶放疗受限制,更能显示出超过单纯放疗的优势。
尽管近10年来,对骨转移癌发生机制、防治方法等方面进行了大量研究,目前仍未找到有效的根治手段。骨转移癌的放射治疗是一种姑息性治疗,以减轻或控制骨痛,预防或减少病理性骨折等相关症状发生,保持骨的稳定性为治疗目的。因此,设计照射方式时应多方面考虑,以既方便、经济,止痛效果又好,而且不出现严重的治疗反应为原则。对预期生存期短的患者可给予大分割。有些患者局部放疗1~2次后,疼痛不仅没有好转。甚至加重者,可能与放疗后组织充血有关,其后可以逐步缓解。
综上所述,放疗联合唑来膦酸治疗骨转移癌,止痛效果好,使患者活动能力得到了改善。与单纯放疗比较未增加明显毒副作用,是一种临床值得应用的恶性肿瘤骨转移癌治疗方法,特别是对多发骨转移灶患者,有部分病灶不能行放疗者。临床上,需要医生根据患者具体情况,合理选用治疗方法,最大限度地减轻患者的痛苦,提高生存质量,延长生存期。
本研究未对患者生存率进行研究,且病例数偏少,故目前该方案治疗优点需要大宗的临床试验进一步研究,及治疗结束后如何巩固疗效有待更进一步研究。
[1]孙燕,石远凯.癌症疼痛的处理[M].北京:人民卫生出版社,2007:258-260.
[2]谷锐之.肿瘤放射治疗学[M].北京:北京医科大学中国协和医科大学联合出版社,1993:817.
[3]陆军,邓敬兰,赵海涛,等.脊柱转移癌放疗联合椎体成形术治疗的前瞻性研究[J].中华放射肿瘤学杂志,2005,14(1):42.
[4]Evdokiou A, Abrinidis A. Induction of cell death of human osteogenic sarcoma cells by zoleroniacid resembles anoikis[J]. Bone,2003,33(2):216.
[5]Nevile-Webbe H, Coleman R E. The use of zoledronic acid in the management of metastatic bone disease and hypercalcagemia[J]. Palliat Med,2003,17(6):539.
[6]吴瑾,周莉华,蒋晓东.唑来膦酸联合放疗治疗骨转移癌的临床疗效[J].现代肿瘤医学,2008,16(1):110-111.
[7]吴云峰,雷侠.单纯放疗与放疗联合唑来膦酸治疗骨转移瘤临床观察[J].现代肿瘤医学,2008,16(1):112-113.
[8]朱国培摘译.美国放射学院的合理治疗原则[J].中华放射肿瘤学杂志,2000,9(4):287.
