55%溴化锂溶液中Na2MoO4-B复合缓蚀剂对碳钢的缓蚀行为研究
2013-11-30李杰兰梁成浩黄乃宝
李杰兰,梁成浩,黄乃宝
(1.大连海事大学交通运输装备与海洋工程学院,辽宁 大连 116026;2.辽宁师范大学化学化工学院,辽宁 大连 116029)
溴冷机是以热能作为动力,以水为制冷剂,LiBr溶液为吸收剂,制取高于0℃的冷量,作为空调或生产工艺过程的冷源.溴冷机耗电少、无毒、无污染、无爆炸危险、安全可靠,可采用工业废热、余热、太阳能等低品质的热能,并且可使用天然气、煤气等多种多样的能源形式,是一种节能型的设备.为提高溴冷机的热效率,三效式和多效式制冷机的工作温度和LiBr溶液浓度也更高,然而LiBr溶液在高温高浓度的条件下对碳钢等金属具有很强的腐蚀性[1-3],添加缓蚀剂是解决这一问题最经济有效的方法.可用于LiBr溶液中的缓蚀剂主要包括具有氧化特性的无机盐,如钼酸盐、铬酸盐、硝酸盐和杂多酸等;和具有吸附特性的有机物,如苯并三氮唑(BTA)等[4-6].
钼酸盐因为无毒且不污染环境作为缓蚀剂得到广泛的应用[7-9].钼酸盐是溴冷机中常用的缓蚀剂,在碱性的LiBr溶液中,对碳钢等金属具有较好的缓蚀作用.但是在高浓度的LiBr溶液中,钼酸盐溶解度较低不易维持有效的缓蚀浓度,而且在高温条件下缓蚀效果并不理想[10,11].有机膦类物质常用作缓蚀阻垢剂[12],将钼酸盐和有机膦复配用于LiBr溶液中金属的缓蚀剂国内尚未见报道.本文将一种有机膦类物质B和Na2MoO4复配得到复合缓蚀剂Na2MoO4-B,并考察了它对高温55%LiBr溶液中碳钢的缓蚀行为.
1 实验
55%LiBr溶液由日本三洋公司提供,所用Na2MoO4、LiOH和B均为分析纯试剂,实验材料碳钢的化学成分(质量分数/%)为C 0.12,S 0.02,P 0.02,Si 0.01,Mn 0.35,余量为Fe.将Na2MoO4和B溶于水中搅拌1h配制成复合缓蚀剂,之后加入到55%LiBr+0.07 mol/L LiOH溶液中搅拌1h,配制成B浓度为20 mg/L,Na2MoO4浓度分别为200、400、600和800 mg/L的溶液.
失重实验采用尺寸为3.0 cm×2.0 cm×0.35 cm的碳钢试样.将试样打磨、清洗、脱脂、干燥并精确称重后放入不锈钢高压釜的聚四氟乙烯内衬中,并注入100 mL含一定浓度复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液,用高纯氮气除氧1h,再密封于不锈钢高压釜内.将高压釜在日本KosumosuAT-S13型恒温箱中于设定温度下恒温放置200h后,取出试样,用3 mol/L HCl+1%六次甲基四胺溶液清洗3 min,清洗干燥后称重,根据试样浸泡前后的质量变化来计算腐蚀速度.计算公式如下:
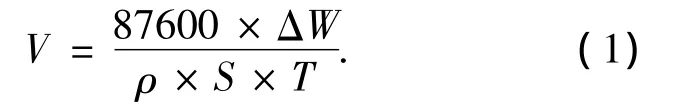
式中,V为腐蚀速度(μm/a),W为碳钢腐蚀前后质量变化(mg),ρ为碳钢密度(g/cm3);S为试样表面积(cm2),T为浸泡时间(h).
电化学实验溶液为不加缓蚀剂和加入不同浓度复合缓蚀剂145℃下的55%LiBr+0.07mol/L LiOH溶液.采用三电极体系:工作电极为工作面积为1cm2的碳钢电极,参比电极为饱和甘汞电极(SCE),辅助电极为Pt电极,加热装置为日本大科电器株式会社生产的GBR20型加热器.采用Princeton Applied Research VMP3电化学工作站进行极化曲线和交流阻抗测试.电化学极化扫描速率为20 mV/min;电化学交流阻抗微扰电压为10 mV,频率范围为1×10-2Hz~1×105Hz,由高频向低频扫描.
采用扫描电镜(SEM)、X-射线衍射(XRD)和EDAX能谱对浸泡在含800 mg/L Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中200h后的碳钢表面进行分析.SEM和EDAX型号为XL-30TMP(荷兰 Philips公司),电压15kV;XRD型号为D/MAX-Ultima+(日本Rigaku Corporation),测量角度范围 20 -100°,扫描速度 4°/min,步长 0.02 min-1,标准靶为Cu.
2 结果与讨论
2.1 失重实验
含不同浓度Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中浸泡200 h的碳钢失重实验结果示于图1.由图可知,当缓蚀剂浓度相同时,碳钢的腐蚀速度随温度升高而增大.譬如,添加150 mg/L Na2MoO4的溶液中,温度为160、200和240℃时,碳钢的腐蚀速度分别为42.16、84.25 和128.3 μm/a;添加 800 mg/L Na2MoO4-B复合缓蚀剂的溶液中,碳钢的腐蚀速度分别为21.05、24.13 和44.11 μm/a.同一温度下,复合缓蚀剂浓度越大,腐蚀速度越低;240℃时,添加800 mg/L Na2MoO4-B复合缓蚀剂的溶液中碳钢的腐蚀速度为44.11 μm/a,而添加150 mg/L Na2MoO4时碳钢的腐蚀速度高达128.3 μm/a,说明 Na2MoO4浓度对碳钢腐蚀速度有较大影响.在实际应用中必须保持Na2MoO4浓度在有效浓度以上,否则缓蚀效果较差.
2.2 电化学测试
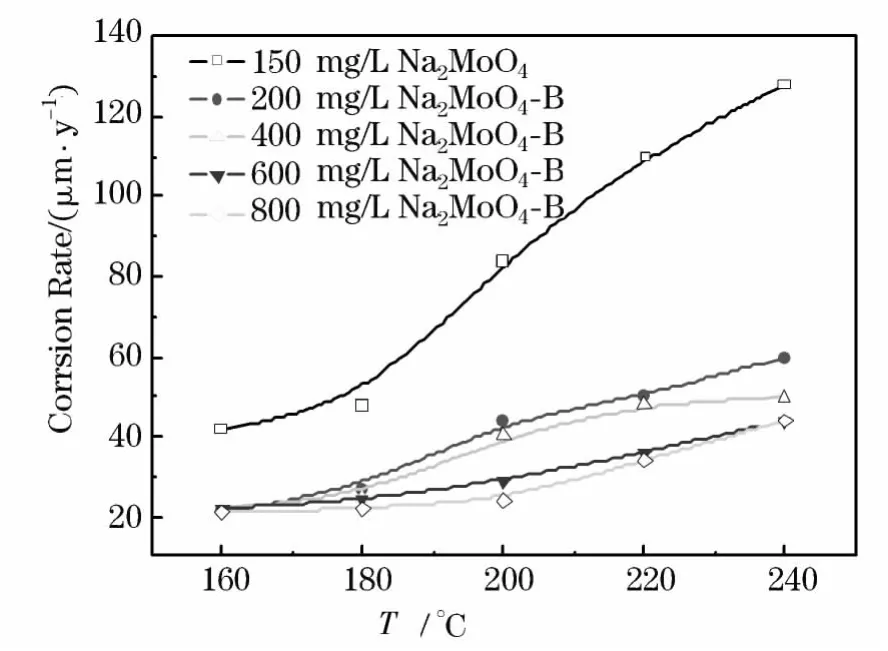
图1 复合缓蚀剂对碳钢腐蚀速度的影响
碳钢在145℃的55%LiBr+0.07 mol/L LiOH溶液中的极化曲线示于图2,含不同浓度Na2MoO4-B复合缓蚀剂时碳钢的腐蚀电位Ecorr、钝化电位区间和钝化电流密度Icorr列于表1.缓蚀效率按下式计算:

式中,η为缓蚀效率,Icorr和I0corr分别为有缓蚀剂和没有缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中碳钢的钝化电流密度.
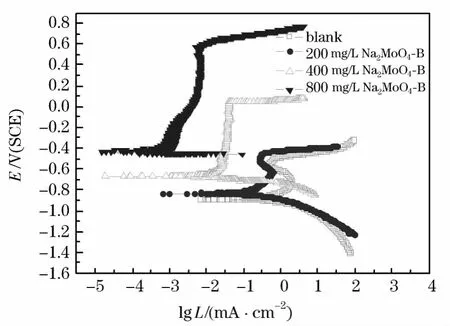
图2 碳钢溶液中的极化曲线

表1 碳钢在沸腾55%LiBr+0.07 mol/L LiOH溶液中的电化学参数
结果表明,随着Na2MoO4-B复合缓蚀剂浓度的增大,碳钢的腐蚀电位Ecorr由无缓蚀剂时的-0.83 V逐渐正移至-0.43 V,阳极极化电流密度显著减小,说明Na2MoO4-B复合缓蚀剂主要是抑制阳极极化过程,在55%LiBr+0.07 mol/L LiOH溶液中该缓蚀剂属阳极型缓蚀剂.没添加缓蚀剂时,阳极极化曲线中的钝化电位区间和钝化电流密度分别为50 mV和0.56 mA/cm2,当Na2MoO4浓度增至800 mg/L时,钝化电位区间和钝化电流密度分别为750 mV和0.0063 mA/cm2,缓蚀效率为98.88%,这表明Na2MoO4-B复合缓蚀剂改善了碳钢的电化学性能.
图3示出碳钢在 55%LiBr+0.07 mol/L LiOH溶液中的交流阻抗测试结果.碳钢在有、无缓蚀剂的溶液中的交流阻抗谱呈压扁的圆弧形,表现出弥散效应的特点.一般认为,交流阻抗谱的弥散效应与试样的粗糙度有关[1].
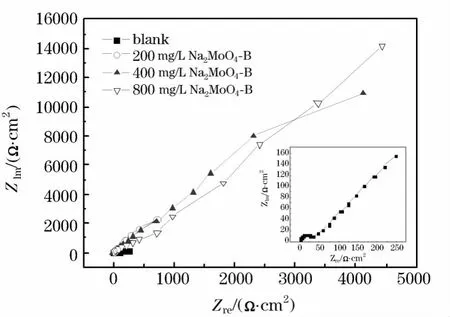
图3 碳钢溶液中的Nyquist图
碳钢在不含和含Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中的电极过程可以用图4(a)和(b)的等效电路拟合[5].

图4 55%LiBr+0.07 mol/L LiOH溶液中碳钢电极的等效电路
其中,Rs是溶液电阻,Q是常相位角元件,Rt是反应电阻,W是Warburg阻抗.常相位角元件Q的阻抗ZQ可以用下式计算[14].
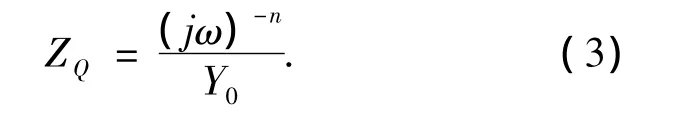
用EC-lab软件对阻抗数据进行拟合,结果示于表2.

表2 缓蚀剂对电化学参数的影响
拟合数据显示,55%LiBr+0.07 mol/L LiOH溶液中加入Na2MoO4-B复合缓蚀剂后,常相位角元件CPE的Y0值由空白时的0.00498 F/cm2逐渐减小至0.000892 F/cm2,反应电阻Rt值大幅增至2.31×105Ω·cm2,比没加缓蚀剂时增大约1000倍,表明碳钢表面生成了致密的钝化膜,增大了腐蚀反应的能垒,降低了碳钢的腐蚀速度.
2.3 表面膜的结构
图5示出碳钢试样在240℃,含有800 mg/L Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中浸泡200 h后的SEM观察照片.从图中可看出,碳钢表面形成一层晶粒状致密的膜层,能有效地阻滞LiBr溶液对碳钢的浸蚀.
碳钢试样在240℃,含有800 mg/L Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中浸泡200 h后表面膜的EDAX分析结果示于图6.表面膜成分主要有Fe、Mo和O元素,其含量分别为57.71%、24.14% 和18.15%.这说明Mo参与了碳钢表面钝化膜形成的历程.
对在240℃含有800 mg/L Na2MoO4-B复合缓蚀剂的55%LiBr+0.07 mol/L LiOH溶液中浸泡200小时后碳钢表面进行了XRD分析,结果示于图7.结果表明,碳钢表面膜主要由Fe3O4、MoO2和MoO3所构成.

图5 碳钢浸泡200 h后的SEM照片
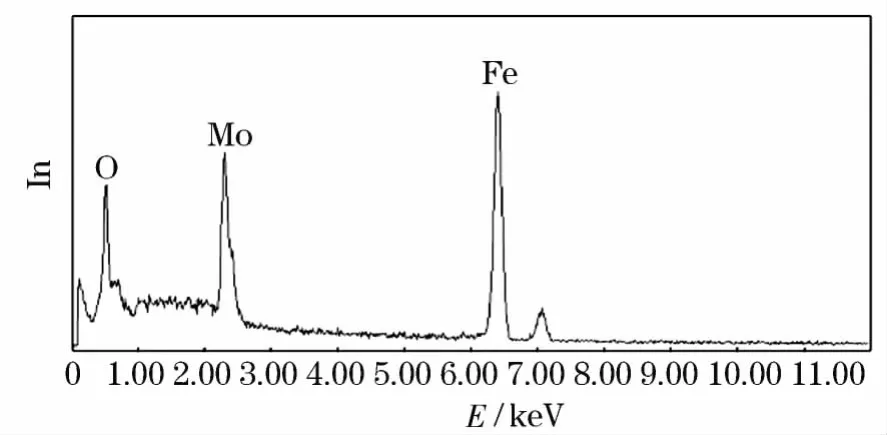
图6 碳钢浸泡200h后的EDAX谱图

图7 碳钢浸泡200h后的XRD分析
Na2MoO4-B复合缓蚀剂在LiBr溶液中的缓蚀作用,主要是通过Na2MoO4的氧化作用在碳钢表面形成一层灰黑色致密的由Fe3O4、MoO2和MoO3组成的钝化膜.Fe3O4是基体 Fe被Na2MoO4氧化而形成,MoO2和MoO3分别是Na2MoO4的还原产物和分解产物[14],这层保护膜将LiBr溶液和碳钢的基体隔离,起到缓蚀作用.Na2MoO4的缓蚀效果取决于浓度,正常情况下Na2MoO4在高浓度LiBr溶液中的溶解度非常有限.B缓蚀剂是一种有效的缓蚀阻垢剂,它可以通过吸附在Na2MoO4晶核的表面,抑制Na2MoO4晶体在LiBr溶液中的成长和析出,提高Na2MoO4的溶解度[15].55%LiBr+0.07 mol/L LiOH 溶液中加入B缓蚀剂后,Na2MoO4浓度可达到800 mg/L以上,可以对碳钢起到较好的缓蚀作用.
3 结论
1)不同温度的55%LiBr+0.07 mol/L LiOH溶液中,添加Na2MoO4-B缓蚀剂后碳钢腐蚀速度显著降低,表明复合缓蚀剂具有优异的缓蚀效果.
2)Na2MoO4-B复合缓蚀剂可提高沸腾55%LiBr+0.07 mol/L LiOH溶液中碳钢的腐蚀电位,拓宽钝化电位区间,降低阳极钝化电流密度,减小常相位角元件CPE的Y0值,增加反应电阻Rt值,改善碳钢的电化学性能.添加 800 mg/L Na2MoO4-B复合缓蚀剂时,缓蚀效率可达98.88%.
3)B缓蚀剂可使 55%LiBr+0.07 mol/L LiOH溶液中Na2MoO4浓度提高到800 mg/L以上.Na2MoO4通过氧化作用使碳钢表面形成一层主要由Fe3O4、MoO2和MoO3组成的致密钝化膜,从而起到较好的缓蚀作用.
[1] BLASCO-TAMARIT E,GARCíA-GARCía D M,GARC íA ANTóN J.Imposed potential measurements to evaluate the pitting corrosion resistance and the galvanic behaviour of a highly alloyed austenitic stainless steel and its weldment in a LiBr solution at temperatures up to 150℃ [J].Corros Sci,2011,53(2):784 – 795.
[2] FERNáNDEZ-DOMENE R M,BLASCO-TAMARIT E,GARCíA-GARCía D M,et al.Thermogalvanic corrosion of Alloy 31 in different heavy brine LiBr solutions[J].Corros Sci,2012,55(2):40 -53.
[3] FERNáNDEZ-DOMENE R M,BLASCO-TAMARIT E,GARCíA-GARCíA D M,et al.Thermogalvanic effects on the corrosion of copper in heavy brine LiBr solutions[J].Corros Sci,2012,63(10):304–315.
[4] HU Z Q,LIANG C H,WU X N.Corrosion behaviors of carbon steel in 55%LiBr solution containing PWVA inhibitor[J].Mater Corros,2011,62(5):444 -448.
[5] LIANG Cheng-hao,HU Xian-qi.Inhibition performance of enhanced-Mo inhibitor for cabon steel in 55%LiBr solution[J].J Iron Steel Res Int,2008,15(1):49-54.
[6] ABD EI MEGUID E A,AWAD N K .Electrochemical pitting corrosion behaviour of-brass in LiBr containing solutions[J].Corros Sci,2009,51(5):1134 -1139.
[7] Al-REFAIE A A,WALTON J,COTTIS R A,et al.Photoelectron spectroscopy study of the inhibition of mild steel corrosion by molybdate and nitrite anions[J].Corros Sci,2010,52(2):422 –428.
[8] LI Xiang-hong,DENG Shu-duan,FU Hui.Sodium molybdate as a corrosion inhibitor for aluminium in H3PO4 solution [J].Corros Sci,2011,53(9):2748 -2753.
[9] EGHBALI F,MOAYED M H,DAVOODI A,et al.Critical pitting temperature(CPT)assessment of 2205 duplex stainless steel in 0.1 M NaCl at various molybdate concentrations[J].Corros Sci,2011,53(1):513–522.
[10] RAMIREZ-ARTEAGA M A,GONZALEZ-RODRIGUEZ,J G ROSALES I,et al.Corrosion inhibition of 70Cu–30Ni alloy in LiBr+ethylene glycol+H2O mixtures by inorganic compounds[J].Mater.Corros.,2011,62(1):41 -46.
[11] ITOH M,MIDORIKAWA M,Izumiya M,et al.Corrosion inhibition of carbon steel by lithium molybdate in concentrated LiBr solution at elevated temperatures[J].Corros Eng,1990,39(6):321 -330.
[12] LABJAR Najoua,LEBRINI Mounim,BEBTISS Foua d,et al.Corrosion inhibition of carbon steel and antibacterial propertiesofaminotris-(methylenephosphonic)acid [J].Mater Chem Phys.,2010,119(1-2):330–336.
[13] MACDONALD J R.Impedance spectroscopy and its use in analyzing the steady state AC impedance response of solid and liquid electrolytes[J].J.Electroanal.Chem.,1987,223,25-50.
[14] LIANG Cheng-hao,HUNANG Nai-bao,GUO Jianwei,et al.Inhibition mechanism of Na2MoO4 for carbon steel in 55%Libr solution[J].Chin J Mech Eng(Engl Ed),2007,20(4):15-18.
[15] SUITOR J W,MARNER W J,RITTER R B.The history and status of research in fouling of heat exchanger in cooling water service[J].Can J Chem Eng,1977,55:374-380.
