TiO2-K2Cr2O7协同体系测定染料浓度实验条件的正交优化
2013-11-29张一平
张一平
(浙江外国语学院科学技术学院,浙江杭州310012)
1 引言
本课题组前期利用TiO2-K2Cr2O7的协同光催化氧化效应,建立了一种基于Cr2被还原为Cr3+,然后分光光度法测定剩余Cr2O72-的快速测定染料浓度的简便、灵敏方法.在该体系中共存的Cr2作为光生电子的受体,提高了协同体系的光催化氧化能力,它能在有机物彻底氧化的同时被定量还原,利用分光光度法快速准确测定光催化体系中Cr2浓度的变化值,即可间接得出该水样中染料的浓度[1].
消解染料的主要影响因素有5个:pH值、TiO2用量、K2Cr2O7初始浓度、反应温度、紫外光照时间.因素较多,若进行全面实验,则实验的规模将很大.假如每个因素取5个不同的状态进行比较,那么就要在55=3125个不同的实验条件下进行实验,难度较大.前期的研究中,我们采用的是单因素轮换法.单因素实验以一个因素为变量,其他因素固定.单因素轮换的缺点是在对实验各因素都不了解,尤其是对其之间的相互作用一无所知的情况下,固定其它因素的水平,这势必会影响实验结果.而正交实验设计可以用部分实验来代替全面实验,通过对部分实验结果的分析,了解全面实验的情况,减少了实验次数.而且,它能够通过极差分析明确各影响因素的主次顺序.因此,本文拟采用正交实验法以降低选择染料最佳消解条件的盲目性.
2 实验部分
实验仪器与试剂、实验方法均参见文献[1].其中,吸光度的变化值ΔA=A0-A,A0为光催化前Cr2的吸光度值,A为光催化后溶液中剩余Cr2O72-的吸光度值.
2.1 正交实验因素水平表的确定
根据光催化氧化测定COD的相关文献[2-8],pH值、TiO2用量、K2Cr2O7初始浓度、反应温度、紫外光照时间等对有机物的光催化消解结果有显著影响.在正交实验中,把实验需要考察的结果称为指标,本文中实验的指标是吸光度的变化值ΔA.在实验中要考察的对实验指标可能有影响的因素简称为因素,本文中需要考察pH值(A)、TiO2用量(B)、K2Cr2O7初始浓度(C)、反应温度(D)、紫外光照时间(E)5个因素.每个因素在实验中要比较的具体条件称为水平,每个因素比较5种不同的条件,如0.5、1.0、1.5、2.0、3.0就是pH值这个因素的5个水平(见表1).

表1 因素水平表
2.2 实验结果及分析
根据表2的实验方案,按各号实验规定的实验条件,进行了TiO2-K2Cr2O7协同光催化氧化体系消解染料甲基橙的实验,用分光光度法测定了光催化前后Cr2O72-吸光度变化值(ΔA),将这25个数据填入表2,极差分析结果见表3.表3中,Ki为某列因素i水平所对应的实验指标和,即每个因素下对应水平为i的实验结果的和.如A因素(pH值)所在列的K1,即为其所有1水平(pH=0.5)所得到的吸光度变化值ΔA的和,K1=0.08+0.153+0.121+0.139+0.168=0.661.在计算完各因素列的Ki值之后,再计算每一列的Ki中最大值和最小值之差,即每个因素下K的最大值减最小值,这个差值称为极差,记作R.例如,第一列(A因素)R=0.831-0.505=0.326.每一列算出的极差大小,反映了该列因素选取的水平变动对指标影响的大小.R越大,说明该因素对实验指标的影响越大,根据R大小,可以判断因素的主次顺序.

表2 正交实验设计与结果

续表2
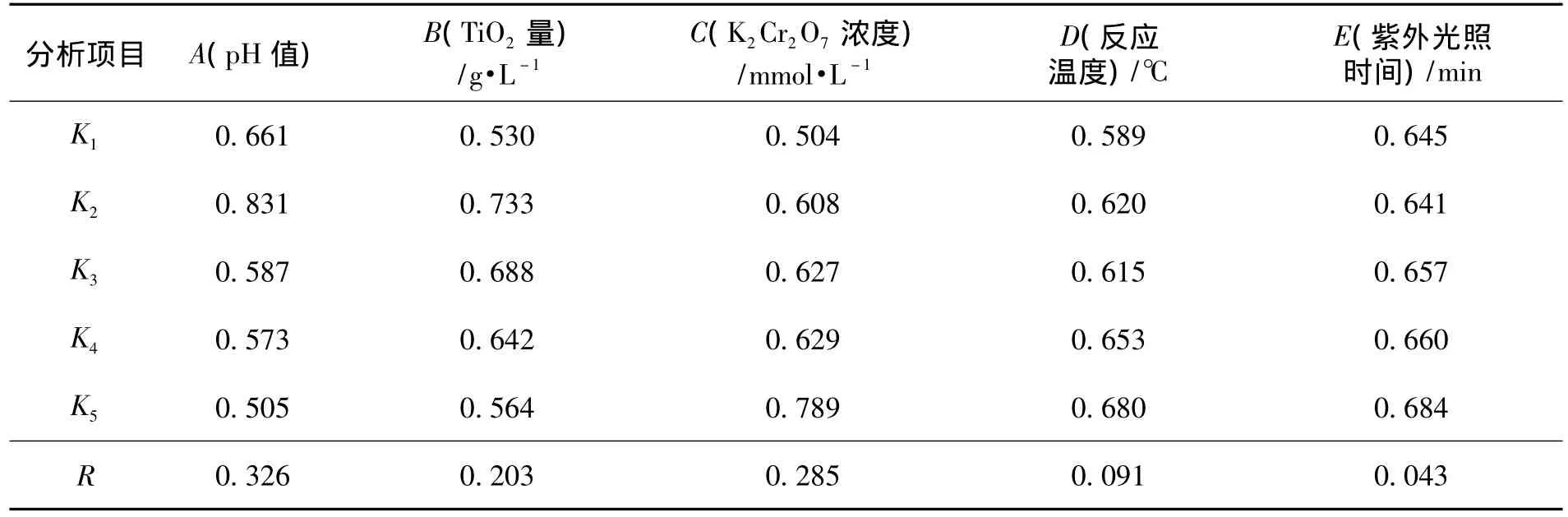
表3 极差分析表
比较 A 列 K1、K2、K3、K4、K5的大小时,可以认为 B、C、D、E 对 A 列 K1、K2、K3、K4、K5的影响大体相同.因此,可以把A列K1、K2、K3、K4、K5之间的差异看作是由于A取了5个不同的水平而引起的.选取因素的水平是与要求的指标有关的,要求的指标越大越好,应该取使指标增大的水平,即各因素列K1、K2、K3、K4、K5中最大的那个水平.所以,我们可以由Ki值大小判断各因素的水平的最优组合,从表3得到的结论是 pH 值为 1.0,TiO2量为 1.0g·L-1,K2Cr2O7的初始浓度为 10mmol·L-1,反应温度为90℃,紫外光照时间为12min为该实验的最佳条件.
A列R值最大,说明因素A水平变动时,指标波动最大,对指标的影响最大,为最主要影响因素.由表3可知,pH值对染料消解的影响是最大的,其次是K2Cr2O7浓度,再次是催化剂用量,反应温度和紫外光照时间的影响较小.pH值和K2Cr2O7浓度反映的是氧化剂因素,催化剂用量反映的是光催化剂因素,反应温度和紫外光照时间反映的是反应条件因素,可见TiO2-K2Cr2O7协同体系的两个组分对染料消解的影响都较大.
3 结论
通过正交实验,本文确定了5个因素对染料消解的影响程度从大到小依次为pH值>K2Cr2O7浓度>TiO2用量>反应温度>紫外光照时间;得出当pH值为1.0,TiO2量为1.0g·L-1,K2Cr2O7的初始浓度为10mmol·L-1,反应温度为90℃,紫外光照时间为12min时,TiO2-K2Cr2O7协同体系对甲基橙模拟废水具有最明显的光催化消解效果.
[1]张一平.TiO2-K2Cr2O7协同光催化氧化体系快速测定染料浓度[J].浙江外国语学院学报,2012(3):103-108.
[2]Fujishima A,Rao T N,Tryk D A.Titanium dioxide photocatalysis[J].Journal of Photochemistry and Photobiology,C:Photochemistry Reviews,2000(1):1-21.
[3]Fujishima A,Zhang X,Tryk D A.TiO2photocatalysis and related surface phenomena[J].Surface Science Reports,2008,63:515-582.
[4]Tong H,Ouyang S,Bi Y,et al.Nano-photocatalytic materials:Possibilities and challenges[J].Advanced Materials,2012,24(2):229-251.
[5]Ai S Y,Li J Q,Yang Y,et al.Study on photocatalytic oxidation for determination of chemical oxygen demand using a nano-TiO2-K2Cr2O7system[J].Analytica Chimica Acta,2004,509(2):237-241.
[6]李成芳,余红敏,彭毛,等.纳米二氧化钛-重铬酸钾协同光催化氧化体系快速测定化学需氧量[J].湖北大学学报:自然科学版,2009,31(1):55-58.
[7]Zhu L,Chen Y,Wu Y,et al.A surface-fluorinated-TiO2-KMnO4photocatalytic system for determination of chemical oxygen demand[J].Analytica Chimica Acta,2006,571:242-247.
[8]Li C F,Song G W.Photocatalytic degradation of organic pollutants and detection of chemical oxygen demand by fluorescence methods[J].Sensors and Actuators B:Chemical Sensors and Actuators B,2009,137:432-436.
