亚微米级球形银钯合金粉末的制备
2013-11-28熊庆丰林智杰姬爱青刘绍宏孙旭东
熊庆丰,林智杰,姬爱青,刘绍宏,3,霍 地,孙旭东
(1.贵研铂业股份有限公司,昆明 650106;2.东北大学 材料各向异性与织构教育部重点实验室,沈阳 110819;3.昆明贵金属研究所,昆明 650106)
作为制造厚膜元件的基础材料,厚膜电子浆料[1]广泛应用于生产陶瓷介质电容器、片状(或圆柱形)电容器等电子元件.纯银导电浆料存在严重的银离子迁移问题,为了有效地控制银离子的迁移[2],人们研制出Ag-Pd合金替代纯银作导电相制成 Ag-Pd导电浆料[3~5].银钯合金粉的质量直接影响电容器的质量.随着电容器的体积越来越小(如手机、手提电脑内的元件),对银钯合金粉的纯度、形貌及粒径的要求越来越严格.微电子工业高速发展的日本及欧美国家在贵金属粉末、导电银浆的研发中居国际领先水平,而我国对电子浆料的研究起步较晚.目前,大部分高精密度的电子产品中的导电浆料是由国外进口的贵金属粉末所配制.
目前,国内有关银钯合金粉的研究报道极少,也鲜见有工业规模生产的报道.过去,我国一般使用进口银钯合金粉生产电容器等电子元件.随着电子元件制造业在我国的迅速发展,在高性能银钯合金粉的研制越来越迫切.生产银钯合金粉的技术关键是如何在批量生产中控制其粒径、粒径分布及形貌[6].国内外电子元件生产要求银钯合金粉具有如下特征:高纯、球状、超细且粒径最好分布在0.24~0.6 μm之间.为满足以上要求,作者采用液相还原法,通过调节分散剂浓度和体系pH值,成功研制出高纯、球形、亚微米级的银钯合金粉体.
1 实验
实验选择硝酸银和硝酸钯为母盐,抗坏血酸为还原剂;选择氨水、氢氧化钠、无水碳酸钠、硝酸调节反应体系pH值;阿拉伯树胶作分散剂.以上试剂均为分析纯.实验步骤:按照摩尔比7∶3分别取硝酸银和硝酸钯配成氧化剂溶液;按与氧化剂摩尔比2∶1取一定量抗坏血酸配成还原剂溶液;取一定量分散剂配成底液.以上溶液均以去离子水为溶剂.根据工艺需要分别调节上述溶液的pH值后,将氧化剂溶液和还原剂溶液对称滴加到底液中.混合的同时水浴控温,磁力搅拌,控制反应温度、搅拌速度和混合的速度一致.所得粉体经过去离子水洗涤3次,然后经过无水乙醇洗涤2次,置于烘箱中80℃干燥获得最终产物.
对第一次分离所得清液进行银离子检验:向清液中加入硝酸,排除碳酸根离子的干扰,然后向清液中加入盐酸至1 mol/L,若有白色沉淀生成,则溶液中银离子没有被还原完全;对干燥收集所得粉末进行称重,计算收率.
用日本岛津公司生产的SSX-550型扫描电子显微镜(SEM)观察其形貌.用XD-3A型X射线衍射仪(XRD)测定粉末物相,测试时,CuK管电压40 kV,管电流300 mA,波长0.1540 nm,扫描范围10(°)~90(°).
2 结果及分析
2.1 pH值的作用
pH值影响着反应速率和体系电荷,因此对所得粉末影响较大.固定其他工艺条件,考察体系pH值对银粉形貌和粒径的影响.图1 c)中所示为未调体系pH值时得到的粉体,其中硝酸银溶液自身的pH为4~5,硝酸钯溶液的pH为一个较大的负值,抗坏血酸溶液为2~3.从图可以看出,pH=-1.00时,得到的颗粒分散性较差,团聚严重;当pH=2.00时,得到球形颗粒,并且颗粒分散性良好,粒径在200~300 nm;当pH值未调节时,得到的粒度分布较宽,并且表现出一定程度的团聚.因此为了得到单分散球形亚微米粉体,可将体系pH值调节到2左右.

图1 不同pH值条件下所得银钯合金粉体的SEM照片Fig.1 SEM micrographs of silver-palladium alloy powders prepared at different pH values(a)—pH= -1.00;(b)—pH=2;(c)—without pH adjustment
2.2 分散剂浓度的影响
固定其他工艺条件,考察不同分散剂浓度对银粉形貌和粒径的影响.随阿拉伯树胶和氧化剂的质量比的降低,颗粒有明显长大的趋势,与此同时,颗粒间团聚也逐渐加剧.从图2 d)可以看出,当质量比为0.01∶1时,这些颗粒为两个或三个近球形颗粒凝并所得,颗粒粒径较大,但团聚严重;从图2 a)可看出,当质量比为0.1∶1时,所得银钯粉颗粒为近球形,分散性较好,表面更加光滑,但颗粒粒径较小,因此为了得到分散性更好的粉末,在不影响粒度的前提下,增加分散剂的用量.
综上得到最优条件为:pH=2.00,分散剂和氧化剂质量比0.1∶1.将最优条件下制得的粉体在500℃下煅烧,观察其形貌(如图3),并进行X射线衍射物相分析(如图4).对照标准晶态银卡片(01-087-0719)和钯的标准卡片(01-087-0637),发现图中的各衍射峰与纯银和纯钯相均不吻合,且相对于主元素峰银峰有向高角度偏移的现象,并表现出面心立方晶体结构的特点,说明所制得的粉体为银钯合金而不是银和钯的机械混合物.图中没有出现其他杂相,说明制得粉体纯度较高.由此工艺所制得的银钯合金粉纯度较高,结晶良好,颗粒呈近球状,表面较光滑,分散性较好,粒径在300~600 nm,分散性较好,上述各指标基本能达到导电浆料的要求.

图2 不同分散剂和氧化剂质量比所得银钯合金粉体的SEM照片Fig.2 SEM micrographs of the silver-palladium alloy powders prepared at different mass ratios of Arabic gum to the oxidant
2.3 反应机理
pH值的作用主要体现在两个方面:一是影响了抗坏血酸的还原电势,从而影响它的还原能力和反应速率;二是影响银、钯离子电位差,从而影响合金化程度.
抗坏血酸是较强的还原剂,常常发生氧化还原反应,产生脱氢抗坏血酸.
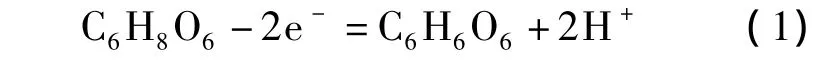
根据能斯特方程,有

可见,pH值越大,抗坏血酸浓度越大,脱氢抗坏血酸浓度越小,抗坏血酸的还原性就越强.

图3 最优条件下制得的粉体在500℃煅烧后所得粉体SEM图Fig.3 SEM micrograph of the powders calcined at 500℃
根据合金化的原理,金属离子的实际电极电势差越接近,则越易实现合金化[7~9],当两种金属离子的标准电极电势之差值小于0.2 V时,可以实现合金化.按照上述原理,通过液相化学还原法,调节银、钯金属离子的实际电势差Δφ小于0.2,可以实现银钯的合金化.从图5中可以看出,在pH<6时,银钯电势差随[NH3]T变化(在2~4 mol/L范围内)波动基本同步[9].而且由图可以查出,电势差在0.2 V处对应的pH值为3.7,故在pH<3.7时,有利于合金化粉的生成.在pH=2附近电势差为零,硝酸银、硝酸钯参加反应的电动势近似相等,可同时被还原,所以Ag-Pb粉颗粒均匀,合金化程度最高.
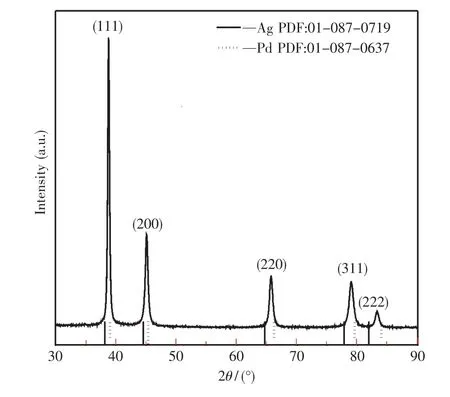
图4 最优化条件下制备的银钯合金粉的XRD图Fig.4 XRD pattern of the obtained Ag-Pd powders
阿拉伯树胶相对分子质量约为20~30万[10],对表面活性剂来说,其相对分子质量越大,空间位阻就越大,体系中颗粒不易团聚.且相同的质量意味着更少的分子数,因此所得颗粒较大.所以,选用阿拉伯树胶作分散剂,能制得粒径较大,分散较好的颗粒.随着阿拉伯树胶浓度的增加[11],一方面,一次颗粒相对不容易凝聚;另一方面,溶液的黏度增加,颗粒扩散的阻力增大了,碰撞的概率就减小了,凝聚就受到抑制.这两方面的作用,最终使得银钯粉颗粒粒径减小,团聚加剧.
计算得到该工艺制备银钯合金收率为95.7%.对分离所得清液进行离子检验:加入盐酸,无沉淀生成.由于氯化银的溶度积为1.77×10-10,因此溶液中银离子浓度小于1.77×10-10mol/L.显然可以认为反应完全,银钯的损失主要来自分离流失和器皿沾染损失.
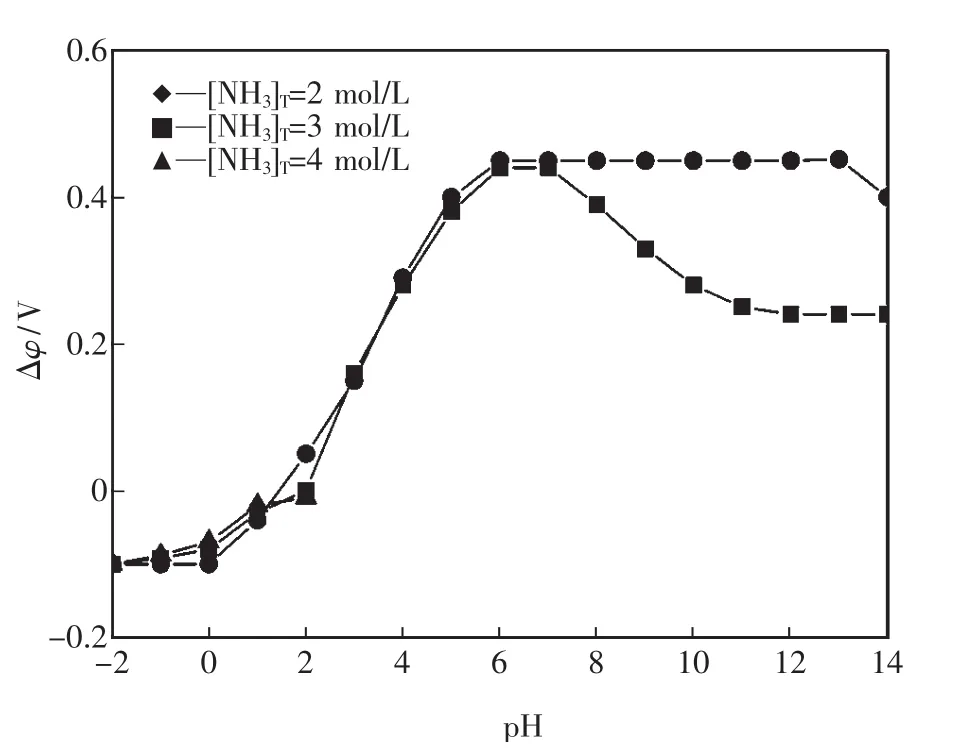
图5 Ag-Pd还原电势差与pH的关系Fig.5 The relationship between the reduction potential difference of Ag-Pd and pH
4 结论
综上所述,采用抗坏血酸做还原剂,制备银钯合金粉的最佳工艺为:用抗坏血酸还原硝酸银/硝酸钯,预先调节反应液pH为2,用阿拉伯树胶作分散剂,阿拉伯树胶与氧化剂的质量比为0.1∶1,混合方式为对称加液,后期可采用500℃烧结.所得粉末纯度高、颗粒为近球形、表面比较光滑、分散性好、平均粒径为300~600 nm,合金化程度高.上述各指标基本能达到导电浆料的要求.
[1] 张勇.厚膜导电浆料技术[J].贵金属,2001,22(4):65-68.
(Zhao Yong.Thick-Film Conductive paste technology[J].Precious Metals,22(4):65 - 68.)
[2]朱晓云.银包铜粉及聚合物导电浆料制备与性能研究[D].昆明:昆明理工大学,2010.
(Zhu Xiaoyun.Study on the synthesis and properties of silver-coated copper powder and polymer conductor slurry[D].Kunming:Kunming University of Science and Technology,2010)
[3]魏建中.银钯内电极与多层陶瓷电容器(MLC)的可靠性[J].电子产品可靠性与环境实验,2002(3):1-3.
(Wei Jianzhong.Ag-Pb Inner electrode and the reliability of multilayer ceramic capacitors(MLC)[J].Electronic Product Reliability and Environmental Testing,2002(3):1 -3.)
[4]陆广广,宣天鹏.电子浆料的研究进展与发展趋势[J].金属功能材料,2008,15(1):48-53
(Lu Guangguang,Xuan Tianpeng.Development tendency and research progress of the electronic paste[J].Metallic Functional Matrials,2008,15(1):48 -53.)
[5]徐磊,张宏亮,刘显杰.电子浆料研究进展[J].船电技术,2012(35):141-146.
(Xu Lei, Zhang Hongliang, Liu Xianjie. Revierws on electronic paste[J].Marine Electric &Electronic Engineering,2012(35):141-146.)
[6]李启厚,肖松文,刘志宏.湿法化学制粉中的粉末结构形貌控制研究进展[J].中国粉体技术,1999,5(2):21-24.
(Li Qihou,Xiao Songwen,Liu Zhihong.Research progress of the control of powder morphology in wet chemical method[J].Chian Powder Science and Technology,1999,5(2):21 -24.)
[7]曹锡章,宋天佑,王杏乔.无机化学[M].北京:高等教育出版社,1997:421-440.
(Cao Xizhang,Song Tianyou,Wang XingqiaoLIU.Inorganic chemistry[M].Beijing:Higher Educatio Press,1997:421-440.)
[8]曹茂盛.超微颗粒制备科学与技术[M].哈尔滨:哈尔滨工业大学出版社,1995:138-141.
(Cao Maosheng.Science and technology of ultrafine powder preparation[M].Harbin:Harbin Institute of Technology press,1995:138 -141.)
[9]韩维儒,朱晋.银钯合金化机理研究[J].中国有色金属学报,1998,8(2):406-409.
(Han Weiru,Zhu ji.Study on the mechanism of silver palladium alloy[J].The Chinese journal of nonferrous metals,1998,8(2):406 -409.)
[10]李祥君.新编精细化工产品手册[M].北京:化学工业出版社,1996:125-235.
(Li Xiangjun.New Handbook of fine chemical products[M].Beijing:Chemical Industry Press,1996:125-235.)
[11] Krassimir P Velikov,Gabby E Zegers,Alfons van Blaaderen.Synthesis and characterization of large colloidal silver particles[J].Langmuir,2003,19(4):1384 -1389.
