活性氧化铝对稀土溶液的吸附除氟实验研究
2013-11-28魏莹莹付红扬何金桂
魏莹莹,付红扬,李 勇,何金桂
(东北大学 材料与冶金学院,沈阳 110819)
稀土元素因其特殊的物理化学性质,广泛应用在冶金、化工、核工业、农业等领域,而被称为“工业维生素”[1].目前,稀土原料及产品主要来自氟碳铈矿,其化学式为REFCO3,是稀土碳酸盐和氟化物的复合盐.氟碳铈矿精矿中的RE2O3含量(质量分数)通常为50% ~53%[2].目前,氟碳铈矿的冶炼通常以湿法浸出+溶剂萃取为主,湿法浸出可采用酸浸出法和碱浸出法.酸浸出法应用较为广泛,其中硫酸浸出法由于有价元素浸出率高,污染环境低等突出特点而备受瞩目.但由于F-极强的配位能力,在浸出液中存在着稳定的[CeF2]2+配离子,后续萃取工艺中易产生乳化现象,致使硫酸浸出+溶剂萃取工艺还未见大规模应用[3].此外,氟元素也是稀土冶炼工业中重要的污染物,产生大量的含氟“三废”,如不对其进行处理,势必对环境造成极大危害和大量的氟资源的严重浪费.氟元素的存在,是稀土冶炼中产生环境污染和资源浪费的主要根源,必须对其进行处理和利用.
目前,工业含氟废水的“除氟”方法主要有吸附法[4~6]、沉淀法[7]、冷冻法、离子交换法[8~9]、电渗析法[10]、电凝聚法[11]、共蒸馏法[12]等,其中吸附法“除氟”具有成本低、工艺简单、吸附率高等优点,除氟吸附剂尤以活性氧化铝的吸附除氟效果最佳,被美国推荐为最佳除氟处理技术.但还未见在稀土溶液中采用该法吸附除氟的报道.本文以活性氧化铝为除氟吸附剂,对含氟硫酸稀土溶液中进行吸附“除氟”研究,使浸出液中[CeF2]2+配离子转变为游离Ce4+而进入后续的萃取流程,而F-不进入萃取流程,从而实现氟/稀土在萃取前的分离.
1 实验与方法
1.1 实验试剂与仪器
硫酸铈、氟化钠、硫酸、硫酸亚铁铵、二苯胺磺酸钠、氢氧化铝、柠檬酸三钠、硝酸钾、硝酸等均为分析纯化学试剂,购自中国国药集团.
PXSJ-216型离子计(上海精密科学仪器公司);PF-1-01型氟离子选择性电极(上海精密科学仪器公司);232型参比电极(上海精密科学仪器公司);JB-1A型磁力搅拌器(上海精密科学仪器公司);XL-100型马弗炉(鹤壁亿欣仪器仪表公司);TG-16型高速离心机(巩义市予华仪器公司);BS-224-S型电子天平(赛多利斯科学仪器公司);PW 3040/60型X射线衍射仪(荷兰Panalytical B.V公司).
1.2 实验方法
1.2.1 活性氧化铝的制备
称取一定量的氢氧化铝,装入刚玉坩埚中并置于马弗炉内,于550℃下焙烧4.0 h,然后冷却至室温,取出,粉碎,过筛,备用[13].
1.2.2 活性氧化铝的吸附除氟实验
本文采用TISAB-氟电极法测c(F-),用硫酸亚铁铵法测c(Ce4+),采用NaOH标准溶液滴定c(H+).
向500 ml烧杯中加入 c(F-)、c(Ce4+)和c(H+)都已知的含氟硫酸稀土溶液250 ml,然后加入一定量活性氧化铝,于25℃下磁力搅拌一定时间,进行吸附除氟实验.最后离心,移取上层澄清液,分别测定 c(F-)、c(Ce4+)和 c(H+).根据式(1)计算氟的吸附率:
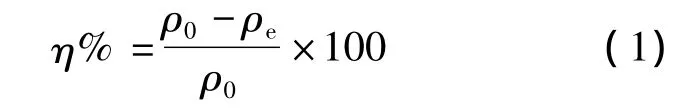
根据式(2)计算氟的吸附容量.

式(1)和式(2)中:V为含氟硫酸稀土溶液体积,ml;ρ0、ρe为吸附前后 F-、Ce4+的质量浓度,mg·L-1;m为活性氧化铝质量,g;q为吸附剂容量,mg·g-1.
2 分析与讨论
2.1 活性氧化铝的表征
通常制备活性氧化铝有氢氧化铝法、拜耳法和溶胶-凝胶法[14],其中氢氧化铝法具有工艺简单、活性强等优点而广泛应用,本文采用此方法制备活性氧化铝.所制得的活性氧化铝的XRD图谱如图1所示.
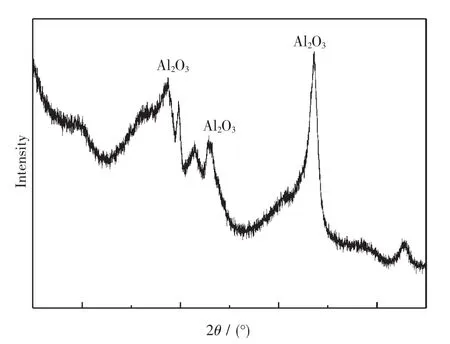
图1 活性氧化铝的XRD图Fig.1 XRD partern of the activated alumina
如图可见,在 2θ=35(°)、45(°)和 65(°)三个衍射吸收峰为γ-Al2O3的特征吸收峰,因此可确定本文制备除氟吸附剂为γ-Al2O3结构,主要反应为:
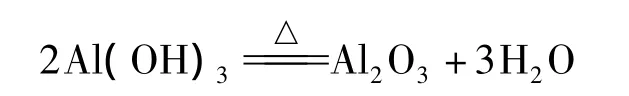
2.2 活性氧化铝的吸附“除氟”实验
2.2.1 酸度对氟吸附率影响
由于Ce4+具有较强的氧化性,在弱酸条件下易发生Ce4+→Ce3+氧化还原反应,而本文的研究体系是Ce4+-F-体系,因此必须保持一定酸度条件,[CeF2]2+配离子中的 F-才可被活性氧化铝吸附而形成游离 Ce4+,从而实现 F-/Ce4+的分离,更有利于活性氧化铝吸附游离态的氟离子.本文为考查酸度对活性氧化铝对Ce4+和F-吸附效率的影响,在不同酸度下的含氟硫酸铈溶液中加入活性氧化铝进行吸附除氟实验,并保持体系中c(F-)/c(Ce4+)=2.0,活性氧化铝用量为20 g·L-1,于 25 ℃下磁力搅拌30 min进行吸附除氟实验.在不同酸度下,F-和Ce4+的吸附率η如图2所示.
由图可见,当酸度(H+浓度)在 0~1.0 mol·L-1范围内,活性氧化铝对 F-的吸附率随着酸度的增加而增大,当酸度为0.6 mol·L-1时,趋于平缓而后再逐渐增大.而活性氧化铝对Ce4+的吸附基本维持在5%左右不变,甚至还出现了随着酸度增加而缓慢降低的现象.由此说明活性氧化铝对F-具有较好的吸附效果,主要是由于Al和F之间有极强的配位性,产生了配位吸附作用[15],而对Ce4+没有吸附作用.因此在较高的酸度下,采用活性氧化铝通过吸附作用可以达到硫酸稀土溶液中的F-/Ce4+分离作用,本文确定的酸度条件为 c(H+)≥0.6 mol·L-1.

图2 不同酸度下活性氧化铝对F-和Ce4+的吸附曲线Fig.2 The adsorption curves of activated alumina for F-and Ce4+at the different acidity
为更直观地说明活性氧化铝对F-的吸附作用,本文对活性氧化铝吸附剂在吸附除氟实验前后分别进行了表面能谱检测,结果如图3所示.图3(a)为吸附前的活性氧化铝的表面元素分布,其主要由Al和O组成,说明本文所用的吸附剂为Al2O3.图3(b)中显示的为吸附后吸附剂表面上有氟元素分布,而未见铈元素存在.由此更直观地说明了活性氧化铝吸附除氟方法是可行的.

图3 活性氧化铝吸附前后的EDS对比图Fig.3 EDS comparison chart before and after the activated alumina adsorption
2.2.2 吸附剂用量对氟吸附率影响
由前述可知,在 c(H+)≥0.6 mol·L-1时,采用活性氧化铝通过吸附作用可达到F-/Ce4+分离目的.因此,本文在 c(H+)=0.6 mol·L-1条件下,改变吸附剂用量,其他条件同前.进行吸附除氟实验,考查吸附剂用量的影响.实验结果如图4所示.
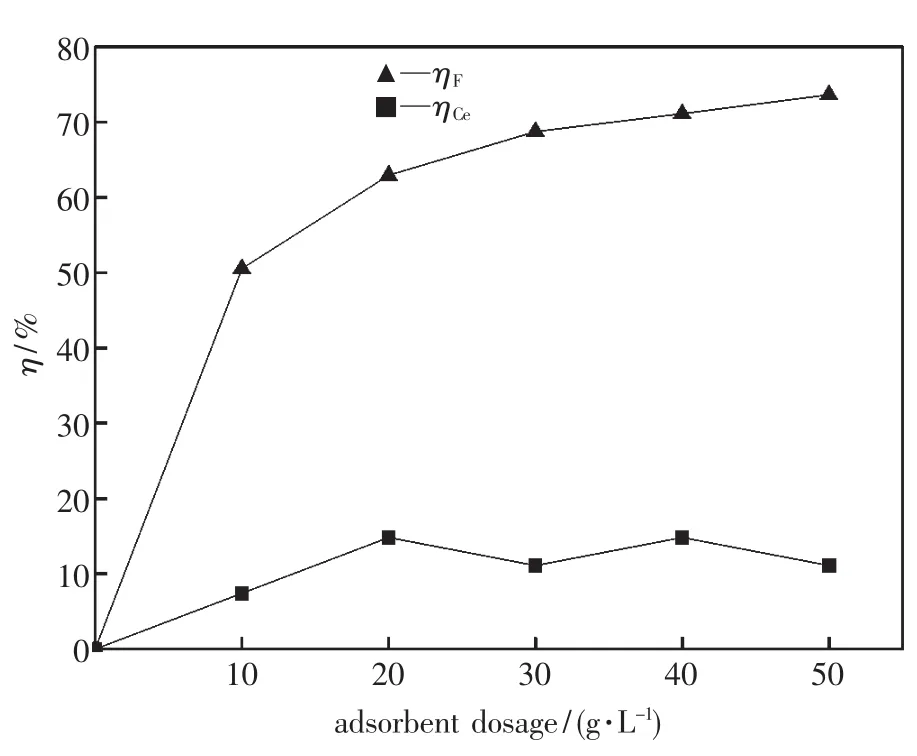
图4 不同吸附剂用量下F-和Ce4+的吸附曲线Fig.4 F-and Ce4+adsorption curve at different adsorbent dosage
由图4可见,随着吸附剂量的增加,F-吸附率逐渐增加,Ce4+吸附率没有明显变化,吸附率最高只达到10%左右.当吸附剂添加量在0~20 g·L-1时,F-吸附率迅速增大,当添加量为30 g·L-1时,F-吸附率达到70%.随后随着吸附剂量的增大,F-吸附率趋于平衡,故本文的吸附剂用量大于 20 g·L-1.
2.3 吸附动力学实验
吸附剂的动力学性能是表征吸附能力的另一个重要参数.本文选择 c(F-)/c(Ce4+)=1.8,c(H+)=0.6 mol·L-1,活性氧化铝用量为20 g·L-1,测定不同时间下的 F-和 Ce4+的吸附量.活性氧化铝的吸附动力学曲线如图5所示.
由图5可知,在初始阶段,氟的吸附速率很快,并在20 min左右接近吸附平衡.而在整个过程中,Ce4+的吸附量几乎始终为零.由此可以说明吸附剂可有效吸附F-离子,但不吸附Ce4+离子,可实现二者的分离.
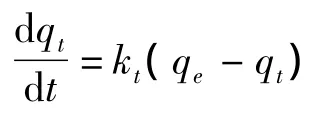

图5 活性氧化铝对氟和铈吸附动力学曲线Fig.5 Activated alumina adsorption kinetics of fluoride and cerium
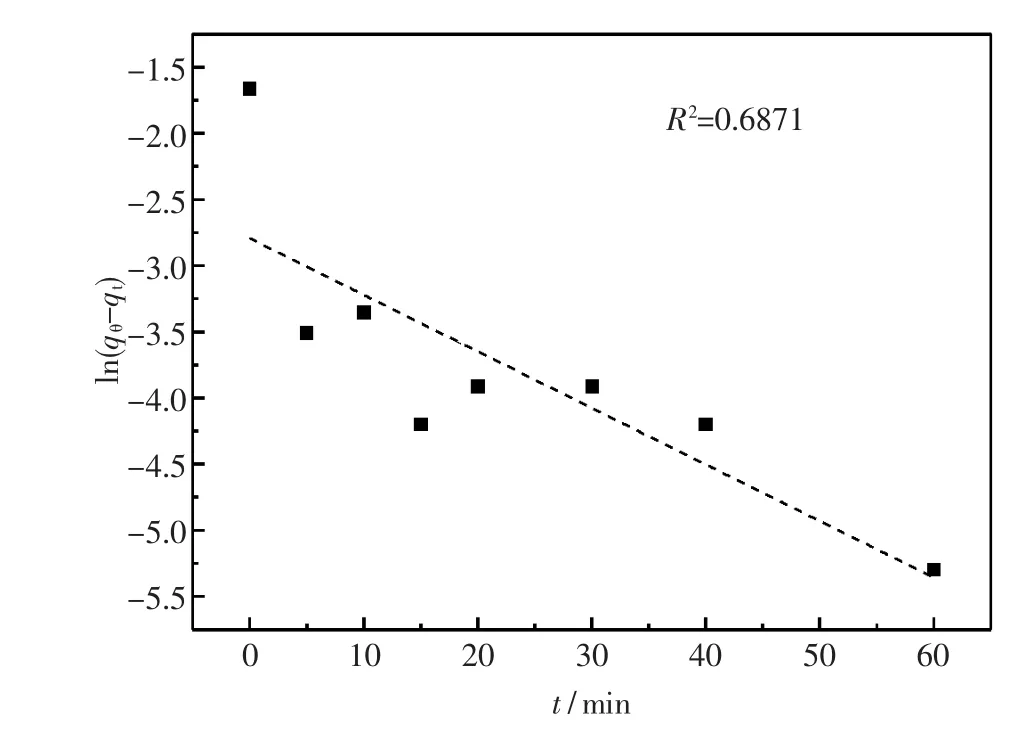
图6 活性氧化铝吸附氟的伪一级动力学模型曲线Fig.6 The pseudo first-order kinetics model curve of activated alumina adsorption fluorine
由图可知,活性氧化铝对氟的吸附按照伪二级模型线性拟合效果较好,相关系数R2>0.99.说明活性氧化铝对氟的吸附是按照二级方式变化的,即平衡吸附量是按照时间t的二次方变化的.这是由于Al3+配位数较大,它能与F-发生多元配位反应,最终能形成[AlF6]3+配离子,活性氧化铝对F-的吸附按照伪二级吸附模型进行,说明了吸附过程是十分复杂的过程.
根据图7的拟合方程,可得到活性氧化铝对氟的吸附伪二级动力学参数k2=322,平衡吸附量 qe=0.186 mg·g-1.
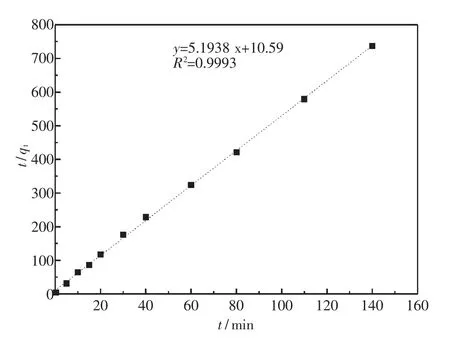
图7 活性氧化铝吸附氟的伪二级动力学拟合曲线Fig.7 The pseudo second-order kinetics model curve of activated alumina adsorption fluorine
3 结论
本文以活性氧化铝为吸附剂,在稀土元素进行萃取分离操作前,对含氟硫酸稀土溶液进行了吸附除氟的实验研究.得出如下结论:
(1)氢氧化铝经550℃焙烧4 h,制备出组成为γ-Al2O3的活性氧化铝.以其为吸附剂,对含氟硫酸稀土溶液进行吸附除氟实验,在c(H+)≥0.6 mol·L-1,吸附剂用量≥2.0 g·L-1,活性氧化铝对F-有较好的吸附率,而对Ce4+几乎没有吸附作用,可实现F-/Ce4+的分离.
(2)活性氧化铝吸附20 min就趋近吸附平衡,平衡吸附量 qe=0.186 mg·g-1.通过线性拟合显示,活性氧化铝吸附氟的过程符合伪二级模型方程:dqt/dt=k2(qe-qt)2,并计算出 k2=322.
[1]徐光宪.稀土[M].北京:冶金工业出版社,1995:4-5.
(Xu Guangxian.Rare Earths[M].Beijing:Metallurgical Industry Press,1995:4 -5.)
[2]Smart J V.Department of natural resource and mine mineral information leaflet[J].Rare Earths ,1999,7(2):361 - 362.
[3]乔军,张存瑞,柳召刚,等.溶液中F-与Ce4+络合行为的研究[J].稀土,1997,18(3):64-67.
(Qiao Jun, Zhang Cunrui, Liu Shaogang, et al.Complexation behavior of fluorine(I)with cerium(Ⅳ)in Solution[J].Rare Earths,1997,18(3):64 -67.)
[4]Raichur A M,Jyoti B M.Adsorption of fluoride onto mixed rare earth oxides[J].Separation and Purification Technology,2001(24):121-127.
[5]张超杰,周琪.含氟水治理研究进展[J].给水排水,2002(12):26-29.
(Zhang Chaojie,Zhou Ji.Reserch progress of the fluoridated water treatment[J].Water & Wastewater Engineering,2002(12):26 -29.)
[6] Krishna Biswas,Kaushik Gupta.Adsorption of fluoride by hydrous iron(Ⅲ)-tin(Ⅳ)bimetal mixed oxide from the aqueous solutions[J].Chemical Engineering Journal ,2009(149):196-206.
[7] Reardon E J,Wang Y.Limestone reactor for fluoride removal from waste waters[J].Environment Science&Technology,2000(34):3247-3253.
[8]刘斐文,肖举强,王萍,等.含氟水处理过程的“吸附交换”机理[J].离子交换与吸附,1991,7(5):378-382.
(LiuFeiwen, XiaoJuqiang, WangPing, etal. The mechanism of adsorption-exchange on treatment process of fluride-containing water[J].Ion Exchange and Adsorption ,1991,7(5):378 -382.)
[9] Reardon J.Limestone reactor for fluorine from the wastewaters[J].Environment Science&Technology,2000,34(15):3247-3253.
[10] Amor Z,Bariou B.Fluorine removal from brackish water by electrodialysis[J].Desalination,2001,133(3):215 -223.
[11]王三反,王文琴,刘义安,等.电凝聚除氟条件的研究[J].水处理技术,1990,16(4):298-03.
(Wang Sanfan,Wang Wenqin,Liu Yian,et al.Experimental studies on factors of fluorine ion disposal using electrocoagulation method [J]. Technology ofWater Treatment,1990,16(4):298 -303.)
[12]周钮明,余春香.吸附法处理含氟废水的研究进展[J].离子交换与吸附,2001,17(5):369-376.
(Zhou Niuming,Yu Chunxiang.Dewelopment on dealing with f- containing wastewater using adsorption methods[J].Ion Exchange and Adsorption,2001,17(5):369 -376.)
[13]时海平,王东田,田美玲,等.活性氧化铝的制备及除氟性能研究[J].苏州科技学院学报,2010,23(3):23-26.
(Shi Haiping,Wang Dongtian,Tian Meiling,et al.A research on preparation of activated alumina and its property of fluriode[J].Journal of Suzhou University of Science and Technology(Engineering and Technology),2010,23(3):23 -26.)
[14]杨志华,余萍,肖定全,等.利用无机盐制备γ-粉末与薄膜的工艺技术研究[J].功能材料,2004,35(37):474-476.
(Yang Zhihua,Yu Ping,Xiao Dingquan,et al.Study on the preparation of γ - Al2O3powder and thin films by sol- gel processes using inorganic precursors[J].Journal of Functional Materials,2004,35(37):474 -476.)
[15] Lounici H,Addour L.Study of a new technique for fluoride removal from water[J].DesaLination ,1979,114:241-251.
[16] Ho Y S,McKay G.(1999)The sorption of Lead(Ⅱ)ions on peat response to comment[J].Water Research,33(16):578-584.
[17] McKay G,Ho Y S.(1999)Pscudo-second-order model for sorption processes[J].Process Biochemistry,34(5):451-465.
