电喷雾质谱在金属配合物研究中的应用
2013-11-21贾晓波卜站伟李兴华赵文善
贾晓波,卜站伟,李兴华,赵文善
(河南大学 化学化工学院,河南 开封 475004)
质谱技术应用领域很广,在天然产物[1-6]、人工合成的中间体[7]、药物[8-9]、合成高分子[10]、氨基酸[11-14]及蛋白质[15-17]等领域均有应用. 但是以金属配合物为代表的非共价键化合物, 由于其键能相对于共价键而言较弱, 在传统质谱电离技术如电子轰击电离源(EI源)等高能量的电离过程中会被破坏,所以传统质谱技术很少用于研究金属配合物等非共价化合物. 随着质谱技术的发展特别是20世纪80年代以后电喷雾电离(ESI)技术(“软电离”技术)的发展,使得质谱方法逐渐成为研究金属配合物、确定未知化合物结构、自组装膜与胶束[18-19]及探索化学反应机理强有力的分析工具之一.
电喷雾电离技术之所以能成为研究金属配合物的工具,是因为电喷雾质谱独特的“软电离”技术,使样品溶液在通过带高电压的不锈钢毛细管柱后形成带电荷的小液滴,然后经过脱除溶剂,使待测物以单电荷或多电荷的形式进入气相,由于在电离过程中不涉及任何高能量的激发过程,对样品的破坏程度很小,因此电喷雾质谱可以用来研究金属配合物及以非共价键结合的化合物.
1 电喷雾质谱研究金属配合物的优势
研究金属配合物的方法很多,如谱学方法(红外光谱法、紫外光谱法、光散射法、荧光法、X射线晶体衍射法、NMR等)、量热法以及色谱法等. 这些方法各有优缺点,如NMR能为结构分析提供丰富的信息,但NMR检测所需的样品必须是纯净的,而样品的提纯又非常困难[20];X射线晶体衍射法需要提供样品的晶体,限制了在结构表征方面的应用. 此外,UV、IR等仅仅可以提供有限的结构信息[21]. 质谱法虽然不能像NMR和X射线晶体衍射法直接提供结构上的精确信息,但是质谱可以提供重要的化学当量信息,对样品的纯度要求不高,所需样品量少、灵敏度高、检测时间短. 相对于其他传统方法,质谱法在研究金属配合物方面具有一些特定的优势,MCLAFFERTY就提出过质谱法有4个“S”即: Specificity, Speed,Sensivvity, Stoichiometry[22]方面的优势. 电喷雾电离过程如图1所示.
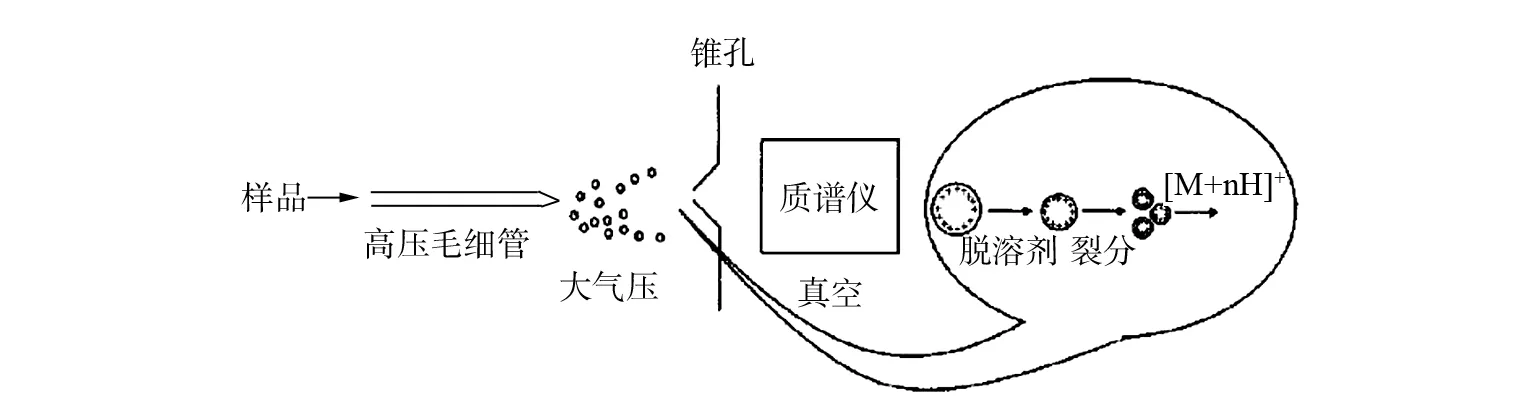
图1 电喷雾电离化过程Fig.1 Electrospray ionization process
2 电喷雾质谱在研究金属配合物中的应用
2.1 测定金属配合物的相对分子质量
由于电喷雾质谱的“软电离”特点,使得金属配合物在电离过程中结构不遭受破坏,从而能得到准确可靠的相对分子质量信息. FENG[23]利用电喷雾质谱检测了不同pH下水溶液中金属蛋白酶(Matrilysin)与金属离子(Zn2+和Ca2+)结合的当量关系. 王志强[24]等利用电喷雾质谱负离子模式测定了反式-二氯四吡啶合钌的电喷雾质谱行为,得到了[RuCl2(py)4(CH3OH)]-离子峰,m/z=485.2. 如图2所示.
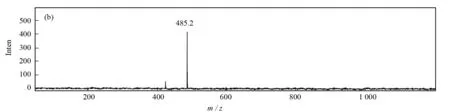
图2 [RuCl2(py)4(CH3OH)]-的电喷雾质谱图Fig.2 ESI-MS spectra of [RuCl2(py)4(CH3OH)]-
孙世国等[25]利用电喷雾质谱研究了2,2′-联吡啶-4,4′-二羧酸乙酯与过渡金属铼的系列配合物,测定了其相对分子质量,总结了不同配合物破碎的难易程度.
2.2 用于金属配合物的结构分析和表征
质谱法测定的相对分子质量是用来表征化合物结构的基本信息,根据分子裂解规律与分子结构之间的关系,通过m/z分子离子峰及其强度,可以推测未知化合物的可能结构.
WU等[26]对双金属氧化钒化合物进行了电喷雾质谱研究,由串联质谱测试产生的碎片离子m/z=214,200和182得知,这些碎片元素组成分别为V2O7、C3NV2O3和V2O5,揭示了化合物中含有V-O-V桥键.
随着电喷雾电离技术和FTICR、FAB以及TOF等高分辨质量分析器的联用,电喷雾质谱能更加精确地测定金属配合物的相对分子质量,为其结构的分析和表征进一步提供了准确、可靠的信息.
2.3 用于研究金属配合物的选择性和稳定性
用电喷雾质谱研究以金属配合物为代表的非共价键化合物的结合选择性常采用竞争的方法,在质谱图中比较不同配合物离子的丰度来评估不同配体的结合选择性. 该方法所需样品极少(通常在nmol级),是衡量体系中结合选择性和亲和力的有效、准确、快速的方法.
GANEM等[27]于1991年首次将电喷雾质谱用于研究免疫蛋白FKBP12和几种不同的免疫抑制药物形成的非共价键化合物,电喷雾质谱在非共价键化合物研究中的应用越来越多并逐渐成为研究的主要手段之一.
KEMPEN等人[28]利用电喷雾质谱考察了侧基分别为甲氧基、羧酸、酯或酰胺的二苯并-15-冠-5-套索醚对Na+、Li+、K+的结合选择性,发现在甲醇溶液中套索醚对Na+的选择性最好.
BLAIR等[29]人利用电喷雾质谱研究Pb2+、Hg2+、Cu2+、Ca2+与二氮-15冠-5的选择性结合,其中Pb2+与笼型穴状配体衍生物结合,Hg2+则与大部分笼型化合物结合. 该方法已经用于评估生化体系中的非共价复合物的亲和力和选择性,如蛋白-药物[30-32]、DNA-药物[32-33]、蛋白-多肽[34]等.
由于有些金属配合物在不同条件下稳定性不同,因此测定金属配合物的结合常数对于选择合成配合物的条件十分重要. 近年来,RAGULAN RAMANATHAN等人[35-38]分别利用电喷雾技术测定了非共价化合物间的结合常数,该方法适合于研究配体和金属离子形成金属配合物的结合常数.
张海震[39]等利用竞争平衡的方法,使用电喷雾质谱测定了络合物的结合常数,推导出了待测络合物[18-冠-6—Na]+、[二苯并-18-冠-6—K]+和[二苯并-18-冠-6—Na]+的结合常数.
YONG等[40]依据电喷雾质谱测定了结合和游离的主、客体离子丰度,计算了一系列套索冠醚-碱金属离子复合物的结合常数.
2.4 用于研究相关反应机理
通过检测有机反应活性中间体,可以跟踪反应进程和探究反应机理. 电喷雾质谱可以迅速检测到反应活性中间体的质核比、同位素分布、以及活性中间体离子的演变过程[41-42]. 目前,该方法在检测反应活性中间体、验证反应机理方面取得了突破性的进展[43-44].
WILSON[45]等验证了电喷雾质谱可以用于检测反应瞬态中间体,他们利用一系列有机膦反应(Wittig、Mitsunobou、Staudinger反应)进行了验证,检测到了所有的离子以及许多中性物种的质子化离子,证明了电喷雾质谱方法可直接用于反应中间体的研究.
ERBERLIN等[46]利用电喷雾质谱研究了Heck偶联反应的机理,成功地捕捉到了反应的活性中间体,为反应机理的论证提供了依据. 如图3所示.
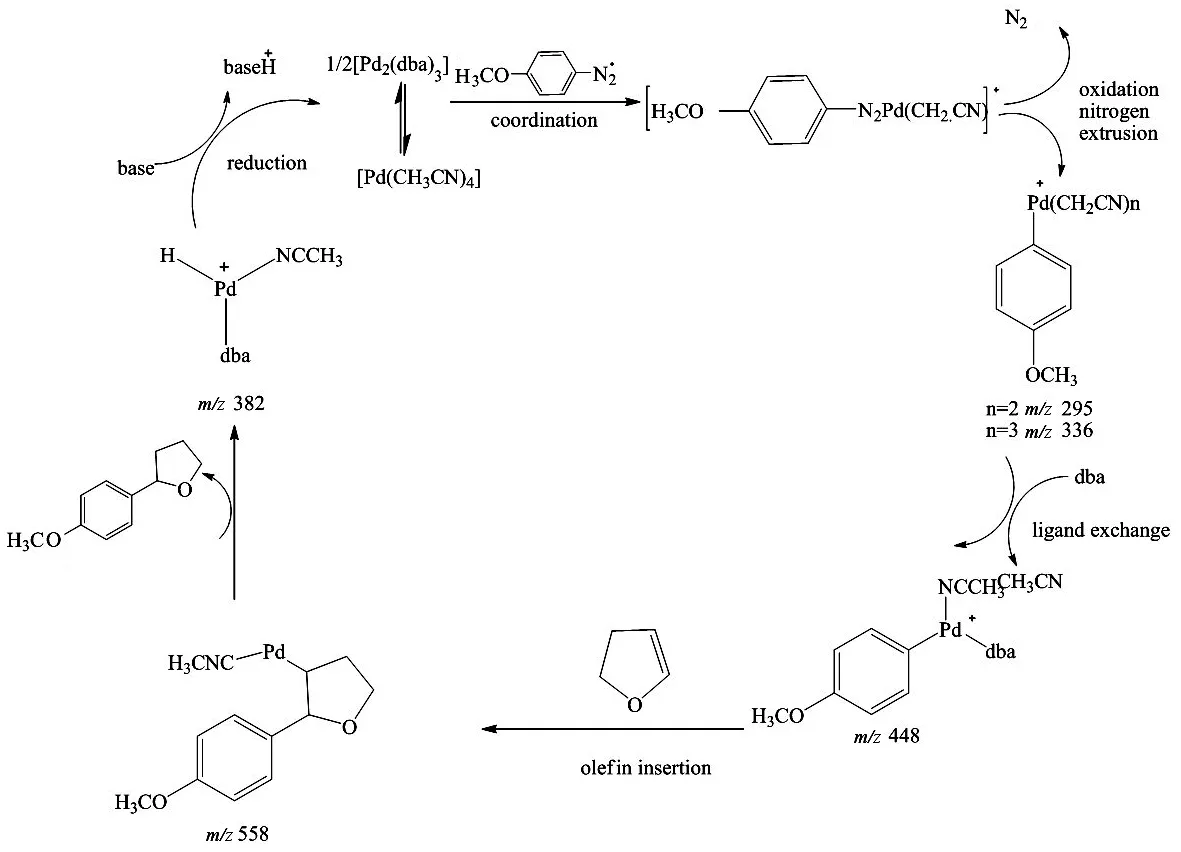
图3 芳烃重氮盐与Heck反应的催化机理Fig.3 Proposed catalytic cycle for the Heck reaction with arene diazonium salts
麻生明[47]等在无水无氧条件下,通过快速冷却的方法降低反应速度,直接利用电喷雾质谱进行了Pd(0)催化的三组分串联双加成环化反应研究,成功检测到了活泼中间体离子(图4),并推测了反应的可能机理. 如图5所示.
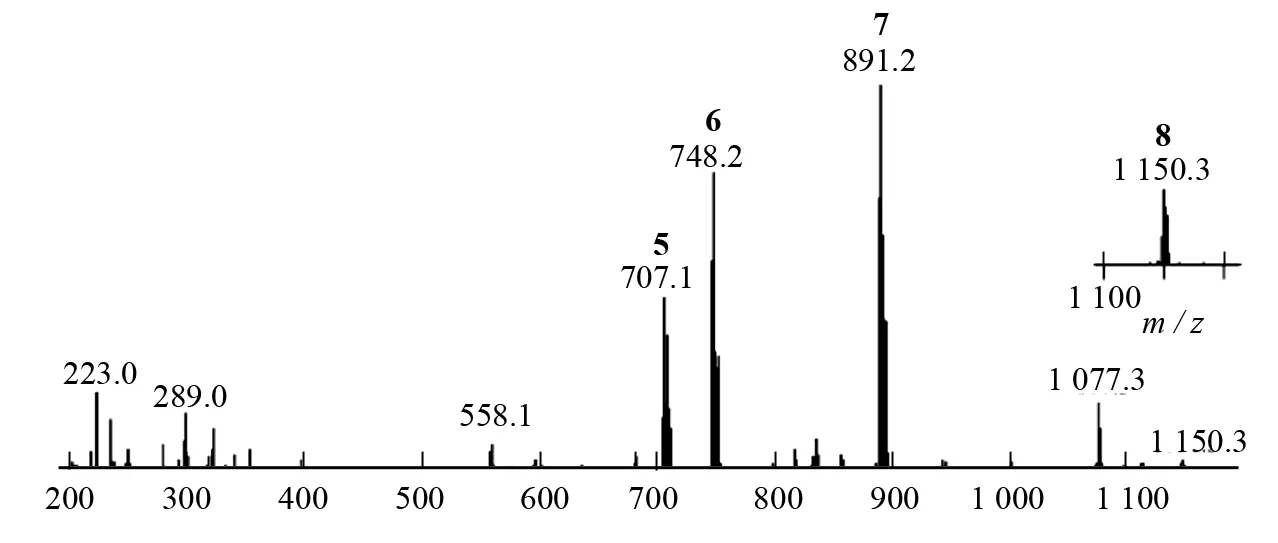
图4 Pd(0)催化的三组分串联双加成环化反应中间体的质谱图Fig.4 Pd(0)-catalyzed three-component tandem double reaction addition-cyclization reaction
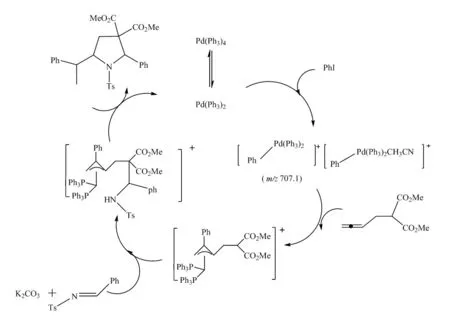
图5 Pd (0)催化三组分串联双加成环化反应研究的机理图Fig.5 The mechanism of Pd(0)-catalyzed three-component tandem double addition-cyclization reaction
RAO Dun Yan等[48]利用电喷雾质谱研究了SalenCr(Ⅲ)1a/DMAP、SalanCr(Ⅲ-)2a/DMAP催化体系催化CO2与环氧丙烷(PO)共聚生成脂肪族聚碳酸酯(PPC)的反应,成功检测到了反应的活性中间体并探讨了可能的反应机理. 如图6所示.
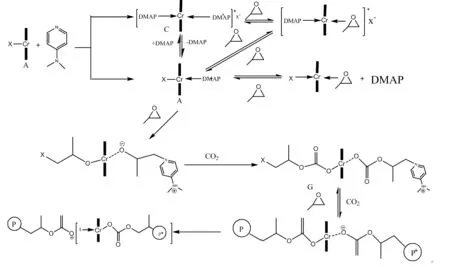
图6 Salan-或Salen-Cr(III)X/DMAP催化CO2/PO共聚反应机理Fig.6 Proposed mechanism of CO2/PO copolymerization catalyzed by binary salan- or salen-Cr(III)X/DMAP systems
ZHANG Xing Hong等[49]利用电喷雾质谱研究了纳米级的DMC(Double metal cyanide complex)催化CO2和PO共聚生成PPC的催化机理,并根据电喷雾质谱检测到的分子量信息,推测了可能的反应机理. 其电喷雾质谱图如图7所示.
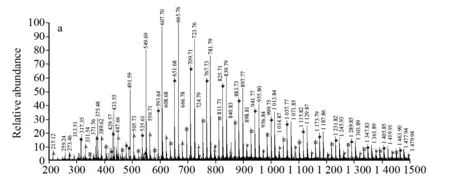
图7 CO2-PO共聚的电喷雾质谱图Fig.7 ESI-MS spectra of the CO2-PO copolymer
本课题组利用电喷雾质谱成功检测到了RuCl3[2,2′-bipy (CH3OH)](2,2′-联吡啶钌配合物)/CTAC(十六烷基三甲基氯化铵)催化体系催化CO2和PO反应生成环状碳酸酯的活性中间体,并提出了可能的反应机理[50](如图8所示).
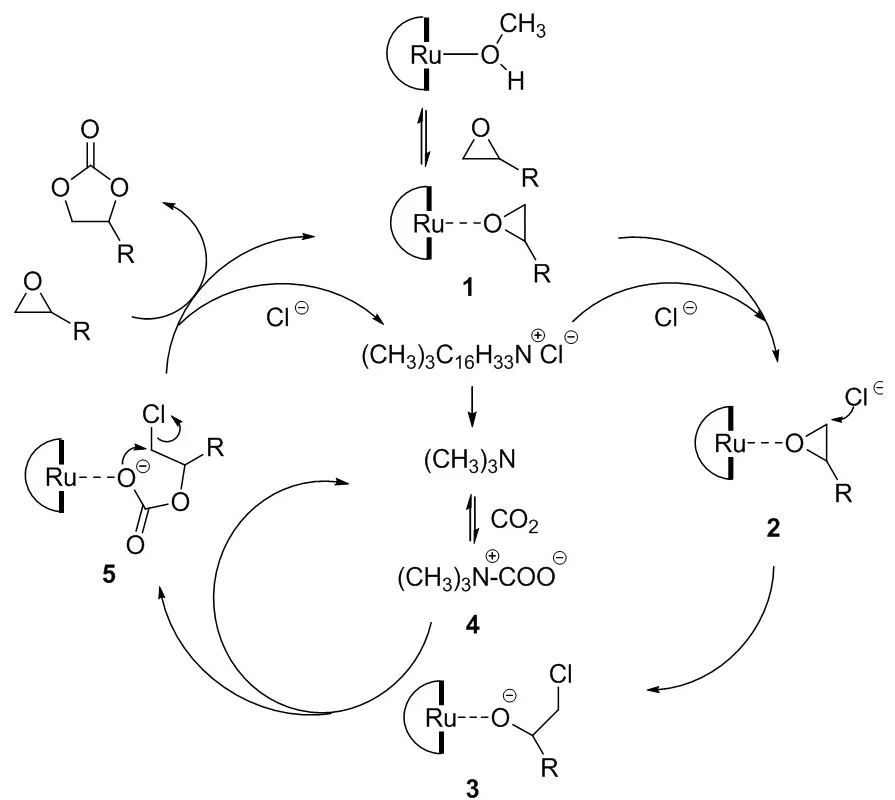
图8 [RuCl3[2,2′-bipy (CH3OH)]/CTAC催化反应机理Fig.8 [RuCl3[2,2′-bipy (CH3OH)]/ CTAC catalytic reaction mechanism
3 仪器参数的选择
电喷雾质谱仪的参数设定以及样品制备等在研究金属配合物中至关重要,会直接影响到金属配合物离子的组成及稳定性[51].
电喷雾离子源部分参数的优化,是测定金属配合物时首先需要考虑的因素. 电喷雾离子源温度在保证能使样品雾化电离的条件下,温度越低越好,以减少配合物中非共价键的断裂和相互作用,但离子源温度降低会降低电喷雾离子化过程中的脱除溶剂的效率,会导致离子峰数目增多、分析灵敏度下降;毛细管和反电极之间的电压或源内裂解电压过高会造成配合物结构的改变,产生碎片离子,给谱图解析带来困难.
GOODLETT等人[52]研究了电喷雾质谱离子源内温度、电压对s多肽链和s蛋白质组成的非共价复合物稳定性的影响,发现温度和电压过高都会造成复合物的分解,引起离子峰消失.
另外如果配合物样品中含有大量不挥发性盐会导致加合离子的形成,降低检测的灵敏度, 给测定分子质量造成困难,因此在调节溶液pH时最好采用乙酸-乙酸铵等挥发性的缓冲盐. 溶剂应尽量选择极性大(易使样品离子化)且不与被测物反应,通常采用的极性溶剂为乙腈、甲醇、水等,因为它们具有显著的质子自递作用,有利于离子的形成.
因此电喷雾质谱的检测条件如温度、电压、样品溶液的pH、有机溶剂的选择等是在研究金属配合物时必须考虑的几个重要因素.
4 总结与展望
综上所述, 电喷雾质谱方法为研究金属配合物的结构、反应活性中间体及探究反应机理打开了一扇窗,独特的“软电离”优势,成为当今质谱最活跃的研究领域,其应用范围比传统质谱有了很大的扩展. 随着具有低流速、超高灵敏度的以纳升级电喷雾质谱仪为代表的新一代质谱仪的出现,可以在最少的样品消耗量下获得高灵敏度,其喷雾产生的液滴体积更小,加速了脱溶剂的进程,降低了脱溶剂所需的温度和热量[54]. 此外,电喷雾电离源与飞行时间 (TOF)和傅立叶变换离子回旋共振 (FTICR) 等新一代高分辨检测器的联用,使电喷雾质谱在分辨率、检测灵敏度、准确性及质量检测范围等方面的性能都有了很大提升. 但随着对样品检测要求的不断提高,电喷雾质谱也暴露出了一些需要提高和完善的地方,如:(1)目前电喷雾质谱的离子化过程需要对溶液进行加热,以脱去溶剂,一些对温度敏感的金属配合物、超分子、蛋白质等就不适合使用. (2)电喷雾技术可以捕捉和跟踪活性中间体(离子型中间体和中性中间体),但是由于一些反应的活性中间体配位方式复杂、相互作用力弱、反应速度较快, 不易被现有的电喷雾质谱所捕获,所有这些都有待于电喷雾质谱技术的进一步发展和完善. 相信不远的将来电喷雾质谱在研究金属配合物及其他方面的应用范围会更加广泛.
参考文献:
[1] VIEGAS C J R,SILVA D H S,PIVATTO M,et al. Lipoperoxidation and cyclooxygenase enzyme inhibitory piperidine alkaloids from Cassia spectabilis green fruits [J]. J Nat Prod, 2007, 70(12): 2026-2028.
[2] CROTTI A E M,LOPES J L C,LOPES N P. Triple quadrupole tandem mass spectrometry of sesquiterpene lactones: a study of goyazensolide and its congeners [J]. J Mass Spectrom, 2005, 40(8): 1030-1034.
[3] LOPES N P,GATES P J,WILKINS J P G,et al. Fragmentation studies on lasalocid acid by accurate mass electrospray mass spectrometry [J]. Analyst, 2002, 127(9): 1224-1227.
[4] WANG Yong,SONG Feng Rui,XU Qing Xuan,et al. Characterization of aconitine-type alkaloids in the flowers of Aconitum kusnezoffii by electrospray ionization tandem mass spectrometry [J]. J Mass Spectrom, 2003, 38(9): 962-970.
[5] FONSECA T,LOPES N P,GATES P J,et al. Fragmentation studies on tetronasin by accurate-mass electrospray tandem mass spectrometry [J]. J Am Soc Mass Spectrom, 2004, 15(3): 325-335.
[6] REALE S,TULLIO A D,SPRETI N,et al. Mass spectrometry in the biosynthetic and structural investigation of lignins [J]. Mass Spectrom Rev, 2004, 23(2): 87-126.
[7] SILVA L F J,LOPES N P. A study on the species present in solutions of hypervalent iodine (III) reagents by electrospray ionization mass spectrometry [J]. Tetrahedron Lett, 2005, 46(36): 6023-6027.
[8] SANTOS M D D,MARTINS P R,SANTOS P A D,et al. Oxidative metabolism of 5-O-caffeoylquinic acid (chlorogenic acid), a bioactive natural product, by metalloporphyrin and rat liver mitochondria [J]. Eur J Pharm Sci, 2005, 26(1): 62-70.
[9] GUARATINI T,GATES P J,CARDOZO K H,et al. Letter: radical ion and protonated molecule formation with retinal in electrospray and nanospray [J]. Eur J Mass Spectrom, 2006, 12(1): 71.
[10] MCEWEN C N,SIMONSICK W J J,LARSEN B S,et al. The fundamentals of applying electrospray ionization mass spectrometry to low mass poly (methyl methacrylate) polymers [J]. J Am Soc Mass Spectrom, 1995, 6(10): 906-911.
[11] DONGRE A R,SOMOGYI A,WYSOCKI V H. Surface-induced dissociation: an effective tool to probe structure, energetics and fragmentation mechanisms of protonated peptides [J]. J Mass Spectrom, 1996, 31(4): 339-350.
[12] HARRISON A G,YOUNG A B,BLEIHOLDER C,et al. Scrambling of sequence information in collision-induced dissociation of peptides [J]. J Am Chem Soc, 2006, 128(32): 10364-10365.
[13] JURCHEN J C,WILLIAMS E R. Origin of asymmetric charge partitioning in the dissociation of gas-phase protein homodimers [J]. J Am Chem Soc, 2003, 125(9): 2817-2826.
[14] YU Ying Qing,STUMPF C L,HILKKA I KENTTMAA. Gas-phase fragmentation of di- and tripeptides via ion-molecule reactions with ClPCl+[J]. Int J Mass spectrom, 2000, 195: 609-623.
[15] FENAILLE F,GUY P A,TABET J C. Study of protein modification by 4-hydroxy-2-nonenal and other short chain aldehydes analyzed by electrospray ionization tandem mass spectrometry [J]. J Am Soc Mass Spectrom, 2003, 14(3): 215-226.
[16] HUDGINS R R,WOENCKHAUS J,JARROLD M F. High resolution ion mobility measurements for gas phase proteins: correlation between solution phase and gas phase conformations [J]. Int J Mass Spectrom Ion Processes, 1997, 165: 497-507.
[17] PAIZS B,SUHAI S. Fragmentation pathways of protonated peptides [J]. Mass Spectrom Rev, 2005, 24(4): 508-548.
[18] BECK J L,COLGRAVE M L,RALPH S F,et al. Electrospray ionization mass spectrometry of oligonucleotide complexes with drugs, metals, and proteins [J]. Mass Spectrom Rev, 2001, 20(2): 61-87.
[19] RAY S S,BALARAM P. 1-Anilino-8-naphthalene-sulfonate (ANS) binding to proteins investigated by electrospray ionization mass spectrometry: correlation of gas-phase dye binding to population of molten globule states in solution [J]. Phys Chem B, 1999, 103(34): 7068-7072.
[20] GUO Qi Xiang,WU Zhi Jun,LUO Zhi Bin,et al. Highly enantioselective oxidative couplings of 2-naphthols catalyzed by chiral bimetallic oxovanadium complexes with either oxygen or air as oxidant [J]. J Am Chem Soc, 2007, 129(45): 13927-13938.
[21] SOMEI H,ASANO Y,YOSHIDA T,et al. Dual activation in a homolytic coupling reaction promoted by an enantioselective dinuclear vanadium (IV) catalyst [J]. Tetrahedron Lett, 2004, 45(9): 1841-1844.
[22] MCLAFFERTY F W. Tandem mass spectrometry [J]. Science, 1981, 214(4518): 280-287.
[23] FENG R, CASTELHANO A L,BILLEDEAU R,et al. Study of noncovalent enzyme-inhibitor complexes and metal binding stoichiometry of matrilysin by electrospray ionization mass spectrometry [J]. J Am Soc Mass Spectrom, 1995, 6(11): 1105-1111.
[24] 齐红卫,王志强,曹婷婷,等. 反式-二氯四吡啶合钌催化CO2制备碳酸丙烯酯机理探讨[J]. 河南大学学报:自然科学版, 2012, 42(01): 42-46.
[25] 孙世国,彭孝军,张 蓉,等. 铼联吡啶配合物的电喷雾质谱研究[J]. 有机化学, 2003, (10): 1135-1138.
[26] WU Zhi Jun,XU Xiao Ying,LUO Shi Wei,et al. Electrospray mass spectrometry and tandem mass spectrometry of bimetallic oxovanadium complexes [J]. J Am Soc Mass Spectrom, 2008, 19(9): 1247-1254.
[27] GANEM B,LI Y T,HENION J D. Detection of noncovalent receptor-ligand complexes by mass spectrometry [J]. J Am Chem Soc, 1991, 113(16): 6294-6296.
[28] KEMPEN E C,BRODBELT J S. A method for the determination of binding constants by electrospray ionization mass spectrometry [J]. Anal Chem, 2000, 72(21): 5411-5416.
[29] BLAIR S M,BRODBELT J S,ALAN P MARCHAND,et al. Evaluation of binding selectivities of caged crown ligands toward heavy metals by electrospray ionization/quadrupole ion trap mass spectrometry [J]. Anal Chem, 2000, 72(11): 2433-2445.
[30] KEMPEN E C,BRODBELT J S,BARTSCH R A,et al. Investigation of alkali metal cation selectivities of lariat ethers by electrospray ionization mass spectrometry [J]. Anal Chem, 1999, 71(24): 5493-5500.
[31] CHENG Xue Heng,CHEN Rui Dan,BRUCE J E,et al. Using electrospray ionization FTICR mass spectrometry to study competitive binding of inhibitors to carbonic anhydrase [J]. J Am Chem Soc, 1995, 117(34): 8859-8860.
[32] TRIOLO A,ARCAMONE F M,RAFFAELLI A,et al. Non-covalent complexes between DNA-binding drugs and double-stranded deoxyoligonucleotides: a study by ion spray mass spectrometry [J]. J Mass Spectrom, 1997, 32(11): 1186-1194.
[33] GABELICA V,PAUW E D,ROSU F. Interaction between antitumor drugs and a double-stranded oligonucleotide studied by electrospray ionization mass spectrometry [J]. J Mass Spectrom, 1999, 34(12): 1328-1337.
[34] SANNES-LOWERY K A,MEI H Y,LOO J A. Studying aminoglycoside antibiotic binding to HIV-1 TAR RNA by electrospray ionization mass spectrometry [J]. Int J Mass Spectrom Ion Phys, 1999, 193(2): 115-122.
[35] RAMANATHAN R,PROKAI L. Electrospray ionization mass spectrometric study of encapsulation of amino acids by cyclodextrins [J]. J Am Soc Mass Spectrom, 1995, 6(9): 866-871.
[36] LOO J A,PEIFENG H ,MCCONNELL P,et al. A study of Src SH2 domain protein-phosphopeptide binding interactions by electrospray ionization mass spectrometry [J]. J Am Soc Mass Spectrom, 1997, 8(3): 234-243.
[37] GREIG M J,GAUS H,CUMMINS L L,et al. Measurement of macromolecular binding using electrospray mass spectrometry. Determination of dissociation constants for oligonucleotide: serum albumin complexes [J]. J Am Chem Soc, 1995, 117(43): 10765-10766.
[38] GRIFFEY R H,HOFSTADLER S A,SANNES-LOWERY K A,et al. Determinants of aminoglycoside-binding specificity for rRNA by using mass spectrometry [J]. Proc Natl Acad Sci, 1999, 96(18): 10129-10133.
[39] 张海震,颜肖慈. 电喷雾离子化质谱测定冠醚与碱金属离子的结合常数[J]. 武汉大学学报:理学版, 2005 (02): 154-156.
[40] YOUNG D S,HUNG H Y,LIU L K. An easy and rapid method for determination of stability constants by electrospray ionization mass spectrometry [J]. Rapid Commun Mass Spectrom, 1997, 11(7): 769-773.
[41] ROBB D B,COVEY T R,BRUINS A P. Atmospheric pressure photoionization: an ionization method for liquid chromatography-mass spectrometry [J]. Anal Chem, 2000, 72(15): 3653-3659.
[42] BERKEL G J V,MCLUCKEY S A,GLISH G L. Electrochemical origin of radical cations observed in electrospray ionization mass spectra [J]. Anal Chem, 1992, 64(14): 1586-1593.
[43] ALIPRANTIS A O,CANARY J W. Observation of catalytic intermediates in the Suzuki reaction by electrospray mass spectrometry [J]. J Am Chem Soc, 1994, 116(15): 6985-6986.
[44] GRIEP-RAMING J,MEYER S,BRUHN T,et al. Investigation of reactive intermediates of chemical reactions in solution by electrospray ionization mass spectrometry: radical chain reactions [J]. Angew Chem Int Ed, 2002, 41(15): 2738-2742.
[45] SANTOS L S,PAVAM C H,ALMEIDA W P,et al. Probing the mechanism of the Baylis-Hillman reaction by electrospray ionization mass and tandem mass spectrometry [J]. Angew Chem Int Ed, 2004, 43(33): 4330-4333.
[46] SABINO A A,MACHADO A H L,ROQUE C D,et al. Probing the mechanism of the Heck reaction with arene diazonium salts by electrospray mass and tandem mass spectrometry [J]. Angew Chem Int Ed, 2004, 43(19): 2514-2518.
[47] GUO Hao,QIAN Rong,LIAO Yuan Xi,et al. ESI-MS studies on the mechanism of Pd (0)-catalyzed three-component tandem double addition-cyclization reaction [J]. J Am Chem Soc, 2005, 127(37): 13060-13064.
[48] RAO Dun Yan,LI Bo,ZHANG Rong,et al. Binding of 4-(N, N-dimethylamino) pyridine to Salen-and Salan-Cr (III) cations: a mechanistic understanding on the difference in their catalytic activity for CO2/epoxide copolymerization [J]. Inorg Chem, 2009, 48(7): 2830-2836.
[49] ZHANG Xing Hong,WEI Ren Jian,SUN Xue Ke,et al. Selective copolymerization of carbon dioxide with propylene oxide catalyzed by a nanolamellar double metal cyanide complex catalyst at low polymerization temperatures [J]. Polymer, 2011, 52(24): 5494-5502.
[50] 卜站伟,王志强,秦 刚,等. 2,2′-联吡啶钌配合物催化CO2制备环状碳酸酯机理研究[J]. 化学学报, 2010(18): 1871-1875.
[51] PRAMANIK B N,BARTNER P L,MIRZA U A,et al. Electrospray ionization mass spectrometry for the study of non-covalent complexes: an emerging technology [J]. J Mass Spectrom, 1998, 33(10): 911-920.
[52] GOODLETT D R,LOO R R O,LOO J A,et al. A study of the thermal denaturation of ribonuclease S by electrospray ionization mass spectrometry [J]. J Am Soc Mass Spectrom, 1994, 5(7): 614-622.
[54] WILM M,MANN M. Analytical properties of the nanoelectrospray ion source [J]. Anal Chem, 1996, 68(1): 1-8.
