高强脉冲电场强化甘氨酸铜螯合反应*
2013-11-21于倩曾新安
于倩,曾新安
(华南理工大学轻工与食品学院,广东广州,510641)
铜是动物和人体必需的微量元素之一,在机体的组成和代谢中起着很重要的作用[1]。一方面,它是肌体中很多金属酶的组成成分,另一方面也是一些蛋白的辅基,对某些蛋白质的合成有促进作用[2]。与无机铜盐相比,氨基酸铜作为第三代铜补充剂具有独特的优势,可以缓解矿物之间的拮抗作用,而且稳定性好,生物学效价高[3],易吸收,因此近年来受到了广泛的关注。目前氨基酸和铜的螯合反应主要采用液相反应,存在反应时间长,效率低的缺点[4]。因此,寻找一种更为高效的合成方法有重要意义。
脉冲电场(pulsed electric fields,PEF)是一种新兴的非热杀菌手段,在保证良好的杀菌效果的同时,对食品的色泽、口感以及营养物质保存较好,成为近年来食品生物领域的研究热点[5-8],脉冲电场对美拉德反应有一定的促进作用[9-11],脉冲电场可显著促进酯化反应,降低其活化能[12-13]。但是,关于PEF处理对螯合反应的影响还未见报道。本文以甘氨酸和硫酸铜为研究对象,研究PEF对该螯合反应的影响。
1 材料与方法
1.1 材料与试剂
主要材料:甘氨酸(分析纯,博奥生物有限公司,上海)、CuSO4·5H2O(分析纯,启轮化学科技有限公司,天津)、甘氨酸铜(分析纯,恒绿源科技有限公司,湖北)、强酸性苯乙烯阳离子交换树脂(ZG107,争光树脂有限公司,杭州)。
1.2 仪器与设备
脉冲电场设备为自主开发(专利号:02152160),由高压脉冲发生器,蠕动泵,处理室和示波器4个部分组成,产生的波为方形波,脉宽为40 μs,频率1 kHz,场强为0~50 kV/cm。其他仪器包括恒温水浴锅(HH-501型,普天仪器制造有限公司,常州);pH计(PF20型,梅特勒托利多公司,瑞士);紫外-可见分光光度计(UV-1800型,岛津公司,日本);傅里叶变换红外光谱仪(Vector 33型,Bruker公司,德国)。
1.3 实验方法
1.3.1 产物的鉴定
二硫腙显色法:分别吸取硫酸铜溶液、反应液(螯合原液)和经过阳离子交换树脂处理后的反应液(主要为螯合态铜离子),加入双硫腙显色剂,摇匀,静置几分钟,观察颜色的变化[14]。
紫外光谱法:将配制好的硫酸铜溶液以及螯合反应的反应液分别用紫外分光光度计进行扫描,观察其紫外吸收曲线。波长扫描范围为190~300 nm,用蒸馏水调零[15]。
1.3.2 常规加热条件下螯合反应最佳条件的确立
将相同浓度的硫酸铜和甘氨酸溶液混合,调节pH值后置于恒温水浴锅中反应,每隔10 min取样,冰浴。用紫外-可见分光光度计测定最大吸收波长下的吸光度,计算产物的生成量。分别考察氨基酸和硫酸铜体积比(螯合比)、溶液pH值、反应温度对单位时间内甘氨酸铜生成量的影响,确定反应条件[16]。
1.3.3 PEF作用下甘氨酸和硫酸铜的反应
在1.3.2中的最优条件下,用恒流泵使样品以50 mL/min通过脉冲电场,处理场强分别10,20,30,40 kV/cm。用示波器监测脉冲电场的波形、场强以及频率。使用水浴锅控温,处理前后维持在50℃左右。在处理室的出口和入口处,用带探头的数显温度计监控温度变化,整个过程温度波动在2~3℃。每隔10 min取样,测定氨基酸铜含量,方法同1.3.2。
1.3.3 红外光谱扫描
采用KBr压片法,分别将少量样品充分研磨后加入干燥的KBr,在红外灯的照射下使其充分混合、压片,置于红外光谱仪内进行扫描,扫描范围400~4 000 nm。
2 结果与分析
2.1 产物鉴定
2.1.1 二硫腙显色结果
由于二硫腙的N原子可提供1个弧电子与金属离子配位,生成易溶于三氯甲烷或四氯化碳的红色络合物[16],可根据鳌合原液的颜色变化对螯合产物进行初步的判断。当向硫酸铜溶液、螯合原液以及树脂处理后的反应液中分别加入双硫腙试剂后,其显色分别为大红色、橙红色以及粉红色。这说明反应后大部分铜离子是以螯合态存在,经过阳离子交换树脂处理后,溶液中的铜几乎都以螯合态存在。
2.1.2 紫外扫描结果
Cu2+在紫外区有较强的吸收,而甘氨酸在紫外区吸收很弱。配制一定浓度的硫酸铜溶液进行扫描,其最大吸收峰在203 nm左右。而硫酸铜和甘氨酸反应液的最大吸收峰在228 nm左右,与Cu2+相比有25 nm的红移,说明溶液中的Cu2+和甘氨酸形成了稳定的配合物。杜俊等用Cu2+和各种氨基酸反应,用紫外扫描法也观察到18~24 nm的红移[17]。硫酸铜和甘氨酸铜的紫外扫描曲线见图1。
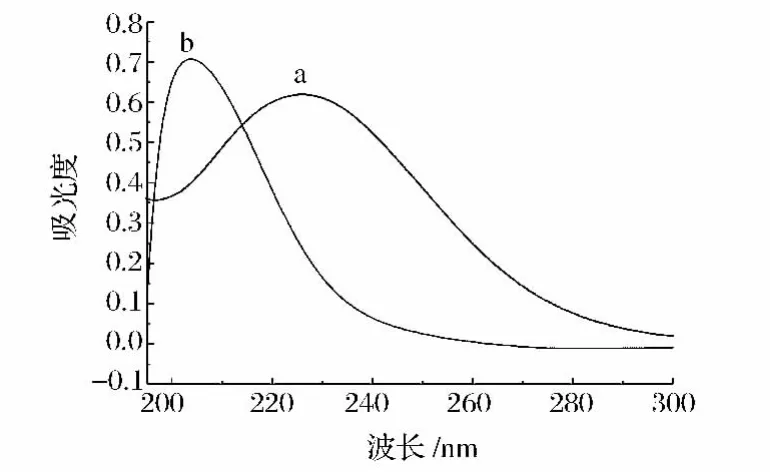
图1 硫酸铜和甘氨酸铜的紫外扫描曲线Fig.1 Ultraviolet scanning curve of copper sulfate and biscopper
2.2 螯合比对螯合反应的影响
金属离子可以和多个氨基酸形成不同的配合物,按照一定的摩尔比结合[18]。螯合比的大小直接影响螯合产物的稳定性,也影响产物的生成量。由图2可知,在相同时间内,随着氨基酸和硫酸铜螯合比的增大,生成的产物量逐渐增大。当螯合比超过2∶1时,产量大幅度降低。当螯合为0.5∶1和3∶1时,产物的最大吸收峰在210 nm左右,与甘氨酸铜标准品相差甚远。通常认为,氨基酸与金属离子配位数1∶1时形成的具有电荷的络合物,易被胶体吸附固定[18],而当形成2∶1的内络盐时,电荷趋于中性,螯合环较为稳定,且易被植物吸收利用。因此,选择2∶1为最佳螯合比。

图2 不同螯合比下甘氨酸铜的生成量Fig.2 Biscopper content under different Chelation rate
2.3 pH值对螯合反应的影响
螯合反应受pH值影响很大,pH值太低,溶液中过多的氢离子会与铜离子竞争,影响螯合反应的进行;pH值太高,铜离子会转化成氢氧化铜,阻碍反应的进行。由图3可以看出,随着pH值的增大,单位时间内甘氨酸铜的产量有所提高。当pH值达到8的时候,吸光值有所增大,但是溶液已经呈碱性,有文献表明,碱性条件下铜离子和氨基酸会发生Biuret反应,生成另一种螯合物[19]。为了防止发生Biuret反应生成不需要的产物,选择pH值为7进行研究。

图3 不同pH下甘氨酸铜的生成量Fig.3 Biscopper content under different pH value
2.4 温度对螯合反应的影响
温度是影响反应速率的重要因素,增大温度可以增加反应物分子间的碰撞速率,从而提高反应速度。紫外扫描光谱显示,温度对产物最大吸收波长的位置影响不大,均在228 nm左右。从图4可以看出,随着反应温度的增大,单位时间内生成的甘氨酸铜持续增多,当温度从50℃升高到60℃时,甘氨酸铜生成量变化减缓。因此,从节能的角度考虑,选择50℃进行研究。
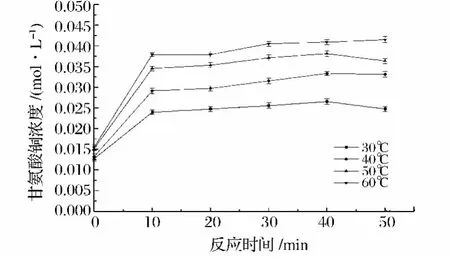
图4 不同反应温度下甘氨酸铜的生成量Fig.4 Biscopper content under different temperature
2.5 PEF处理对螯合反应的影响
在螯合比为2∶1,pH为7.0,温度为50℃的反应条件下,用不同场强的脉冲电场处理反应液,对产物进行紫外光谱扫描,其最大吸收波长仍然是在228 nm左右。由图5可以看出,20 kV/cm的场强处理20 min后,甘氨酸铜产量明显高于未经电场处理的样品。随着电场强度的增大,促进效果增强。当场强达到40 kV/cm,处理时间为50 min时,甘氨酸铜的浓度提高了89%。在整个PEF处理过程中,温度始终通过水浴维持在50℃左右,为了区分热效应和PEF作用,将甘氨酸和硫酸铜混合后分别设在50℃和55℃反应,对比甘氨酸铜产量,结果显示5℃温升对反应影响不大,而本实验中温升不超过3℃,由此可以推断,PEF处理的强化作用主要是非热效应。
氨基酸水溶液在光或超声波等外界条件影响下,共价键会发生均裂,形成自由基等不成对电子的原子团。这些自由基大都不稳定,不能单独存在,倾向于互相结合,或者与其他物质的离子、自由基反应形成新的更稳定的分子[20]。甘氨酸分子一侧有一个氨基,另一侧有一个羧基,在pH值为7的中性条件下,没有H+干扰,两侧的羧基和氨基在不同位置与金属离子络合,形成了螯合物甘氨酸铜。PEF是一种高强度的电场,能瞬时产生高强度电压,有研究表明,PEF处理的油酸中产生了O-2·,从而促使油酸发生氧化为自由基链式反应[21]。当其作用于氨基酸时,可能促使氨基酸产生自由基,从而使氨基酸分子自由基与铜离子迅速螯合,从而加快螯合反应速率。
2.6 红外光谱分析

图5 不同PEF场强处理对甘氨酸铜产量的影响Fig.5 Bicopper content under different PEF intensity
对比许良忠[21]等人做的甘氨酸红外图谱和本研究。2种反应产物的红外图谱(图6)可以看出,pH值为7的条件下,甘氨酸的IR光谱和本实验螯合产物的红外光谱具有明显的差异,主要的吸收峰的位移及强度均发生了变化,说明硫酸铜和甘氨酸的确发生了配位反应。由图中可以看出,υ(NH3+)的吸收带均从3 170 cm-1发生了转移,在3 263 cm-1左右和3 335 cm-1左右出现了υas(NH2)、υs(NH2)吸收峰,说明甘氨酸中的氨基参与了配位反应,形成了相应的甘氨酸配合物[22]。

图6 甘氨酸铜的红外吸收图谱Fig.6 Infrared spectrogram of biscopper

表1 不同处理条件下的甘氨酸铜谱带分布Table 1 The assignmemt of the vibrational spectrum of different biscoppers
羧酸成盐后的非对称与对称伸缩振动的频率之差△υ可以用来来衡量金属与氧M-O形成价键的共价程度。△υ越大,表明金属原子和氧原子共价程度越大,M-O的配位键越牢固[23]。由表1的数据可以算出,经PEF处理前后的甘氨酸铜△υ值分别为208 cm-1和216 cm-1,说明经PEF处理后,甘氨酸铜中的铜原子与氧原子共价程度更深,配位键更牢,从而证明螯合产物的稳定性得到了提高。
3 结论
本文研究了高压脉冲电场对硫酸铜和甘氨酸的螯合反应的影响。结果表明,在螯合比2∶1、反应pH 7.0,反应温度50℃条件下,PEF显著促进了该反应的进行,随着场强的增加,促进效果越明显,且生成产物更为稳定。
[1]李青仁,王月梅.微量元素铜与人体健康[J].微量元素与健康研究,2007,24(3):61-63.
[2]Colin F Mills,Ian Bremner,Ciba Foundation,et al.Biological roles of copper[M].Excerpta Medica,1980:71-85.
[3]吴信,印遇龙,邢芳芳,等.国内外微量元素氨基酸螯合物的应用研究进展[J].营养与饲料,2008(3):68-72.
[4]黄雪,廖列文,冯光炷,等.氨基酸微量元素螯合物合成方法研究进展[J].安徽农业科学,2010,38(11):6 053-6 054.
[5]张艳,王圣开,崔俊林.PEF在食品加工中的应用[J].农产品加工,2012(9):154-157.
[6]陶晓赟,王寅,陈健.高压脉冲电场对蓝莓汁杀菌效果及品质的影响[J].2012,38(7):94-97.
[7]钟葵,胡小松,陈芳,等.脉冲电场对果胶酯酶的活性及构象的影响[J].2005,21(2):149-152.
[8]李迎秋,陈正行.高压脉冲电场对大豆分离蛋白功能性质的影响[J].农业工程学报,2006,22(8):194-198.
[9]Guan Y G,Hua L,Han Z,et al.,Effects of pulsed electric field treatment on a bovine serum albumin-dextran model system,a means of promoting the Maillard reaction[J].Food Chemistry,2010,123(2):275-280.
[10]Wang J,Guan Y G,Yu S J,et al.,Study on the Maillard reaction enhanced by pulsed electric field in a glycin-glucose model system[J].Food and Bioprocess Technology,2011,4(3):469-474.
[11]Guan Y G,Wang J,Yu S J,et al.,A pulsed electric field procedure for promoting Maillard reaction in an asparagine-glucose model system[J].International Journal of Food Science& Technology,2010,45(6):1 303-1 309.
[12]曾新安,刘新雨.脉冲电场对乳酸乙醇酯化反应的影响[J].华南理工大学学报,2011,39(12):127-13.
[13]Lin Z R,Zeng X A,Yu S J,et al.Enhancement of ethanol-acetic acid esterification under room temperature and non-catalytic condition via pulsed electric field application[J].Food and Bioprocess Technology,2012,5(7):2 637-2 645.
[14]吴茹怡,曾里,曾凡骏.复合氨基酸螯合物鉴定方法的研究[J].食品科技,2006(3):104-107.
[15]杜俊,高峰,陶海升,等.光度法测定Cu(Ⅱ)-氨基酸配合物组成[J].安徽师范大学学报,2003,26(3):256-258.
[16]舒绪刚,李大光,林娜妹,等.一种测定氨基酸微量元素螯合物螯合率的检测方法[P]:CN200810198628.1.2009-02-18.
[17]石锐,刁新平,辛延钊.微量元素-氨基酸螯合物的研究及应用[J].饲料博览,2000,6:15-17.
[18]滕冰,舒绪刚.关于微量元素氨基酸螯合物的几个问题[C].珠海:饲料营养研究进展——第五届全国饲料营养学术研讨会,2006-10-11~13.
[19]张小燕,杜建强,李亚萍,等.复合氨基酸螯合铜的制备工艺研究[J].西北大学学报,2002,32(1):156-161.
[20]甘林火,翁连进,邓爱华.制备氨基酸螯合钙的研究进展[J].氨基酸和生物资源,2008,30(1):44-46.
[21]梁琦,杨瑞金.高压脉冲电场对乳状液体系中油酸氧化的影响[D].无锡:江南大学,2009:19-20.
[21]许良忠,文丽荣.过渡金属-甘氨酸配合物的IR光谱[J].光谱实验室,2002,19(5):641-643.
[22]李德广,杜相革.甘氨酸螯合铜的合成及表征研究[J].安徽农业科学,2009,37(5):1 897-1 898.
[23]Nakamoto K.Infrared and Raman Spectra of Inorganic and Coordination Compounds[M].New York,Academic Press,1978:62-67.
