单体碳数对脂肪酶N435催化合成直链聚酯的影响
2013-11-20杨金明
杨金明,张 敏
(1. 陕西省轻工业研究设计院,陕西省西安市 710054;2. 陕西科技大学化学与化工学院,陕西省西安市 710021)
脂肪族聚酯是一种可进行多种形式生物降解的高聚物。传统的脂肪族聚酯生产采用的高温金属催化剂法存在耗能高、有金属残留等缺点[1]。酶催化法是一种新型的环境友好绿色化学技术,这种方法可以在温和条件下高效地合成脂肪族聚酯,有着传统聚合方法难以比拟的优势,成为代替金属催化法的有效途径。酶尤其是脂肪酶的应用为聚酯合成技术开辟了一条新途径。酶催化合成聚酯具有许多突出的优点:可在多种不同的介质中反应;酶本身来源于可循环资源,无毒无害;可使反应在温和的条件下进行[2]。
作者已系统地报道了采用脂肪酶N435催化丁二酸二乙酯和1,4-丁二醇的聚合,获得了较高相对分子质量的聚丁二酸丁二酯(PBS)[3-4]。本工作研究了脂肪酶催化不同碳数的直链型二醇与二酯的合成以及与甘油的共聚合[丁二酸二乙酯与1,4-丁二醇的反应式见式(1)],分析了单体碳数与甘油对脂肪酶催化合成聚酯的影响。

1 实验部分
1.1 原料
乙二酸二乙酯,丁二酸二乙酯,己二酸二乙酯,甘油,1,4-丁二醇,己二醇,二苯醚,均为化学纯,未经处理直接使用,陕西化玻有限公司生产。固定化南极假丝酵母脂肪酶,N345(有效活性为每克脂肪酶中含有7 000个1-丙基月桂酸基团),日本协和医药株式会社生产。离子交换树脂,VPOC1600,表面积为110~150 m2/g,平均孔径为100 nm,德国朗盛公司生产。
1.2 测试与表征
核磁共振碳谱(13C-NMR)用德国布鲁克公司生产的Bruker DPX 300 NMR型核磁共振波谱仪记录。聚合物的重均分子量(Mw)用美国Waters公司生产的1515型凝胶渗透色谱仪测定,三氯甲烷为洗脱液,流速为1.0 mL/min,试样浓缩至2 mg/mL,注入量为100 μL[3]。
1.3 固定化脂肪酶N345负载的实验方法和负载条件
固定化南极假丝酵母脂肪酶N345的制备采用物理吸附方法,载体选用大孔离子交换树脂VPOC1600[4]。取1~2 g的VPOC1600,加入三角烧瓶中,加入10 mL浓度为0.05 mol/L,pH=7的磷酸盐缓冲溶液,再加入2~4 mL脂肪酶N345溶液,在35 ℃下水浴振荡2~6 h,取出三角烧瓶,将得到的树脂在35 ℃下真空干燥6~12 h,即可得到固定化脂肪酶N345[5]。
1.4 脂肪酶催化合成聚酯的多级催化法
将1.0 g脂肪酶N435(100 Pa,25 ℃,真空干燥24 h),17.0 g丁二酸二乙酯,8.0 g的1,4-丁二醇和0.1 g水加入到溶剂中,搅拌反应2 h。然后减压蒸馏,将溶剂全部蒸出(溶剂回收待处理再利用),在真空下搅拌反应1 h,恢复常压,再加入0.1 g水,同样量的溶剂,常压反应2 h,重复此过程24 h[6]。反应结束后,得到的白色固体加入三氯甲烷溶解后过滤,滤液加入甲醇纯化,得到PBS。滤渣为脂肪酶345,可重复使用[7]。
2 结果与讨论
2.1 二醇碳数对脂肪酶N435催化丁二酸二乙酯与二醇反应的影响
在80 ℃,水、酶质量分数分别为0.1%,0.5%的无溶剂体系下[8],用脂肪酶N435催化丁二酸二乙酯和不同二醇反应合成脂肪族聚酯。结果表明:乙二醇难以被催化与二酯进行酯交换反应,而1,2-丙二醇相对较易被脂肪酶N435催化与二酯进行酯交换反应,二醇碳链越长,获得产物的Mw越大、相对分子质量分布(Mw/Mn)越窄(见表1)。这说明碳链越长的二醇更易于被脂肪酶N435催化与二酯进行酯交换反应。
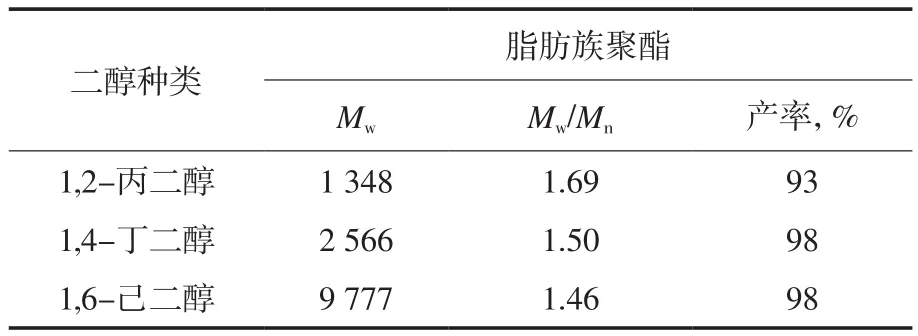
表1 无溶剂下丁二酸二乙酯与不同二醇反应的产率和产物性能Tab.1 Yield and properties of the polyesters synthesized from diethyl succinate and different diols under solvent-free conditions
在80 ℃,水、酶、反应物质量分数分别为0.1%,5.0%,25.0%的二苯醚体系中[8],用脂肪酶N435催化丁二酸二乙酯和不同二醇反应48 h,合成脂肪族聚酯。由表2可知:在二苯醚中催化二醇和丁二酸二乙酯反应均得到了比在无溶剂下Mw更高、Mw/Mn更窄的产物。在二苯醚中产率相对较低是因为产物后期处理,洗脱二苯醚过程中产物损失造成的。
脂肪酶N435催化二酯和二醇反应,Mw随着二醇碳链的增长而增大,Mw/Mn随着二醇碳链的增长而变窄。这说明碳链长的二醇更容易被催化与二酯反应。这是因为碳链越长,两端羟基极性作用越弱,越容易被脂肪酶活性点捕获,使其脱除质子形成活性中间体[9]。

表2 二苯醚中丁二酸二乙酯与不同二醇反应的产率和产物性能Tab.2 Yield and properties of the polyesters synthesized from diethyl succinate and different diols in diphenyl ether
无论是无溶剂体系还是二苯醚溶剂体系中,乙二醇均难以被催化与二酯进行酯交换反应,而1,2-丙二醇相对较易被脂肪酶N435催化与二酯进行酯交换反应,说明对于带有非极性侧链的二醇比主链同碳数的直链型二醇更易被脂肪酶N435催化与二酯进行酯交换反应。这是因为非极性侧链弱化了两端羟基的极性作用,使其容易被脂肪酶N435活性点捕获并剥夺羟基上的质子,形成活性中间体[5]。
2.2 二酯碳数对脂肪酶N435催化1,4-丁二醇与二酯反应的影响
在80 ℃,水、酶质量分数分别为0.1%,0.5%的无溶剂体系下,用脂肪酶N435催化1,4-丁二醇和不同二酯反应合成脂肪族聚酯。结果表明:乙二酸二乙酯难以被催化与1,4-丁二醇进行酯交换反应,而二酯的碳链越长获得产物的Mw越大,Mw/Mn越窄(见表3)。这说明碳链越长的二酯越容易被脂肪酶N435催化与1,4-丁二醇进行酯交换反应。

表3 无溶剂下1,4-丁二醇与不同二酯反应的产率和产物性能Tab.3 Yield and properties of the polyesters synthesized from 1,4-butanediol and different diesters under solventfree conditions
在80 ℃,水、酶、反应物质量分数分别为0.1%,5.0%,25.0%的二苯醚体系中,用脂肪酶N435催化1,4-丁二醇和不同二酯反应48 h,合成脂肪族聚酯。由表4可知:在二苯醚中催化二酯和1,4-丁二醇反应均得到了比在无溶剂条件下相应Mw更高的产物,己二酸二乙酯与1,4-丁二醇反应可以获得Mw为24 816,Mw/Mn为1.09的聚酯。但在二苯醚中乙二酸二乙酯同样难以被催化与1,4-丁二醇进行酯交换反应。在二苯醚中产率相对降低是因为产物后期处理,洗脱二苯醚过程中产物损失造成的。
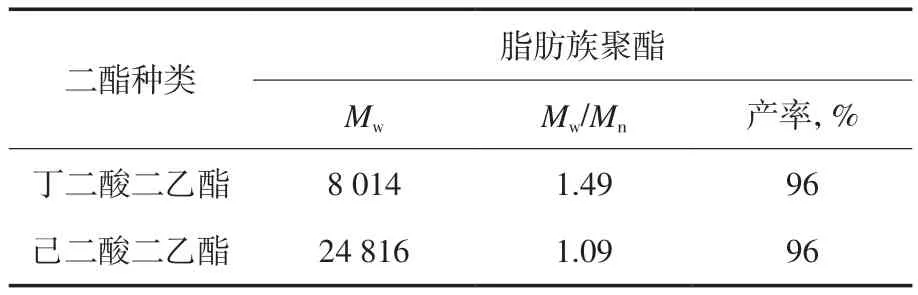
表4 二苯醚中1,4-丁二醇与不同二酯反应的产率和产物性能Tab.4 Yield and properties of the polyesters synthesized from 1,4-butanediol and different diesters in diphenyl ether
对比表1与表3、表2和表4可知:碳数相同的二酯比二醇容易被脂肪酶N435催化获得Mw较高的聚酯。这可能是短链二酯的端基比二醇除了具有极性效应外还具有共轭效应,对脂肪酶N435的催化反应影响更明显。
由表4还可知:脂肪酶N435催化二酯和1,4-丁二醇反应,Mw随着二酯碳链的增长而增大,Mw/Mn随着二酯碳链的增长而变窄。这说明碳链长的二酯更容易被催化与1,4-丁二醇反应。这可能是碳链越长,两端酯基共轭作用和极性作用均减弱,酯键的稳定性就相对碳链短的二酯减弱,被脂肪酶活性点捕获,使其越容易质子化或者离子化形成活性中间体[10]。
2.3 甘油对脂肪酶N435催化1,4-丁二醇与丁二酸二乙酯聚合的影响
甘油特有的星形结构可以使聚酯支化或交联,加入甘油可以获得较高Mw的聚酯。在80 ℃,水、酶质量分数分别为0.1%,0.5%的无溶剂体系下,用脂肪酶N435催化1,4-丁二醇、丁二酸二乙酯与甘油共聚合24 h,合成PBS。由表5可知:所得的PBS随甘油摩尔分数的增加,Mw先增加后减小,Mw/Mn先变窄后变宽,而产率随甘油摩尔分数的增加而减小。这是因为随着甘油的加入,活性端与甘油反应形成交联结构,从而使Mw增大;但是当甘油加入量达一定程度后,特别是甘油的羟基数量超过活性点数量时,甘油在反应前期就会将活性点结合完,造成缩聚合终止,从而使Mw降低。Mw/Mn随甘油加入先变窄后变宽,这是由于随甘油加入,低Mw的PBS链段容易先被交联,使Mw/Mn降低;当甘油加入量达一定程度后,甘油在反应前期就会将活性点结合完,造成缩聚合终止,使反应不均一,从而Mw/Mn变宽。由于加入甘油过多,Mw降低,Mw/Mn变宽,产物中的低聚物成分变多,因此,在用三氯甲烷纯化时,低Mw的产物易被洗脱,造成产率降低。

表5 无溶剂下丁二酸二乙酯、1,4-丁二醇、甘油的摩尔比对产物的影响Tab.5 Effect of molar ratio of diethyl succinate, 1,4-butanediol and glycerol on the polyesters under solvent-free conditions
在80 ℃,水、酶、反应物质量分数分别为0.1%,5.0%,25.0%的二苯醚体系中,用脂肪酶N435催化1,4-丁二醇、丁二酸二乙酯、甘油共聚合48 h,合成PBS。由表6可知:所得PBS随甘油摩尔分数的增加,Mw先增加后减小,Mw/Mn先变窄后变宽,而产率随甘油摩尔分数的增加而减小。这与在无溶剂体系下反应的结果相同,影响原因也一致。

表6 二苯醚中丁二酸二乙酯、1,4-丁二醇与甘油的摩尔比对产物的影响Tab.6 Effect of molar ratio of diethyl succinate, 1,4-butanediol and glycerol on the polyesters in diphenyl ether
3 结论
a)无论在无溶剂状态下还是在有机溶剂中,长链的二醇和长链的二酯均比短链的二醇和二酯容易被脂肪酶催化合成相应的聚酯。其中,采用脂肪酶N435催化己二酸二乙酯与1,4-丁二醇反应可以获得Mw为24 816,Mw/Mn为1.09的聚酯。
b)用脂肪酶N435催化1,4-丁二醇、丁二酸二乙酯与甘油共聚合可以获得较高Mw,低Mw/Mn的PBS。在无溶剂和二苯醚中获得的PBS均随甘油摩尔分数的增加,Mw先增加后减小,Mw/Mn先变窄后变宽,而产率随甘油摩尔分数的增加而减小。
[1] 张敏,杨金明,宋洁,等. 脂肪酶在催化合成脂肪族聚酯中的应用[J]. 塑料, 2009, 38(2): 54-56.
[2] 杨金明,张敏. PBS结晶影响因素的研究[J]. 胶体与聚合物,2010, 28(3): 116-119.
[3] 张敏,杨金明,宋洁,等. 脂肪酶N435催化合成PBS[J]. 塑料,2010, 39(4): 73-76.
[4] 杨金明,汤粤豫,张敏. 脂肪酶N435在低沸点溶剂中催化合成PBS[J]. 工业催化,2011, 19(1): 62-67.
[5] Andreas S Bommarius, Bettina R Riebel. 生物催化——基础与应用[M]. 孙志浩,许建和,译. 北京:化学工业出版社,2006:205-206.
[6] Sachiko Okajima, Reiko Kondo, Kazunobu Toshima, et al.Lipase-catalyzed transformation of poly(butylene adipate)and poly(butylene succinate) into repolymerizable cyclic oligomers[J]. Biomacromolecules, 2003, 236(4): 1514-1519.
[7] Uyama H, Kobayashi S. Enzyme-catalyzed polymerization to functional polymers[J]. J Mol Catal B Enzyme, 2002, 785(7):1-11.
[8] Deng F, Gross R A. Ring-opening bulk polymerization of ε-caprolactone and trimethylene carbonate catalyzed by lipase Novozym 435[J]. Int J Biomol, 1999, 25(1/2/3): 153-159.
[9] Bisht K S, Henderson L A, Gross R A, et al. Enzyme-catalyzed ring-opening polymerization of ω-pentadecalactone[J]. Macromolecules, 1997, 30(8): 2705-2711.
[10] Lanne C, Boeren S, Vos K, et al. Rules for optimization of biocatalysis in organic solvents[J]. Biotechnology Bioengineering,1987, 30(10): 81- 87.
