碱的类型对剩余污泥碱性发酵及脱水性能的影响
2013-11-20苏高强霍明昕汪传新郑冰玉王淑莹彭永臻
苏高强,霍明昕,汪传新,郑冰玉,王淑莹,彭永臻
(1.北京工业大学 北京市水质科学与水环境恢复工程重点实验室;北京市污水脱氮除磷处理与过程控制工程技术研究中心,北京 100124;2.东北师范大学 城市与环境科学学院,长春 130024)
中国大部分污水处理厂都采用活性污泥法处理废水,污水厂在运行过程中势必会产生大量的剩余污泥,因此如何实现剩余污泥的减量化、稳定化、无害化和资源化是污水处理行业所面临的重大问题。在城市生活污水处理过程中普遍存在着碳氮比低的问题,往往需要投加外碳源以达到脱氮除磷的目的,而投加的外碳源不仅会增加运行成本,而且在污水处理过程中会转化为剩余污泥,进一步增加剩余污泥的产量。研究发现剩余污泥在碱性条件下发酵会产生大量的易降解有机物如挥发性短链脂肪酸(SCFAs)[1-2],这些易降解的有机物可以为污水生物脱氮除磷提供碳源,且剩余污泥在发酵过程中能实现污泥减量,因此剩余污泥碱性发酵为实现污泥的资源化和减量化提供了一个新的思路。由于剩余污泥在发酵后需要将污泥和发酵液分开,以便提取发酵液,而污泥的脱水性能是影响发酵液和污泥分离的一个重要影响因素,因此需要对污泥的脱水性能进行评价。
碱的类型对剩余污泥的水解和脱水性能有着重要影响。肖本益等[3]考 察 了 KOH、NaOH 和Ca(OH)2对剩余污泥融 胞的影响发现 KOH 和NaOH对剩余污泥溶解性化学需氧量(SCOD)的增加效果要好于 Ca(OH)2。Kim 等[4]也发现 KOH和NaOH对剩余污泥SCOD的增加效果要好于Mg(OH)2和Ca(OH)2。尹军等[5]发现 NaOH 对剩余污泥SCOD的增加效果要好于CaO。Neyens等[6]指出使用Mg(OH)2和Ca(OH)2处理的剩余污泥的脱水性能好于使用KOH和NaOH处理的污泥。文献中主要考察了各种碱作为预处理手段对剩余污泥水解和脱水性能的影响,碱的类型对剩余污泥水解,产酸以及脱水性能的长期的影响还鲜见报道。KOH、NaOH、Ca(OH)2和 Na2CO3是4种常用的碱,这4种碱和其他碱相比性质稳定,且价格较低,为此实验考察了厌氧环境中,温度35℃条件下,使用KOH、NaOH、Ca(OH)2和 Na2CO3这4种碱控制剩余污泥的pH为10,剩余污泥的水解产酸特征、脱水性能以及减量情况,为实际工程应用提供理论指导。
1 试验的材料与方法
1.1 试验装置及运行方法
污泥碱性发酵试验在35℃的恒温培养箱中进行,反应器为4个1L的广口试剂瓶,各反应器分别添加900mL的剩余污泥,分别使用8mol·L-1的KOH、NaOH、Ca(OH)2和 Na2CO3颗粒调节剩余污泥的pH值为10,曝氮气3min以驱除反应器顶部的氧气,而后使用橡胶塞密闭,橡胶塞上开3个孔,其中2个孔插入pH电极和玻璃棒实时监测pH和取样,另外一个孔用于投加碱调节反应器的pH值,反应器的pH值每天调节2次,控制pH变化不超过0.2。使用磁力搅拌器对反应器搅拌,转速控制在100±10rpm。反应器共运行14d,取样周期为2d。
1.2 污泥的来源与性质
剩余污泥取自本实验室的A/O工艺的二次沉淀池,剩余污泥在使用之前先淘洗3次,污泥的各项指标如下:pH值6.86;溶解性化学需氧量(SCOD)88mg·L-1;总化学需氧量(TCOD)11117mg·L-1;氨氮25mg·L-1;正磷酸盐16mg·L-1;总悬浮固体(TSS)7000mg·L-1;挥发性悬浮固体(VSS)5545mg·L-1;挥发酸(VFA)0mg·L-1。
1.3 测定方法
取样后在4000rpm的转速下离心20min,离心后使用0.45μm微孔滤膜过滤,滤液用来分析SCOD、氨氮、正磷酸盐、蛋白质、SCFAs以及Na+和K+,滤渣用来分析TSS和VSS。pH、TSS、VSS、SCOD、TCOD、氨氮、正磷酸盐测量均采用国家标准方法[7];蛋白质采用福林-酚试剂法测量[8];SCFAs使用安捷伦6890N气相色谱仪测量;Na+和K+采用高效液相色谱仪(761Compact IC/瑞士万通)测量;污泥脱水性能使用毛细管吸收时间(CST)测定仪(340M/Triton)测定。每个指标测量2次,取平均值为试验数据。
2 结果与讨论
2.1 剩余污泥的水解和产酸特征
碱性条件下剩余污泥的水解伴随着胞外聚合物(EPS)的溶解和微生物细胞的破裂[3]。随着水解过程的进行颗粒状的有机物如蛋白质和多糖不断溶解进入液相,SCOD随之改变,因此SCOD可以用来表征污泥的水解情况。剩余污泥溶出的蛋白质和多糖等有机物在溶出后被水解为氨基酸和单糖,而后可以被产酸细菌用于产挥发性脂肪酸。这些短链脂肪酸主要由乙酸、丙酸、丁酸、异丁酸、戊酸和异戊酸组成,将其浓度换算为COD而后相加,总和除以VSS浓度比值为总挥发性有机酸(TVFA)。挥发酸作为一种有效的碳源能够进行脱氮除磷,解决生活污水中缺乏碳源的问题[9]。不同的碱处理条件下剩余污泥水解和产酸情况如图1所示。
由图1可知SCOD的变化可分为3个阶段:1)0~2d,SCOD快速溶出阶段;2)2~10d,SCOD慢速溶出阶段;3)10~14d,SCOD下降阶段。SCOD浓度的变化与SCOD的溶出与消耗有关,在阶段1使用 KOH、NaOH、Ca(OH)2、Na2CO3处理的污泥,SCOD的溶出速率较快,溶出的SCOD量分别占SCOD最大溶出量的87%、73%、84%、81%,这是因为在开始阶段污泥中存在大量易水解的物质,且消耗SCOD的微生物如产甲烷细菌的活性受到抑制,SCOD的溶出速率要远大于消耗速率。在阶段2,由于大部分易水解的物质在阶段1已经被消耗完,且产甲烷的细菌活性开始恢复,导致SCOD增长速率变的缓慢。在阶段3由于产甲烷微生物得到驯化,开始利用SCOD产甲烷,且易水解的物质更少,SCOD的消耗速率大于溶出速率从而导致SCOD的下降。Vlyssides等[10]的研究也表明在碱性和中温条件下污泥的水解可以分快速水解阶段和慢速的水解阶段,在快速水解阶段VSS的去除率占到总去除率的64%~85%。对于产酸,在各种碱处理的条件下,TVFA在0~12d内不断增加,12d后TVFA逐渐减少或开始稳定。12d时,使用 KOH、NaOH、Ca(OH)2、Na2CO3处理的污泥产生的TVFA分别为200、212、147、210mg(COD)·g-1(VSS)。
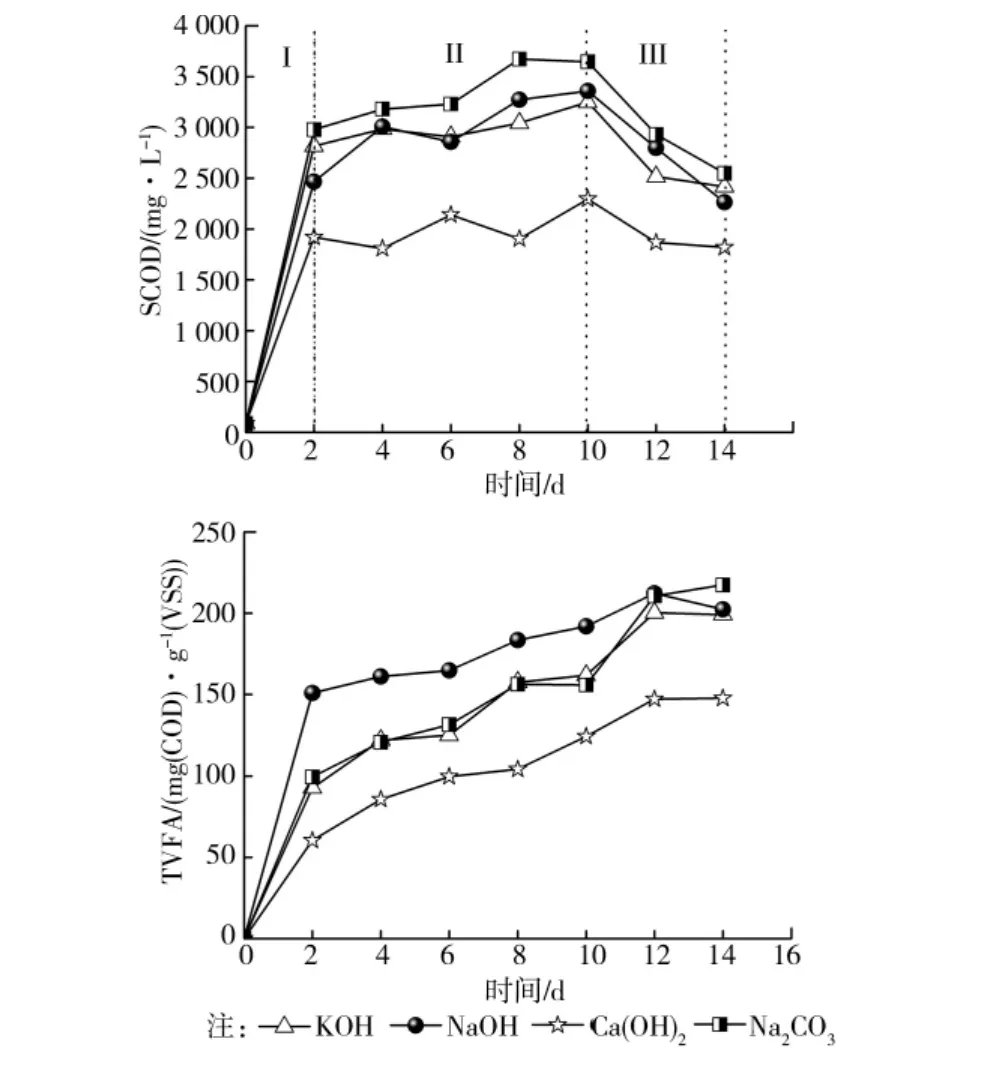
图1 碱的类型对污泥水解和产酸的影响
从图1可以看出4种碱性条件下剩余污泥的水解能力排序为:Na2CO3> NaOH ≈ KOH > Ca(OH)2,而产酸能力排序为:NaOH > KOH ≈Na2CO3> Ca(OH)2。 肖本益等[3]、Li 等[11]和Stuckey等[12]的研究也指出二价碱条件下剩余污泥的水解能力要小于一价碱条件下的。一价碱中含有一价离子如Na+和K+,能与稳定胞外聚合物结构的高价离子进行交换,从而使EPS结构变得疏松,利于EPS的溶出。由于维持pH为10需要投加大量的Na2CO3,污泥发酵液中含有高浓度的 Na+(4~14d时,Na+浓度为3822~4160mg·L-1),而高浓度的Na+更容易破坏EPS结构和破碎细胞,从而导致该条件下污泥溶出的SCOD最多,但同时高浓度的Na+会抑制产酸细菌生长,导致该条件下产酸并不是最高。而对于KOH和NaOH,虽然2种条件下WAS水解能力相当,但NaOH条件下产酸要比KOH条件下要高。这是因为4~14d时,NaOH条件下发酵液中Na+浓度为1524~1662mg·L-1,KOH条件下K+浓度为2589~2833mg·L-1,只有当Na+浓度为3500mg·L-1时才会对微生物生长产生抑制,而当K+浓度为2500mg·L-1时就会对微生物生长产生抑制[13]。而含有Ca2+的Ca(OH)2能使EPS结构更加稳定,不利于EPS的溶出,因此该条件下 WAS溶出的SCOD最少,而SCOD低会限制污泥的产酸能力,导致污泥产生TVFA在4种碱性条件下最少。
表1对比了本文和参考文献的研究条件和实验结果,从表1可以看出大部分参考文献中的研究主要是将碱处理当做一种预处理手段,处理时间较短,大部分为0.5~24h,且进行预处理的目的主要是为了提高剩余污泥的产甲烷性能[6,12,14,16]。只有少部分参考文献考察了长时间内碱处理对剩余污泥水解的影响,且文献中考察的碱主要是NaOH[17]。而本文考察了长时间内剩余污泥在KOH、NaOH、Ca(OH)2和Na2CO3这4种碱性条件下的水解和产酸情况,且进行碱性发酵的目的主要是提高剩余污泥产挥发酸的量。从表1还可以发现本实验条件下SCOD的溶出率较高温和高pH条件下剩余污泥SCOD 的溶出率要低[11-12,16-17],原因为本实验的主要目的是为了产挥发酸,而在高温或高pH条件下产酸细菌的活性会被抑制甚至被杀死。不同于肖本益等的报道[3],本文研究结果表明KOH条件下剩余污泥SCOD溶出量和NaOH基本相等,这是因为本实验条件下剩余污泥在碱性条件下处理时间较长(10d),碱和污泥反应的更充分。
2.2 产酸组成情况
Elefsinioti等[18]指出反硝化优先利用乙酸,其次为丁酸(包括异丁酸和正丁酸)和丙酸,最后是戊酸(包括异戊酸和戊酸)。Chen等[19]指出适宜作为除磷碳源的两种有机酸为乙酸和丙酸,从短期看乙酸作碳源效果较好,而从长期看丙酸要比乙酸作碳源效果好。可见产酸的组成情况对其作碳源被利用具有重大的影响。各碱性条件下污泥发酵12d时产生的VFA组成情况如图2所示。
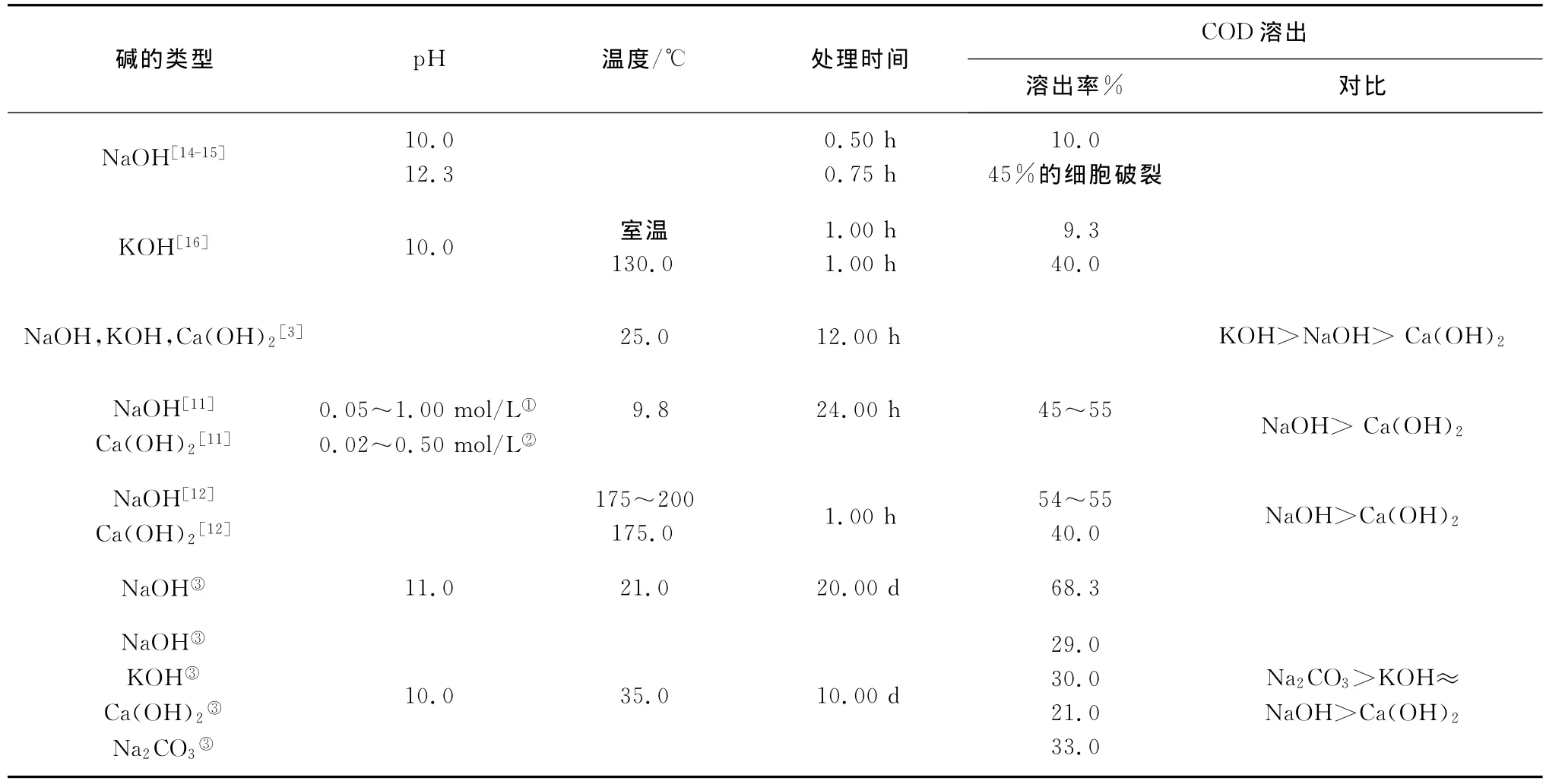
表1 不同碱性条件下剩余污泥的水解能力
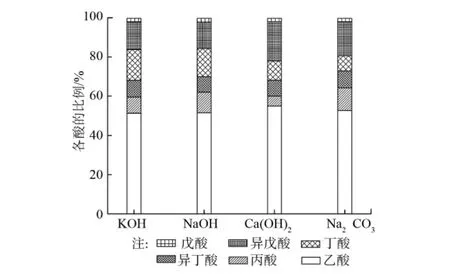
图2 不同碱处理条件下各酸的比例
从图2可以看出无论任何碱性条件,乙酸的含量总是最高,戊酸含量最少。KOH、NaOH、Ca(OH)2、Na2CO3条件下乙酸的含量分别为51%、52%、55%和53%。KOH和NaOH条件下SCFAs组成情况较相似,都是乙酸>丁酸>异戊酸>丙酸>异丁酸>戊酸;Ca(OH)2条件下,乙酸>异戊酸>丁酸>异丁酸>丙酸>戊酸;Na2CO3条件下,乙酸>异戊酸>丙酸>异丁酸>丁酸>戊酸。Mcinerney等[20]指出乙酸、丙酸、异丁酸、丁酸可以直接从蛋白质和多糖发酵中产生,但大分子量的异戊酸和戊酸主要与蛋白质发酵有关。Liu等[21]也指出异戊酸和戊酸则主要是由蛋白质脱氨基以及斯蒂克兰反应产生。
2.3 氨氮和磷的释放情况
Chen等[19]、Jiang等[22]、Yuan等[23-24]的研究发现剩余污泥在碱性发酵过程中会释放出大量的氨氮和正磷酸盐,而氨氮和正磷酸盐的存在势必会影响污泥发酵液用于脱氮除磷,为此考察了剩余污泥碱性发酵过程中氨氮和磷的释放情况。图3为各碱性条件下氨氮和正磷酸盐的释放情况。

图3 不同碱处理条件下氨氮和正磷酸盐的释放情况
从图3可以看出无论是任何碱性条件,发酵液中氨氮都呈不断上升的趋势,这是由于剩余污泥主要由一些微生物絮体组成含有大量的蛋白质,蛋白质在水解过程中会不断产生氨氮。从上图还可以看出氨氮的释放量与SCOD的溶出量顺序一致,均为Na2CO3>NaOH≈KOH>Ca(OH)2。从图1可以看出Na2CO3条件下,剩余污泥的水解能力最强,有较多的蛋白质被水解,因此释放的氨氮最多,而Ca(OH)2条件下剩余污泥水解能力最弱,释放的氨氮量也较少。对于正磷酸盐,Na2CO3条件下呈不断上升的趋势,KOH和NaOH条件下呈先升后降的趋势,而Ca(OH)2条件下从开始就呈不断下降的趋势。Na2CO3条件下水溶液中的Ca2+和 Mg2+在碱性条件下首先与CO32-结合而不会和PO43-结合,PO43-在该条件下能够不断积累。在KOH和NaOH条件下当PO43-达到一定的浓度,会与水溶解中的Ca2+,Mg2+以及NH4+结合生成羟基磷灰石或鸟粪石沉淀,使得PO43-减少。而在Ca(OH)2条件下,PO43-可以直接和Ca2+结合生成沉淀从而导致PO43-从发酵开始就开始减少。
2.4 污泥的脱水性能
剩余污泥的脱水性能可以被用来评价发酵液和污泥分离的难易程度,各种碱条件下污泥CST随时间变化如图4。

图4 不同碱处理条件下污泥脱水性能变化情况
从图4可以看出,任何碱性条件下,剩余污泥的脱水性能在发酵过程中均恶化,原因为碱性条件破坏了污泥的结构,同时污泥释放出了大量的蛋白质(2d,各碱性条件下蛋白质的释放量为221~471mg·L-1)[11]。Dogǎn等[14]也指出剩余污泥在pH=10的条件下处理0.5h污泥的脱水性能会恶化。而Erdincler等[15]在pH=12.3的条件下处理纯种细菌0.45h,发现脱水性能得到改善。出现不同结果的原因为剩余污泥是絮体结构而纯种细菌为分散的个体,剩余污泥在碱处理过程中会不断破碎变成细微的颗粒,脱水性能因此恶化;而纯种细菌在碱处理过程中会释放出高分子的有机物,这些高分子有机物会产生絮凝作用,改善细菌的脱水性能。KOH条件下,剩余污泥的CST在2d后变化稳定,在508.3~554.4s之间变化。NaOH条件下,在6d时,CST增加到555.8s后变化开始稳定。在Na2CO3条件下,4d时CST升到最大值531.8s,而后下降,CST在6~14d开始稳定,在373.8~411.7s之间变化。Ca(OH)2条件下,CST在4d时达到最大值103.7s,而后开始不断下降,14d时下降至32.1s。
从图4还可以发现0~4d时KOH条件下污泥的脱水性能要比NaOH条件下差,在4~14d时2种碱性条件下污泥的脱水性能相当。Neyens等[6]的报道也指出剩余污泥在KOH和NaOH条件下处理1h,KOH条件下污泥的脱水性能要差,并指出导致这种现象的原因为K+和Na+同污泥中高价离子交换能力,以及同污泥中高聚化合物架桥方式不同。而经过长时间的处理,2种碱性条件氢氧根对污泥絮体结构破坏较严重,消弱了K+和Na+的破坏作用,导致两种条件下污泥的脱水性能相当。KOH和NaOH条件下处理的污泥的脱水性能较Na2CO3和Ca(OH)2相比都较差,与 Neyens等的报道一致[6]。这是因为Na2CO3和Ca(OH)2能与污泥发酵液中的Ca2+和Mg2+以及PO43-形成沉淀,有利于污泥的絮凝。Ca(OH)2条件下污泥的脱水性能最好,EPS在碱性条件下带负电,Ca2+带有较高的正电荷能起到架桥的作用,增加污泥絮体的尺寸,密度和抗剪切能力,因此能改善污泥的脱水性能[25]。Li等[11]的研究指出当NaOH和Ca(OH)2的浓度均为0.05~0.2mol/L时,Ca(OH)2条件下剩余污泥的脱水性能要好于NaOH条件下;而当NaOH和Ca(OH)2浓度均为0.3~0.5mol/L时,NaOH 条件下剩余污泥的脱水性能要好于Ca(OH)2条件下;并解释出现这种情况的原因为在高浓度的碱性环境下,污泥中较细微的污泥颗粒和胶体物质能够被溶解。本实验条件下NaOH的浓度在0.05mol/L左右,得出的结论与Li等[11]的报道相符。
2.5 污泥的减量情况
各种碱性条件下,VSS随时间的变化情况如图5所示。

图5 各种碱性条件下VSS的减量情况
从图5可以看出VSS基本随时间呈不断下降的趋势,14d后KOH、NaOH、Ca(OH)2和 Na2CO3条件下VSS的去除率分别达到了46.2%、52.4%、29.4%、57.2%。Na2CO3条件下 VSS的去除率最高的原因主要是该条件下污泥水解能力较强(见图1),使得更多的VSS转化为SCOD。另外VSS的去除也可以分为2个阶段:1)0~4d为快速去除的阶段,该阶段KOH、NaOH、Ca(OH)2和Na2CO3条件下VSS去除量分别占到总去除量的73.6%、64.7%、95.9%和80.3%;2)4~14d为慢速去除阶段,该阶段各碱性条件下VSS去除的量小于总去除量的40%。
对于TSS,在KOH、NaOH和Na2CO3条件下,14d后由初始的7000mg·L-1下降至5156、4096、4420mg·L-1。在Na2CO3条件下 WAS的VSS去除率最高,但由于使用Na2CO3控制反应器pH为10需要投加的量较多,导致该条件下TSS的去除率没有NaOH条件下高。而在Ca(OH)2条件下,TSS不降反升,TSS由7000mg·L-1上升至7392mg·L-1。
3 结 论
考察了 KOH、NaOH、Ca(OH)2、Na2CO34种碱对剩余污泥水解产酸以及脱水性能的影响。得出如下结论:
1)KOH和NaOH条件下,剩余污泥的水解能力相当,在2种条件下SCOD的溶出量以及氨氮和正磷酸盐的释放量都比较接近;且这2种条件下污泥的脱水性能也相当,在4种碱性条件下最差。
2)NaOH条件下发酵,污泥的产酸量最高,且TSS的去除率最高。
3)Ca(OH)2条件下,污泥的脱水性能最好,氨氮和正磷酸盐的释放量最少;但污泥的水解能力,产酸能力以及污泥减量情况最差。
4)Na2CO3条件下,污泥的水解能力和VSS的去除率最高;但氨氮和正磷酸盐的释放量最多。
[1]Gao Y Q,Peng Y Z,Zhang J Y,et al.Biological sludge reduction and enhanced nutrient removal in a pilot-scale system with 2-step sludge alkaline fermentation and A2O process [J].Bioresource Technology,2011,102(5):4091-4097.
[2]Kang X R,Zhang G M,Chen L,et al.Effect of initial pH adjustment on hydrolysis and acidification of sludge by ultrasonic pretreatment [J].Industrial and Engineering Chemistry Research,2011,50(22):12372-12378.
[3]肖本益,刘俊新.污水处理系统剩余污泥碱处理融胞效果研究[J].环境科学,2006,27(2):319-323.Xiao B Y,Liu J X.Study on treatment of excess sludge under alkaline condition [J].Environmental Science,2006,27(2):319-323.
[4]Kim J,Park C,Kim T H,et al.Effects of various pretreatments for enhanced anaerobic digestion with waste activated sludge [J].Journal of Bioscience and Bioengineering,2003,95(3):271-275.
[5]尹军,臧立新,于海侠,等.超声与碱预处理低有机质剩余污泥特性分析[J].环境工程学报,2009,3(1):179-182.Yin J,Zang L X,Yu H X,et al.Characteristics of waste activated sludge with low VSS content by ultrasonic and alkaline pretreatment [J].Chinese Journal of Environmental Engineering,2009,3(1):179-182.
[6]Neyens E,Baeyen J,Creemer C.Alkaline thermal sludge hydrolysis[J].Journal of Hazardous Materials,2003,97(1/2/3):285-314.
[7]国家环境保护局《水和废水监测分析方法》编委会.水合废水监测分析方法 [M].北京:中国环境科学出版社,2002.
[8]Lowry O H,Rosebrough N J,Farr A L,et al.Protein measurement with the Folin phenol reageant [J].Journal of Biological Chemistry,1951,193:265-275.
[9]Tong J,Chen Y G.Recovery of nitrogen and phosphorus from alkaline fermentation liquid of waste activated sludge and application of the fermentation liquid to promote biological municipal wastewater treatment[J].Water Research,2009,43(12):2969-2976.
[10]Vlyssides A G,Karlis P K.Thermal-alkaline solubilization of waste activated sludge as a pre-treatment stage for anaerobic digestion [J].Bioresource Technology,2004,91(2):201-206.
[11]Li H,Jin Y Y,Mahar R,et al.Effects and model of alkaline waste activated sludge treatment [J].Bioresource Technology,2008,99(11):5140-5144.
[12]Stuckey D C,Mccarty P L.The effect of thermal pretreatment on the anaerobic biodegradability and toxicity of waste activated sludge[J].Water Research,1984,18(11):1343-1353.
[13]格雷迪.废水生物处理[M].张锡辉,刘勇弟,译.北京:化学出版社,2004.
[14]Dogǎn I,Sanin F D.Alkaline solubilization and microwave irradiation as a combined sludge disintegration and minimization method [J].Water Research,2009,43(8):2139-2148.
[15]Erdincler A,Vesilind P A.Effect of sludge cell disruption on compactibility of biological sludges [J].Water Science and Technology,2000,42(9):119-126.
[16]Valo A,Carrere H,Delgenes J P.Thermal,chemical and thermo-chemical pre-treatment of waste activated sludge for anaerobic digestion [J].Journal of Chemical Technology and Biotechnology,2004,70(11):1197-1203.
[17]Chen Y G,Jiang S U,Yuan H Y,et al.Hydrolysis and acidification of waste activated sludge at different pHs[J].Water Research,2007,41(3):683-689.
[18]Elefsiniotis P,Wareham D G,Smith M O.Use of volatile fatty acids from an acid-phase digester for denitrification[J].Journal of Biotechnology,2004,114(3):289-297.
[19]Chen Y G,Randall A A,Mccue T.The efficiency of enhanced biological phosphorus removal from real wastewater affected by different ratios of acetic to propionic acid[J].Water Research,2004,38(1):27-36.
[20]Mcinerney M J.Anaerobic hydrolysis and fermentation of fats and proteins[G]//Zehnder A J B.Biology of Anaerobic Microorganisms.New York:John Wiley &Sons Inc.,1988:373-417.
[21]Liu X L,Liu H,Chen Y Y,et al.Effects of organic matter and initial carbon-nitrogen ratio on the bioconversion of volatile fatty acids from sewage sludge[J].Journal of Chemical Technology and Biotechnology,2008,83(7):1049-1055.
[22]Jiang S,Chen Y G,Zhou Q,et al.Biological short-chain fatty acids (SCFAs)production from waste-activated sludge affected by surfactant [J].Water Research,2007,41(14):3112-3120.
[23]Yuan Q,Oleszkiewicz J A.Biomass fermentation to augment biological phosphorus removal [J].Chemosphere,2010,78(1):29-34.
[24]Yuan Q,Sparling R,Oleszkiewicz J A.VFA generation from waste activated sludge:Effect of temperature and mixing[J].Chemosphere,2011,82(4):603-607.
[25]Guan B H,Yu J,Fu H L,et al.Improvement of activated sludge dewaterability by mild thermal treatment in CaCl2solution[J].Water Research,2012,46(2):425-432.
