喹唑啉类衍生物的合成及其抗肿瘤活性*
2013-11-19陈舒忆吕同杰严和平欧阳贵平
陈舒忆, 吕同杰, 严和平, 欧阳贵平
(1. 贵州大学 精细化工研究开发中心 教育部绿色农药和农业生物工程重点实验室,贵州 贵阳 550025; 2. 红河学院 理学院,云南 蒙自 661100)
自吉非替尼作为治疗非小细胞肺癌的药物上市以来,随着埃罗替尼、拉帕替尼的相继出现,喹唑啉类化合物日益受到研究者的重视,目前已有数个喹唑啉类化合物进入临床试验阶段[1]。
表皮生长因子受体(EGFR)酪氨酸激酶是广泛分布在哺乳动物上皮细胞膜上的多功能糖蛋白,是细胞外信号传递到细胞内的重要枢纽。酪氨酸激酶介导的细胞生长信号通路在癌症形成和发展过程中起重要作用,能调控细胞增殖、新陈代谢、细胞存活和凋亡以及各种生长机制[2]。临床研究表明,EGFR在许多肿瘤患者中有过表达[3],因而抗肿瘤药物的研发常常以EGFR为靶标。喹唑啉类化合物具有良好的生物活性,对EGFR有很强的抑制作用,且具有较高的选择性[4],此类化合物能选择性地与EGFR结合,竞争性阻碍EGFR与ATP结合,抑制EGFR自身酪氨酸激酶活化,干扰EGFR的信号传导,致使肿瘤癌细胞凋亡。
本研究以吉非替尼为先导,设计合成了一系列喹唑啉衍生物,并进行初步抗肿瘤活性测试,以期能筛选出高活性化合物。参照文献[5,6]方法,以异香草醛(1)为起始原料,与1-溴-3-氯丙烷缩合反应,然后与盐酸羟胺生成腈类中间体3; 3经硝化、还原,与N,N-二甲基甲酰胺二甲缩醛反应,再与3-氯-4-氟苯胺反应合环,最后与一系列的芳香醚(Ⅰa~Ⅰh)反应,合成了8个喹唑啉类衍生物8a~8h(Scheme 1),其结构经1H NMR,13C NMR和MS确证。并测定了8对人乳腺癌细胞Bcap-37的体外抑制活性。
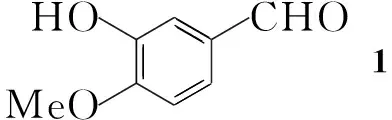



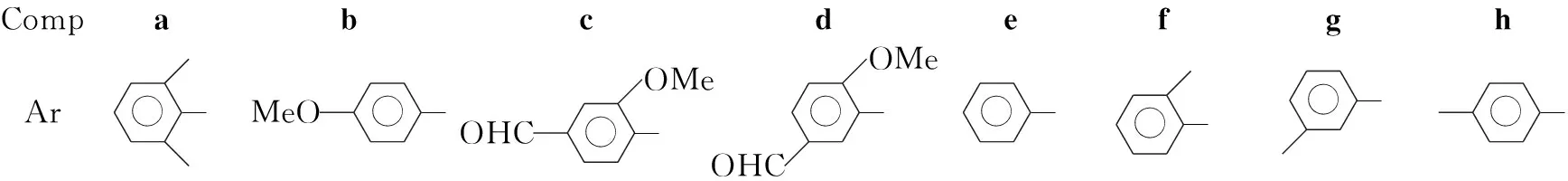
CompabcdefghAr--MeO-OHCOMe-OHCOMe----
Scheme1
该合成方法操作简便,省去基团的保护及去保护,有效际避免了氯化试剂带来的环境污染,收率较高。
1 实验部分
1.1 仪器与试剂
X-4型显微熔点仪(温度计未校正);ECX-500型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Agilent 1100 MSD-Trap-VL型质谱仪;BIO-RAD 680型酶标仪。
2~7参考文献[7]方法合成。7:收率58.3%, m.p.142 ℃~146 ℃;1H NMRδ: 2.27(m, 2H), 3.82(t,J=7.02 Hz, 2H), 3.98(s, 3H), 4.30(t,J=5.75 Hz, 2H), 7.15(d,J=8.0 Hz, 1H), 7.25(t,J=8.0 Hz, 1H), 7.80(m, 1H), 7.85(s, 1H), 8.12(m, 1H), 8.51(s, 1H); EI-MSm/z: 396.2{[M+H]+}。柱层析用硅胶,200 目~300 目;其余所用试剂均为分析纯。
1.2 8的合成(以8a为例)
在三口瓶中依次加入71.00 g(2.52 mmol), 2,6-二甲基苯酚(Ⅰa) 0.61 g(5.00 mmol), K2CO30.76 g(5.00 mmol)和DMF 15 mL,搅拌下回流反应4 h(TLC跟踪)。冷却至室温,倾入水中静置析晶,过滤,滤饼经硅胶柱层析[洗脱剂:V(氯仿) ∶V(甲醇)=20 ∶1]纯化得淡黄色固体8a0.66 g。

表 1 合成8的实验结果Table 1 Experimental results of synthesizing 8

表 2 8的NMR数据Table 2 NMR data of 8
续表2

Comp1H NMR δ(J/Hz)13C NMR δ8h2.22(s, 3H), 2.29(m, 2H), 3.94(s, 3H), 4.15(t, J=5.75, 2H), 4.31(t, J=5.75, 2H), 6.85(s, 1H), 6.87(s, 1H), 7.07(s, 1H), 7.09(s, 1H), 7.44(t, J=9.15, 1H), 7.80(m, 1H), 7.84(s, 1H), 8.12(d, J=9.15, 1H), 8.51(s, 1H), 9.55(s, 1H)20.59, 29.23, 56.40, 64.55, 66.15, 103.02, 107.84, 109.27, 114.78, 116.94, 119.21, 122.83, 123.98, 129.74, 130.38, 137.31, 147.55, 148.73, 152.69, 153.18, 154.94, 156.52, 156.83
用类似的方法合成白色固体8b~8h,实验结果见表1, NMR数据见表2。
1.3 体外抗肿瘤活性测定
8的体外抗肿瘤活性初步筛选试验均以DMSO作空白对照,阿霉素作为阳性对照。采用MTT法测定8对人乳腺癌细胞Bcap-37的抑制作用。
取对数生长期的乳腺癌细胞Bcap-37,以2×103个/孔接种于96孔板中,每孔100 μL。在5%CO2气氛中于37 ℃置含10%FBS的PRMI 1640培养基中培养,使细胞贴壁。待细胞生长90%左右时,吸掉培养基,每孔加入200 μL含不同浓度供试化合物的含血清培养基,每个供试化合物设2个剂量组(1 μmol·L-1, 10 μmol·L-1),每组设6个平行孔,对照组加入与药等体积的溶剂,继续培养至试验设计时间。去除上清,每孔加入100 μL浓度为0.5 mg·mL-1的MTT溶液(1×PBS配制)。于37 ℃避光温育4 h;每孔再补加10% SDS 100 μL,再培养10 h。从培养箱中取出,静置30 min(使其冷却),置振板器上振荡10 min(使结晶物充分溶解)。于酶标仪595 nm处测量各孔吸收值(OD值)。试验设空白对照组(细胞、化合物溶媒、培养液、MTT和DMSO)和调零组(培养基、MTT和DMSO),按下式计算供试化合物对肿瘤细胞的抑制率(%)。

2 结果与讨论
8的体外抗肿瘤活性测试结果见表3。由表3可见,除8c和8d外,8a,8b,8e~8h对乳腺癌细胞Bcap-37抑制率较高,部分抑制率与对照药剂阿霉素相当。根据目前对喹唑啉衍生物活性的研究[8]可知,对于4-苯胺基-6,7-二取代喹唑啉类化合物,4-位苯胺基与6-或7-位取代基团对化合物的活性有至关重要的作用。文献[9]报道4-位苯胺基的H替换为F, Cl, Br或I可提高抗肿瘤活性。本试验通过对喹唑啉6-位长链上苯醚结构的研究得知,含甲氧基、甲基等供电子基团能增强化合物对乳腺癌细胞Bcap-37的抑制活性;而含有醛基等吸电子基团的化合物抗肿瘤活性不明显。
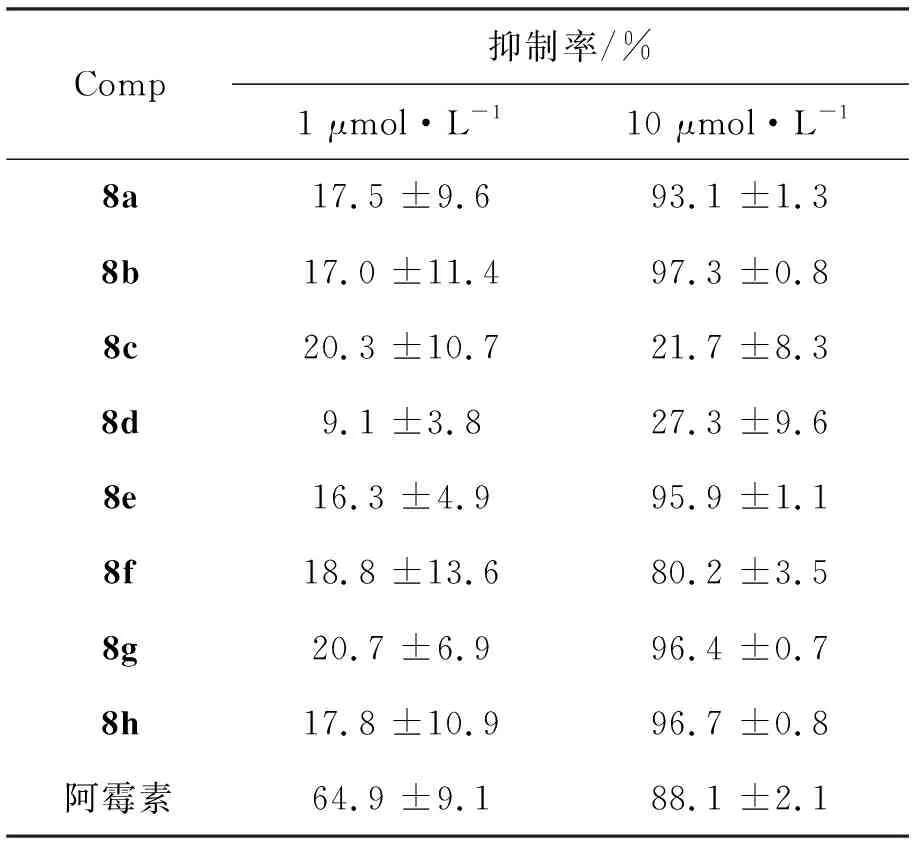
表 3 8的体外抗肿瘤活性*Table 3 Antitumor activities of 8 in vitro
*测试方法见1.3
3 结论
本文以异香草醛为原料,经醚化、氰基化、硝化、还原、合环后,再与一系列芳香醚反应,设计合成了8个喹唑啉类化合物,并用MTT法测定其抗肿瘤活性。初步活性测试结果表明,具有喹唑啉环基本结构的化合物8a~8h均对乳腺癌细胞Bcap-37具有一定程度的体外抑制作用,部分化合物抑制率与对照药剂阿霉素相当,显示了较好的抗肿瘤活性。
[1] 张万年,缪震元. 抗肿瘤创新药物研究进展[J].中国新药杂志,2010,19(24):2277-2289.
[2] Mendelsohn J. Blockade of receptors for growth factors:An anticancer therapy-the fourth annual Joseph H.burchenal american association for cancer research clinical research award lecture[J].Clin Cancer Res,2000,6:747-753.
[3] Wong A J, Bigner S H, Bigner D D,etal. Increased expression of the epidermal growth factor receptor gene in malignant gliomas is invariably associated with gene amplification[J].Medical Sciences,1987,84:6899-6903.
[4] Khaled Abouzid, Samia Shouman. Design,synthesis and in vitro antitumor activity of 4-aminoquinoline and 4-aminoquinazoline derivatives targeting EGFR tyrosine kinase[J].Bioorganic & Medicinal Chemistry,2008,16:7543-7551.
[5] Chandregowda V, Venkateshwara Rao G, Chandrasekhara Reddy G. Convergent approach for commercial synthesis of gefitinib and erlotinib[J].Org Process Res Dev,2007,11:813-816.
[6] Chandregowda V, Venkateshwara Rao G, Chandrasekhara Reddy G. One-pot conversion of 2-nitrobenzonitriles to quinazolin-4(3H)-ones and synthesis of Gefitinib and Erlotinib hydrochloride[J].Heterocycles,2007,71:39- 48.
[7] 吕同杰,欧阳贵平. 吉非替尼的合成[J].广州化工,2010,38(12):154-156.
[8] 白俊生. 新型4-氨基喹唑啉类化合物的设计与合成[D].长春:吉林大学,2009.
[9] 刘靖,王林,杨晓明. 多靶点蛋白酪氨酸激酶抑制剂的研究进展[J].国际药学研究杂志,2009,36(3):161-171.
