法国对注射皱纹填充剂产品的监管
2013-11-12张建民编译
张建民(编译)
(上海昊海生物科技股份有限公司,上海 200052)
2008年我国批准了第一个透明质酸类注射皮肤填充剂产品,标志着我国注射美容皮肤填充剂市场进入了快速理性的发展阶段。本刊2011年第2期介绍了美国《FDA对注射美容产品的监管》,2012年第4期介绍了《美国法国及我国批准上市注射美容皮肤填充剂比较及建议》。本文将介绍法国对注射美容填充剂产品的监管。
1 概述
法国市场上约有28家国内外生产企业生产的近109种批准上市的注射皱纹填充剂(Injectable wrinkle fillers)产品。在注射皱纹填充剂产品中,可吸收材料透明质酸类产品占96.33%。慢吸收材料产品占2.75%,不可吸收材料产品只占0.92%。在法国注射皱纹填充剂按医疗器械分类归属于植入类产品。由于注射皱纹填充剂产品侵入性特性,预示着使用产品后可能伴随着潜在的并发症发生。因此,法国国家医药保健品安全局管理部门(ANSM)对这些产品有着严格的监控和检查程序。
2 医疗器械产品的风险评估
以医疗为目的医疗器械产品和用于整形美容目的(如注射皱纹填充产品)的医疗器械产品效益风险比的评估是不同的。以医疗为目的器械产品在医疗应用中的疗效是客观的、可测的,并可直接影响到病人的健康,而成功的整形美容手术主要还是取决于病人的感受和满意程度。在医学治疗上被认为可以接受的风险,是完全不同于为了达到整形美容以改善目的为主的治疗而产生的风险。
3 市场监管
在法国注射皱纹填充剂作为医疗器械,生产商必须在生产的产品上标有已通过CE认证的标识和产品生产必须符合欧洲指令93/42/EEC(2007/47/EC修改版)要求。CE标志是产品在欧洲市场上自由通行贸易的保证。由于注射皱纹填充剂具有对人体健康构成潜在的高风险,因此这类产品在法国归属于器械IIb/III管理。
3.1 监管职责
在法国注射皱纹填充剂产品投放入市场必须由生产商或授权代表或经销商报送法国国家医药保健品安全局管理部门(ANSM)。生产商主要负责生产的器械产品上市,欧盟主管部门负责医疗器械市场监管。
该部门机构担负着对市场所有医疗器械按规定进行监管:
对上市备案产品进行市场监控,特别侧重于新上市的产品;
对生产商进行检查;
对市场采集的产品或早已上市的产品样品进行检测。
当监管机构认定产品可能危及患者(使用者)健康或安全的情况下,可以采取一切适当的临时措施,从市场上撤回这些产品,禁止或限制其市场准入。
3.2 假冒和伪劣产品
在互联网上购买的注射皱纹填充剂产品通常都是通过邮寄进入法国市场,使得对这部分产品的监控就非常困难,通过这种非法途进入法国的产品意味着这些产品摆脱了法国ANSM的常规监控。在互联网上购买的注射皱纹填充剂产品虽然有的他们是早已上市的品牌,但是有的产品并没有标带CE的标志。
在互联网上购买注射皱纹填充剂产品的质量和产品储存条件都是没有保证的,网购者收到假冒或感到可能由于不当的储存或运输条件导致过期、质量很差的产品时一定要及时给予上报,这些产品也可能是采用伪造或是质量很差的原料加工生产的。一旦发现假冒伪劣产品,国家ANSM将会在网站上给予通告公示。
4 对注射皱纹填充剂相关的主要风险认识和提示
在皮肤内注射入填充材料引进了导致有可能引发皮肤反应的异物,由这些异物导致的副反应大多数是短暂的如发红,水肿等(见表)。但是有些副反应可能是受诸多外部因素的影响,如产品特性、注射技术、注射部位、注射量等,还有可能是一些个别的因素影响(如病人的耐受性和病人的病史)。与产品使用有关的主要风险在产品使用说明书中都已列出(如血肿,红斑等)。不太常见的风险如肉芽肿的发生,主要与慢吸收材料和不可吸收材料产品有关。肉芽肿是在产品注射后几个月或甚至几年后发生。
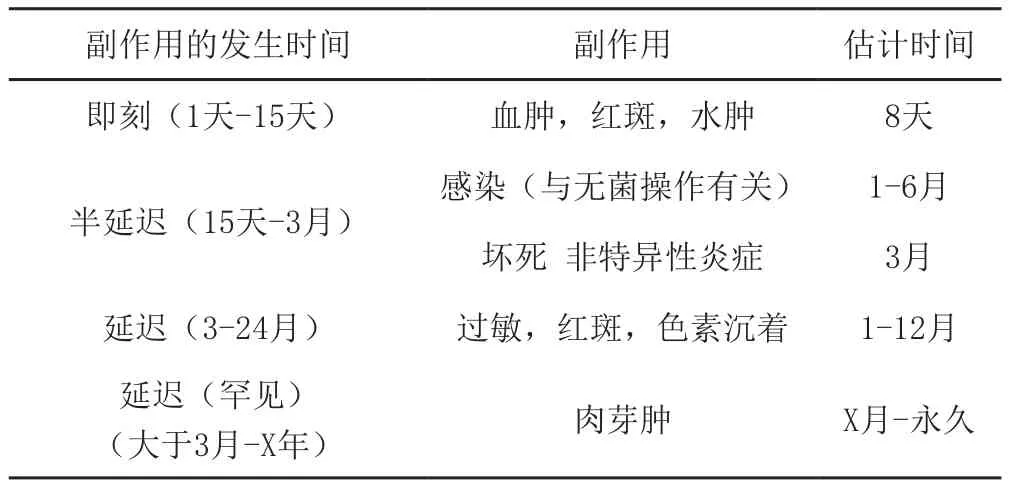
表1 注射皱纹填充剂产品副作用发生的时间、症状
4.1 不可吸收材料注射除皱填充剂
法国健康卫生部门不建议在注射美容中使用不可吸收材料的产品,主要是这些产品具有延迟性、不可控及严重不良反应的风险。若干年后再注射其他各种产品或在为其他整形注射目的治疗时可能会增加这些不良反应症状出现的风险。
不可吸收材料产品的使用经验显示:产品相关的副反应延迟发生(如肉芽肿)通常是因为产品的永久存在。同样如果产品永久性存在在皮肤中更会引发炎症类副反应。当这些延迟反应出现时,它们的影响就像产品一样往往是永久性的,是难以治疗的。
鉴于已经获得使用某些不可吸收材料的产品经验:使用如德美丽(DERMALIVE,已经由厂商DERMATECH在2007年撤回)主要导致延迟肉芽肿发生的产品(注射后2-10年)。因此,病人必须被告知不可吸收材料产品用于注射整形美容目的是不予推荐的。(注:法国已经退出市场的不吸收产品参见本刊2012年第4期介《美国法国及我国批准上市注射美容皮肤填充剂比较及建议》)
4.2 对注射除皱填充剂的风险认识
基于现有的认识,使用注射除皱填充剂的相关风险频率很难界定,原因如下:
时间范围不足:这是一个新兴的市场,会有许多新的产品和新的材料应用于临床;
缺乏预警体系的报告:接受注射除皱填充剂的患者相当分散,很难收集反映与注射这些产品相关不良事件的实际人数的有关数据;
发生副作用往往与单个特定产品有关,而不是一类产品。此外,有时候风险与生产商产品的生产过程(如:污染)、产品的流变性(如:产品的形式、粘性等)有关。
5 产品的追溯和预警体系
5.1 产品的追溯
鉴于注射皱纹填充剂产品具有侵入性特性,且接受过整形注射的受试者相当分散,按照法国的法规作为医疗器械注射皱纹填充剂每支必须能被追溯。
5.2 预警体系
法国对医疗器械不良事件预警系统旨在防止不良事件的再次发生及提示可能严重不良事件的风险。对此执业医疗专业人士有义务必须向国家ANSM报告发生的不良反应事件,以便及早预防或及时采取有效措施。接受注射的病人也能向ANSM报告关于副作用的情况,但这通常是通过病人的临床医生来报告的。
为病人和专业医护人员特别设计的不良事件报告表可以通过互联网向国家ANSM的网站报告。这些报告将会及时由包括外部专家在内的专家组一起商讨评判,并要求必须对直接与产品有关的问题进行评估。
国家医药保健品安全管理部门(ANSM)的任务是根据评估情况马上发出警告并建议整顿、检查整改措施的落实,如果是严重危险,并已确认与产品有关的不良反应或作出产品临时退市的决定。
6 对医疗机构及公众的建议
注射皱纹填充剂是一种长效(非永久)、侵入性(微创)外科手术器械。产品的“侵入性”特性警示有使用后会有潜在的并发症和副作用。此外,这些产品作为整形美容手术用于健康的求美患者身上,而这些患者分散较广,健康主管机构必须在信息流通、市场监管和预警系统方面进行严格监控。
6.1 对医疗机构临床医生的建议
法国ANSM正在建立整形注射美容手术的管理体系。注射过程是一项具有重要专业技术特性的手术过程,有着具有重要的具体技术要求的特点。因此目前注射除皱填充剂都是由整形外科医生、皮肤科医生和接受过特殊专业培训的临床医生来开展。
6.1.1 使用注射除皱填充剂前
临床医生必须询问病人的病史:
是否有严重的过敏史;
是否有过敏反应(急性过敏反应);
是否对局部麻醉过敏;
是否耐受抗生素或糖皮质激素;
是否有异常出血;
注射部位的状况(预先存在的疤痕,感染等)。
临床医师必须询问病人:以前注射治疗使用过什么产品,特别是对先前注射过产品的特点和性质。因为在注射过非吸收材料产品的同样部位注射可吸收材料产品是不可取的。
临床医师建议选择的产品:必须是符合国家现行法规上市的产品,必须根据产品使用说明书中的信息注射在面部有针对性的目标部位区域和深度。
注射皱纹填充剂后可能伴随的风险和副作用告知患者很重要(见上表)。应当指出的是:延迟反应的发生(基本上注射的是永久性材料产品)和产品本身一样,对注射部位的影响往往是永久性的。注射永久性材料产品后产生的副作用影响的永久性,使得这些副作用很难治疗。
使用非吸收材料产品用于整形美容是不可取的。非吸收注射皱纹填充剂的使用经验表明,延迟并发症(如肉芽肿)的发生通常是永久性产品材料存在的缘故。
6.1.2 使用注射皱纹填充剂期间和使用后
可追溯性是最关键的。
注射手术:注射的次数和两次注射之间的长短间隔;使用的产品;
面部注射位置;注射产品的量;
病人的注射治疗数据必须保存15年,能随时提供所有的以“整形日志”形式记载的与注射相关的病人的信息资料。有任何副作用必须向国家ANSM申报。
6.2 对公众患者的建议
注射除皱填充剂产品的使用该根据产品说明书注射入皮肤规定的深度(真皮浅层、真皮深层等)和面部区域(唇部、眉间、鼻唇纹等)。产品的注射深度在使用说明指定的以外和(或)在使用说明指定的以外用于身体的其他任何部位的注射都有可能对人体的健康造成严重的后果。
6.2.1 注射除皱填充剂使用前
要知道注射皱纹填充剂后可能引发的风险和副作用是很重要的。
病人必须告知医师自己的所有病史;
必须告知医师以前是否使用过注射皱纹填充剂,使用的是哪一种填充剂,因为在注射过不可吸收材料产品的同一部位不宜再使用可吸收材料产品;
不可吸收材料产品用于注射填充整形美容是不可取的。不可吸收注射皱纹填充剂的使用经验表明,延迟并发症(如肉芽肿)的发生通常是永久性产品材料存在的缘故,如果用的是永久性产品这类炎症反应更有可能发生。
6.2.2 使用注射皱纹填充剂期间和之后
所有有关下列的文件(整形美容注射病史)必须保留15年,注射手术:注射产品次数和两次注射之间的长短间隔;
使用的产品;
面部注射位置;
注射产品的量。
任何不良的反应,必须亲自或由您的医生向国家ANSM报告。
[1]张建民. 法国对注射美容产品注射皱纹填充剂的监管. 上海食品药品监管情报研究,2012(10):15.
