棉籽油加氢脱氧制备第二代生物柴油
2013-11-05董广达王玉军张卫东骆广生
董广达,王玉军,张卫东,骆广生
(1. 清华大学 化学工程联合国家重点实验室,北京 100084;2. 北京化工大学 化学工程学院,北京 100029)
生物柴油作为当前备受关注的可再生能源,是石化柴油最有潜力的替代燃料。通过酯交换反应得到的脂肪酸酯类化合物属于第一代生物柴油。奚立民等[1]通过阳离子交换树脂催化油脂制得脂肪酸甲酯(FAME),并建立了动力学模型。第二代生物柴油是以动植物油为原料,通过加氢脱氧、异构化等反应最终得到类似柴油组分的链烷烃类化合物。较之第一代生物柴油,第二代生物柴油在化学结构上与石化柴油完全相同,不含氧和硫,具有与柴油相近的黏度、较低的密度和较高的十六烷值,同样质量单位的发热值更高,可以更大比例添加到石化柴油中[2]。
油脂加氢所用催化剂主要有过渡金属催化剂和贵金属催化剂[3]。da Rocha等[4-6]发现,通过Ni-Mo,Ni-W,Co-Mo等催化剂的作用,在300~360℃、压力不低于3 MPa的反应条件下,可直接将植物油中的甘油三酯转化成烷烃类化合物,反应过程中的副产物为丙烷、CO2和水。Jozef等[7]以精炼棕榈油和猪油为原料,柴油收率分别达到89.0%和92.1%。Gong等[8]对麻疯树油进行加氢脱氧,可以得到82%(w)的液态烷烃。Simacek等[9]以菜籽油为原料,采用硫化态催化剂,在液态空速1 h-1的条件下进行加氢反应,得到的柴油组分质量收率为80%。Krar等[10]采用氧化态催化剂对葵花籽油进行加氢,得到的柴油组分质量收率为73.8%。
我国人口众多,发展生物柴油应做到不与民争粮争油,因此对生物柴油的研究从原料上受到一定制约。同时我国也是产棉大国,棉花产量呈逐年上升趋势,2010年我国棉籽油产量达1.60 Mt。但棉籽油中含有大量棉酚,不宜长期食用,同时随着人民物质生活水平的提高,棉籽油的食用率呈下降趋势,所以以棉籽油为原料生产生物柴油符合我国的实际国情。目前,通过酯交换反应,可将棉籽油转化成FAME,生产第一代生物柴油[11-14]。以棉籽油为原料,通过加氢脱氧、加氢脱羰等反应直接生成第二代生物柴油的研究鲜有报道。
本工作基于我国实际国情,以棉籽油为原料制备第二代生物柴油,考察了不同工艺条件下棉籽油加氢脱氧反应的效果,得到了较好的反应条件。
1 实验部分
1.1 药品与试剂
三级棉籽油:晨光生物科技集团股份有限公司,脂肪酸组成见表1;拟薄水铝石(SB粉):CA,Condea公司;MoO3:AR,国药集团化学试剂有限公司;硝酸镍、硝酸、柠檬酸:AR,北京化工厂;甲基纤维素:CA,北京化工厂;田菁粉:CA,响水宏润植物胶有限公司;正辛烷:AR,天津市福晨化学试剂厂;1,4-二异丙基苯:AR,百灵威科技有限公司。

表1 棉籽油脂肪酸的组成Table 1 Composition of fatty acids in cottonseed oil
1.2 催化剂的制备
称取一定质量比的SB粉、MoO3、甲基纤维素、田菁粉和柠檬酸,通过小型混合机搅拌5 min使其充分混合均匀,然后将粉状固体混合物与浓度为1 mol/L的硝酸按质量比1∶1混捏,放入成型机挤条成型,在烘箱中于80 ℃下干燥10 h,再于马弗炉中于600 ℃下焙烧4 h,得到直径为1 mm的条状催化剂前体Mo/γ-Al2O3。将该前体剪成长0.5 cm左右的小段,采用饱和浸渍法将其浸渍在质量浓度为0.25 g/mL的硝酸镍溶液中,浸渍后的颗粒在烘箱中于80 ℃下干燥10 h,再于马弗炉中550 ℃下焙烧4 h,制得Ni-Mo/γ-Al2O3催化剂。
1.3 催化剂的表征
采用日本电子株式会社的JEM-2010型高分辨透射电子显微镜进行TEM表征,工作电压120~200 kV,放大倍率为(1~6)×105倍;采用日本理学公司的D/MAX-ⅢA型X射线衍射仪进行XRD表征,Cu Kα射线;采用Quantachrome公司的QUADRASORBSI型全自动多站比表面积和孔径分析仪进行N2吸附-脱附表征,测定前在200℃、真空条件下脱气5 h,测定比表面积时采集相对压力为0.10~0.30之间的吸附点,用BET法计算比表面积和孔体积,用BJH法计算平均孔径及孔径分布。
1.4 实际体系反应评价
将催化剂颗粒装填在高温高压微型固定床反应器中,反应管内径15 mm,催化剂颗粒装填量为12 mL。首先对催化剂进行活化,在温度300 ℃、压力2 MPa、液态空速3.0 h-1、氢气与原料液流量比(氢油比)200的条件下,以3%(w)的CS2正己烷溶液为预硫化剂活化催化剂7 h。配制20%(w)的棉籽油正辛烷溶液作为原料液,在一定温度、压力下进行加氢脱氧反应。原料液采用平流泵平稳进料,产品液取样时间间隔1 h。采用岛津公司GC-2014型气相色谱仪分析产物,采用毛细管色谱柱(30 m×0.25 μm,极性柱)和氢火焰离子化检测器,柱温100 ℃,进样口温度320 ℃,检测器温度300℃,分流比40。
采用Elementar公司varial-ELⅢ型元素分析仪分析原料液与产品液中的氧含量,用脱氧率(RHDO)表示脱氧效果。RHDO的计算公式如下:

式中,wi为原料试样中氧元素的质量分数;w0为产品试样中氧元素的质量分数。
2 结果与讨论
2.1 棉籽油加氢脱氧理论收率的计算
油脂加氢脱氧的反应路径见图1。

图1 油脂加氢脱氧的反应路径Fig.1 Reaction mechanism of the hydrodeoxygenation of oils.
植物油的主要成分为甘油三酯,在其脂肪酸组成中含有大量的不饱和键。在加氢脱氧反应过程中,首先是对不饱和键进行加氢饱和,得到饱和的甘油三酯;再通过进一步的反应,酯键逐步断裂,脂肪酸以脱氧或脱碳的形式脱除H2O,CO2,CO,生成目标产物,即柴油烷烃。在催化剂的作用下,伴随着酯键的断裂,脱氧和脱碳反应同时进行。根据反应机理及棉籽油中脂肪酸的组成(见表1),计算棉籽油完全脱氧生成生物柴油的理论收率(Y):

式中,Mi为目标产物的相对分子质量;M0为甘油三酯的相对分子质量。经计算,棉籽油完全脱氧转化成生物柴油的理论收率为79.65%~84.43%。
2.2 棉籽油加氢脱氧的反应结果
2.2.1 GC分析结果
棉籽油加氢脱氧反应前后的GC谱图见图2,GC测试采用内标法。
由图2可见,保留时间约为4.5 min的峰归属于内标物1,4-二异丙基苯;反应后的棉籽油的GC谱图中,保留时间为5.0~7.0 min的范围内依次分布了分离效果良好的C15~18的峰。

图2 棉籽油加氢脱氧反应前(A)后(B)的GC谱图Fig.2 GC spectra of the cottonseed oil before(A) and after(B) hydrodeoxygenation.
2.2.2 不同反应条件下的收率及脱氧率
不同反应条件下生物柴油的质量收率见图3,目标组分的质量收率见表2。在反应过程中,每间隔1 h取样进行气相色谱分析,通过实验发现反应2~3 h后,收率变化不大,反应达到稳定状态。由图3可见,随反应温度的升高,产物的收率逐渐增大,反应温度由320 ℃升至340 ℃时,收率有较大幅度的提高,说明催化剂的活化温度位于该温度范围。同时还发现,随反应压力的升高,产物收率增大。提高液态空速,收率呈下降趋势。
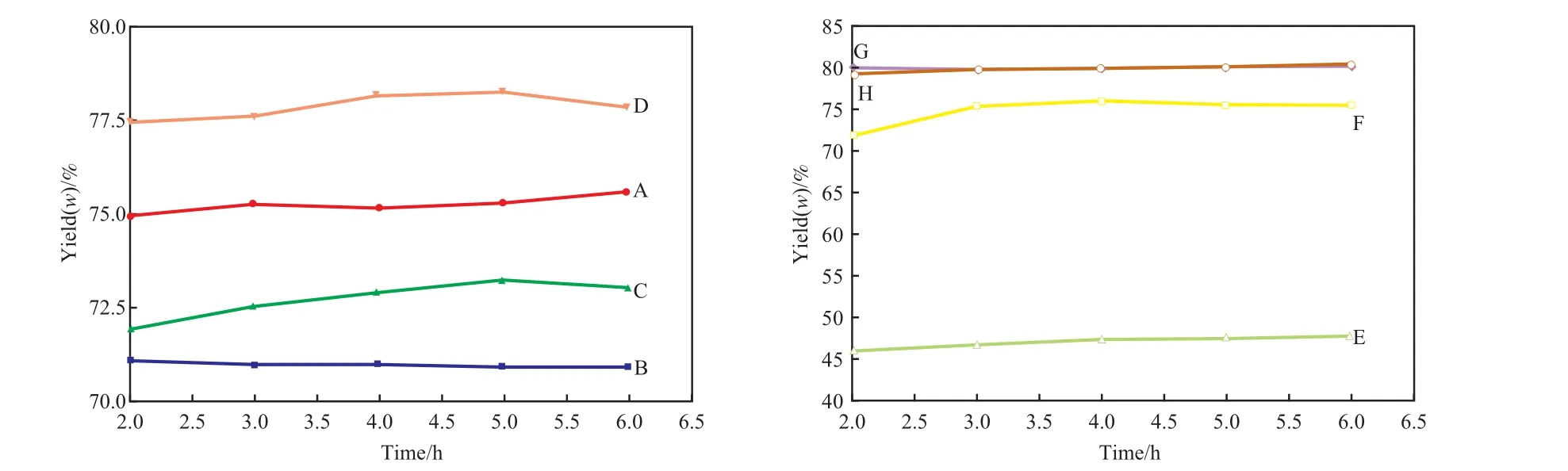
图3 不同反应条件下生物柴油的质量收率Fig.3 The yields of biodiesel under different reaction conditions.
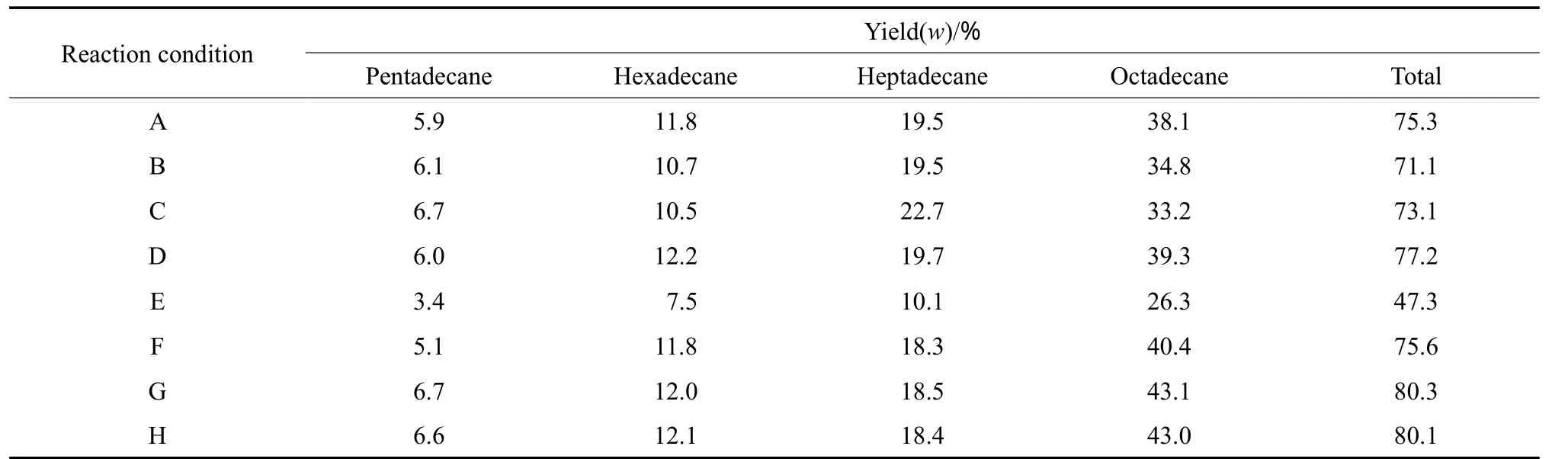
表2 不同反应条件下目标组分的质量收率Table 2 The mass yields of the target components under different reaction conditions
不同反应条件下生物柴油的脱氧率见表3。由表3可见,在360 ℃、4 MPa、LHSV=1.00 h-1条件(反应条件G)下,脱氧率最高,为99.2%,与产品质量收率相对应。通过脱氧产物(C16和C18)与脱羰产物(C15和C17)收率的比值可以发现,随反应温度的升高及液态空速的增大,有利于脱羰反应的进行;随反应压力的升高,有利于脱氧反应的进行,这与Bezergianni等[15]报道的研究结果一致。

表3 不同反应条件下的脱氧率Table 3 The deoxidizing rates(RHDO) under different reaction conditions
2.2.3 生物柴油的物性分析
所得生物柴油的物性分析结果见表4。

表4 生物柴油的物性表征结果Table 4 Physical properties of the obtained biodiesel
2.2.4 催化剂的寿命
对Ni-Mo/γ-Al2O3催化剂进行了长时间的评价,评价结果见图4。催化剂装填在反应管中连续运行70 h,生物柴油的收率无明显降低。在原料液中加入一定量的CS2,对催化剂进行补硫,累计运行150 h,催化效果与初始催化效果持平。

图4 Ni-Mo/γ-Al2O3催化剂的寿命Fig.4 Age of the Ni-Mo/γ-Al2O3 catalyst.
2.3 催化剂的表征结果
2.3.1 催化剂的物相组成
Ni-Mo/γ-Al2O3催化剂的XRD谱图见图5。

图5 Ni-Mo/γ-Al2O3催化剂的XRD谱图Fig.5 XRD spectrum of the Ni-Mo/γ-Al2O3 catalyst.
由图5可见,催化剂试样在2θ=37.12°,45.94°,66.90°处出现明显的γ-Al2O3特征峰,只在2θ=23.74°,27.05°处出现不太明显的MoO3衍射峰,表明通过混捏法加入的MoO3在载体中分散良好。
2.3.2 催化剂的比表面积及孔结构
BET表征结果显示,Ni-Mo/γ-Al2O3催化剂的比表面积为169.8 m2/g,平均孔体积为0.21 mL/g,平均孔径为4.92 nm。Ni-Mo/γ-Al2O3催化剂的孔分布见图6。由图6可见,Ni-Mo/γ-Al2O3催化剂的孔径主要集中分布在4~6 nm之间,油脂大分子的分子尺寸一般在2~4 nm之间[16],因此Ni-Mo/γ-Al2O3催化剂适宜大分子的油脂分子进入孔道与活性组分反应。从图6可以看出,催化剂的N2吸附-脱附曲线呈明显的回滞环,属于IUPAC的H1型,表明其孔主要为两端开口的管分布均匀的圆筒状孔,孔分布较窄,这与孔分布结果相符合。

图6 Ni-Mo/γ-Al2O3催化剂的孔分布Fig.6 Pore distribution on the Ni-Mo/γ-Al2O3 catalyst.
2.3.3 催化剂的结构形貌
预硫化后Ni-Mo/γ-Al2O3催化剂呈活化态,其TEM照片见图7。

图7 硫化态Ni-Mo/γ-Al2O3催化剂的TEM照片Fig.7 TEM image of the sulfureted Ni-Mo/γ-Al2O3 catalyst.
由图7可以观察到Ni-Mo/γ-Al2O3催化剂形成的硫化物微晶层数为6~10层,长度为8~18 nm,硫化物微晶分布均匀。根据Ni-Mo-S活性相理论[17],多层堆垛的硫化物微晶为Ⅱ型活性中心。这些催化活性中心的活性位由相邻的多个Mo配位不饱和位或S阴离子空穴构成[18],位于多层Ni-Mo-S微晶粒的边、角处(底层除外)。
图8为硫化态Ni-Mo/γ-Al2O3催化剂TEM面扫描照片,Mo元素与S元素的分布可以完全对应,说明催化剂中Mo元素分布在催化剂载体孔道的表面,在预硫化过程中可以完全活化。同时印证了Mo与载体之间的作用较弱,因此Ni-Mo/γ-Al2O3催化剂表现出了很高的活性。

图8 硫化态Ni-Mo/γ-Al2O3催化剂TEM面扫描照片Fig.8 TEM area-scan images of the sulfureted Ni-Mo/γ-Al2O3 catalyst.
3 结论
1)棉籽油可以通过加氢脱氧的方式直接转化成第二代生物柴油,通过在不同反应条件下的对比, 360 ℃、4 MPa、棉籽油液态空速1.00 h-1的反应条件为最优条件,得到的生物柴油质量收率为80.3%,脱氧率为99.2%,接近理论范围。
2)通过混捏-浸渍结合的方法制备的负载型纳米Ni-Mo/γ-Al2O3催化剂,具有较高的活性,值得进一步推广。
[1] 奚立民,柯中炉. 阳离子交换树脂催化油脂副产物制备生物柴油的动力学研究[J]. 石油化工,2011,40(4):408 -413.
[2] Naik S N,Vaibhav V G,Prasant K R,et al. Production of First and Second Generation Biofuels:A Comprehensive Review[J]. Renew Sustain Energy Rev,2010,14(2):578 - 597.
[3] 翟西平,殷长龙,刘晨光. 油脂加氢制备第二代生物柴油的研究进展[J]. 石油化工,2011,40(12):1364 - 1369.
[4] da Rocha F D N,Brodzki D,Djega-Mariadassou G. Formation of Alkanes,Alkylcykloalkanes and Alkylbenzenes During the Catalytic Hydrocracking of Vegetable Oils[J]. Fuel,1993,72(4):543 - 549.
[5] Donnis B,Egeberg R G,Blom P,et al. Hydroprocessing of Bio-Oils and Oxygenates to Hydrocarbons. Understanding the Reaction Routes[J]. Top Catal,2009,52(3):229 - 240.
[6] Kubicka D,Simacek P,Zilkova N. Transformation of Vegetable Oils into Hydrocarbons over Mesoporous-Alumina-Supported CoMo Catalysts[J]. Top Catal,2009,52(1/2):161 - 168.
[7] Jozef M,Jan C,Ludmila J,et al. Second Generation Diesel Fuel from Renewable Sources[J]. J Clean Prod,2010,18:917 - 926.
[8] Gong Shaofeng,Shinozaki Akira,Shi Mingliang,et al.Hydrotreating of Jatropha Oil over Alumina Based Catalysts[J].Energy Fuels,2012,26:2394 - 2399.
[9] Simacek P,Kubicka D,Sebor G,et al. Fuel Properties of Hydroprocessed Rapeseed Oil[J]. Fuel,2010,89(3):611 - 615.
[10] Krar M,Kasza T,Kovacs S,et al. Bio Gas Oils with Improved Low Temperature Properties[J]. Fuel Process Technol,2011,92(5):886 - 892.
[11] 韩明汉,陈和,王金福,等. 生物柴油制备技术的研究进展[J]. 石油化工,2006,35(12):1119 - 1124.
[12] 王璐,陶玲,赵福生,等. 文冠果种仁油与棉籽油制备生物柴油对比实验[J]. 农业机械学报,2010,41(10):103 - 106.
[13] 卡巴罗,沈本贤,李泓. 棉籽油制备生物柴油的研究[J].当代化工,2008,37(5):483 - 484.
[14] 张欢,孟永彪. 用棉籽油制备生物柴油[J]. 化工进展,2007,26(1):86 - 89.
[15] Bezergianni S,Kalogianni A,Vasalos I A. Hydrocracking of Vacuum Gas Oil-Vegetable Oil Mixtures for Biofuels Production[J]. Bioresour Technol,2009,100(12):3036 - 3042.
[16] 潘秋月,王大喜,高金森. 重油特征分子尺寸的精确计算方法[J]. 石油学报:石油加工,2007,23(4):63 - 67.
[17] Dugulan A I,Craje M W J,Kearley G J. High-Pressure in Situ Mossbauer Emission Spectroscopy Study of the Sul fidation of Calcined Co-Mo/Al2O3Hydrodesulfurization Catalysts[J]. J Catal,2004,222(1):281 - 284.
[18] Babich I V,Moulijn J A. Science and Technology of Novel Processes for Deep Desulfurization of Oil Re finery Streams:A Review[J]. Fuel,2003,82(6):607 - 631.
